基于中医传承辅助平台与网络药理学探析中药干预新型冠状病毒感染后遗症肺纤维化的作用机制
卫博凯,胡 静
上海中医药大学中医学院,上海 201203
肺纤维化(pulmonary fibrosis)是以上皮细胞受损、正常的肺泡组织受损、成纤维细胞增殖活化、细胞外基质异常沉积为特点,以特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)为代表的多种肺间质性疾病的病理改变[1]。肺纤维化的发展过程中常伴随有干咳、咳少量白色泡沫样痰、食欲减退、消瘦乏力、进行性呼吸困难,晚期则多见杵状指、发绀等症状,部分患者可发展为肺心病,最终因呼吸衰竭死亡[2]。美国IPF 的平均发病率为每10 万人10~60 例,并且在65 岁以上的老年人群中发病率是平均值8~50 倍,国内尚无相关流行病学统计[3]。新型冠状病毒(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)感染导致的肺纤维化是其最主要后遗症之一[4]。现有药物如吡非尼酮及尼达尼布不仅无法完全逆转肺纤维化的进展,并且对因SARS-CoV-2 感染而导致的肺纤维化,学界仅建议二者可能是潜在治疗药物,尚无二者介入的时间点推荐以及相关临床研究证明其干预的有效性[5]。近年来中医药在肺纤维化的治疗中展现了2 项独特的优势,即单用中药制剂可显著延缓患者肺纤维化进程以及中药复方与化学药合用能有效减少具有强副作用的化学药用量[6-7]。目前中医药干预SARS-CoV-2感染后遗症肺纤维化已有初步理论及临床研究成果,但仍缺乏大范围病例研究及学界公认的方剂组合[8-9]。因此,本研究通过中医传承辅助平台V3.0 检索2000 年1 月—2023 年6 月纳入具有明确疗效的中医药治疗肺纤维化的临床研究,探析其组方规律与用药特点,并运用网络药理学方法探析核心药物组合的有效成分、作用靶点及信号通路,为干预SARS-CoV-2 感染后遗症肺纤维化提供思路,整体研究思路见图1。

图1 整体研究思路Fig.1 Overall research idea
1 资料与方法
1.1 资料来源与筛选
自中国知识资源总库(CNKI)、万方数据知识服务平台(Wanfang Data)的检索栏中以“肺纤维化”“间质性肺病”“矽肺”“尘肺”为关键词,检索2000 年1 月—2023 年6 月公开发表且可浏览全文的文献,纳入中医药参与治疗的临床论文共118 篇。
1.2 纳入标准
(1)文献均为临床试验论文;(2)病例符合肺纤维化的诊断标准;(3)具有明确中药组成的方剂、中成药或具有中医特色的其他制剂;(4)文献中证明有良好的临床疗效。
1.3 排除标准
(1)非临床试验的文献;(2)患者分组治疗不明确;(3)患者少于30 例;(4)适用证型治法分类不明确。
1.4 数据规范化处理
以《中国药典》2020 年版为标准,将中药名称数据进行规范化处理,如“麦门冬”规范为“麦冬”、“山萸肉”规范为“山茱萸”、“全瓜蒌”规范为“瓜蒌”等。
1.5 数据录入及分析
使用中医传承辅助平台V3.0 建立中药治疗肺纤维化数据库,并进行证候分型-治则治法统计、用药频次统计、药物四气五味及归经统计、组方规律分析。
1.6 中药化合物筛选及靶点预测
通过对中医药临床治疗肺纤维化的用药频次统计、关联规则分析获取最佳药物组合,将相关中药输入中药系统药理学分析平台(TCMSP)、中药成分数据库(TCMID)、化学专业数据库(CD),得出最佳药物组合的有效成分及靶点。将所检索到的中药主要化合物代入SwissADME 数据库分析,以药动学中GIabsorption 满足high,以及类药性中“Lipinski、Ghose、Veber、Egan、Muegge”5 项筛选原则满足至少2 项为条件筛选有效化合物。将筛选后的化合物代入SwissTarget Prediction 数据库进行靶点预测。
1.7 疾病靶点收集及共同靶点构建
通过GeneCards 数据库、OMIM 数据库以及TTD 数据库以“pulmonary fibrosis”“COVID-19”为关键词,获取相关疾病的关键靶点以及靶点在疾病中的相关性评分(relevance scores),并与中药有效化合物共有的靶点取交集为研究对象。
1.8 基因互作网络分析
基于核心药物组合的化合物及靶点,利用Cytoscape 3.72 软件构建“化合物-靶点”网络,依据参数度值(degree)、中心度值(betweenness centrality)及亲中心度值(closeness centrality)筛选核心化合物。通过STRING 数据库进行共靶点的蛋白互作分析(protein-protein interaction,PPI),并将结果导入 Cytoscape 3.72 执行可视化,通过omicShare 进行京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路富集分析并可视化。根据KEGG 通路富集分析的结果,结合“1.5”项筛选出的核心中药组方中不同功效的中药类别,采用累加计算法,在不同的重要信号通路下累加计算每类中药与疾病交集靶点的相关性评分。
1.9 中药核心成分与关键靶点分子对接分析
从PubChem 数据库检索中药成分化学式,并使用ChemDraw19.0 进行3D 化。从PDB 数据库下载关键靶点的3D 结构格式,运用PyMOL 软件对蛋白质进行去水、加氢等操作,利用Auto Dock 软件将化合物及靶蛋白格式转换,运行Autodock Vina进行对接分析并可视化。结合能小于0 kcal/mol(1 kcal=4.2 kJ)说明配体与受体可以自发结合,结合能小于−5 kcal/mol 说明结合度良好。
2 结果
2.1 疾病分类与辨证论治
中医药治疗肺纤维化的研究主要集中在IPF 63篇,其后依次为肺纤维化(未注明具体病名)34 篇、尘肺病11 篇、放射性肺纤维化8 篇、百草枯中毒2篇。其中涉及合病研究19 篇,分别为社区获得性肺炎与肺纤维化合病4 篇、慢性阻塞性肺疾病与肺纤维化合病4 篇、类风湿关节炎与肺纤维化合病3 篇、结缔组织病与肺纤维化合病3 篇、干燥综合征与肺纤维化合病2 篇、肺癌与放射性肺纤维化合病1 篇、焦虑症与肺纤维化合病1 篇,肺源性心脏病与尘肺病合病1 篇。在用药剂型上主要以汤剂为主(82 篇),其后依次为颗粒剂14 篇、注射液10 篇、胶囊9 篇、丸剂2 篇、离子导入1 篇。在辨证方面,证候分型前10 位依次为气虚血瘀证、气阴两虚证、痰瘀阻肺证、血瘀证、肺肾两虚证、痰瘀阻络证、肺肾气虚证、外感毒邪证、瘀阻肺络证以及肺气亏虚证。而在治法治则方面以活血化瘀为主,前10 位其余治法治则依次为益气养阴、补益肺肾、化痰通络、补益肺气、养阴润肺、通经活络、活血通络、补肺健脾以及清热化痰,见图2。

图2 频次前10 位的证候分型及治法治则Fig.2 Syndromes classification and treatment methods (top 10 in frequency)
2.2 用药规律及性味归经
对纳入的118 篇中医药治疗肺纤维化方剂中的185 味中药(使用频次1 078 次)进行统计分析(表1)。使用频次前20 位的药物主要包括4 大类:补气类(黄芪、甘草、党参、白术、茯苓)、活血化瘀类(当归、丹参、川芎、地龙、桃仁、红花、赤芍、三七、莪术)、养阴类(麦冬、五味子、生地黄)以及止咳化痰类(半夏、陈皮、浙贝母、苦杏仁、桔梗)。在功效上,上述药物依次以补虚类(424 次)、活血化瘀类(179 次)、化痰止咳平喘类(155 次)、清热类(87 次)、平肝熄风类(47 次)等为主。在性味上,上述药物的四气排序依次为温(456 次)、寒(323次)、平(268 次)、凉(17 次)、热(14 次);五味排序依次为甘(619 次)、苦(530 次)、辛(308 次)、咸(80 次)、酸(54 次)。在药物归经上排序依次为肺经(624 次)、脾经(465 次)、心经(442 次)、肝经(430 次)、胃经(256 次)、肾经(228 次)、大肠经(74 次)、胆经(59 次)、膀胱经(29 次)、小肠经(17 次)、三焦经(3 次)、心包经(2 次)。
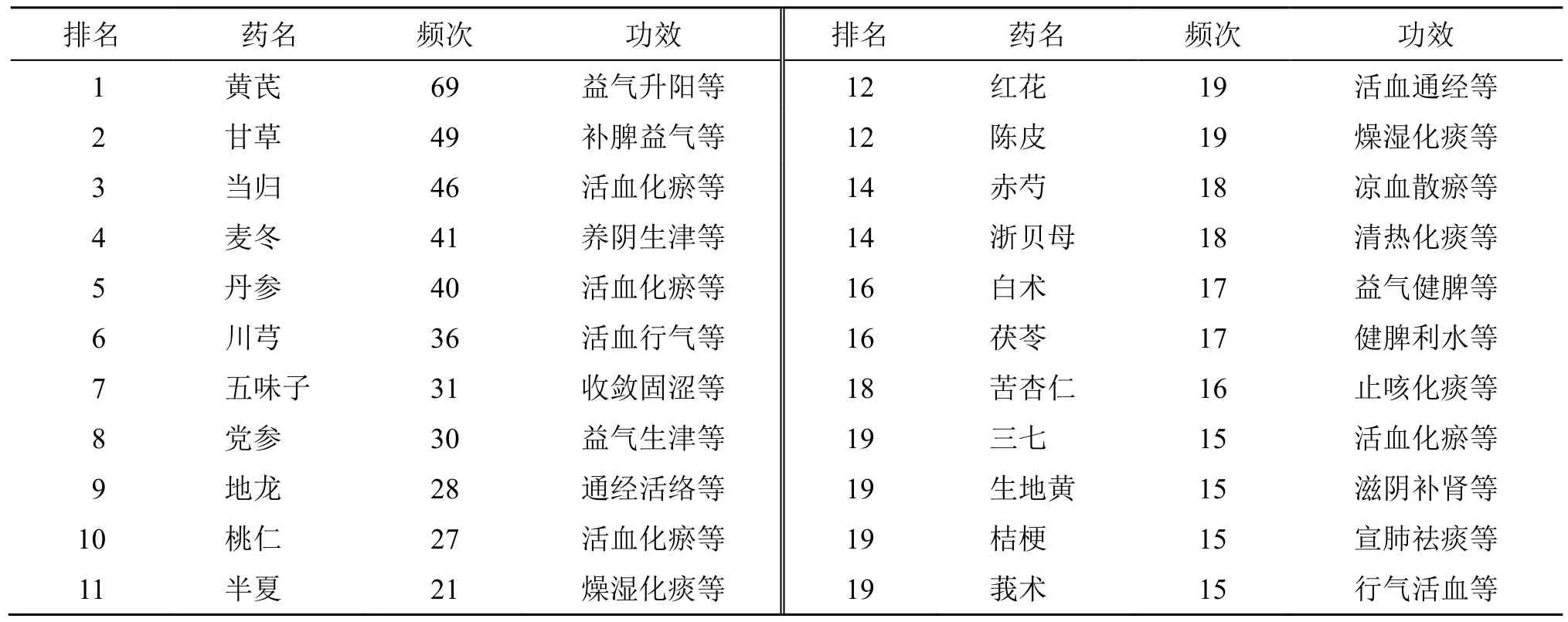
表1 中药使用频次统计 (前20 位)Table 1 Analysis of frequency of TCMs (top 20)
2.3 组方规律分析
设置支持度≥10、置信度≥0.6 为初始参数分析用药规则。支持度=支持度个数/总处方数量,置信度是方剂中A 药出现时,B 药出现的概率。支持度越高,说明方剂用药越集中;置信度越高,说明用药配伍关联性越高。在上述支持度、置信度设置条件下,筛选出频次前20 位中药组合模式,见表2。在参数设置为支持度≥10、置信度≥0.6 时,得出重要中药组合21 味:黄芪、麦冬、川芎、丹参、当归、甘草、太子参、补骨脂、莪术、赤芍、苦杏仁、陈皮、五味子、茯苓、地龙、半夏、党参、白术、红花、浙贝母、桃仁。将上述21 味中药按功效可分为补气类(黄芪、太子参、甘草、茯苓、党参、白术)、活血类(川芎、丹参、当归、红花、桃仁、地龙、莪术、赤芍)、养阴类(麦冬、五味子)、补阳类(补骨脂)、止咳化痰类(半夏、陈皮、苦杏仁、浙贝母)共5 类。将参数设置为支持度≥15、置信度≥0.6 时,得出核心中药10 味:黄芪、当归、甘草、川芎、丹参、麦冬、党参、五味子、桃仁、地龙。将参数设置为支持度≥20、置信度≥0.6 时,得出核心中药9 味:黄芪、当归、甘草、川芎、丹参、麦冬、党参、五味子、地龙。将参数设置为支持度≥20、置信度≥0.8 时,得出核心中药组合3 味:当归、川芎、黄芪,见图3。

表2 中药组合频次 (前20 位)Table 2 Frequency of TCM combinations (top 20)

表3 黄芪-当归-川芎中药有效成分Table 3 Active compounds of Astragali Radix-Angelicae Sinensis Radix-Chuanxiong Rhizoma

图3 不同支持度下中药药物组合网络Fig.3 TCM combination network with different support degrees
2.4 确定黄芪-当归-川芎为核心药物组合
通过中药使用频次分析得出,黄芪使用频次位居第1 位(69 次),当归使用频次位居第3 位(46次),川芎使用频次位居第6 位(36 次);通过不同支持度下组方规律分析得出,当归、川芎、黄芪组合的频次为25 次;通过中药组合关联规则分析得出,川芎→当归、川芎→黄芪、黄芪、川芎→当归、当归、川芎→黄芪组合的置信度均≥0.8。综上分析结果,确定“黄芪-当归-川芎”为临床上中医治疗肺纤维化核心药物组合。
2.5 黄芪-当归-川芎有效成分-疾病靶点构建
通过TCMSP、TCMID、中药证候关联数据库、CD 数据库及文献检索共收集黄芪有效成分48 种、当归有效成分37 种、川芎有效成分28 种。经过SwissADME 数据库筛选出黄芪有效成分13 种、当归有效成分15 种、川芎有效成分13 种,其中共有成分 3 种,见表 3。将以上有效成分代入SwissTargetPrediction 数据库整理后筛选出黄芪潜在治疗靶点427 个、当归潜在治疗靶点399 个、川芎潜在治疗靶点264 个,删除重复值后共获得黄芪-当归-川芎潜在治疗靶点501 个。从GeneCards数据库收集整理肺纤维化与COVID-19 共病的关键靶点2 911 个,与黄芪-当归-川芎潜在治疗靶点取交集获得共同靶点121 个。可以初步认为黄芪-当归-川芎通过121 个靶点对SARS-CoV-2 感染后遗症肺纤维化产生干预作用。将共同靶点与中药有效成分代入Cytoscape 3.72 进行可视化分析,通过Network Analyzer 分析度值、中心度值及亲中心度值,筛选出前 5 位中药有效成分为核心成分:山柰酚(kaempferol,HQ10,来源于黄芪)、槲皮素(quercetin,HQ13,来源于黄芪)、顺式阿魏酸(cisferulic acid,DG5,来源于当归)、洋川芎内酯(senkyunolide,MIX3,来源于当归、川芎)、川芎哚(perlolyrine,CX1,来源于川芎),见图4。

图4 黄芪-当归-川芎有效成分-疾病共同靶点网络分析Fig.4 Network analysis of common targets of active compounds and disease of Astragali Radix-Angelicae Sinensis Radix-Chuanxiong Rhizoma
2.6 PPI 网络分析
基于STRING 数据库对黄芪-当归-川芎干预SARS-CoV-2 感染后遗症肺纤维化的121 个共同靶点进行蛋白互作分析,设定interaction score 为hightest confidence(0.900)并将结果导入Cytoscape 3.72 软件进行进一步拓扑分析,按照度值由大到小,结合中心度值及亲中心度值综合判断筛选出前8 位靶点为AP-1 转录因子亚基(AP-1 transcription factor subunit,JUN)、核因子-κB 亚基(NF-κB subunit,RELA)、肿瘤坏死因子(tumor necrosis factor,TNF)、白细胞介素6(interleukin 6,IL6)、肿瘤蛋白p53(tumor protein p53,TP53)、丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)1、蛋白激酶B1(protein kinase B1,AKT1)、MAPK14,如图5 所示。
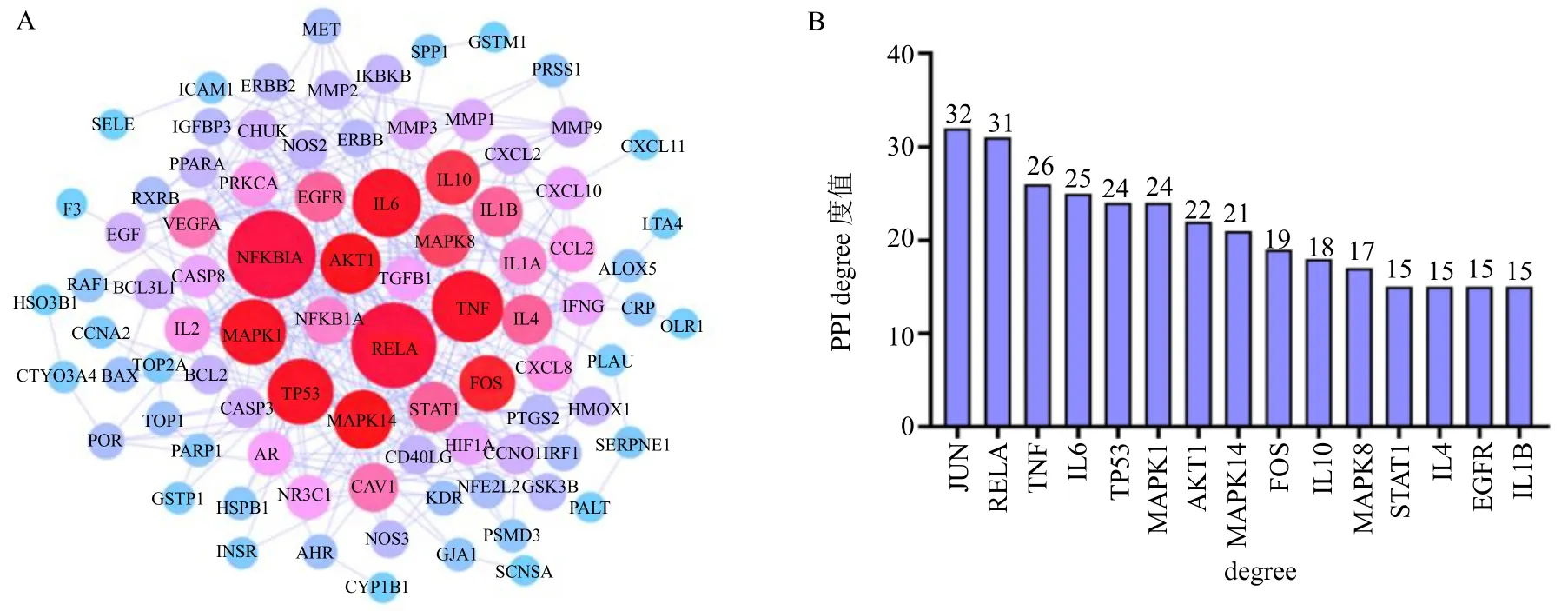
图5 PPI 网络分析结果Fig.5 Results of PPI network analysis
2.7 KEGG 通路富集分析
将上述共同靶点进行KEGG 通路富集分析,结果提示黄芪-当归-川芎对SARS-CoV-2 感染后遗症肺纤维化的干预作用主要集中在晚期糖基化终末产物-晚期糖基化终末产物受体(advanced glycation end products-receptor for advanced glycation end products,AGE-RAGE)信号通路、白细胞介素-17(interleukin-17,IL-17)信号通路、肿瘤坏死因子(tumor necrosis factor,TNF)信号通路、流体剪切力与动脉粥样硬化等信号通路上。进一步对KEGG 通路进行注释分析发现,在人类疾病方面主要涉及包括病毒感染、细菌感染在内的感染性疾病,此外包括癌症、心血管疾病、内分泌与代谢性疾病、免疫性疾病等;在环境信息处理方面涉及信号转导、信号分子与相互作用;在组织系统方面主要涉及免疫系统,此外还包括内分泌系统、循环系统等,见图6。

图6 KEGG 通路富集分析结果Fig.6 Results of KEGG pathway enrichment analysis
为进一步探索中医药治疗肺纤维化的用药特点,结合组方规律分析结果,以118 篇中医药治疗肺纤维化方剂中的185 味中药的前10%,即核心组方中(中药21 味)按照中药功效分类可分为补气类、活血类、养阴类、补阳类及止咳化痰类共5 类,进行进一步的KEGG 通路富集分析,以探明每类中药在治疗SARS-CoV-2 感染后遗症肺纤维化的共性与特点。Relevance scores 是GeneCards 数据库基于Elasticsearch 7.11 对蛋白靶点与疾病的相关性的评分,评分越高说明该靶点在该疾病中具有越重要的作用。在共性上,将5 类中药与SARS-CoV-2 感染后遗症肺纤维化的共靶点分别进行KEGG 通路富集分析,取每类中药KEGG 通路富集前20 位的共有通路进行relevance scores 评价,结果提示补气类与活血类中药在COVID-19 及肺纤维化中的相关性评分相对最高,其治疗SARS-CoV-2 感染后遗症肺纤维化的作用通路主要富集在AGE-RAGE 信号通路、IL-17 信号通路、流体剪切力与动脉粥样硬化通路、癌症相关信号通路与TNF 等信号通路上,见表4、5。在特点上,将5 类中药各自的独有靶点与SARS-CoV-2 感染后遗症肺纤维化的共靶点进行分析,发现补气类的独有靶点5 个:OLR1、MAPK10、HSD3B1、ATP5F1B 与FASLG;活血类的独有靶点19 个:TGM2、TNFRSF1A、TNFRSF1B、ABCC4、EDN1、ALB、EDNRA、SELP、TLR2、NPM1、MMP10、G6PD、CD14、KCNK2、NFKB1、ECE1、ITGB3、TRPV1 与CTNNB1;补阳类的独有靶点3个:CD80、CD40 与CD86;养阴类的独有靶点24个:GPI(CM000681.2)、LDHA、OAT、ASNS、CPT2、GPI(KI270866.1)、SHMT2、SLC25A13、ARG1、GLUD1、GPT、F13A1、PFAS、TPI1、SDHA、LDHB、GOT2、MMP12、PDHB、LTF、MTR、PC、LDHA与KYNU;止咳化痰类的独有靶点4 个:CYCS、EPHB2、CD163 与CREB1。将上述独有靶点分别进行KEGG 通路富集分析,结果发现补气类独有靶点主要富集在神经营养因子信号通路、麻疹、乙型肝炎等信号通路上;活血类独有靶点主要富集在流体剪切力与动脉粥样硬化通路、沙门氏菌感染、TNF等信号通路上;补阳类独有靶点主要富集在Toll 样受体信号通路、产生IgA 的肠道免疫网络、病毒性心肌炎等信号通路上;养阴类独有靶点主要富集在碳代谢、氨基酸合成、精氨酸生物合成等信号通路上;止咳化痰类独有靶点主要富集在肺结核、卡波西肉瘤相关疱疹病毒感染、人巨细胞病毒感染等信号通路上,见表6。

表4 5 类中药在COVID-19 中的相关性评分Table 4 Relevance scores of five kinds of TCMs in COVID-19
2.8 中药核心成分与关键靶点分子对接
根据“2.5“项所筛选出的中药核心成分山柰酚(kaempferol)、槲皮素(quercetin)、顺式阿魏酸(cisferulic acid)、洋川芎内酯(senkyunolide)、川芎哚(perlolyrine)及“2.6”项筛选出的关键靶点JUN(PBD ID: 5FV8)、RELA(PBD ID: 3QXY)、TNF(PBD ID:5UUI)、IL6(PBD ID: 1ALU)、TP53(PBD ID: 3ZME)、MAPK1(PBD ID: 5BVE)、AKT1(PBD ID: 1UNQ)、MAPK14(PBD ID: 5XYY)进行分子对接分析。结果表明,中药核心成分与关键靶点的总体结合能良好,一定程度上体现了黄芪-当归-川芎多成分、多靶点干预SARS-CoV-2 感染后遗症肺纤维化的潜在机制,见图7-A。其中结合能最低的成分-靶点分别为槲皮素-AKT1 与槲皮素-MAPK1,结合能均为−9.7kcal/mol;随后为槲皮素-MAPK14 与槲皮素-JUN,结合能均为−9.4 kcal/mol;之后为山柰酚-MAPK1 与山柰酚-MAPK14,结合能均为−9.2 kcal/mol;最后为山柰酚-AKT1 与山柰酚-JUN,结合能均为−9.0 kcal/mol,见图7-B~I。槲皮素和山柰酚与多数核心靶点结合能总体最佳,川芎哚与多数核心靶点结合能总体较好,提示黄芪-当归-川芎药物组合中槲皮素、山柰酚与川芎哚是其多靶点干预SARS-CoV-2 感染后遗症肺纤维化的最关键核心成分。
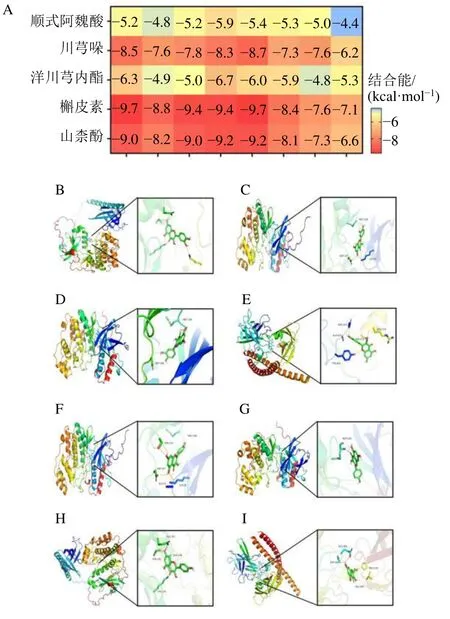
图7 分子对接分析结果Fig.7 Analysis results of molecular docking
3 讨论
肺纤维化是现代病理学名称,是以IPF 为代表的多种肺间质性疾病的病理表现,与中医经典著作中疾病的命名无直接对应。目前学界认为肺纤维化的致病因素以痰、毒、瘀、虚为重,病机以本虚标实为多,病位涉及肺、脾、肾为主,在病名上多从“肺痹”“肺萎”论治[1,18-19]。目前临床上各家针对肺纤维化具体的辨证治法尚无定论,故本研究对2000年1 月—2023 年6 月具有明确疗效的中医药治疗肺纤维化的118 篇临床研究文献进行整理归纳以探求其特点与共性。上述临床研究在辨证方面多从气虚血瘀证、气阴两虚证、痰瘀阻肺证、血瘀证而论,在治法上多从活血化瘀、益气养阴、补益肺肾而治。其中涉及的185 味中药中,使用频次前20 味的高频中药中补气类中药占据5 味,且黄芪、甘草的使用频次最高,此外活血化瘀类中药占据9 味,主要以当归、川芎、丹参为主,余以养阴、止咳化痰之药,这与目前学界对肺纤维化“本虚标实”的认识相符。在组方规律分析方面,设置支持度≥10、置信度≥0.6 为参数分析用药规则后,随着支持度提高,补气类与活血化瘀类中药在频次上所占比重逐渐提升,而当支持度≥20、置信度≥0.8 时仅剩“黄芪-当归-川芎”组合。该结果表明临床上补气类与活血化瘀类中药广泛用于肺纤维化的治疗,且具有益气活血特点的“黄芪-当归-川芎”是最核心、最常用的药物组合。正如《读医随笔》中“气虚不足以推血,则血必有瘀”与《医林改错》中的“元气既虚,必不能达于血管,血管无气,必停留而为瘀。”强调了气对血的推动作用,气虚推动无力而导致血瘀,无气则必瘀。中医经典中“黄芪-当归-川芎”的配伍广泛出现,如《济阴纲目》中黄芪四物汤、《医林改错》中补阳还五汤、《外科正宗》中调和营卫汤等治疗各类瘀血内阻而正气已虚之疾病,因此对于肺纤维化治疗当注重补气与活血并用而促进瘀血的消散。
目前国内SARS-CoV-2 感染流行的奥密克戎变异株主要引起无症状感染和轻症感染,但对于免疫力低下人群、老年人群患者仍有较大患重症的风险而危及生命[20-21]。SARS-CoV-2 感染患者与凝血功能异常关系密切,在住院的患者中静脉栓塞和肺动脉栓塞的发生率分别为17%和7.1%[22],并且在重症患者中静脉栓塞的发生率更高(28%)[23]。研究表明,肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)和IL-6 等炎症因子是SARS-CoV-2 感染患者血栓形成的重要因素[24-25],而早期使用抗凝疗法与更好的预后相关[26]。此外SARS-CoV-2 感染可导致多种严重的后遗症,尤其是肺纤维化的发生。1 项英国的研究分析发现超过11%的患者在出院240 d 内的肺CT 显示出纤维化样改变[27]。另1 项对出院2 年后患者的队列研究发现39.7%的患者有不同程度的纤维化样改变[28]。对重症SARS-CoV-2 感染患者康复半年后的CT 中发现超过三分之一的患者发生肺纤维化[29],并且在30 例因SARS-CoV-2 感染去世患者的尸检中发现有43%发生严重的肺纤维化[30]。近期1 项研究发现老年SARS-CoV-2 感染患者发生包括肺纤维化在内的严重后遗症的比例更高,其发生机制与其较弱的免疫应答相关,而适度的免疫激活有助于对SARS-CoV-2 的清除[31]。上述结果表明SARS-CoV-2 感染后遗症肺纤维化在重症及老年患者中发生比例更高,因此尽早使用抗凝疗法,适当提升机体免疫力与减少重症发生率,降低SARS-CoV-2 感染后遗症肺纤维化的发生及更好的预后相关,这与中医学界对肺纤维化用药选择及治法不谋而合。
通过对“黄芪-当归-川芎”核心药物组合进行网络药理学分析发现槲皮素、山柰酚、川芎哚、洋川芎内酯与顺式阿魏酸是其核心药物成分,AKT1、MAPK14、MAPK1、JUN 等是其主要干预靶点。AKT1 是一种丝/苏氨酸激酶,主要通过磷脂酰肌醇-3-羟激酶(phosphatidylinositol-3-hydroxykinase,PI3K)/AKT 信号通路介导炎症反应、血管生成及细胞增殖凋亡等,研究发现SARS-CoV-2 感染患者肺脏中更高的AKT1 表达与更严重的肺损伤及肺纤维化相关[32],并且AKT1 是连花清瘟胶囊及清肺排毒汤干预SARS-CoV-2 感染的重要靶点之一[33-34]。JUN、MAPK1 及MAPK14 均属于MAPK 信号通路,该通路的激活与SARS-CoV-2 感染及肺纤维化关系密切。SARS-CoV-2 的感染能促进MAPK14 的磷酸化[35],并且SARS-CoV-2 感染患者外周血中表现出更高水平的MAPK1 与JUN[36]。PI3K/AKT 信号通路及MAPK 信号通路的激活对肺纤维化具有显著的促进作用,在博来霉素造模的肺纤维化大鼠模型中 AKT1 的表达显著上升[37],p38 MAPK(MAPK14)可激活转录因子JUN,促进巨噬细胞及中性粒细胞的聚集从而促进肺纤维化的发展[38]。此外,分子对接结果提示槲皮素、山柰酚与川芎哚可能是“黄芪-当归-川芎”核心药物组合多靶点干预SARS-CoV-2 感染后遗症肺纤维化的最关键核心成分,顺式阿魏酸与洋川芎内酯同样具有一定的药用潜力。槲皮素广泛存在于黄芪、三七、连翘等多种中药中,具有广泛的抗炎、抗病毒及抗氧化功效[39]。目前已有多项生物信息学研究提示槲皮素对SARSCoV-2 具有潜在的抑制作用,但仍未见详细的机制研究[33,40-41]。在临床研究中,槲皮素联合抗病毒药物有效地降低了患者血清中碱性磷酸酶、乳酸脱氢酶及C 反应蛋白水平,减少患者住院时间[42]。相似的是,近期的一项荟萃分析发现槲皮素能有效降低患者的住院率以及重症率[43]。在抗肺纤维化的相关研究中,槲皮素的作用机制研究较为成熟,在动物模型中能有效减少肺脏TNF-α、IL-6 等炎症因子的表达及羟脯氨酸含量,减少胶原纤维面积,其机制与抑制转化生长因子β1(transforming growth factor beta 1,TGF-β1)/p38 MAPK/核因子-κB(nuclear factor-κB,NF-κB)信号通路,减少氧化应激反应,抑制烟酰胺腺嘌呤二核苷酸磷酸氧化酶 4(nicotinamide adenine dinucleotide phosphate oxidase 4,NOX4)-p62 信号途径等有关[44-46]。但目前未见槲皮素抗肺纤维化的相关临床研究,因此进一步探究槲皮素抗SARS-CoV-2 感染的机制与特点,以及开展抗肺纤维化的临床研究是其未来的重要研究方向。山柰酚同样存在于包括黄芪在内的多种中药中,药理学研究表明其具有抗炎、抗氧化、抗抑郁等功效,对癌症及心脑血管疾病具有一定治疗作用[47]。目前未见山柰酚干预SARS-CoV-2 的临床及机制研究,而其抗纤维化的机制主要与恢复E-钙黏蛋白水平,抑制上皮细胞间充化(epithelial-mesenchymal transition,EMT)的发生等有关[48],因此仍需进一步基础与临床研究以阐明其作用机制。川芎哚主要存在于川芎、当归之中,目前除早期文献报道其抗血小板、抗血栓、改善血流动力学的作用外,近期尚无相关抗炎、抗凝作用的研究报道,这可能与其代谢快、药效维持时间较短有关[49-50]。结合分子对接分析结果,如何解决川芎哚代谢快、药效维持时间较短的弊端,以及探索川芎哚在抗炎、抗纤维化的潜能可能是其未来重点研究方向。洋川芎内酯是当归、川芎的主要活性成分之一,能通过抑制NOD样受体热蛋白结构域相关蛋白3(NOD-like receptor thermal protein domain associated protein 3,NLRP3)、氨基末端激酶(jun kinase,JNK)、细胞外信号调节激酶(extracellular signal-regulated kinase,ERK)信号通路发挥抑制炎症的作用[51-52]。虽然目前未见其干预SARS-CoV-2 及抗肺纤维化的研究,但分子对接的结果提示具有良好的研究前景。阿魏酸广泛存在于当归、阿魏、升麻等中药中,具有良好的抗炎、抗凝作用。在体内,阿魏酸能降低小鼠炎症模型中IL-1β、IL-6 的表达水平,抑制大鼠凝血酶的活性、延长出血时间、抑制动静脉血流旁路血栓的形成[53-54];在体外,阿魏酸可降低SARS-CoV-2的病毒滴度发挥抗病毒的功效[55]。总体而言,“黄芪-当归-川芎”核心药物组合中核心药物成分均具有一定干预SARS-CoV-2 及抗肺纤维化的功效,但缺乏深入的机制研究及临床研究结果加以验证。
KEGG 通路富集分析是一种从复杂调控网络角度对生物的基因集合进行通路富集归纳的分析手段,是研究生物功能的重要方法之一[56]。“黄芪-当归-川芎”核心药物组合干预SARS-CoV-2 感染后遗症肺纤维化的共同靶点主要富集在IL-17 信号通路、TNF 信号通路、AGE-RAGE 信号通路、流体剪切力、动脉粥样硬化通路等与感染性疾病、免疫系统关联性较强的信号通路,一定程度说明了抗感染、抗凝血与免疫调节是其最重要的机制。结合组方规律分析结果,发现21 味中药组合中补气药与活血药在基于 KEGG 通路富集分析的肺纤维化与COVID-19 相关性评分远超补阳类、养阴类与止咳化痰类中药,进一步说明了补气药与活血药的联用是学界最常用的药物选择。同时在5 类中药独有靶点的KEGG 通路富集分析上,补气类中药主要富集在神经营养因子信号通路,养阴类中药则富集在氨基酸合成与精氨酸生物合成等信号通路上,从一定程度体现了这2 类中药“补虚”的特点;活血类中药主要富集在流体剪切力与动脉粥样硬化这一与中医理论中“血瘀”概念极其相关的通路,彰显了其活血化瘀的功效;止咳化痰类中药主要富集在肺结核通路等与呼吸系统密切相关的信号通路上;而补阳类中药主要富集在与免疫激活密切相关的Toll 样受体信号通路,体现了阳气温煦推动、抵御外邪之特色。上述研究结果为中医药干预SARS-CoV-2 感染后遗症肺纤维化提供了信号通路的参考,尤其针对不同中药功效上的特点,为后续相关药物研究提供部分证据支持。
本研究受限于研究方法仍存在许多不足。首先,中医药治疗肺纤维化学界尚无治法方药的标准与定论,因此纳入文献在方药种类选择上较分散,需在组方规律分析初步筛选中纳入更多药味进行全面的分析,但限于网络药理学的分析手段,如无法区分如生甘草与炙甘草、生地黄与熟地黄,本研究仅能通过纳入前10%中药作为初步筛选条件,最大化避免上述的限制,导致在进行KEGG 通路富集分析的相关性评分时所能纳入的补阳类与养阴类中药种类较少。其次,由于所纳入的临床文献存在包括汤剂、颗粒剂、注射液等多种剂型,且部分文献未公布中药用量,无法对中药进行全面的剂量区间统计。最后,受限于分子对接技术特点,目前仅能确定中药成分对核心靶点的结合能高低,无法确定对结合靶点的抑制或激活,未来需结合转录组学及实验验证进一步阐释。
4 结论
综上所述,本研究基于中医传承辅助平台与网络药理学,发现中医药治疗肺纤维化临床研究中辨证以气虚血瘀证、气阴两虚证、血瘀证居多,治法以活血化瘀法为重,用药以补气药和活血化瘀药为主,在组方规律上“黄芪-当归-川芎”是核心药物组合,其核心成分包括槲皮素、山柰酚、川芎哚等,核心靶点包括AKT1、MAPK14、MAPK1、JUN 等,通过AGE-RAGE 信号通路、IL-17 信号通路、TNF 信号通路、流体剪切力与动脉粥样硬化等信号通路发挥干预SARS-CoV-2 感染后遗症肺纤维化的作用。
利益冲突所有作者均声明不存在利益冲突

