我国类改良型中药新药再评价研究现状
钟林江 卢文婷 蒋庆佳 李思成 唐焓嫣 罗琴琴 邓昊旻 潘迎志

摘 要:目前已上市的类改良型中药新药存在制备工艺不同、剂型有异、质量标准不一与用法用量有别等问题,结合中成药再评价研究思路,对我国已上市类改良型中药新药的现存问题、用药困惑和再评价研究进行了探讨,以期为类改良型中药新药的研究提供参考.
关键词:类改良型中药新药;低水平重复;再评价研究;研究现状
中图分类号:R288
文献标志码:A
0 引 言
改良型中药新药首次出现在国家市场监督管理总局2020年1月22日发布的《药品注册管理办法》(以下简称《办法》)中,系指改变已上市销售中药、天然药物给药途径、剂型,且具有临床应用优势和特点,或增加功能主治等的制剂.包括不同给药途径或吸收部位之间相互改变的制剂;改变已上市销售中药、天然药物剂型的制剂,即在给药途径不变的情况下改变剂型的制剂;中药增加功能主治,或天然药物增加适应症的制剂;已上市中药生产工艺或辅料等改变引起药用物质基础或药物吸收利用明显改变的制剂等.由于这些制剂在此前的各版新药注册法规中已被批准上市,不能按2020年版《办法》中的改良型中药新药进行归类管理,故称其为类改良型中药新药[1].类改良型中药新药的个别品种批准文号及生产厂家较多,从而存在低水平重复等问题,且目前缺少针对已上市类改良型中药新药的相关管理和技术法规等相关文件,导致其质量参差不齐.本文旨在系统讨论类改良型中药新药的再评价研究手段,分析目前类改良型中药新药存在的问题,以期为类改良型中药新药的研究提供参考.
1 类改良型中药新药概况
1.1 类改良型中药新药分类历史沿革
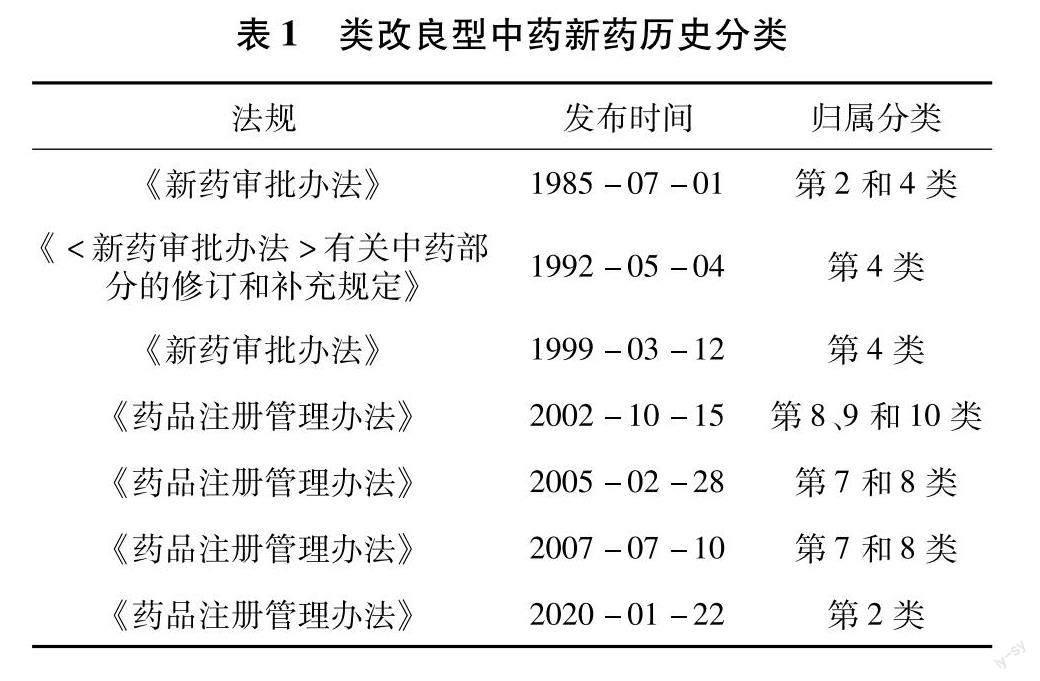
类改良型中药新药在此前的各版新药注册法规中,存在类似分类,且这类制剂随着《办法》的变更,所归属的药品分类不一致,具体见表1.
在2002年版《办法》至2007年版《办法》中,类改良型新药是指改变国内已上市销售药品剂型的制剂,《办法》中规定只要符合国家标准即可减免相关研究,大大降低了上市难度,直接导致了业内严重的低水平重复现象[2].尤其是 2005年版《办法》规定中药改剂型而生产工艺无质的改变可以减免临床研究,类改良型中药新药的质量标准只要符合国家法定标准即可减免相关研究,且当时的中药标准对产品的质量可控性有限,结果导致大量中药改剂型和仿制品种重复申报,如六味地黄系列制剂涉及胶囊、软胶囊和大蜜丸等10个(亚)剂型,全国有797 个批准文号.
1.2 准入条件不稳定,批准的药品不能满足临床需求
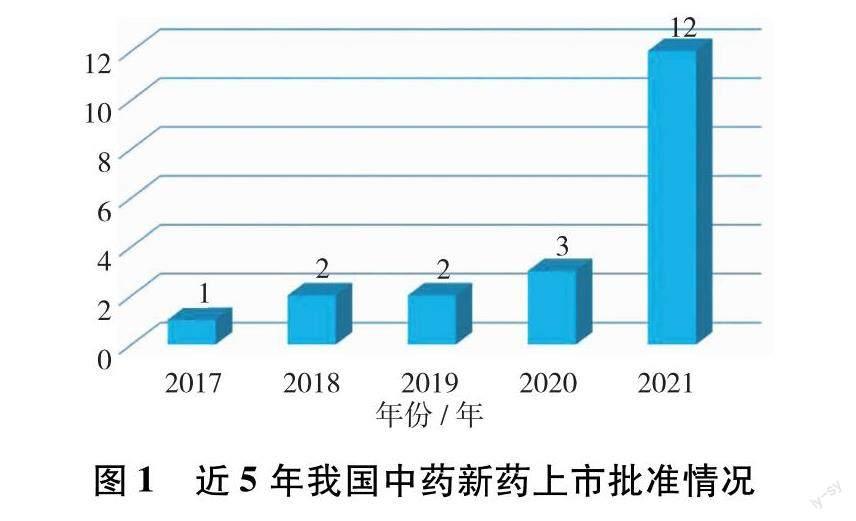
根据2005年版《办法》中的注册制度,大量中药改剂型和仿制品种重复申报,再加上当时的独家品种和剂型可以单独定价,使得当时为增加药品规格的各种补充申请事项大幅增加,造成了大量低水平重复药品上市,缺少高质量的类改良型中药新药[3].2007年版《办法》参照化学药品仿制药的定义提出了中药仿制药的概念,要求已上市类改良型中药新药药效物质基础应与对照药保持一致,有效遏制了中药的低水平重复申请,但也导致了类改良型中药新药的上市较为困难.随着2020年版《办法》的提出,中药的注册分类总体上由 9 类简化为 4 类,即中药创新药、中药改良型新药、古代经典名方中药复方制剂与同方同名药.中药新药的注册上市申请出现了上升趋势,2021年批准上市了12个中药新药,但没有改良型中药,详见图1及表2.
1.3 剂型有异,容易引起临床用药困惑
复方丹参系列制剂(丸、片、胶囊、颗粒和滴丸)在2020年版《中华人民共和国药典》(以下简称《中国药典》)[4]中的功能主治为活血化瘀、理气止痛.用于气滞血瘀所致的胸痹,症见胸闷、心前区刺痛;冠心病心绞痛见上述证候者.但在临床用药中,复方丹参滴丸常作为冠心病急救用药,治疗心绞痛;而复方丹参片只能作为冠心病常规用药[5].康艳生等[6]对复方丹参系列制剂的临床疗效观察比较发现,复方丹参滴丸治疗冠心病心绞痛相较于复方丹参片(颗粒和胶囊)具有更好的疗效,且能够更有效地改善患者症状、炎症情况及机体氧化应激损伤.
2 类改良型中药新药再评价研究现状
目前,我国批准的中成药批准文号数量达 56 914个,在这众多的批准文号中不乏同一个药品处方的不同剂型与同一种药品多个厂家的品种,易导致药品的质量参差不齐.《中国药典》等标准中药品存在重复、同名同方而生产工艺和质量控制方法不同,以及同名异方等混乱现象;同时,由于中药前期审批标准低,导致中药新药在上市前缺乏改变剂型和给药途径的血清药物化学和药动学实验,以及具有中医药特点的Ⅰ期临床试验,质量可控性差;且现行《办法》中,第 2.4 类改变已上市中药生产工艺或辅料的情况,容易与药品上市后变更注册中的生产工艺或辅料产生混淆,增加了药品上市难度.目前,我国逐渐将工作重点从药品的上市前审批转移到上市后的评价.刘涛等[7]提出了基于中成药工艺与质量控制的再评价模式,通过药品质量再评价,不但避免了药品生产的低水平重复,还能促使药品生产企业对药品生产工艺和设备进行技术改造,推动药品质量的提高.本文从我国中成药再评价现状出发,对我国类改良型中药新药的再评价方法进行了论述,主要包括处方、工艺、质量标准、作用机制及临床再评价方面.
2.1 处方再评价
目前,已上市类改良型中药新药品种存在药味混乱、用量不一等问题,因此有必要对其处方进行再评价研究,明确中成药的基本处方.研究发现[4],小柴胡泡腾片中姜半夏在处方中的比例与小柴胡片、胶囊及颗粒不一致;桂枝茯苓丸用赤芍,桂枝茯苓片及胶囊用白芍,不同剂型之间所用药材种类不同;蛇胆陈皮片用陳皮,蛇胆陈皮胶囊与散剂用陈皮(蒸),处方药材的制法也有区别.针对以上问题,急需开展对已上市改良型中药新药的处方再评价研究工作,对于处方再评价,应包括处方组成、用量、药材基原、药用部位、饮片炮制规格及炮制方法等.多基原的药材应固定基原,固定药材产地,明确详细炮制工艺路线和关键工艺参数.药材/饮片应符合国家药品标准和药品注册标准,以及省、自治区与直辖市药材标准和/或炮制规范等,若不能满足质量控制需要的,应研究完善其质量标准.所用提取物应符合相应制剂要求和国家相关规定,明确已上市改良型中药新药的处方,以保证产品质量.
2.2 工艺再评价
工艺研究是中药新药研究的重要内容之一,并与整个中药新药研发过程息息相关,包括原辅料、质量标准、有效性和安全性等方面.中成药的工艺路线是中药生产工艺科学性、合理性和可行性的基础和核心.已上市的类改良型中药新药中,因原辅料、提取工艺、浓缩干燥工艺、制剂成型工艺、辅料及包材的不同,以及溶媒种类、受热时间和温度等条件的不同,容易引起物质基础的改变,进而导致制剂之间的质量差异,而其标识的功能主治却完全一致,故须对已上市的类改良型中药新药开展工艺再评价研究,明确相应工艺.已有学者发现,相同制剂的不同剂型之间因为工艺问题会引起产品质量间的差异.例如,朱红梅等[8]以化学成分转移率为指标,采用对比试验对双黄连口服液、颗粒、片剂及栓剂的各个工序进行了研究,结果表明,制备工艺对指标成分转移率有显著影响,为了成型的需要,一些工艺过程中化学成分损失严重,工艺不同导致不同剂型中所含物质基础不同;根据物质的药效作用,双黄连制剂在临床应用时针对抗菌、抗炎及解热作用应采用不同的剂型,以达到更好的临床疗效.刘德军等[9]采用高效液相色谱法(HPLC)对银翘解毒系列制剂的制备过程中各环节金银花中绿原酸的转移率及相对于上一步的保留率进行了研究,结果发现,各工艺流程对绿原酸转移率有较大影响.刘涛等[10]以延胡索乙素与欧前胡素含量的转移率为指标,采用综合评分法,对元胡止痛软胶囊、口服液、片剂及胶囊不同剂型的提取、浓缩、精制及成型工艺进行评价研究,结果表明,在不同剂型的工序中,各个剂型工艺过程各成分转移率各不相同,如元胡口服液在成型过程中,其所含的欧前胡素损失率达99%,表明元胡止痛系列制劑其内在质量及疗效可能存在差异.
2.3 质量标准再评价
中成药现行质量标准中,多是对指标成分的定性鉴别或定量测定.选取1种或2种成分进行含量测定可能代表某个药理作用指标,但不能表征其复杂成分群的整体效果,且中成药功能主治多样,不能仅以含量高低说明某个方面药效的差别.2020年版《中国药典》[4]中,对于改良型中药新药,缺少能表征其成分群或药效的相关标准,且同种制剂的不同剂型间质量控制方式也存在不同.例如,薄层色谱鉴别中,八珍丸的薄层鉴别项为甘草和白芍,八珍颗粒的薄层鉴别项则为党参、当归、川芎和白术,所鉴别药材存在差异;四君子丸的薄层鉴别项为甘草中的甘草酸,而四君子颗粒的薄层鉴别项为甘草中的甘草苷和甘草酸,鉴别同种药材中不同成分.含量测定项中,生脉饮的含量测定项为五味子甲醇,生脉胶囊的含量测定项为人参皂苷Rg1.
已上市的类改良型中药新药中大部分药品存在此类问题,现有的一系列评价手段可有效地对已上市类改良型中药新药进行再评价,主要包括指纹图谱(特征图谱)、药效作用值、活血(抑菌)体外活性测定、谱—效关系、光谱法和一测多评等方法.罗廷顺等[11]对藿香正气系列制剂的指纹图谱研究发现,9个批次藿香正气系列制剂的相似度均大于0.90,表明不同剂型或同剂型不同批号样品中共有峰所对应的药材生产工艺有一定的差异.刘钱等[12]以药效作用值为指标,对双黄连口服液、片剂及颗粒药效进行研究,结果发现,双黄连片剂抗炎、解热及抗菌作用最强,体内外药效研究也表明双黄连片剂在抗炎、解热及抗菌作用方面较其他2种剂型显著.伍利华等[13]通过建立金莲花口服液、片剂、颗粒及胶囊与抑菌活性的谱—效关系,对金莲花系列制剂4种剂型进行再评价,结果表明,金莲花4种制剂指纹图谱相似度良好,金莲花口服液抑菌生药量最小,金莲花口服液剂型质量较优.胡一冰等[14]采用紫外、红外及近红外光谱评价方法,对六味地黄系列制剂进行质量再评价研究,结果显示,六味地黄系列制剂的光谱图存在一定差异,其整体光谱相似度在0.309~0.985之间,P值在0.000~0.143之间,表明六味地黄系列制剂物质基础存在一定差异,且药效物质基础可能不同.吕佳佳等[15]采用一测多评法同时测定牛黄上清系列制剂中 7 种成分的含量,结果发现,牛黄上清系列制剂中7种成分含量的计算值与实测值无显著差异,一测多评法可较好地控制牛黄上清系列制剂的质量.
2.4 作用机制再评价
中药成分复杂,其药效是通过多成分与多靶点共同作用的结果.已上市类改良型中药新药制备工艺的差别,势必会导致成分的差异,对潜在靶点的作用可能也会有所不同.采用现代研究方法,对各种剂型之间作用机制进行再评价,是一种有效的再评价研究方式.罗虹等[16]采用网络药理学技术筛选出六味地黄系列制剂治疗2型糖尿病、高血压和肾病综合征的共有32个核心活性成分,并测定了其中含量较高的13种活性成分,对6种相同处方的不同剂型进行含量测定,结果表明,六味地黄系列制剂存在一定的内在质量差异,在一定程度上揭示了六味地黄系列制剂药效可能不完全一样.
2.5 临床再评价
中药上市后临床再评价指的是根据医药学的最新学术水平,从药理学、药剂学、临床医学、药物流行病学、药物经济学及药物政策等方面,对已经批准上市的药品在社会人群中的疗效、不良反应、用药方案、稳定性及费用等是否符合安全、有效和经济的合理用药原则做出科学评价[17].目前,大部分改剂型或改给药途径的已上市类改良型中药新药未进行临床实验,或临床实验受研究病例数较少、缺乏严格的对照设计、受试人群范围窄、用药条件控制较严,以及缺乏分级量化指标等诸多因素的限制,使得其上市前的有效性和安全性评价不充分.因此,需开展对已上市的类改良型中药新药的临床再评价研究[18-19].
从安全性、有效性及经济性方面可较好地对已上市中成药开展临床再评价研究.安全性再评价应包括不良反应报告、监测、评估和获益评估,有效性再评价应包括适应证、临床用药剂量和疗程、联合用药、合并用药和特殊人群用药,经济再评价应在保证安全性和有效性的前提下,开展最小成本分析、成本效果分析、成本效益分析和成本效用分析再评价模式[17].张怡颖等[20]通过整理中国知网数据库中关于连花清瘟制剂上市后临床再评价的相关文献,对连花清瘟(片剂、胶囊和颗粒)的有效性、安全性和经济性文献进行分析,结果发现,连花清瘟制剂存在发生不良反应的可能性,联合用药表明,连花清瘟胶囊具有相似的经济性与更好的治疗效果.
3 结 语
2020年版《办法》明确将中药范围重新界定为中药创新药、中药改良型新药、古代经典名方中药复方制剂及同名同方药等.其中,中药改良型新药是首次出现的分类,是鼓励中药二次开发基本导向的充分体现,也为中药大品种培育提供了新的发展方向[21].改良型中药新药是体现临床应用的一大优势分类,新版《办法》赋予了其新药的属性,为保证其安全、有效和稳定,在吸取既往改剂型和改给药途径品种的经验教训上,应参照中药创新药的相关要求进行临床试验,同时改良型中药新药的研发,应依据临床需求进行,这样既能保护原研企业的知识产权,又能提高企业的创新积极性[22].目前,已上市的类改良型中药新药依然存在着制备工艺不同、剂型有异、质量标准及用法用量有别,以及部分品种临床数据缺失等问题,可能导致药效物质基础的改变,因此,对其药效不能一概而论.
本文依据中成药再评价研究思路,对已上市类改良型中药新药的再评价研究进行了初步探讨,认为再评价研究应包括处方、工艺、质量、作用机制及临床使用等方面,其评价的核心是保障药品质量,在研究过程中,应考虑现有再评价手段对于评价品种适用性问题,如优化工艺和提高质量标准的同时大幅增加了检测成本.因此,对于类改良型中药新药的再评价应从多个方面综合考虑,通过对已上市类改良型中药新药的再评价研究,可提高药品质量,解决低水平重复等问题.
参考文献:
[1]王琦,曾志坚,林伟斌.藿香正气系列制剂组方、制法及剂型分析[J].中国药业,2010,19(20):76-77.
[2]瞿礼萍,唐健元,张磊,等.我国中药注册分类的历史演变、现状与问题[J].中国中药杂志,2022,47(2):562-568.
[3]唐健元.关于中药注册分类的思考和建议[J].中国中药杂志,2020,45(16):4004-4008.
[4]国家药典委员会.中华人民共和国药典[S].北京:中国医药科技出版社,2020.
[5]张翠莲,王彪,刘芳,等.5种复方丹参口服制剂质量标准对比分析与启示[J].中国药事,2021,35(4):390-396.
[6]康艳生,刘静静,张伟,等.复方丹参颗粒、复方丹参胶囊、复方丹参片与复方丹参滴丸对冠心病心绞痛患者疗效、炎性因子及氧化应激指标的影响[J].药物评价研究,2020,43(2):287-292.
[7]刘涛,苟小军,郭晓恒,等.基于中成药工艺与质量控制的再评价模式商建[J].中草药,2011,42(10):1873-1877.
[8]朱红梅,刘涛,李鹏程,等.双黄连系列制剂制备工艺再评价[J].中成药,2017,39(5):1087-1090.
[9]刘德军,张源源,张爱丽,等.银翘解毒软胶囊制备过程中绿原酸转移率[J].中国实验方剂学杂志,2011,17(21):23-26.
[10]刘涛,冯晶晶,李鹏程,等.元胡止痛系列制剂4种工艺比较[J].中成药,2017,39(4):851-854.
[11]罗廷顺,石桂兰,耿玲.藿香正气系列制剂指纹图谱研究[J].中国现代应用药学,2020,37(14):1714-1718.
[12]刘钱,张文文,姚运秀,等.基于药效作用值的双黄连系列制剂再评价研究[J].中草药,2019,50(4):903-909.
[13]伍利华,钟林江,杨俊莉,等.基于体外抑菌作用的金莲花系列制剂谱—效关系研究[J].中国测试,2019,45(11):51-56.
[14]胡一冰,羅虹,潘春晖,等.基于光谱法的六味地黄系列制剂质量再评价研究[J].成都大学学报(自然科学版),2020,39(4):368-373.
[15]吕佳佳,王莎,周昌艳,等.一测多评法测定牛黄上清系列制剂中7种成分的含量[J].遵义医学院学报,2018,41(2):219-224.
[16]罗虹,刘博文,杨慧,等.基于网络药理学及活性成分测定的六味地黄系列制剂质量研究[J].中草药,2020,51(21):5462-5477.
[17]谢雁鸣,王燕平,王永炎,等.中药上市后临床再评价及Ⅳ期临床试验的基本要求[J].中国中药杂志,2011,36(20):2764-2767.
[18]陈玉欢,凌霄,李春晓,等.中药上市后临床再评价研究思路探讨[J].中国新药杂志,2021,30(24):2262-2267.
[19]何伟,谢雁鸣,王永炎.中药上市后临床再评价研究若干问题思考[J].中国中药杂志,2010,35(12):1641-1643.
[20]张怡颖,崔唐明,许吉.连花清瘟制剂上市后临床再评价文献分析[J].中成药,2022,44(2):549-554.
[21]杨洪军.改良型新药:中药大品种培育新方向[J].中国药理学与毒理学杂志,2021,35(10):726.
[22]孙昱,孙国祥,李焕德.FDA 505(b)(2)改良型新药的申报情况对中药改良型新药的启发思考[J].中南药学,2021,19(3):369-375.
(责任编辑:伍利华)
Research Status of Class-Modified Traditional Chinese Medicine New Drugs and Their Revaluation in China
ZHONG Linjiang1,LU Wengtin 2,JIANG Qingjia3,LI Sicheng3,
TANG Hanyan3,LUO Qinqin1,DENG Haomin1,PAN Yingzhi1
(1.Chengdu Dikang Pharmaceutical Co.,Ltd.,Chengdu 610000,China;2.College of Pharmacy,Guangxi University of Traditional Chinese Medicine,Nanning 530200,China;3.College of Pharmacy,Chengdu University,Chengdu 610106,China)
Abstract:At present,there are some problems in the listed class-modified traditional Chinese medicine new drugs,such as different preparation processes,different dosage forms,different quality standards,different usage and dosage.Combined with the idea of Chinese patent medicine reevaluation research,the author discusses the revaluation research of listed class-modified traditional Chinese medicine new drugs in China,in order to provide reference for the research of class-modified traditional Chinese medicine new drugs.
Key words:class-modified traditional Chinese medicine new drugs;low-level repetition;revaluation research;research status

