用于锂离子电池的四嗪环连接的共轭微孔聚合物电极性能研究
张梦慧,高 超,施 磊,马明明,章 冲,孙呈郭,杜 杨,胡炳成
(南京理工大学化学与化工学院,江苏 南京 210094)
1 前 言
作为一种高效的电子移动电源,二次电池以其体积小、寿命长和环境友好等优点得到了迅速发展[1,2]。与其他二次电池相比,锂离子电池(lithium-ion batteries,LIBs)具有输出电压高、能量密度高、自放电小等优势[3-6]。LIBs的性能主要依赖电极材料的性能。相比于传统无机电极材料,有机电极材料因储量丰富,毒性低以及结构多样性等特点备受关注。此外,随着对锂储存机理的深入理解,越来越多结构新颖的有机分子被设计开发出来提高电池性能[7-9]。因此,有机材料有望成为下一代LIBs的电极材料[10]。而为了避免有机小分子在电解质中的溶解降低电池容量及可持续性[11-13],常常需要对具有电化学活性的有机单元进行固载。
共轭微孔聚合物(conjugated microporous polymers,CMPs)作为一种有机多孔材料,具有较大的比表面积、较高的稳定性以及独特的微孔结构,在气体吸附[14]、储能[15]、多相催化[16]和光电子学[17,18]等领域展现出巨大的应用潜力。由于具有高孔隙率,CMPs不仅能够提供丰富的孔道促进Li+的传输,而且能够提供更多可接触的氧化还原活性中心,从而确保高能量存储容量和快速动力学。此外,CMPs中的共轭骨架还能够提高导电性,进一步改善电化学反应动力学[19,20]。因此,CMPs在LIBs电极材料领域的应用引起了广泛的关注。例如,2015年,Zhang等[21]将一种苯并噻二唑类CMP用作LIBs负极材料,该材料在0.2 A·g-1电流密度下循环400圈后仍有312 mAh·g-1的比容量;2018年,Zhang等[22]将含噻吩的CMPs作为锂离子电池负极材料,该CMPs在45 mA·g-1下放电容量高达1215 mAh·g-1,而在0.5 A·g-1下循环1000圈后比容量能够保持在663 mAh·g-1,具有优异的倍率性能和循环稳定性;2019年,Molina等[23]合成了基于蒽醌的CMP,将它作为LIBs阴极材料测试时,该CMP表现出较高的比容量(≈100 mAh·g-1),在循环5000圈(2C)和80 000圈(30C)后,分别能够保持初始容量的90%和60%;2022年,Yang等[24]通过Sonogashira-Hagihara交叉偶联反应制备了一种卟啉类CMP负极材料,该CMP在1 A·g-1循环1000圈之后比容量可达1200 mAh·g-1。因此,将具有氧化还原活性的结构单元引入CMPs骨架中有望获得性能优异的LIBs电极材料。
1,2,4,5-四嗪(1,2,4,5-tetrazine,Tz),又称s-四嗪,是一种经典的缺电子芳香族体系。由于高度缺电子的特性,Tz可以作为氧化还原活性单元通过接受一个电子形成稳定的阴离子自由基来加速充放电过程。此外,Tz还可以为Li+的吸附提供位点。因此,Tz作为LIBs电极材料中的活性单元有望改善电池性能。本文以氰基前体和水合肼为构筑前体,通过关环和还原两步反应合成2种由Tz连接的CMPs TZF和TBFZ,合成路线如图1所示。并进一步研究了TZF和TBFZ作为LIBs负极材料时的电化学性能。
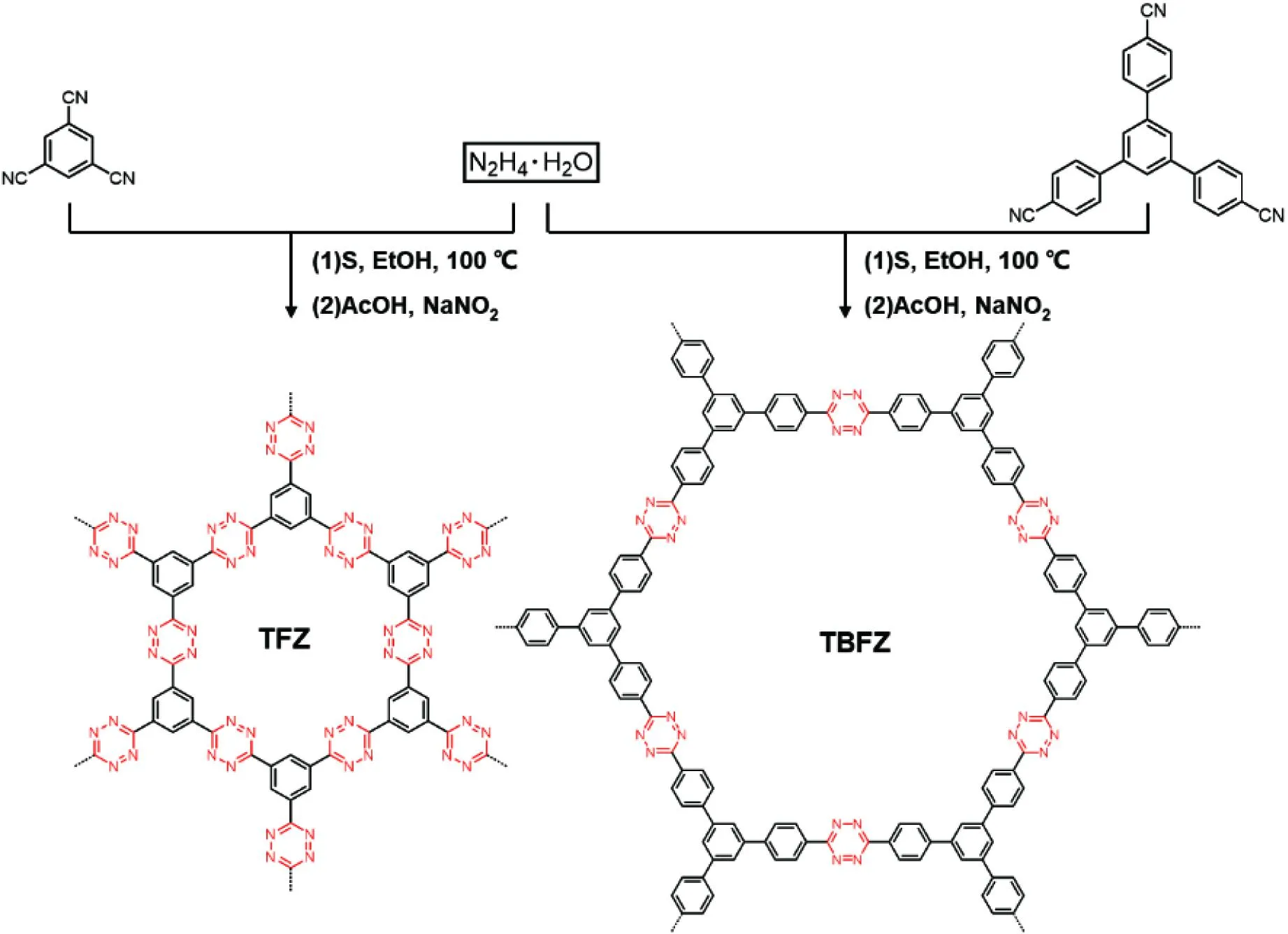
图1 TZF和TBFZ的合成路线和结构示意图
2 实 验
2.1 实验试剂
4-氰基苯硼酸(98%,上海毕得医药科技股份有限公司),1,3,5-三溴苯(98%,上海毕得医药科技股份有限公司),1,3,5-苯三氰(98%,上海麦克林生化科技有限公司),四(三苯基膦)钯(98%,上海毕得医药科技股份有限公司),无水硫酸镁(98%,上海麦克林生化科技有限公司),水合肼(85%,国药集团化学试剂有限公司),二茂铁(99%,上海迈瑞尔生化科技有限公司),N-甲基吡咯烷酮(AR,上海迈瑞尔生化科技有限公司),聚四氟乙烯(AR,成都市科龙化工试剂厂),硫(AR,国药集团化学试剂有限公司),炭黑(98%,上海毕得医药科技股份有限公司),铜箔(正影豪金属材料商行)。
2.2 实验仪器
采用Nicolet iS10红外光谱仪对原料、TZF和TBFZ进行红外表征;采用Bruker-AXS D8 Advance X射线衍射仪对TZF和TBFZ晶体结构进行表征;采用AVANCE III WB 400 MHz固体核磁共振谱仪对TZF和TBFZ进行骨架结构表征;采用日本电子JSM-IT500HR扫描电子显微镜对TZF和TBFZ形貌进行表征;采用STA 449 F5 Jupiter热重分析仪对TZF和TBFZ热稳定性进行表征。在LAND CT3001A型电化学设备上进行充放电性能测试。在BioLogic Science Instruments电化学工作站(VSP-300)上表征锂离子的循环伏安(cyclic voltammetry,CV)和阻抗等电化学性能。
2.3 材料合成
2.3.1 共轭微孔聚合物的合成
TFZ的合成:将1,3,5-苯三氰(0.12 g,0.71 mmol·L-1)和硫(0.3 g,9.37 mmol·L-1)置于25 mL圆烧瓶中,再加入水合肼(5 mL),在乙醇溶剂(10 mL)中回流24 h。反应后过滤得浅黄色固体,之后将该浅黄色固体悬浮于冰醋酸/水(60 mL/40 mL)混合液中,冷却至0 ℃,再加入亚硝酸钠水溶液(1.81 g,5 mL),反应体系变成红色。将上述反应体系过滤后用四氢呋喃充分洗涤,干燥后得到目标产物。通过元素分析可得该目标产物可得各元素原子百分数:C:53.09%,H:2.79%,N:19.86%。
TBFZ的合成:将1,3,5-三(4-氰基苯基)苯(0.27 g,0.71 mmol·L-1)和硫(0.3 g,9.37 mmol·L-1)置于25 mL圆烧瓶中,然后再加入水合肼(5 mL),在乙醇溶剂(10 mL)中回流反应24 h,得到浅黄色固体。随后,过滤并将浅黄色固体悬浮于冰醋酸/水(60 mL/40 mL)混合液中,冷却至0 ℃,再加入亚硝酸钠水溶液(1.81 g,5 mL),反应体系变成红色。将上述体系过滤并将过滤产物用四氢呋喃充分洗涤,干燥后得到目标产物。元素分析该目标产物可得各元素原子百分数:C:72.7%,H:2.79%,N:19.86%。
2.3.2 锂电池的组装
分别以TZF和TBFZ为活性物质,炭黑为导电添加剂,聚四氟乙烯为粘结剂,按照6∶3∶1的质量比进行混合,加入适量的N-甲基吡咯烷酮研磨成料浆。将研磨的料浆均匀涂敷在铜箔上,在80 ℃真空干燥箱中干燥12 h后切片称重,每个电极片直径为12 mm,负载量为0.6~0.8 mg。将准备好的电极片转入充满氩气气氛的手套箱中(H2O浓度小于0.001 mg·kg-1,O2浓度小于0.001 mg·kg-1)进行组装。组装采用2032系列纽扣式电池壳,电解液选用LiPF6(1 mol·L-1)为溶质,碳酸乙烯和碳酸二乙酯(体积比为1∶1)为溶剂,隔膜选用Celgard 2325型微孔膜,金属锂片为对电极。
3 结果与讨论
3.1 结构与表征

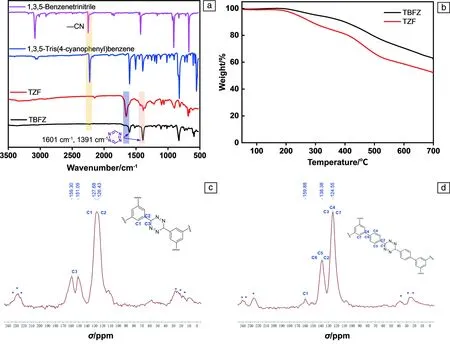
图2 1,3,5-苯三氰、1,3,5-三(4-氰基苯基)苯、TZF和TBFZ的FT-IR光谱(a);TZF和TBFZ的TG曲线(b);TZF(c)和TBFZ(d)的固体NMR图谱
采用氮气吸脱附测试仪对TZF和TBFZ的孔道性质进行了分析。如图3a和3b所示,在相对压力小于0.1时,TZF和TBFZ对氮气的快速吸附表明其结构中存在丰富的微孔,而在较高的相对压力下也表现出较高的氮气吸附,说明它们的结构中还可能存在介孔或大孔。基于吸脱附曲线,可得出TZF和TBFZ的BET比表面积分别为59.7和2144.0 m2·g-1,孔体积分别是1.21和3.04 cm3·g-1。通过密度泛函理论模型计算,TZF和TBFZ的孔径分布如图3a和3b中插图所示,它们的微孔孔径分别集中在1.7和1.4 nm,同时都含有部分的介孔结构。图3c和3d分别为TZF和TBFZ的扫描电子显微镜照片,由图可知TZF和TBFZ形貌呈石头状颗粒,粒径约为100 nm。
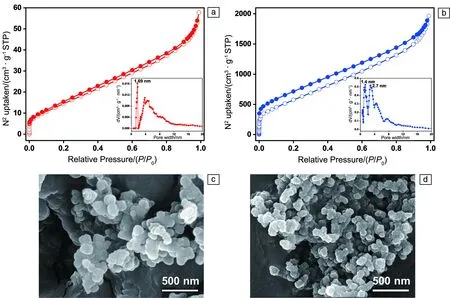
图3 TZF(a)和TBFZ(b)的N2吸附/脱附等温线和孔径分布曲线,TZF(c)和TBFZ(d)的SEM照片
3.2 电化学性能检测
TZF和TBFZ作为LIBs负极材料的电化学性能如图4所示。图4a和4b分别为TZF和TBFZ前5次的CV曲线。第一次循环中均能观察到明显的阴极峰,但在后续循环中消失,原因是电解液不可逆的分解以及固体电解质界面(solid electrolyte interphase,SEI)膜的形成[25]。而相较于TZF,TBFZ的初始还原电压更低,表明它延伸一个苯环之后接受电子的能力变弱了。此外,TZF在1.06/0.78 V和2.34/1.71 V处也表现出更强的氧化还原峰,该信号峰对应于Tz的氧化还原反应,说明结构中更高的Tz含量赋予了TZF更丰富的Li+活性中心。而且多个阴极峰表明在TZF的电化学还原中存在多步嵌Li+的过程,阴极峰强度在还原过程中的逐渐减弱也说明氧化还原活性单元Tz逐步吸附Li+[26,27]。需要指出的是,后续4个循环中TZF的循环伏安曲线几乎重叠,表明TZF作为LIB负极材料表现出高度可逆的氧化还原反应和良好的循环稳定性。图4c和4d给出了TZF和TBFZ在0.1C下的充放电曲线,起止电势范围设置为0.01~3.00 V(vs. Li+/Li)。TZF在1.68~0.68 V(vs. Li+/Li)之间呈现出倾斜的充放电平台,这与CV结果一致。TZF和TBFZ分别表现出62.0和35.5 mAh·g-1的可逆充电容量和在0.1C下循环2次后稳定的充放电行为,根据CV曲线,可知第1次循环的不可逆容量是由于SEI膜的形成。
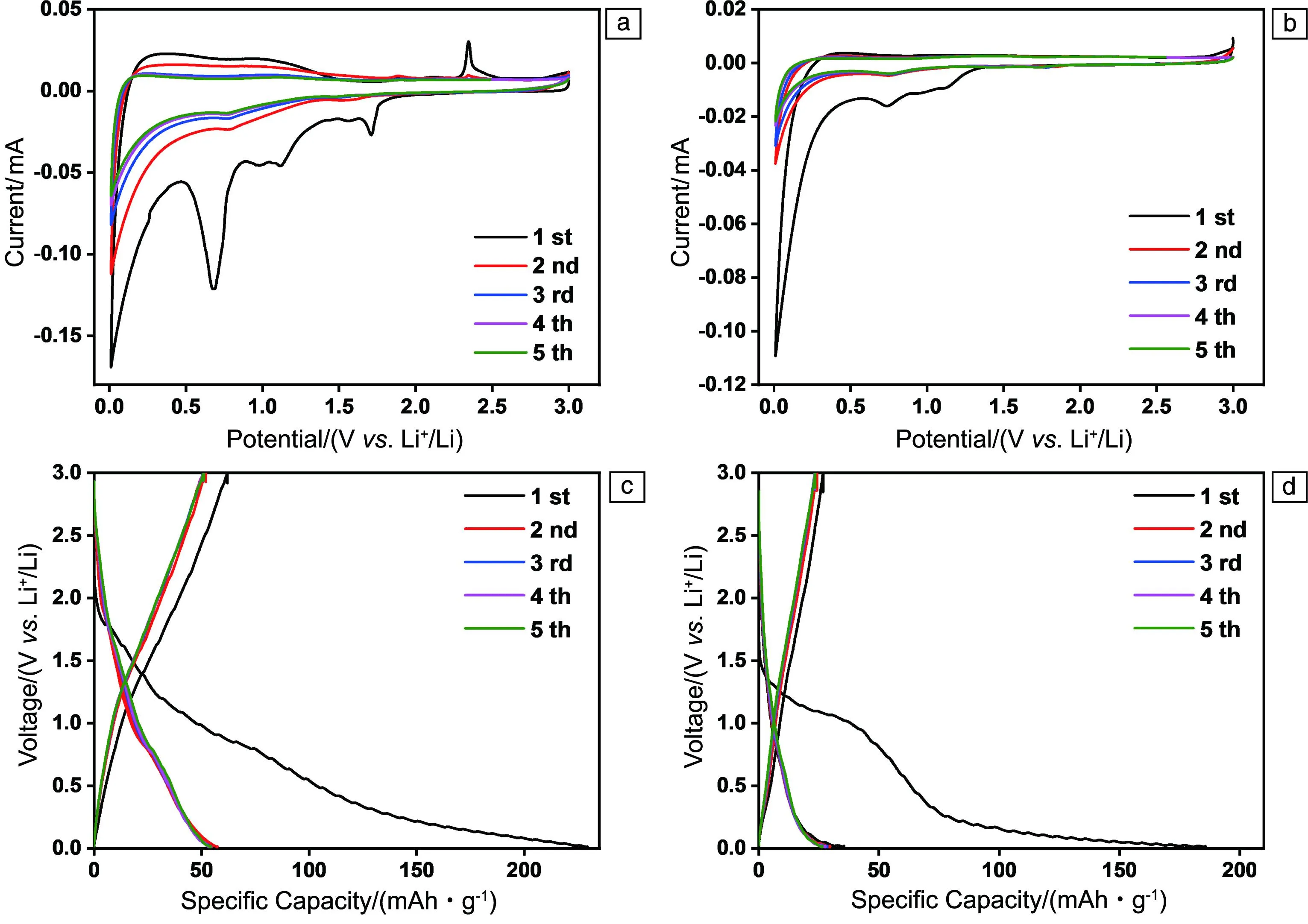
图4 TZF(a)和TBFZ(b)的循环伏安曲线,TZF(c)和TBFZ(d)的前5次充放电曲线
为了解TZF和TBFZ中可逆充电容量差异的原因,通过固体紫外可见吸收光谱和CV曲线计算了它们的最高占据轨道(HOMO)和最低未占据轨道(LUMO)能级。通过固体紫外-可见吸收光谱可知,TZF和TBFZ的禁带宽度分别为2.03和2.04 eV(图5a和5b)。图5c和5d记录了TZF和TBFZ的CV曲线。参考二茂铁/二茂铁(Fc+/Fc)的氧化还原电位,计算得到TZF和TBFZ的LUMO能级分别为-3.80和-3.66 eV。根据禁带宽度得TZF和TBFZ的HOMO级分别为-5.83和-5.70 eV。根据分子轨道理论,LUMO能级低意味着更大的电子亲和力,说明TZF的n型掺杂能力更强,从而使它展现出更高的可逆充电容量。
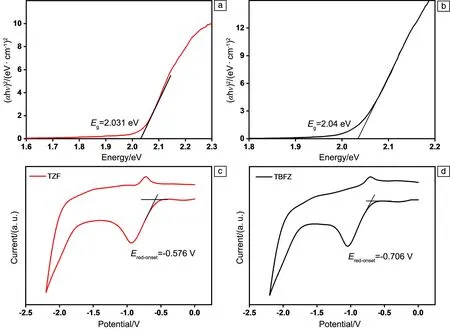
图5 TZF(a)和TBFZ(b)的带隙谱图,TZF(c)和TBFZ(d)的循环伏安曲线
为进一步展示TZF和TBFZ作为锂电池负极材料的电化学性能,对它们进行了倍率测试和循环测试(图6a),结果表明,当倍率重置到0.1C时,可逆容量均能得到恢复,显示出优秀的倍率性能,说明经高速锂化/脱锂处理后的四嗪类共轭微孔聚合物电极具有良好的结构稳定性。通过恒电流充放电测试表征了TZF和TBFZ负极材料在0.1C下的循环性能(图6b),在循环200多圈后可逆充电容量没有减弱,说明它们都具有较好的循环性能。此外,扫描电子显微镜照片显示TZF和TBFZ负极材料在循环后仍能保持纳米粒子的形貌(图6c~6f)。
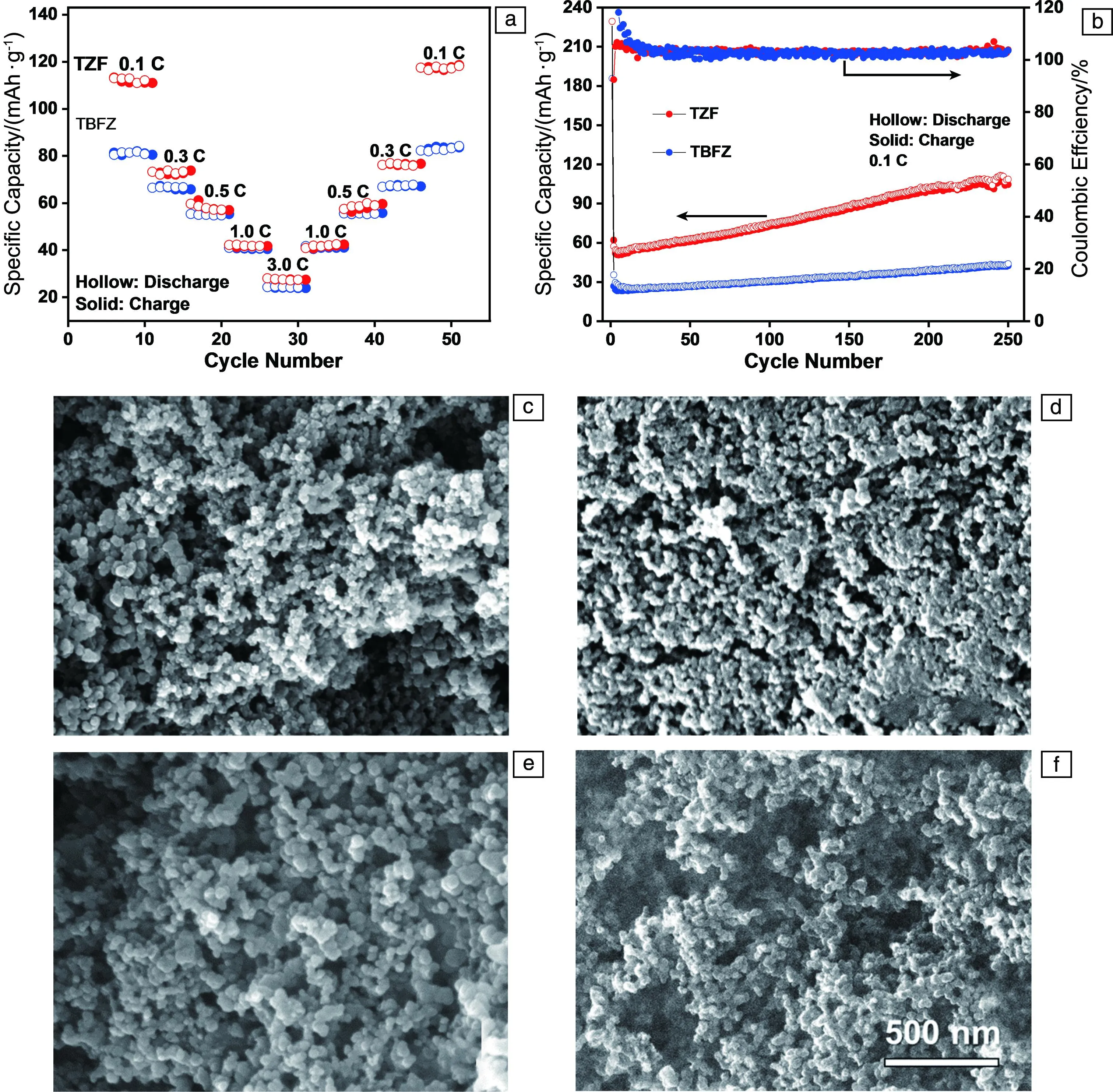
图6 TZF和TBFZ的倍率性能(a),TZF和TBFZ在0.1C下的循环性能(b),TZF(c,d)和TBFZ(e,f)负极材料在1.0C下循环前(c,e)和循环200圈后(d,f)的SEM照片
需要指出的是,图6b中TZF作为锂电池负极材料在经过250次循环后可逆比容量从62.0增长到108.6 mAh·g-1,增长了约75%,表明这种材料需要很长的激活期。为继续了解比容量的异常增加,研究了TZF电极材料在不同倍率下的循环性能(图7a)。在0.1,0.5和1.0C的电流密度下都能够清晰地观察到TZF放电容量的增长,当放电倍率上升到3.0C时,TZF放电容量增加不明显,可知放电倍率越小,TZF放电容量增加的趋势越明显。在0.1和0.5C的电流密度下,可逆比容量都是先下降再稳定上升一段,最后会出现一定的波动,而电流密度为1.0C时后面比容量一直保持平稳的增长,在循环1000次之后,比容量由40提高到139 mAh·g-1,库伦效率始终接近100%。在前数十次循环中锂离子的可逆容量下降是由于形成了SEI膜。而后续的增长可能是因为循环过程中电解液的渗透激活了孔道内部的活性单元,导致电极材料电阻降低改善了锂的扩散动力学[28]。为验证这一点,通过电化学交流阻抗谱测试对TZF在1.0C电流密度下循环的不同阶段进行了测试,测试的频率范围为0.1 Hz~100 kHz(图7b)。高频在实轴上的截距表示电解质的电阻Zreal,而低频率的倾斜线是反映了Li+扩散到电极材料的情况。结果表明,随着循环圈数的增加,由高频和中频区形成的半圆形直径逐渐减小,电极和电解液界面的电荷转移阻抗减小,从100圈时的501.7减小到1000圈后的172.8 Ω。同时,通过计算得到Li+扩散系数,如表1所示,TZF随着循环圈数的增加,Li+扩散系数不断增加,与循环试验的快速激活行为相吻合。
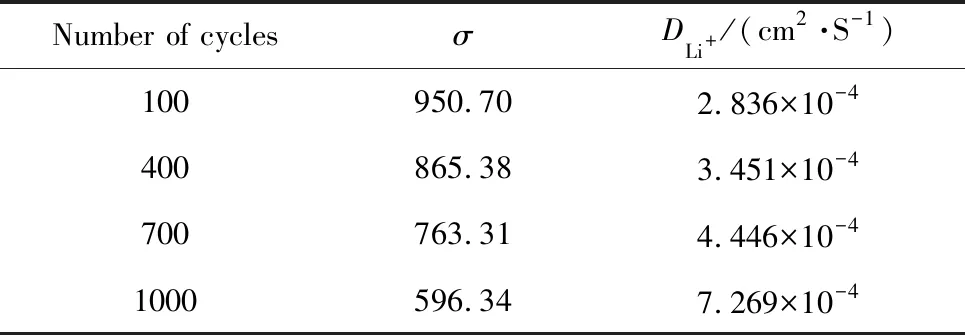
表1 TZF在1.0C时不同循环次数下的锂离子扩散系数
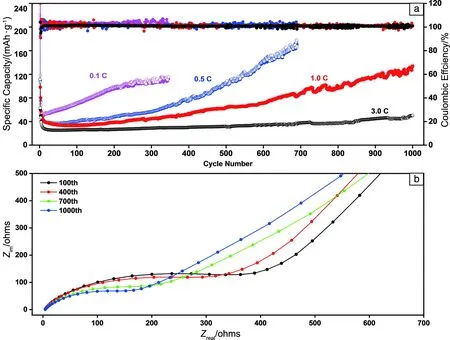
图7 TZF在不同倍率下的循环性能(a),TZF在1.0C下不同循环圈数时的阻抗(b)
4 结 论
本工作以Tz为连接单元,制备了具有氧化还原活性的共轭微孔聚合物TZF和TBFZ,并将它们作为锂离子电池负极材料研究其电池性能。通过傅里叶变换红外光谱、固体核磁共振谱、热重分析及氮气吸脱附测试等方法对所合成的聚合物的组成、结构及孔道性质进行了表征,表明其共轭多孔结构。电化学相关测试表明,TZF展现出比TBFZ更好的电化学性能,原因主要是TZF中活性单元Tz含量更高,而且更低的最低未占据轨道能级使它具有更大的电子亲和力。此外,在不同的电流密度下循环后,TZF比容量均有不同程度的提高,在1.0C下循环1000次之后,比容量由40提高到139 mAh·g-1,并且库伦效率始终接近100%,说明TZF作为锂离子电池负极材料表现出良好的氧化还原活性及循环稳定性。

