急性髓系白血病患者应用维奈克拉联合去甲基化药物治疗的临床效果
唐晶晶,包雯婷,宋苏永
福州市第一总医院血液科,福建福州 350009
急性髓系白血病(acute myeloid leukemia, AML)为常见血液系统恶性肿瘤性疾病,患病群体多为老年人,发病率有逐年升高的趋势[1]。一般此类患者的标准治疗方案是诱导缓解治疗、巩固治疗、维持治疗,最为常见的治疗药物为阿扎胞苷,该药属于一种去甲基化药物,作用在机体中,可以将S期细胞杀死,并具有直接性细胞毒性[2]。但是单独使用一种药物,其去甲基化持续时间较短,因此需要对患者施以维持治疗,这样往往会导致其机体无法耐受而产生多种不良反应,进而影响其治疗效果[3]。基于此,需要联合其他药物共同治疗。维奈克拉能够抑制B细胞淋巴瘤因子2,与阿扎胞苷联合用药已经成为不耐受强诱导化疗及老年AML患者的一线治疗新标准[4]。为研究两种药物联合的临床价值,本文简单随机选取2021年1月—2022年12月福州市第一总医院的60例急性髓系白血病患者为研究对象,现报道如下。
1 资料与方法
1.1 一般资料
简单随机选取因急性髓系白血病入本院接受治疗的60例患者为研究对象,按随机抽签法分为对照组30例和观察组30例。对照组男18例,女12例;年龄45~73岁,平均(65.25±2.62)岁。观察组男17例,女13例;年龄46~75岁,平均(65.38±2.58)岁。结合年龄、体能、合并症等预后因素分析,两组患者均不适合进行强诱导化疗。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。本次研究已经得到医学伦理委员会通过。
1.2 纳入与排除标准
纳入标准:经诊断患有急性髓系白血病的初治患者;对研究详情知晓,并签署告知协议书;有正常认知。
排除标准:预估生存时间不足半年者;同时患有其他血液疾病者;同时存在传染性病毒感染者;暂未明确分型者。
1.3 方法
对照组治疗方案:应用阿扎胞苷注射液(国药准字H20193278;规格:100 mg/瓶),以皮下注射方式给药,每次75 mg/m²,1次/d,共7 d,1个疗程为4周,总计治疗8周。
观察组治疗方案:阿扎胞苷方法和对照组相同,增加维奈克拉(国药准字HJ20200055;规格:100 mg/片),以口服方式给药,首次100 mg,次日200 mg,从第3天开始400 mg,并维持该剂量,用药1次/d,本组同样连续治疗8周。
1.4 观察指标
临床疗效:在患者连续治疗8周后对其近期临床疗效进行统计,具体包括完全缓解(骨髓原始细胞比率<5%,各种体征及症状全部消失)、部分缓解(骨髓原始细胞比率≥5%且≤20%,各种体征及症状得到良好改善)、未缓解(上述情况都不符合),临床总疗效=完全缓解率+部分缓解率。
血液学指标:具体包括骨髓血原始细胞比率、白细胞计数、血小板计数,在治疗前、治疗8周后分别对其空腹外周血进行采集,然后借助型号为BC-5000的迈瑞五分类血球仪血液细胞分析仪测定后获取。
实验室指标:具体包括肿瘤坏死因子-α、干扰素-γ,在治疗前、治疗8周后分别采集患者空腹状态下的外周血5 mL,按照3 000 r/min的标准离心10 min,离心半径为8 cm,指标测定方法为酶联免疫吸附试验。
不良反应发生率:观察治疗8周后不良反应发生情况,具体包括胃肠道不良反应、感染、血液学不良反应等。
1.5 统计方法
采用SPSS 22.0统计学软件处理数据,符合正态分布的计量资料以()表示,行t检验,计数资料用例数(n)和率(%)表示,行χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较
观察组临床总疗效高于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组患者临床疗效比较
2.2 两组患者血液学指标比较
治疗前两组患者血液学指标比较,差异无统计学意义(P>0.05);治疗后两组患者骨髓原始细胞比率均有降低,且观察组显著低于对照组,差异有统计学意义(P<0.05);治疗后两组患者其他血液学指标均有升高,且观察组高于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组患者血液学指标比较()
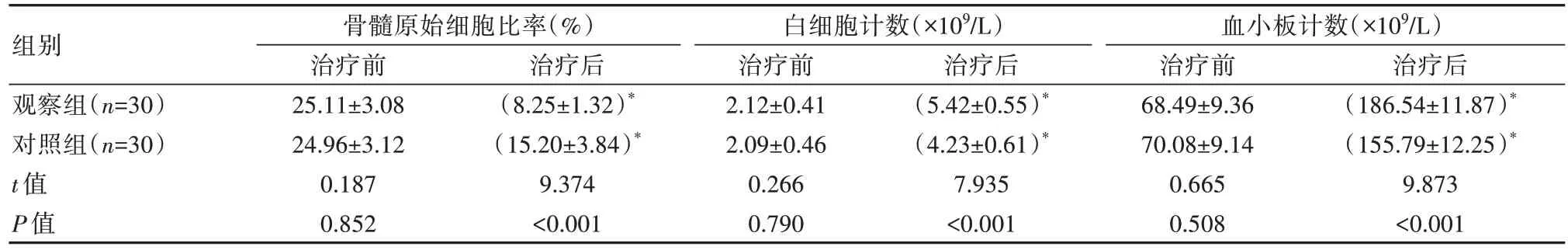
表2 两组患者血液学指标比较()
注:和同组治疗前相比,*P<0.05。
组别观察组(n=30)对照组(n=30)t值P值治疗后(186.54±11.87)*(155.79±12.25)*9.873<0.001骨髓原始细胞比率(%)治疗前25.11±3.08 24.96±3.12 0.187 0.852治疗后(8.25±1.32)*(15.20±3.84)*9.374<0.001白细胞计数(×109/L)治疗前2.12±0.41 2.09±0.46 0.266 0.790治疗后(5.42±0.55)*(4.23±0.61)*7.935<0.001血小板计数(×109/L)治疗前68.49±9.36 70.08±9.14 0.665 0.508
2.3 两组患者实验室指标比较
治疗前两组患者实验室指标比较,差异无统计学意义(P>0.05);治疗后两组患者肿瘤坏死因子-α均有降低,观察组低于对照组,差异有统计学意义(P<0.05);治疗后两组患者干扰素-γ均有升高,观察组高于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组患者实验室指标比较[(),pg/mL]

表3 两组患者实验室指标比较[(),pg/mL]
注:和同组治疗前相比,*P<0.05。
组别观察组(n=30)对照组(n=30)t值P值干扰素-γ治疗后(72.49±8.63)*(58.96±7.59)*6.448<0.001肿瘤坏死因子-α治疗前260.65±24.04 259.47±24.21 0.189 0.8504治疗后(89.93±11.51)*(130.27±20.36)*9.447<0.001治疗前39.95±8.24 41.04±8.81 0.494 0.6225
2.4 两组患者不良反应发生率比较
观察组出现2例胃肠道不良反应、1例感染、1例血液学不良反应,不良反应发生率为13.33%(4/30);对照组出现1例胃肠道不良反应、2例感染;2例血液学不良反应,不良反应发生率为16.67%(5/30)。两组患者不良反应发生率对比,差异无统计学意义(χ2=0.120,P>0.05)。
3 讨论
急性髓系白血病的临床特征包括髓系干细胞、髓系祖细胞异常增殖及分化受阻、凋亡受抑等,属于一种常见的血液系统恶性肿瘤疾病[5]。患病群体多为老年人,临床主要是对患者采取强化治疗及异体造血系统抑制治疗方案,但是大部分患者受到年龄、身体健康状况、合并基础疾病等因素的影响,往往会使其临床治疗难度进一步增加[6]。
对于不耐受强诱导化疗及老年AML患者,目前临床一般会使用到去甲基化药物对患者实施治疗,并以阿扎胞苷最为多见,该药为胞嘧啶核苷类似物的一种,作用在机体中,能够将细胞DNA途径有效阻断,并有效抑制RNA复制进程,从而促进S期细胞凋亡[7]。虽然能够起到一定的治疗效果,但是单一用药具有很大的局限性,且患者的症状无法长时间保持缓解状态,因此有很多不足之处[8]。本研究中,观察组增加使用维奈克拉,最终产生的治疗效果更为理想。数据显示:观察组临床总疗效(86.33%)明显高于对照组(56.67%)(P<0.05);本结果和陈涛等[9]研究中提到观察组治疗总有效率为78.79%高于对照组(54.55%)(P<0.05)的结果一致。分析原因:维奈克拉是一种小分子B细胞淋巴瘤因子2抑制类药物,能够具有较为广泛的抗肿瘤后活性,由于B细胞淋巴瘤因子2家族属于调控线粒体细胞死亡信号、生存信号的关键因子,会将抗凋亡分子、促凋亡分子和效应蛋白之间产生作用,使内源性细胞凋亡通路得到调控[10]。因此将其联合使用后,能够对内源性细胞凋亡信号通路活性起到促进作用,致使恶性细胞快速凋亡[11]。同时,该药还可以将静止期白血病干细胞充分清除,因此在临床中具有较高活性,对提升患者临床疗效具有重要作用[12]。同时,阿扎胞苷能够对造血细胞分化起到促进作用,诱导细胞DNA去甲基化,使髓细胞白血病因子-1水平显著降低,促使恶性肿瘤细胞凋亡速度也会显著加快。不过由于髓细胞白血病因子-1属于急性髓系白血病发病过程中的重要抗凋亡蛋白,因此很容易发生机体耐药问题[13]。将其与维奈克拉联合使用后,能够诱导内源性细胞凋亡,且二者可形成协同作用,使髓细胞白血病因子-1含量显著降低,进一步促进恶性细胞凋亡速度,进而减少恶性细胞对阿扎胞苷的耐药性[14]。在本研究中,治疗后两组骨髓原始细胞测定结果均降低,其中观察组数据相对更低(P<0.05);治疗后两组白细胞计数和血小板计数均升高,且观察组更高(P<0.05)。说明该方法更加有助于改善患者的血液学指标。其中骨髓原始细胞比率在临床中主要是针对急性髓系白血病患者临床疗效进行反映的重要指标,未分化骨髓细胞是一种原始细胞,一般主要存在于骨髓内,如果其指标超出20%,则往往会使患者机体造血功能发生改变,进而确诊为急性白血病[15]。同时,由于急性髓系白血病患者往往会有白细胞和血小板计数异常的情况,因此也可通过这两项指标来评价患者的治疗效果。通过采取联合用药的治疗方案,维奈克拉的恶性细胞凋亡作用能够在短时间内起效,原始细胞数量得以降低,并将临床治疗活性进一步提升。在本研究中,观察组治疗后肿瘤坏死因子-α显著较对照组更低,干扰素-γ显著较对照组更高(P<0.05)。由此能够看出,在使用两种药物联合治疗以后,可以形成更为理想的抗炎效果。主要因为维奈克拉能够使线粒体细胞外膜通透性发生变化,增加半胱天冬酶活性,有效调控基因因子释放炎症因子的进程,进而降低患者机体血清炎症因子水平。二者联合使用,能够使患者机体中的活性氧有效提升,从而形成更好的抗炎效果。另外对比二者不良反应发生率,差异无统计学意义(P>0.05),进一步看出联合用药不会提升患者机体不良反应,具备良好的用药安全性。
综上所述,通过维奈克拉与去甲基化药物联合治疗,能够显著提升急性髓系白血病患者的临床总疗效,更好地改善各种临床指标,且不会增加不良反应,因此具有较好的治疗安全性。

