新冠疫情防控不同时期深圳地区无偿献血人群新冠病毒抗体检测结果∗
邬林枫 陈婷婷 王皓飚 刘衡 李彤 王立林 许晓绚 曾劲峰
(深圳市血液中心,广东 深圳 518035)
2019 年12 月,新型冠状病毒(SARS-CoV-2)感染人类引起的疫情迅速蔓延[1-3],3 年多来全球各国疫情反反复复,且出现多种毒株流行[4-6],对世界各地的社会、经济、生活造成了破坏性的影响。在国内外疫情防控形势严峻复杂的情况下,我国经过多次的防控政策调整,不断补充、调整新型冠状病毒感染的防控方案直至现行的第10 版[7]。2022 年11 月11 日,国务院联防联控机制公布“进一步优化疫情防控的二十条措施”[8],2022 年12 月7 日,公布“进一步优化疫情防控的十条措施”[9],2022 年12 月26 日,发布新冠病毒感染将由“乙类甲管”调整为“乙类乙管”[10]。随着深圳逐步落实国家疫情防控措施,新冠病毒感染者不断增加,危、急、重症新冠感染患者人数也在上升。本中心依据上级相关文件[11-13]指示开展新冠感染康复者恢复期血浆采集、检测、制备和发放等血液保障工作,切实做好新形势下血液安全和血液保障工作。现将本中心这段时期对深圳地区献血人群进行新冠病毒抗体检测的情况报告如下。
1 材料与方法
1.1 标本来源 1)深圳市血液中心2022 年9 月30 日—10月3 日、11 月3—6 日、12 月27—31 日、2023 年1 月6—18 日4 个时间段的无偿献血者标本4 768 份。来自献血者4 646名(男性3 047,性女1 599),年龄18~61 岁,平均年龄34.9岁,A 型1 302 名、B 型1 210 名、O 型1 737 名、AB 型397 名。2)于第4 时间段(2023 年1 月6—18 日)17—18 日对该两日献血者感染新冠的情况进行征询,征询后采集献血者标本527 份,其中有319 名献血者在新冠疫情管控措施放开(即实施“二十条措施”[8])后曾感染新冠病毒且处于康复期。
1.2 试剂与仪器 新型冠状病毒核酸检测试剂盒(江苏新波公司,批号:20221025),2019-nCoV 总抗体检测试剂盒(万泰生物公司,批号:NC0A20221002B)。PreNATⅡ核酸提取纯化仪(江苏新波公司),ABI 7500 荧光PCR 仪(赛默飞公司),FAME24/20 酶免检测仪(哈密尔顿公司),Xantus150 加样仪(深圳爱康公司),Sunrise 酶标仪(帝肯公司)。
1.3 方法
1.3.1 标本纳入标准 所有检测标本均按«血站技术操作规程(2019 版)»[14]、«血站新冠病毒感染防控工作指引(第二版)»[13]等相关文件规定进行无偿献血征询和健康检查,合格后进行血液和标本采集。
1.3.2 标本采集与处理 用EDTA-K2抗凝管静脉采集献血者全血标本6 mL,2 000×g 离心10 min,分离红细胞和血浆,用深孔留样板留取500 μL 血浆用于新冠病毒核酸和抗体检测,未能及时检测的标本置于冰箱-20℃冻存。取1 深孔板,每孔加生理盐水980 μL,吸取血浆标本20 μL 加入对应孔,振荡仪振荡10 min 混匀,再取1 深孔板,每孔加生理盐水950 μL,吸取稀释后标本50 μL 加入对应孔,振荡仪振荡10 min 混匀,得到稀释1 000 倍的标本,用于新冠病毒抗体检测。
1.3.3 检测方法 核酸检测(NAT)采用8 混检测模式,检测无反应性则8 份标本均为无反应性,若检测有反应性,则分别对8 份标本大单独进行检测判断是否有反应性。抗体检测采用酶联免疫吸附试验(ELISA)法,检测程序依据厂家试剂盒说明书进行。
1.3.4 结果判定 检测结果的判断标准参照厂家说明书。核酸检测以循环阈值(cycle threshold,Ct)≤35 为有反应性,抗体检测标本吸光度值大于等于临界值为有反应性,即标本吸光度值与临界值比值(S/CO)≥1.0 为有反应性。
1.4 统计学分析 用Excel 2010 对数据进行收集、汇总和统计,用SPSS 26.0 统计分析数据,χ2检验中的Fisher 确切概率法分析分类变量资料,采用双侧检验,P<0.05 为差异有统计学意义,T 检验统计分析样本S/CO 值,P<0.05 为差异有统计学意义。
2 结果
2.1 新冠病毒核酸检测结果 4 768 份献血者标本新冠病毒核酸检测均为无反应性。
2.2 新冠病毒抗体检测结果 见表1~3,图1~3。
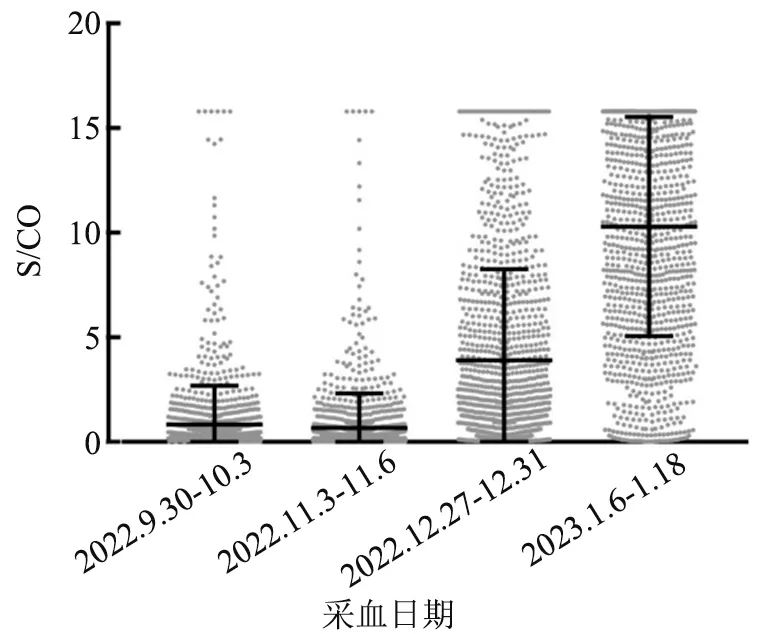
图1 不同采血日期献血者抗体检测值分布散点图

图2 2023 年1 月6—18 日不同性别献血者标本抗体检测值分布散点图
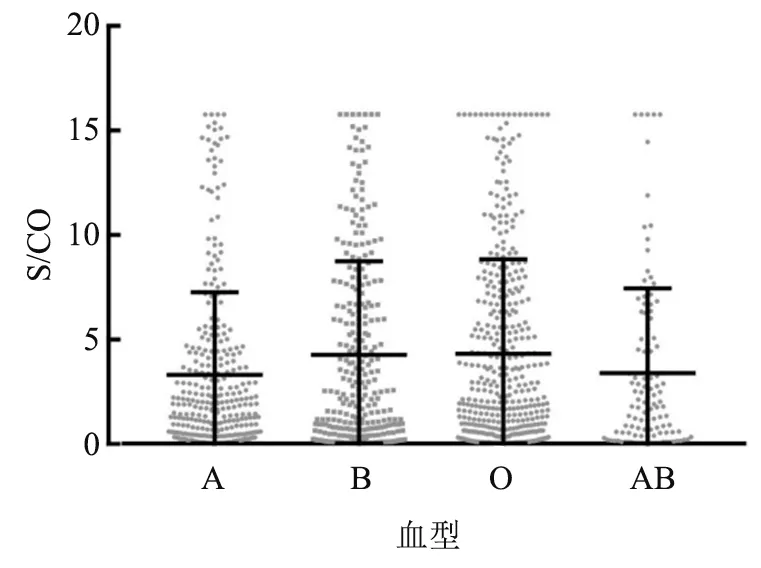
图3 2022 年12 月27—31 日不同血型献血者标本抗体检测值分布散点图
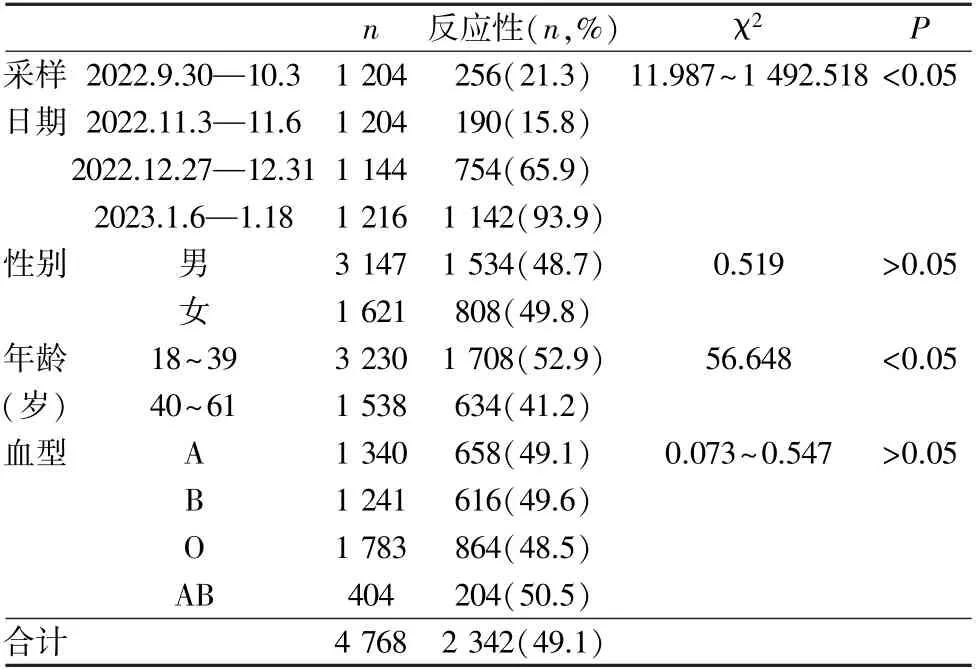
表1 献血人群新冠抗体检测结果
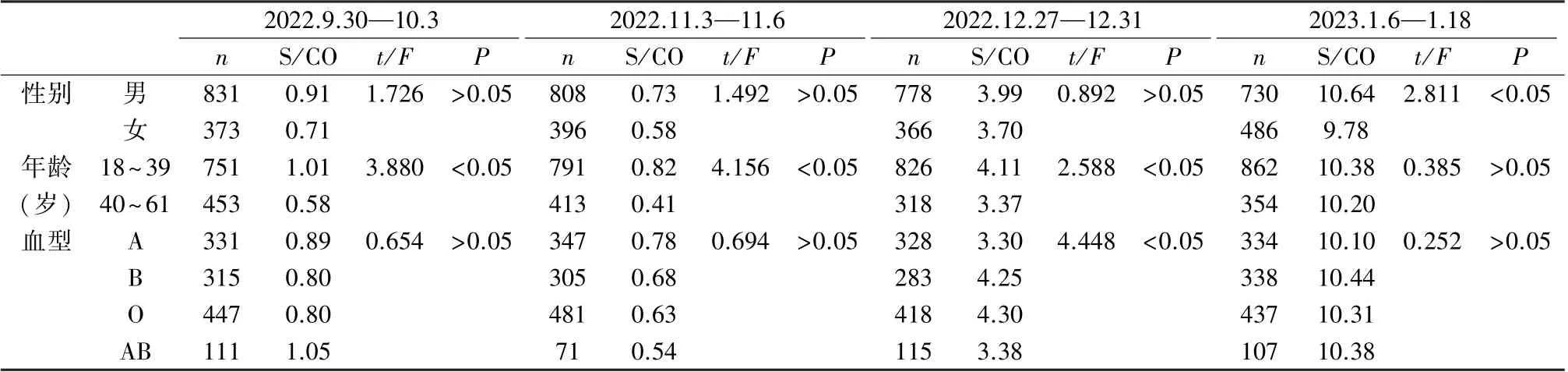
表2 不同时间段内不同性别、年龄、血型献血者新冠抗体检测值结果分析

表3 2023 年1 月17—18 日献血者、新冠康复期献血者抗体检测结果比较
3 讨论
依据«新冠肺炎康复者恢复期血浆临床治疗方案(试行第三版)»要求“新冠病毒血清/血浆总抗体定性检测呈阳性且320 倍稀释后按照试剂说明书要求检测仍为阳性反应”[12]。在本研究中的标本,特别是2023 年1 月6—18 日采集的标本,320 倍稀释后检测有反应性的S/CO 值大部分超出实验室酶标仪的检测高限,经前期预实验、试剂盒特性以及实验室自身条件等综合考虑,将实验方案中稀释倍数调整为1 000 倍。
SARS-CoV-2 侵入人体后诱导宿主细胞产生IgA、IgM 和IgG,称为总抗体。我们应用ELISA 双抗原夹心法对献血者血浆标本进行总抗体检测,由于双抗原夹心法具有高灵敏度的特性,所以采用的策略是对标本进行1 000 倍稀释,稀释后标本按照试剂说明书要求进行检测,结果为阳性反应且献血前征询为近期有新冠病毒感染并处于康复期的献血者血浆制备成新冠康复者血浆。在治疗病毒性疾病过程中取得一定的治疗效果[15-19],同样在新冠疫情爆发初期,就有对COVID-19 患者进行恢复期血浆输注治疗安全性和有效性的探讨[20-21]。需要注意的是,恢复期血浆治疗也有一些局限性,如发生输血反应,抗体依赖性增强(ADE)等[22-24]。
本研究主要是对深圳地区献血人群的血浆标本进行SARS-CoV-2 核酸和总抗体检测。核酸检测针对新型冠状病毒2 段保守基因序列ORF1ab 基因(开放读码框1ab)和N 基因(核壳蛋白),总抗体同时可以针对几种蛋白,如核衣壳蛋白和刺突蛋白,与中和试验的抗刺突蛋白检测有相似之处,总抗体检测可以较高程度地反映SARS-CoV-2 特异性的中和抗体水平[25],从而为基层医疗机构提供简单有效的方法评价SARS-CoV-2 特异性抗体水平。
深圳地区献血人群新冠总抗体检测结果显示不同性别、血型的人群产生抗体的情况没有明显差异性,而不同年龄段比较而言,18~39 岁的献血者反应性率和检测(S/CO)值均较高,可能跟年轻人体内免疫系统较强有关,能针对新冠病毒迅速启动免疫应答。从采样日期看,2022 年11 月3—6 日较2022 年9 月30 日—10 月3 日采集标本的反应性率和检测(S/CO)值都低,此2 个时间段处于新冠疫情严防严控时期,在社会上并未产生大面积的感染,有可能是注射新冠肺炎疫苗产生的抗体在衰减。2022 年12 月27—31 日较2022年11 月3—6 日采集标本的反应性率和检测值均大幅上升,正是由于深圳逐步实施“进一步优化疫情防控二十条、十条措施”[8-9],市民大面积感染新冠病毒所致。2022 年12 月底是“进一步优化疫情防控的十条措施”20 d 后,也正是第1 批新冠病毒感染者康复的时间,在这个时间段献血者新冠病毒抗体水平骤增是必然的,随着感染高峰期过后的时间段2023年1 月6—8 日,也是高峰期感染者康复的时间,所以反应性率达到93.9%,检测(S/CO)值高达10。
比较不同采样时间段内不同性别、血型献血者标本的检测(S/CO)值,2023 年1 月6—18 日时间段,男性献血者标本的检测(S/CO)值稍高于女性,2022 年12 月27—31 日时间段,B 型和O 型血献血者标本检测(S/CO)值也稍高于A 型血和AB 型血。产生此结果的原因可能是在疫情爆发期间,血液中心在献血招募时对人群有意识的征询选择导致,但也不能排除自然规律使然。
就同一时间段(2023 年1 月17—18 日)检测结果看,全部献血者和新冠康复期献血者的新冠抗体检测反应性率无差异(P>0.05),可能与以下因素相关:献血者均经过献血前征询和检查,已排除新冠病毒接触史和新冠感染期,征询结果为“未感染新冠病毒”的献血者属于无症状感染且已康复,接种新冠疫苗产生高滴度抗体,也可能是此时间段深圳地区市民处于全体免疫状态。
本研究对4 768 份献血者标本进行了新冠病毒核酸检测,结果为均无反应性,标本稀释1 000 倍抗体检测反应性率为49.1%,而新冠疫情防控措施放开后[9]的抗体反应性率为65.9%,对新型冠状病毒感染实施“乙类乙管”前后[10]标本稀释1 000 倍后检测反应性率更是高达93.9%,检测(S/CO)值高达10,抗体的高反应性率和高检测值(S/CO>10),在人群中形成了良好的免疫屏障,可以初步判定经输血传播新型冠状病毒的风险极小。
利益冲突:所有作者均声明不存在利益冲突。

