颈椎椎间孔螺钉、侧块螺钉、椎弓根螺钉生物力学强度有限元分析
陈建清,叶春平,赵刘军,黄维运,曹 扬
1.金华市人民医院脊柱外科,金华 321000
2.宁波市第六医院骨科,宁波 315040
颈椎后路内固定技术已广泛运用于颈椎退行性疾病、创伤、肿瘤、感染及畸形等的治疗。目前,在临床上运用最多是椎弓根螺钉(PS)和侧块螺钉(LMS)内固定。PS 较长且通过骨质最硬的椎弓根,具有较强的把持力,能够提供最佳的初始稳定性[1-2];但因技术难度高,且可能发生椎动脉、神经根损伤,硬膜撕裂或食管穿孔等严重并发症,限制了其临床应用[3]。LMS 内固定技术较PS 难度相对低,并发症发生率低,手术安全性高,但初始稳定性弱,对于需要坚固固定及严重骨质疏松的患者,LMS 不能提供充分的稳定性,可能导致内固定失效[4-5]。
2014 年,Aramomi 等[6]提出了新型颈椎后路内固定技术——椎间孔螺钉(PVFS)内固定,该技术选择侧块中垂线内移1 mm 与相邻上位椎体下关节突交点作为进钉点,钉道方向为上内倾20°~ 25°,矢状面上与终板平行。Kim 等[7]在针对颈椎PVFS置钉的解剖学参数研究中发现,除C7外,C3~6横突孔均位于椎体后缘之前,基于此解剖结构的特点,椎体后缘常作为PVFS 置钉的安全线。在临床实际置钉过程中,术中通过拍摄颈椎侧位X 线片来监测螺钉尖深度,避免螺钉尖越过椎体后缘,可最大限度地避免椎动脉损伤,保证手术安全性。另外,PVFS 能够提供良好的生物力学稳定性,体外拔出力实验[8]显示其平均直接拔出力234 N,优于LMS的158 N。
为进一步研究PVFS 的生物力学特性及其与PS、LMS 的生物力学差异,本研究采用三维有限元方法建立PVFS、LMS 及PS 内固定模型,并分析比较3 种模型的活动度(ROM)及螺钉、螺钉-骨界面最大应力。
1 材料与方法
1.1 实验对象
以1名22岁健康男性志愿者为研究对象,无颈椎病史,摄颈椎正侧位、斜位及过伸过屈位X线片,排除颈椎病变。采用飞利浦 brillionce 64排螺旋CT系统(GE公司,美国)获取数据,扫描参数:120 kV,125 mA,层厚0.625 mm,范围C2~ T1;所采集数据以标准dicom 格式保存,共获得260 张图像。软件:Windows 7 X 64 Professional Edition(MicroSoft 公司,美国);Mimics 16.0(Materialise 公司,比利时);Geomagic 12.0(3D Systems 公司,美国);Pro/E5.0(PTC公司,美国);ABAQUS 6.14(达索公司,法国)。
1.2 模型建立
完整下颈椎骨性模型(对照组):将CT 扫描dicom 格式图像导入Mimics 16.0 软件,建立C3~7模型,保存为二进制stl 格式,导入Geomagic 12.0 软件进行曲面构建并分离皮质骨和松质骨,拟合空间封闭的非均匀有理化样条曲面(nurbs),均以iges 格式导出。在Pro/Engineer 5.0 软件中完成各个椎体的实体化。参考CT 原始数据,构建椎间盘、髓核的三维模型。
在Pro/Engineer 5.0软件中建立C5/C6节段PVFS、LMS 和PS 内固定重建模型:PVFS 组包括4 枚长12.0 mm、直径4.5 mm 的螺钉及2 根连接杆;LMS组包括4 枚长14.0 mm、直径3.5 mm 的螺钉及2 根连接杆;PS 组包括4 枚长24.0 mm、直径3.5 mm 的螺钉及2 根连接杆。单元及材质赋予:皮质骨、松质骨、椎弓根采用高阶四面体单元C3D4,关节突关节、终板、髓核采用高阶四面体单元C3D8;纤维环及各韧带(前纵、后纵、棘间、棘上、关节囊、黄、横突间韧带)采用 TRUSST3D2 单元模拟,并设置其属性为只承受张力;内固定器(螺钉及连接杆)采用C3D4 单元。各组织参照文献[9]赋予材质属性(表1)。

表1 各部位单元类型和材质属性Tab.1 Unit type and material property of each site
1.3 有限元建模及数据测量
对照组模型所有小关节处设置为接触,摩擦系数为0;椎间盘、髓核、终板相互之间为绑定关系,并通过网格加密方式验证模型的有效性。针对模型网格,采用4万、8万、16万、32万和64万等级的网格加密分析椎骨应力,结果表明,达到64 万个网格数量等级后,结果变化误差在5%以内,兼顾计算效率,椎骨采用50~ 70 万个网格等级。在模型验证通过后,在对照组模型上模拟手术操作,在Pro/E 软件中模拟C5,6椎板切除减压,螺钉置入,建立PVFS组、LMS 组和PS 组三维模型(图1)。导入ABAQUS后,除了前述设置外,螺钉与椎骨、螺钉与连接棒、螺钉与螺帽之间设置为绑定接触。约束C7下终板所有自由度,在C3上终板加载头颅载荷75 N,力矩为1 N/m,以模拟前屈后伸、左右侧曲、左右旋转6 种运动。然后进行计算,提取数据并计算各组C5/C6节段ROM、螺钉及螺钉-骨界面应力。
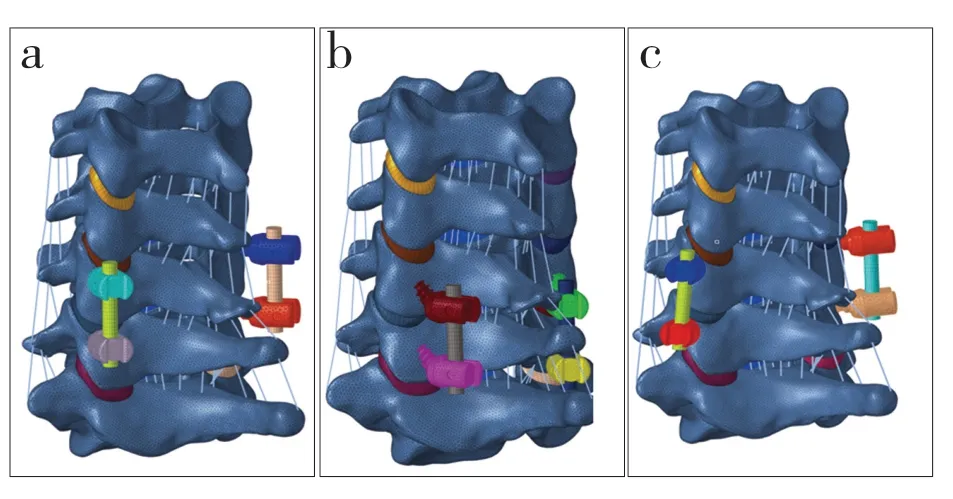
图1 3组有限元模型Fig.1 Finite element model of 3 groups
2 结果
实验建立了正常人下颈椎(C3~7)有限元模型,共获得654 982 个单元,869 841 个节点,通过网格加密方法验证了本模型的有效性。PVFS 组有限元模型获得639 846 个单元,850 923 个节点;LMS 组有限元模型获得2 648 732个单元,859 105个节点;PS 组有限元模型获得650 953 个单元,861 843 个节点。与对照组相比,6 种工况下PVFS、LMS 及PS组C5/C6节段ROM 均降低:前屈(-66.9%,-56.2%,-72.8%),后伸(-53.3%,-49.4%,-63.9%),左侧曲(-60.2%,-55.3%,-64.9%),右侧曲(-61.7%,-57.3%,-65.8%),左旋(-38.8%,-35.4%,-49.1%),右旋(-41.7%,-37.9%,-51.4%)。3 组模型中,PS组ROM 最小,PVFS 组次之(图2)。3 组螺钉应力均主要集中在根部,且在后伸时应力最大;3 组螺钉应力相比,PS 组最小,PVFS 组次之,LMS 组最大(图3)。PS组螺钉-骨界面应力最小,PVFS组次之,LMS 组最大(图4)。3 组螺钉、螺钉-骨界面应力云图见图5~10。
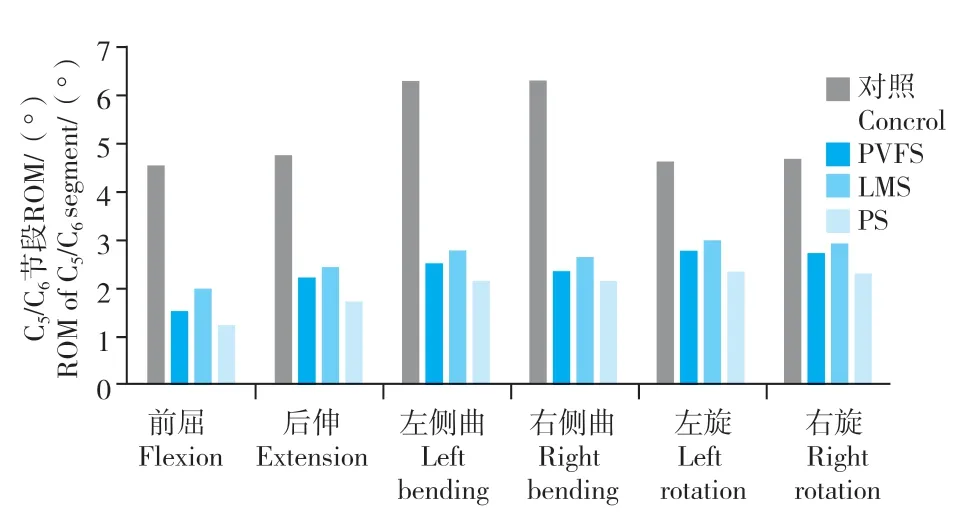
图2 C5/C6 节段ROMFig.2 ROM of C5/C6 segment

图3 各组螺钉所受最大应力Fig.3 Maximum stress on screws of each group
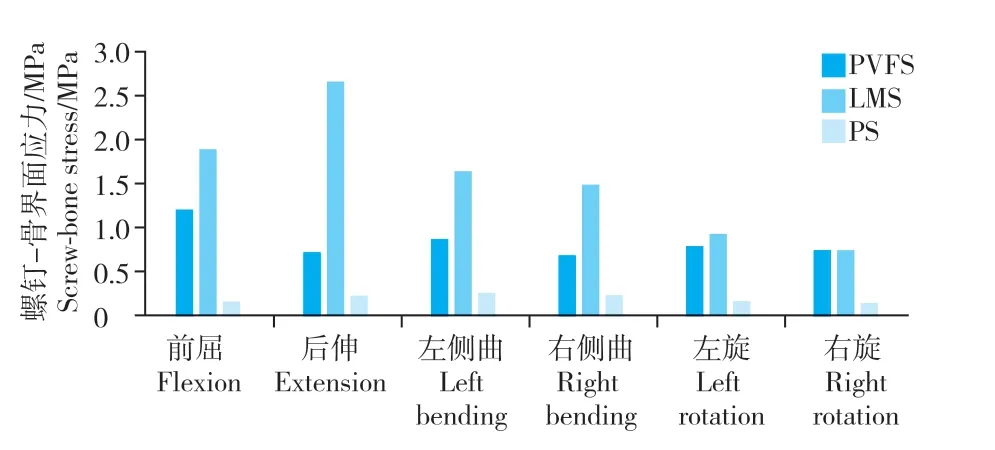
图4 各组螺钉-骨界面所受最大应力Fig.4 Maximum stress on screw-bone interface of each group

图5 PVFS 组螺钉应力Fig.5 Screw stress of PVFS group

图6 PVFS 组螺钉-骨界面应力Fig.6 Screw-bone interface stress of PVFS group
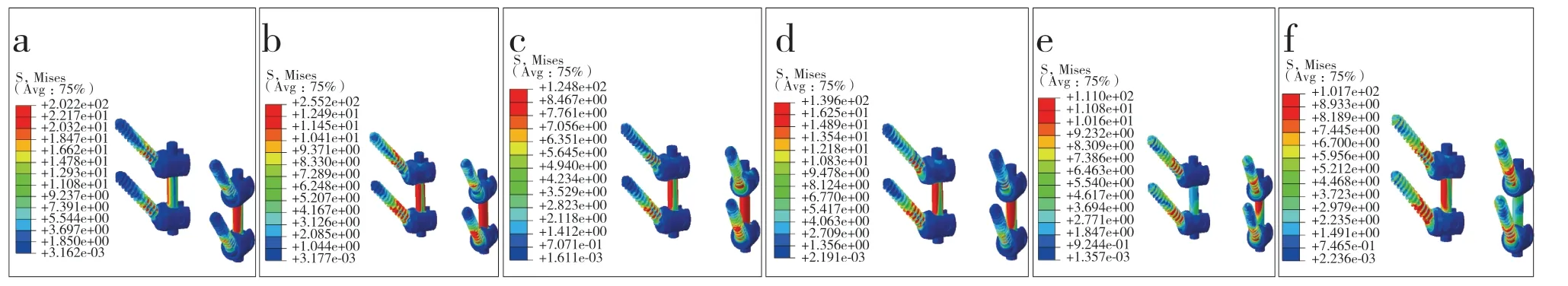
图7 LMS组螺钉应力Fig.7 Screw stress of LMS group

图8 LMS组螺钉-骨界面应力Fig.8 Screw-bone interface stress of LMS group
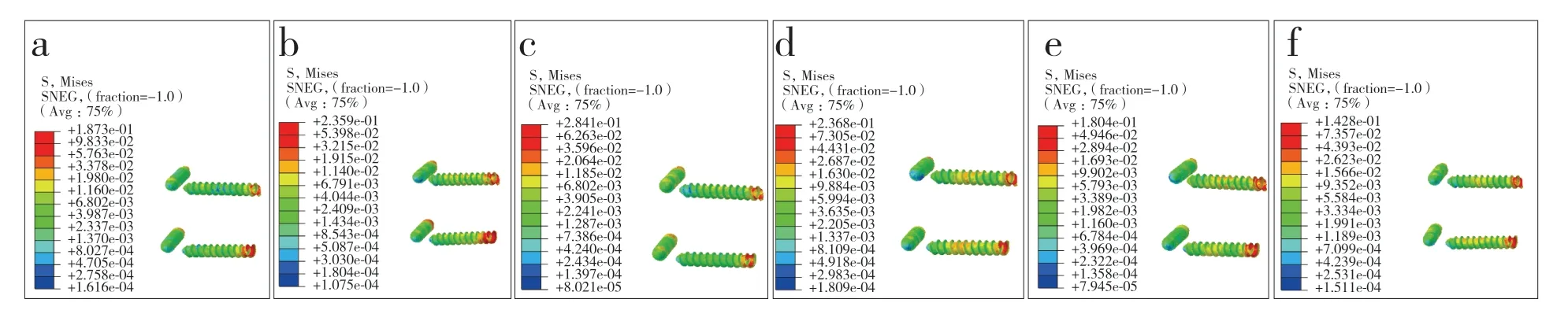
图9 PS组螺钉应力Fig.9 Screw stress of PS group

图10 PS组螺钉-骨界面应力Fig.10 Screw-bone interface stress of PS group
3 讨论
本研究运用三维有限元方法分析了颈椎PVFS、LMS 和PS 生物力学特性,结果表明,在手术节段ROM、螺钉应力及螺钉-骨界面应力方面,PS最小,PVFS 组次之,LMS 组最大。选用“粗短”螺钉的椎间孔内固定技术的术后稳定性优于LMS 内固定,螺钉松动及内固定失败风险低于LMS 内固定,力学优越性仅次于PS内固定。
3.1 稳定性比较
颈椎内固定手术的稳定性至关重要,尤其是对老年骨质疏松患者。在本研究中,3 种螺钉内固定手术节段的ROM 较对照组分别下降了-53.7%、-48.6%和-61.3%,手术节段ROM 的下降提示3 种螺钉均能提供满意的稳定性,且PVFS的固定强度强于LMS,稍弱于PS。既往研究中,在尸体上测量螺钉轴向拔出力是生物力学工程中标准化实验方法,能在一定程度上反映螺钉的固定强度[10]。Maki 等[8]测 得PVFS 的拔出力为(234±144)N、LMS 为(158±81)N;陈希等[11]在老年骨质疏松标本测得PVFS 的拔出力为(327±18)N,LMS 为(305±11)N。上述研究都证实PVFS 的力学强度高于LMS,与本研究结果一致。
颈椎不同解剖位置的骨密度存在明显差异,椎弓根平均骨密度比侧块和椎板高15%[12]。有研究[13-14]证实,螺钉固定轨迹局部的骨密度与螺钉拔出力有关。PVFS 内固定技术,类似短的PS 内固定,螺钉把持了部分椎弓根骨质,解释了PVFS 较LMS具有更强把持力及更高稳定性的原因。Schreiber等[13]报道钉道轨迹CT 值可能与骨密度相关,局部更高的CT 值代表更高的局部骨密度,局部钉道骨密度越高,螺钉获得的把持力更大。Tsuda 等[15]测量了PVFS、LMS和PS的钉道轨迹CT值,结果提示,PVFS 钉道轨迹的CT 值均高于LMS,在C5/C6节段甚至高于PS。
PVFS 钉道轨迹无论是骨密度还是CT 值均高于LMS,再次说明其具有更强的稳定性。Tsuda 等[15]还在PVFS 钉道横断面发现高密度区域,而LMS、PS 钉道未发现。高密度区域的出现可能与颈椎退行性骨质增生有关,而颈椎退行性骨质增生最先发生在关节突关节。PVFS 内固定技术进钉点靠近关节突关节,导致PVFS 能够把持相对坚硬的骨质,从而获得更强的力学稳定性。从进钉点位置、钉道轨迹来看,PVFS 充分把持了坚硬骨质,其力学稳定性可能与PS 相当,这还需要进一步生物力学实验和临床研究证实。
3.2 螺钉应力比较
螺钉的高应力可能会削弱内固定系统的抗疲劳性和长期稳定性,增加不融合的风险。本研究结果显示,PVFS 和PS 在侧曲和旋转时所受应力相近,均小于LMS;在前屈后伸时,PS 组最小,PVFS 组次之,LMS 组最大。长期高应力容易致使螺钉疲劳性断裂,导致内固定失败。Shimizu 等[16]报道,在PVFS 的临床应用中发生3 枚螺钉松动断裂,均发生在固定节段的两端,中间节段没有出现松动、断裂,故中间节段固定时建议使用PVFS固定。
3.3 骨-螺钉界面应力比较
骨-螺钉界面松动是颈椎内固定失败的常见原因,临床上LMS 松动发生率更高[17]。从本研究应力云图(图5~ 10)上可观察到3 种螺钉骨-螺钉界面最大应力主要集中在螺钉头部的骨质。长期高应力作用导致骨质被破坏,螺钉松动应先发生在头部。Weiser等[18]对疲劳测试后的椎体进行CT检查发现,螺钉头部周围出现骨质缺损,说明螺钉松动是螺钉周围骨质逐步破坏的过程。
本研究结果显示,PS 螺钉-骨界面平均应力最小,PVFS 次之,LMS 最大,螺钉松动的概率也依次增大。但螺钉松动还与螺钉的直径和长度相关[19],螺钉直径对拔出力强度和维持螺钉周围骨质的存续具有积极的作用,使用粗螺钉可把持更多的骨质,若要破坏骨质需承受更大应力;在螺钉头部骨质破坏后松动开始,增加螺钉置入深度能够避免螺钉脱出。本研究中PVFS组采用直径为4.5 mm的粗螺钉,PS 组螺钉(24.0 mm)较PVFS 和LMS 长,对维持术后稳定性有重要作用。
3.4 研究局限性
本研究仅对单节段内固定进行了比较,多节段内固定实验可能会出现不同的结果。Shimizu等[16]的PVFS 临床研究发现,固定节段两端采用PVFS 更容易发生断裂、松动,多节段PVFS 内固定是否会出现固定节段两端螺钉-骨界面应力比中间节段更大,这还需进一步的研究。
对于骨质疏松或需要坚强内固定的颈椎病患者,往往需要后路内固定来增强颈椎稳定性。本研究的有限元模型是基于具有良好骨质的年轻志愿者建立的,模型的骨皮质、骨松质的弹性模量和泊松比设置也是参考既往常规模型设置。有研究[20-21]通过降低骨皮质、骨松质的弹性模量,结合老年患者CT 数据来建立“骨质疏松”的颈椎有限元模型。杨九杰等[21]通过上述方法建立“骨质疏松”颈椎内固定重建模型,与正常骨质内固定重建模型相比,固定节段ROM 明显增加,需要通过增加钢板厚度来获得相同的稳定性,但其并未对螺钉和螺钉-骨界面应力进行分析比较。因此,PVFS 在骨质疏松椎体中的力学性能还需进一步建立更加逼真的“骨质疏松”模型来加以分析。
综上,与传统颈椎后路内固定方式相比,PVFS能够提供良好稳定性,可以作为后路内固定方式的一种补充。

