UPLC-MS/MS 法测定软糖中低添加量甲钴胺含量
◎ 蔡桂珠,林岱滨,张敬锴
(广东亿超生物科技有限公司,广东 汕头 515000)
目前,作为可以对人体产生治疗或保健作用的维生素B12有氰钴胺、羟钴胺、腺苷钴胺和甲钴胺[1]。其中,甲钴胺对神经组织具有良好的传递性,可促进核酸-蛋白-脂肪的代谢,可修复损伤了的神经组织,临床上多用于糖尿病神经障碍、多发性神经炎等周围神经疾病[2]。
当前,国内的甲钴胺片中甲钴胺添加量大部分是0.5 mg/片,2020 版《中国药典》也针对相应的规格制定标准检测方法[3]。
甲钴胺在美国市场作为维生素B12缺乏症的补充剂被广泛使用[4-8],国内也有报道使用HPLC 方法测定类似添加级别的软糖产品的含量测定方法[9]。因此,开发一个可用于产品中甲钴胺低添加量的含量测定方法,对于国内外贸出口膳食补充剂生产企业相关产品的质量控制具有参考意义。
1 方法
1.1 仪器与试药
QTRAP 4500 超高效液相色谱-串联质谱仪(SCIEX)、多管式涡旋混合器;甲钴胺对照品(93.9%)(中国食品药品检定研究院),批号:100692- 202006;乙腈(HPLC 级)(美国默克),含量≥99.90%;甲酸(HPLC 级)(美国默克),含量≥99.90%。
1.2 色谱条件
色谱柱:ACQUITY UPLC BEH C18 2.1×50 mm(1.7 μm),序列号:04223208 115169;流动相:乙腈(A)-0.1%甲酸(B),梯度洗脱(见表1);柱温:40 ℃;进样体积:10 μL。
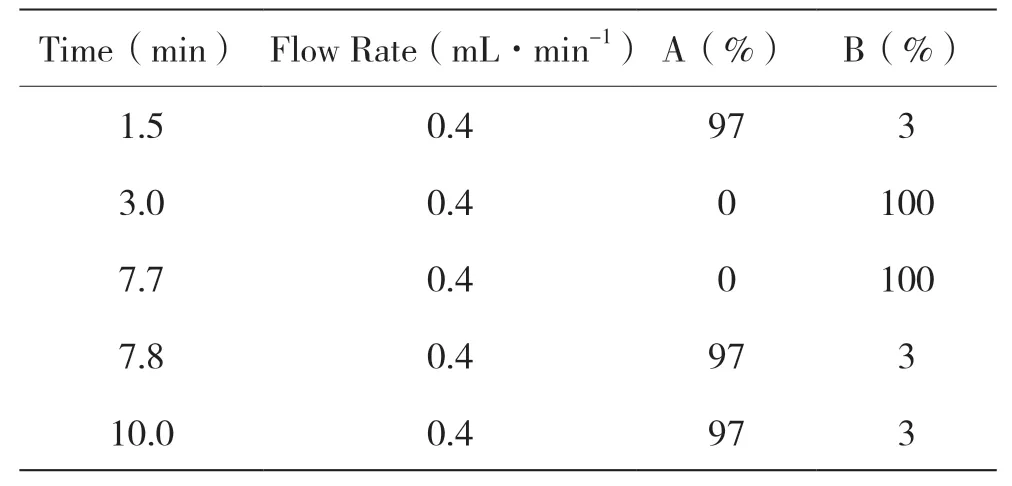
表1 梯度洗脱条件表
1.3 质谱条件
离子源模式:ESI,正模式,MRM;IS:5500;TEM:500;GAS1: 50;GAS2:60;离子对信息见表2。
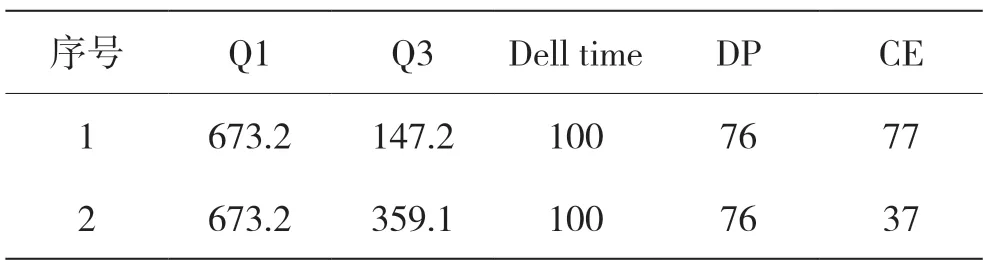
表2 离子对信息表
1.4 供试品溶液制备
称取1.0 g 含有甲钴胺的软糖于50 mL 具塞塑料离心管中,加水至20 mL,密塞置于多管式涡旋混合器,2 500 rpm 涡旋10 min。然后置于高速离心机,10 000 rpm 离心2 min。上清液经0.22 μm 滤膜过滤,收集滤液,即为供试品溶液。
1.5 标准曲线制备
准确称取适量甲钴胺标准品加水溶解定容,配制成浓度为0.1 mg·mL-1的甲钴胺标准储备溶液,棕色瓶保存。分别吸取一定体积的甲钴胺标准储备溶液,加水稀释,制备一系列标准溶液,标准工作曲线溶液浓度为10、20、100、200、1 000 ng·mL-1,按上述色谱条件,采用超高效液相色谱-串联质谱仪分析,以浓度为横坐标,以测得峰面积为纵坐标绘制标准曲线。
1.6 测定方法
将供试品溶液按上述色谱条件进行超高效液相色谱-串联质谱仪测定,采用外标法通过上述标准曲线计算其浓度。
2 方法学验证
照ICH Q2(R1)Validation of Analytical Procedures:Text and Methodology 开展方法学验证活动。
2.1 专属性
取甲钴胺软糖阴性样品,依上述方法制备处理、检测,测定图谱如下所示。由图1、图2 可知,不存在干扰情况。因此,该色谱-质谱条件可行。
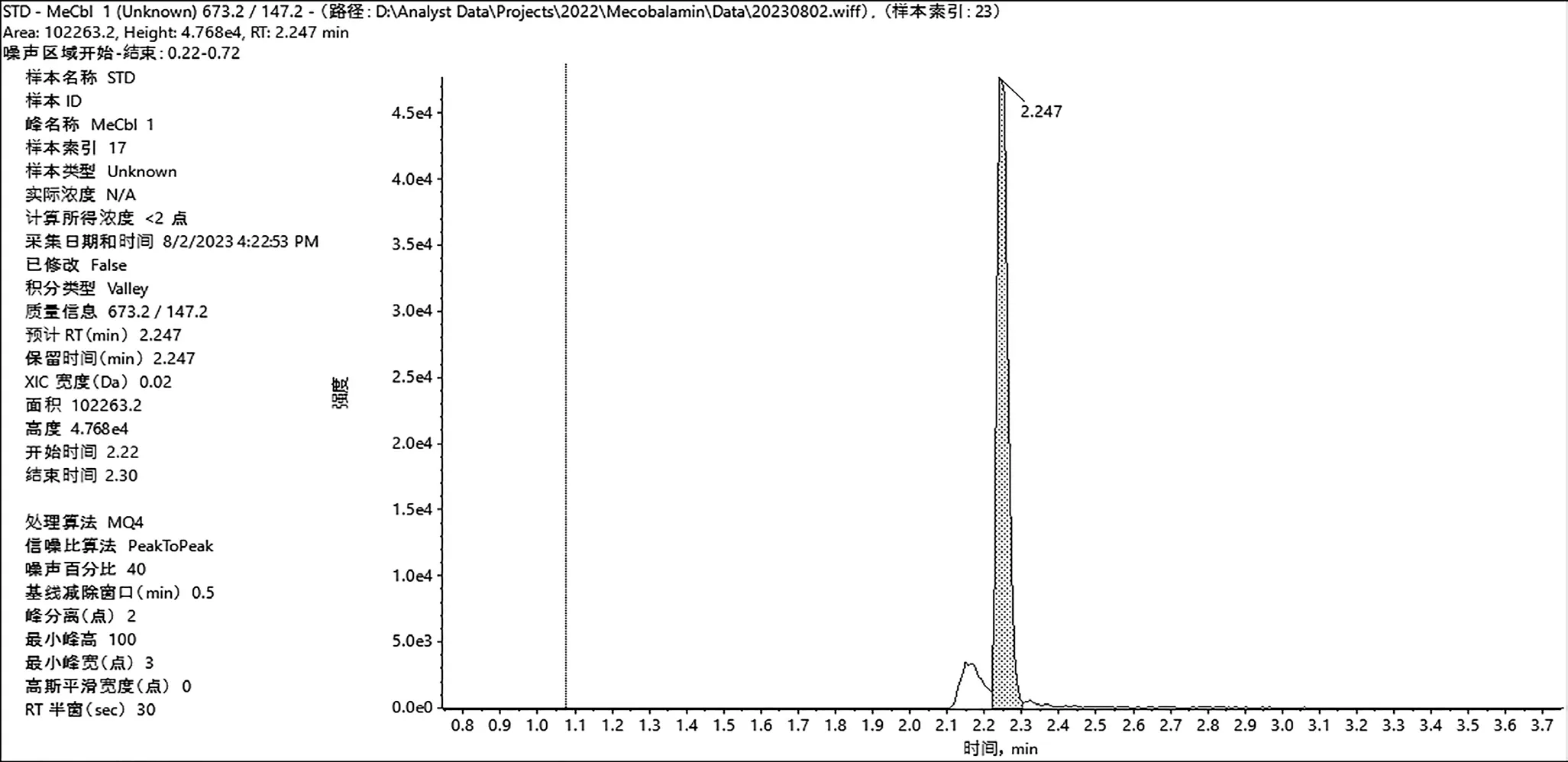
图1 对照品图谱图
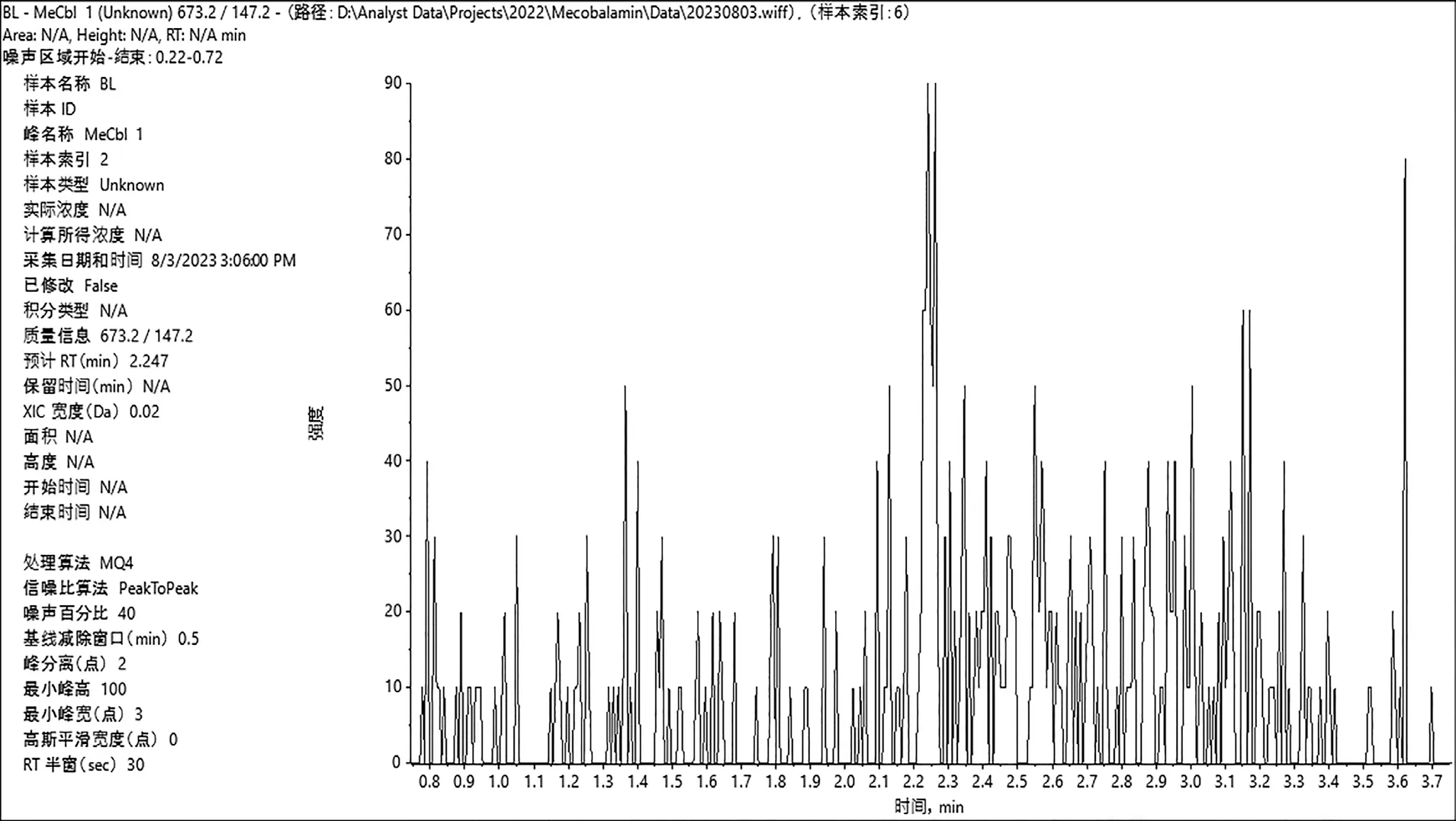
图2 甲钴胺阴性样品图谱图
2.2 线性范围与检测限、定量限
配制甲钴胺浓度为10、20、100、200、1 000 ng·mL-1的曲线,拟合获得回归方程为y=76.461x-768.11,R2=0.999 8,表示在10~1 000 ng·mL-1浓度范围内,有良好线性。
分别取甲钴胺软糖阴性样品加标,信噪比法测定,结果显示溶液浓度为10.91 ng·mL-1时,信噪比为13.31,即在供试品称样量为1 g,稀释倍数为50 mL 时,测得甲钴胺检出限约为0.2 μg·kg-1,定量限约为0.5 μg·kg-1。
2.3 精密度与准确度
取甲钴胺软糖阴性样品,分别加入一定量的甲钴胺标准品溶液,依上述方法制备处理、检测,使之成为理论浓度分别约为20、100、500 ng·mL-1的样品,每个浓度平行操作3 份,照1.2 色谱条件、1.3 质谱条件上机测定,计算各组样品含量的RSD%(结果见表3)。
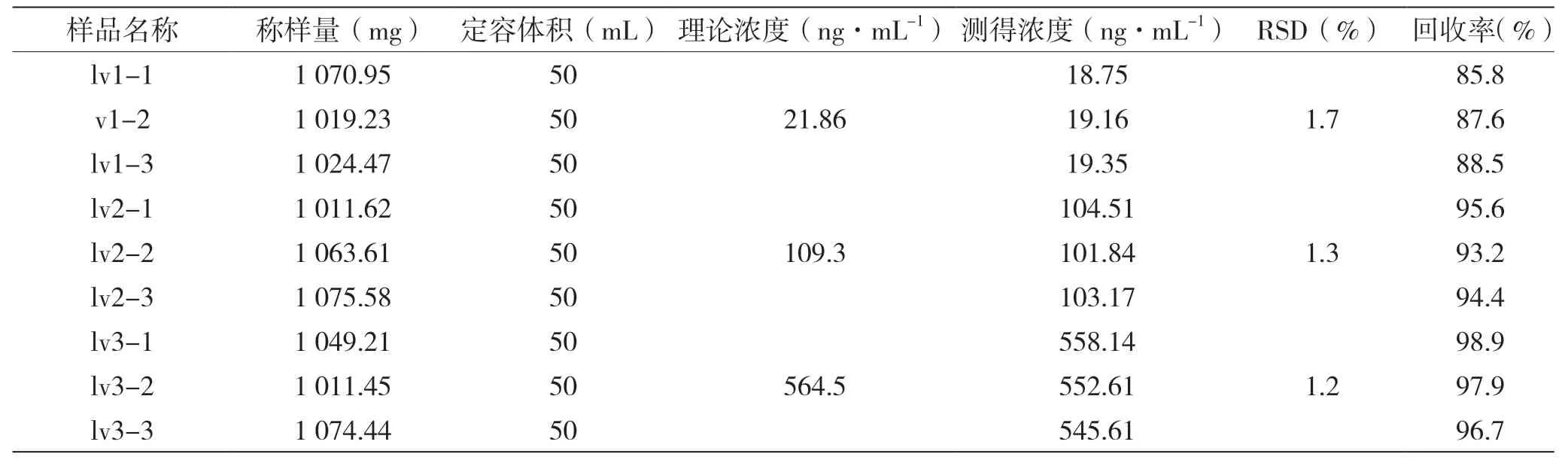
表3 测定甲钴胺软糖阴性样品精密度和准确度表
试验结果显示,甲钴胺软糖阴性样品3 个浓度水平加标准确度分别为1.7%、1.3%、1.2%,3 个浓度水平加标回收率在85.8%~98.9%,均达到可接受标准。
3 结语
实验结果显示,该方法在10~1 000 ng·mL-1有良好线性;在小于0.1 mg·kg-1的添加级别,精密度RSD 为1.2%~1.7%,符合RSD ≤5% 的要求;在小于0.1 mg·kg-1的添加级别,加标回收率为85.8%~98.9%,符合60%~120%的要求[10]。因此,该方法可为软糖中较低含量的甲钴胺测定提供参考依据。

