复发性新生儿坏死性小肠结肠炎27 例临床分析
林洁楠,刘慧慧,林晨越,寿铁军
新生儿坏死性小肠结肠炎(NEC)是新生儿尤其早产儿阶段一类较严重的胃肠道疾病,其主要临床特征是急性肠缺血和坏死。目前对于NEC 缺乏针对性的特殊治疗,主要为禁食、胃肠减压、抗生素及手术治疗等。而在治疗成功的NEC 患儿中,4%~10%的患儿可能会出现复发,即复发性新生儿坏死性小肠结肠炎(RNEC)[1]。目前对RNEC 的研究较少,此外临床上不少复发病例还呈爆发性进展致死的情况。因此,寻找RNEC 的影响因素,寻找早期诊断、评估RNEC的指标并尽早进行干预具有重要意义。基于此,本文回顾性分析27 例RNEC 患者的临床资料,探索有关NEC 复发的影响因素,现报道如下。
1 资料与方法
1.1 一般资料 选取2019 年11 月至2022 年1 月期间宁波市妇女儿童医院收治的RNEC 患儿27 例(复发组,n=27),同期选取109 例单发的NEC 为对照组,其中复发组根据复发时是否手术又分为保守组(n=18)和手术组(n=9)。纳入标准:(1)符合《实用新生儿学》及改良Bell分期诊断标准[2-3],且临床诊断为NEC 的患儿;(2)于出生后28 d 以内初次发病;(3)单发组患儿至2022 年底均未复发;(4)复发组患儿为NEC 初次发病经治疗后恢复到完全喂养后1个月再次确诊;(5)患儿及孕母病历资料真实且相对完整。排除标准:(1)具有先天性消化道畸形、先天性胆道闭锁、有腹部手术史的病例;(2)资料缺失较多或转入其它医院的病例。本研究经宁波市妇女儿童医院医学伦理委员会审批通过。
1.2 方法 从电子病历系统中收集患儿的病例资料:一般资料,包括性别、胎龄、出生体质量、确诊日龄、住院天数、喂养方式、Bell分期及疾病转归;围产因素,包括胎膜早破有无、分娩方式、有无宫内感染、有无产前使用激素、有无产前使用抗生素、新生儿窒息史及Apgar评分;患儿相关合并情况,包括有无合并败血症、新生儿高胆红素血症、凝血功能障碍、呼吸窘迫综合征、新生儿贫血、有无行新生儿脐静脉置管术(UVC)或中心静脉置管(PICC)、治疗时是否使用枸橼酸咖啡因及确诊前24 h 有无输注红细胞(RBC);影像学检查,包括腹部X片评分及腹部超声评分[4];实验室检查,包括患儿确诊前24小时的RBC、白细胞(WBC)、血小板(PLT)、中性粒细胞百分比(GR%)、C 反应蛋白(CPR)、降钙素原(PCT)、D-二聚体(D-D)、纤维蛋白原、乳酸、血糖及pH 值。
1.3 统计方法 采用SPSS 26.0 统计软件进行数据分析,计数资料采用检验;计量资料以均数±标准差或中位数(四分位间距)表示,组间比较采用t或Mann-Whitney U 检验。P <0.05 表示差异有统计学意义。
2 结果
2.1 两组一般资料比较 两组患儿性别、确诊日龄、喂养方式差异均无统计学意义(均P >0.05);胎龄、出生体质量及住院天数差异均有统计学意义(均P<0.05),见表1。所有病例在确诊时均根据改良Bell 分期诊断标准进行评分。其中单发组IA 11 例,IB 11例,II A 70 例,II B 14 例,IIIA 1 例,IIIB 2 例;复发组患儿中IA 4 例,IB 4 例,IIA 18 例,IIIB 1 例。两组改良Bell 分期差异无统计学意义(=4.954,P >0.05)。单发组84 例行保守治疗,25 例因病情迅速进展且保守治疗无效(如发生门静脉积气、气腹、腹壁红斑及肠坏死等)行手术治疗,患儿均预后良好,无死亡病例。复发组中18 例行保守治疗,9 例行手术治疗,其中3例于术后死亡,死亡病例术中可见肠道广泛坏死。
2.2 两组围产因素比较 两组胎膜早破、产前激素和抗生素的使用、新生儿窒息史及Apgar 评分差异均无统计学意义(均P>0.05);两组分娩方式、宫内感染差异均有统计学意义(均P <0.05),见表2。

表2 两组围产因素比较 例(%)
2.3 两组患儿合并症情况比较 两组合并新生儿败血症、呼吸窘迫综合征、新生儿贫血及确诊前48 h输注RBC 差异均无统计学意义(均P >0.05);两组合并新生儿高胆红素血症、凝血功能障碍、行UVC 或PICC 操作及使用枸橼酸咖啡因差异均有统计学意义(均P <0.05),见表3。
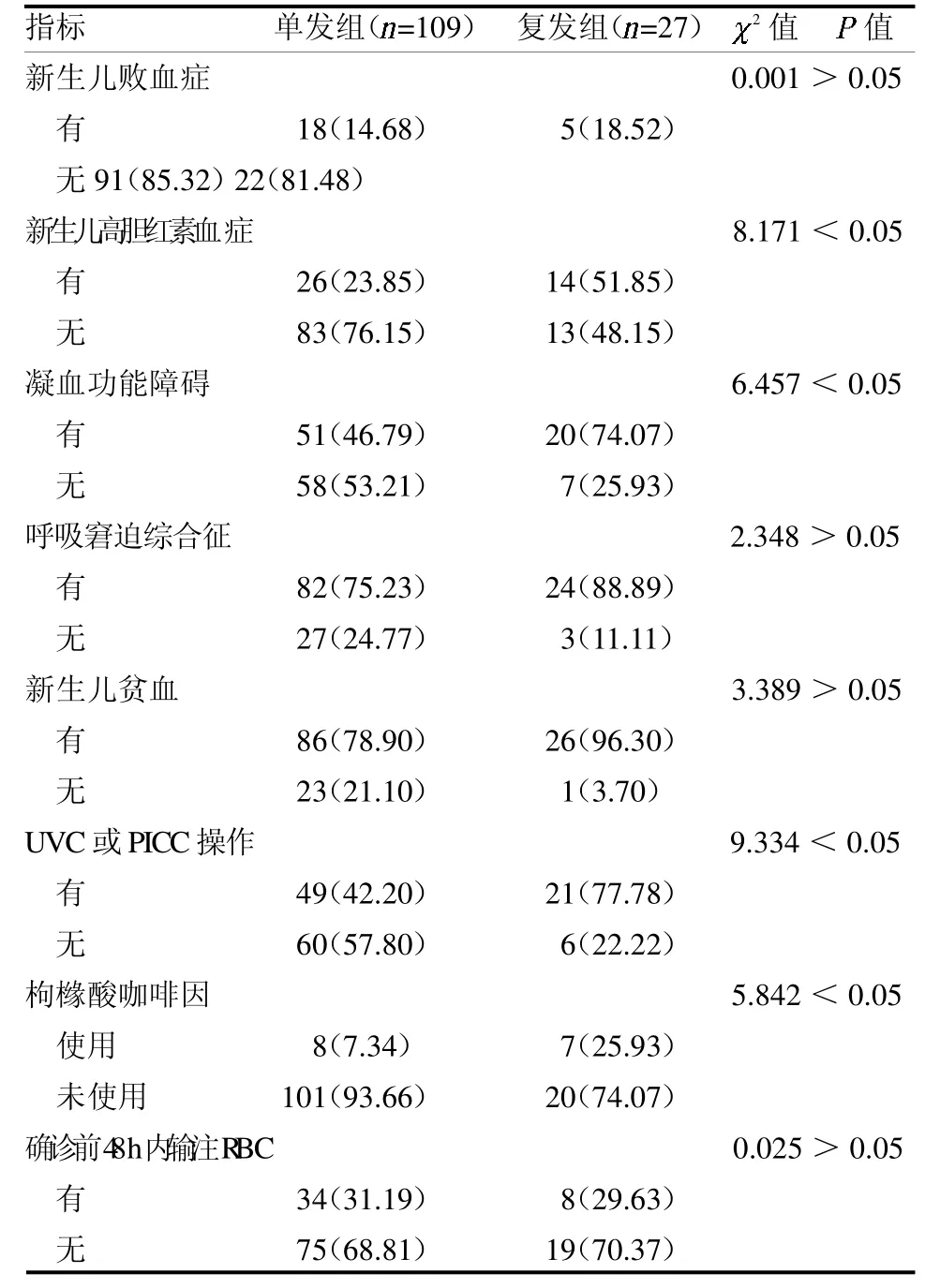
表3 两组患儿合并症情况比较 例(%)
2.4 复发组治疗方法的影响因素分析 根据复发时是否手术分为保守组(n=18)和手术组(n=9)。两组X 线评分、RBC、PLT、GR%、CRP、血清白蛋白、纤维蛋白原、血糖及pH 值差异均无统计学意义(均P >0.05);两组超声评分、WBC 及乳酸差异均有统计学意义(均P >0.05),见表4。

表4 复发组不同治疗方式的分组比较
3 讨论
NEC是一种急进性的获得性新生儿肠道炎症性急症,早期表现为喂养不耐受、胃潴留、腹胀、呕吐及血便等,目前主要采用Bell 评分为主要诊断标准。目前有关NEC的研究主要集中在初次患病的患儿,对于复发性患儿则涉及较少。
NEC 的复发可能与早产、极低出生体质量、重大先天性异常或持续性心血管损伤相关[5]。本研究结果显示新生儿胎龄及出生体质量与NEC 复发有关,这与上述文献结论相符。胎龄越小,新生儿肠道越脆弱,此时肠道中有益菌群数量较少,肠道屏障发育不成熟,通透性高。相比于足月儿,早产儿在受到病原菌刺激后易引起过度反应,引起肠道损伤甚至坏死。
研究显示,宫内感染、胎盘早剥、产前药物暴露及孕期吸烟等均为NEC发病的高危因素[6-7],本研究也发现宫内感染与NEC 复发有关。羊水是首先进入胎儿肠道的液体,吞咽羊水带来的促生长发育作用约占胎儿生长发育的15%[8],当羊水感染时,细菌及其产物可通过消化道途径进入胎儿体内,导致炎症细胞的合成以及炎症介质的大量释放,引起新生儿肠黏膜坏死[9]。此外在研究中发现分娩方式与NEC复发有关,这与相关报道相一致[10],分析原因可能是分娩时病原菌进入胎儿体内造成感染。
本研究发现合并新生儿高胆红素血症或凝血功能障碍与NEC 的复发相关。这两种合并症均与促进肠道血栓形成相关,并能够增加患儿肠道负荷,从而进一步加重肠道损伤[11-12]。此外本研究发现,UVC或PICC及治疗时使用枸橼酸咖啡因也与NEC复发相关,UVC 或PICC 置管不当可引起胃肠道血液循环出现障碍,造成胃肠道功能异常[13];而枸橼酸咖啡因的使用会刺激患儿呼吸中枢,增加每分钟通气量,同时增加机体对二氧化碳升高的敏感性,降低二氧化碳的阈值,会引发心动过速、婴儿喂养不耐受等情况,并会加重肠道负担[14-15],甚至引起NEC 复发。
研究显示,NEC 会引起炎症指标升高[16],PCT、CRP、PLT 及血清蛋白等血清学标志物可以帮助判断NEC的手术最佳时机[17],这与本研究的部分结论相类似。NEC 患儿的WBC 计数可以升高、正常或降低,而WBC 计数降低的患儿往往预后更差。本研究发现WBC和乳酸在RNEC患儿保守与手术间比较有差异,RNEC 手术组患儿白细胞水平更低,分析原因可能与RNEC手术组患儿感染更重,导致机体免疫应答异常,白细胞产生了贴壁现象甚至向血管外迁移有关。
相关研究表明,超声检查可以对肠道进行形态、血流分布、肠蠕动特点和肠道外间接征象等进行综合分析,更有利于早期识别NEC 患儿危重症,还可以作为判断NEC 患儿手术时机的参考依据[18]。与X 线相比,超声相对更细致和全面[19-20]。因此在临床上推进NEC 患儿超声检查的应用有重要意义。
本研究仍存在一定不足:本研究仅对在本院住院治疗的病例进行分析研究,未对转入其他医院的病例进行跟踪;纳入病例出院后虽均于本院门诊复查,但并未对其远期的生活质量、喂养情况等相关资料进行进一步综合分析评估。这也为接下来进一步的研究提供了思考。
利益冲突 所有作者声明无利益冲突

