非瘢痕子宫妊娠子宫不完全性破裂1例并文献复习
王敏,安荣,张静,齐琦,许飞雪,2*
(1.兰州大学第一临床医学院,兰州 730000;2.兰州大学第一医院妇产科,甘肃省妇科肿瘤重点实验室,兰州 730000)
一、病例资料
患者,女,34岁,G2P1,主因“停经9月余,间断阴道流液1 h余”于2023年3月12日收住兰州大学第一医院产科。平素月经规律,初潮14岁,经期5 d,月经周期30 d,月经量中,色暗红,偶有痛经及血块,末次月经:2022年6月8日。患者曾因双侧输卵管梗阻于我院生殖中心移植鲜胚2枚,两周后查血β-HCG阳性,B超检查提示单枚胚胎存活,确诊宫内孕。停经40余天出现恶心、呕吐、乏力、嗜睡等早孕反应,上述症状未予特殊处理,持续2月后自行消失,孕早期无放射线及有毒物质接触史,未服过药物。孕中晚期无头晕、眼花、双下肢水肿等不适。定期产前检查,孕期产检无异常,孕程顺利,无保胎史。2023年3月12日02:00无明显诱因出现阴道流液,色清,量少,无阵发性下腹痛,无阴道流血,无肛门坠胀感,自觉胎动正常,我科以“(1)胎膜早破;(2)体外受精-胚胎移植(IVF-ET)术后;(3)妊娠39+4周,G2P1,头位”收住。既往史:患者2021年因双侧输卵管梗阻于当地医院行腹腔镜下双侧输卵管通液术。婚育史:已婚,配偶体健。曾于2012年顺产1足月活女婴,产程顺利,其女现体健。否认结核、肝炎等传染病史及接触史,否认食物、药物过敏史。个人史及家族史无特殊。
入院查体:体温36.2℃,心率87次/min,呼吸20次/min,血压123/86 mmHg。腹膨隆与孕周相符,宫底剑突下3指,胎位头位,胎心148次/min,内诊:宫颈居中,质中,宫口未开,胎膜已破,羊水清亮,先露部棘上3 cm,骨盆内测量未见明显异常。入院后完善相关检查检验,产科超声检查示:(1)宫内妊娠,单活胎;(2)胎儿脐动脉血流频谱正常范围,胎位头位,双顶径95 mm,股骨长69 mm,腹围365 mm,羊水深度57 m;胎盘位于子宫前壁,厚度24 mm,胎盘成熟度Ⅰ级;胎儿脊柱排列整齐,颈部未见脐带压迹及彩色血流环绕,四腔心结构可见,胎心胎动(+),彩色多普勒血流显像(CDPFI):可见胎心搏动血流信号,脐动脉两条;脐动脉血流测定:脐动脉收缩期最大峰值流速(S):47 cm/s,脐动脉舒张末期流速(D):21 cm/s,S/D值:2.3,心率(HR)140次/min。肝功能各项指标:白蛋白(ALB)39.8 g/L(正常参考值40~55 g/L),碱性磷酸酶(ALP)174.3 U/L(正常参考值35~100 U/L),总胆汁酸(TBA)14.1 μmol/L(正常参考值0.5~10 μmol/L);血常规:C-反应蛋白(CRP)4.77 mg/L(正常参考值0~4 mg/L);术前出凝血指标+D-二聚体检测:活化部分凝血活酶时间(APTT)23.8 s(正常参考值25.4~38.4 s),D-二聚体:1.68 μg/ml(正常参考值0~0.5 μg/ml),纤维蛋白原降解产物(FDP)4.59 μg/ml(正常参考值0~2.01 μg/ml),余检查指标无明显异常。
考虑到孕妇破膜时间大于12 h,入院后给予头孢呋辛钠预防感染,缩宫素2.5 U静脉泵入行引产治疗。患者病情发展详细信息见表1。
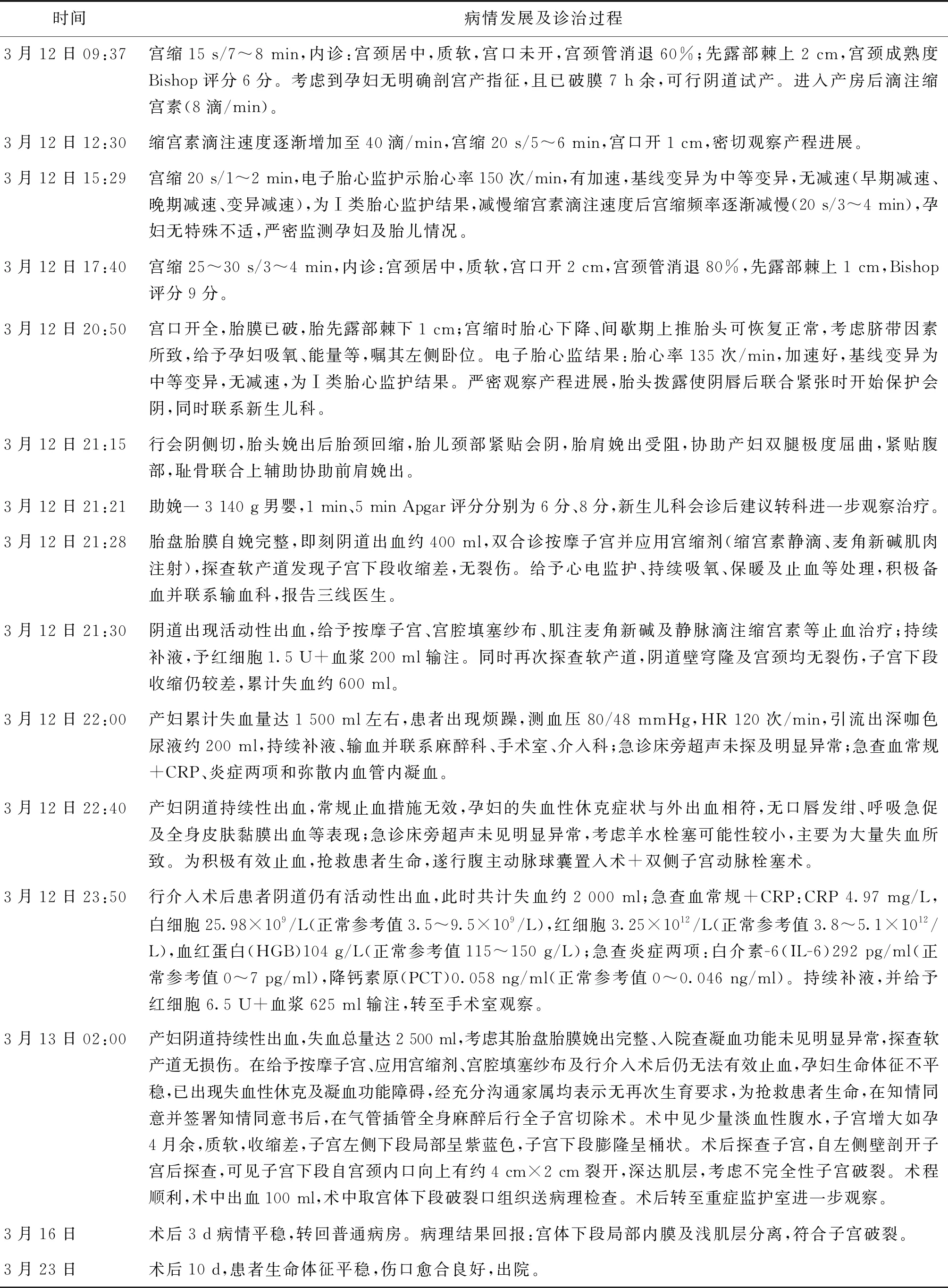
表1 患者病情发展及诊治过程
二、讨论
子宫破裂是产科的严重并发症,因子宫破裂导致的孕产妇死亡率约为1.4%,新生儿死亡率约为12%,孕产妇子宫切除术率为20%~31%[1-2]。子宫破裂大多继发于有子宫瘢痕的孕产妇,而瘢痕的定义不再局限于剖宫产所导致的子宫瘢痕,妇科侵入性操作所导致的瘢痕也包括在内。近年来在临床工作中发现非瘢痕子宫破裂(Unscarred Uterine Rupture,UUR)的发病率有所上升,其主要原因包括多次人工流产清宫术、子宫肌瘤剔除术以及前次分娩时宫腔操作等。在You等[3]纳入研究的30例子宫破裂患者中,6例孕妇为URR,其中3例既往有宫腔操作史。URR虽不常见,但却会对孕产妇及新生儿造成潜在的、不可预测的生命危险,因而对其进行深入分析研究是极有必要的。
1.URR的危险因素:URR破裂多发生于妊娠晚期[3],相较于瘢痕子宫破裂,URR没有明确的病因。回顾关于URR的文献发现,导致UUR发生的危险因素包括高龄(≥35岁)、医源性子宫穿孔、腹部创伤、子宫结构先天异常(双子宫等)、多产次、多胎妊娠、引产药物使用不当、胎盘植入、头盆不称及较短的妊娠间隔期等[3-6]。此外,遗传因素也在其中发挥一定作用,有文献报道埃莱尔-当洛综合征(Ehlers-Danlos syndrome,EDS)Ⅳ型可导致URR、早产、围产期出血、大血管破裂等[7]。还有文献报道,子宫动静脉畸形、子宫憩室及子宫内膜异位症会影响子宫壁的容受性,也可能是URR的高危因素[8]。但是,这些因素导致URR发生并不常见,对临床实践指导意义不大。
关于辅助生殖技术(ART)是否是URR发生的危险因素,目前尚无研究证实。虽然行ART后发生URR在文献中也有报道,但此类患者在行ART之前大多有高龄、多次清宫、子宫肌瘤剔除、输卵管切除等病史,这无法明确说明ART是URR发生的直接危险因素[9]。Takashima等[10]报道了1例患者在行IVF-ET术后,孕11周时发生了自发性子宫破裂,分析其原因可能是因为发生了剖宫产瘢痕部位妊娠(CSP),但关于IVF-ET与子宫破裂之间是否存在一定的因果关系尚无法得知。
结合文献分析本例孕妇发生URR的原因,该孕妇因双侧输卵管梗阻行腹腔镜下双侧输卵管通液术,术后仍未受孕而行IVF-ET助孕,两次手术操作及术中存在电热损伤都可能与本次发生子宫破裂有关。本例孕妇系第2次妊娠,详细询问病史,该孕妇无妇科子宫手术操作史,自诉第1次阴道分娩过程顺利,无骨盆狭窄、头盆不称及胎位异常等导致梗阻性难产的因素存在,胎盘胎膜自娩完整,产后出血不多。因此,考虑第1次阴道分娩中存在子宫损伤的可能性较小。URR的发生是多种因素相互作用的结果,往往非单一因素所致,在临床工作中应全面详细询问病史,提高对URR发生的警惕性,告知患者相关注意事项,最大程度地降低因发生URR导致的对孕产妇及新生儿的伤害。
2.URR的临床表现与诊断:由于URR发生的病因、位置、大小等各异,临床表现也各有不同。典型的URR征象主要表现为电子胎心监护异常、急性腹痛和阴道出血,部分可出现低血压、低血容量性休克、血尿、呕吐、腹部压痛等表现[9,11]。此外,破裂发生的时间和部位不同相应的临床表现也会有所差异。例如,子宫下段发生破裂时可能会出现典型的子宫破裂征象,而宫底部破裂时血液在腹腔内积聚,腹膜刺激症状轻,临床症状不典型[12-13],甚至部分仅表现为剖宫产时偶然发现的隐匿性子宫破裂[4],因此,URR通常不易引起临床医生的重视,容易出现诊断延误,因而采取手术干预的时机也较晚。本例患者亦是如此,由于其病变和临床表现不典型,在阴道活动性出血无法有效治疗时行全子宫切除术后剖查子宫才发现了子宫下段破裂。
目前,仅凭临床表现及体格检查很难诊断URR,影像学检查如超声、CT和磁共振成像对于早期诊断有一定的提示作用。超声检查可发现妊娠位置异常、子宫壁薄和胎盘附着异常等[14]。有研究报道,妊娠中晚期子宫下段厚度小于2.3 mm与分娩期间严重并发症(如子宫破裂和出血)的发生相关,但目前还没有理想的诊断方法推荐[15]。对于原有的解剖结构已发生改变或超声检查无法诊断的孕妇,使用磁共振成像作为一种额外的诊断工具可能有一定作用[16]。不可忽视的是,因为在临床工作中没有特异有效的诊断及预测手段,临床医生更应该全面综合分析患者的一般情况及各项检查、检验结果,动态观察患者的病情变化,最大程度避免遗漏诊断。
3.URR的管理和预后:早期手术干预和有效的胎儿及新生儿复苏是子宫破裂成功治疗的关键。治疗的目的主要是有效止血,修复子宫损伤,降低孕产妇和胎儿的死亡率[9]。根据患者的情况和外科医生的专业能力进行破裂部位的手术修复或全/次全子宫切除。子宫切除术适用于孕妇生命体征不平稳,经评估需切除子宫者,最终是否进行子宫切除术取决于患者的生育要求、子宫的损伤程度、患者的血液动力学情况,以及产科医生修复复杂性子宫破裂的技术等。对于既往有子宫破裂的孕妇在胎儿胎肺成熟后应立即进行择期剖宫产[10,13]。必须强调的是,非瘢痕子宫妊娠期自发性子宫破裂是子宫切除的独立危险因素[17]。本例产妇阴道持续性出血,初步评估病情后考虑为大量失血所致,行腹主动脉球囊置入术+双侧子宫动脉栓塞术后仍无法有效止血,产妇生命体征不平稳,开腹探查切除子宫后探查子宫才发现子宫下段不完全性破裂。
关于子宫破裂孕妇的临床结局,目前尚无统一结论。一些研究比较了瘢痕子宫和无瘢痕子宫发生子宫破裂后孕产妇及新生儿临床的结局,发现URR的损害性更大,胎儿死亡率更高[18]。一方面是URR临床表现隐匿且不典型,发现时机较晚;另一方面是因为瘢痕子宫破裂多发生在上次的瘢痕处,而URR多发生在子宫肌层,该区域血管相对较多,大出血风险高[4]。一项回顾性研究发现URR的新生儿胎龄明显大于瘢痕子宫破裂者,且新生儿体重也较重[3]。Arbab等[14]认为近一半的原发性子宫破裂病例在确诊前均通过阴道分娩,而经阴道分娩发生子宫破裂的病例比经剖宫产分娩发生破裂的病例接受全子宫切除术可能性更大。由于对URR的警惕性不高,发生产后出血时采取的所有措施都集中于治疗子宫收缩乏力,此类的延迟诊断也导致了较高的子宫切除率。但Ofir等[19]进行的研究发现瘢痕子宫破裂与URR比较,二者导致的孕产妇或围产儿发病率没有显著差异,孕产妇失血量亦无显著差异,且与正常分娩相比,URR产妇的分娩过程比较顺利[3]。关于远期妊娠的风险,部分行子宫修补术的URR患者在子宫修补术后会发生复发性破裂,峡部区发生破裂者进行修补后多无剖宫产并发症,但宫底部发生破裂的患者在修补后的几周可能再次出现复发性破裂[5]。对于既往有UUR病史且保留子宫的患者其最佳受孕时间和选择性剖宫产的时机在既往文献中尚没有达成共识,未来仍需临床大数据深入分析研究。
虽尚未证实IVF-ET是URR的直接危险因素,但在因输卵管因素不孕的患者中它可能是一个促进因素。对于通过IVF-ET受孕并出现急性腹痛和胎儿心率异常的女性,应考虑子宫破裂的可能。一旦怀疑子宫破裂,应及时完善各项检查进行评估,并根据患者病情发展及时采取干预措施或手术。对于希望保留生育功能的患者,应根据破裂的大小、位置和患者的一般情况决定是否进行破裂部位的修补。既往有宫腔操作史的多胎妊娠增加了妊娠期间子宫破裂的发生率,因此建议在行ART时慎重考虑胚胎的移植数量。
综上所述,URR是一种不常见的但危及生命的产科并发症,并非所有的URR都出现腹痛、低血容量、阴道持续性出血和胎心监护异常等临床表现,在临床工作中保持对URR的警惕是很重要的。同时,不仅是妊娠期及分娩期要加强管理,在妇科诊疗中对于有生育要求的患者进行临床干预决策时也应有URR发生的意识,做好宣教,避免多次人工流产及宫腔操作,严格把控剖宫产指征,降低URR发生的医源性因素。

