他克莫司致神经系统不良反应文献分析
陈慧颖,陈冠儒,彭 寅,邓 芳#(.安徽省儿童医院药剂科,合肥 33000; .安徽省儿童医院肾内科,合肥 33000)
他克莫司是一种钙调磷酸酶抑制剂,因其免疫抑制作用强于环孢素A,且不良反应较少,因此在器官移植、肾病综合征等疾病中应用广泛[1]。他克莫司口服生物利用度个体差异性极大,临床应用过程中如用药不当易出现不良反应。目前,国内外关于他克莫司导致神经系统不良反应的报道逐渐增多,且导致严重后果,应引起重视[2]。国内对他克莫司导致不良反应分析的文献较多,但未对他克莫司导致神经系统不良反应进行分析。因此,本研究收集国内外他克莫司致神经系统不良反应的个案报道,以期获得丰富且完整的病例资料,对病例资料进行回顾性分析,为临床合理用药提供依据。
1 资料与方法
1.1 资料来源
资料来源于文献检索。以“他克莫司不良反应”“他克莫司癫痫”“他克莫司后部脑白质病”“他克莫司神经系统”“TAC ADR”“TAC epilepsy”“TAC nervous system”和“tacrolimus posterior reversible encephalopathy syndrome”为检索词,检索2011年5月至2021年5月在中国知网、维普数据库、万方数据库及PubMed发表的关于他克莫司引起神经系统不良反应的个案报道。
1.2 方法
采用文献统计法,总结分析检索到的相关文献,提取患者性别、年龄、移植类型、不良反应发生时间、不良反应发生时患者临床症状、他克莫司血药浓度、不良反应处理措施、转归等有效信息进行统计分析。排除资料不全以及记录不完整的文献,剔除综述文献以及非不良反应报道的文献。将收集到的资料录入Excel软件,进行统计分析。
2 结果
2.1 文献检索结果
共检索到符合纳入标准的个案报道文献37篇,涉及45例患者,其中国外患者28例,国内患者17例。
2.2 患者一般情况
45例患者中,男性患者25例,女性患者20例;年龄为14个月至65岁,平均年龄为(36.07±18.71)岁,<18岁9例,18~50岁24例,>50岁12例,见表1。
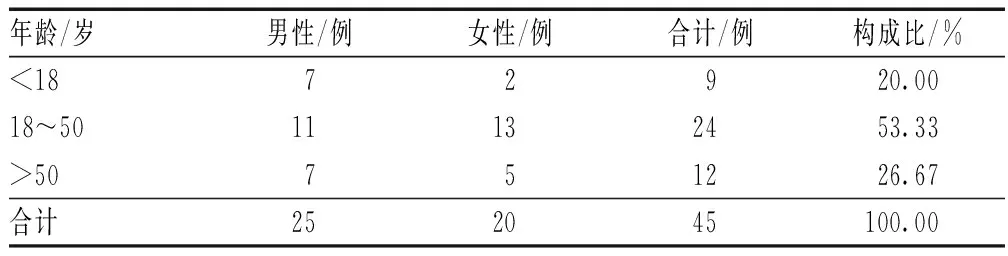
表1 不同年龄段他克莫司致神经系统不良反应患者的性别分布Tab 1 Gender distribution of patients with nervous system adverse drug reactions induced by tacrolimus in different age groups
2.3 移植器官与原发疾病分布
45例患者中,肺移植7例,肝移植12例,肾移植16例,心脏移植3例,造血干细胞移植4例,膜性肾病1例,小肠移植1例,多器官移植(肝、肠和胰腺联合移植)1例。
2.4 他克莫司给药情况及神经系统不良反应发生时间
45例患者中,详细报告了免疫治疗方案的有34例,其中他克莫司联合吗替麦考酚酯以及泼尼松最多(22例),见表2;具体描述了他克莫司口服给药剂量的有28例,均为1日2次给药,日剂量为0.5~14.0 mg,依据药品说明书(肝移植:1日0.1~0.2 mg/kg;肾移植:1日0.15~0.30 mg/kg),均未超说明书用法与用量;均描述了不良反应发生时间,为用药后3 d至11年,主要发生于用药后1个月内,见表3。

表2 34例患者的他克莫司联合其他药物的免疫治疗方案Tab 2 Immunization regimen of tacrolimus in combination with other drugs in 34 patients
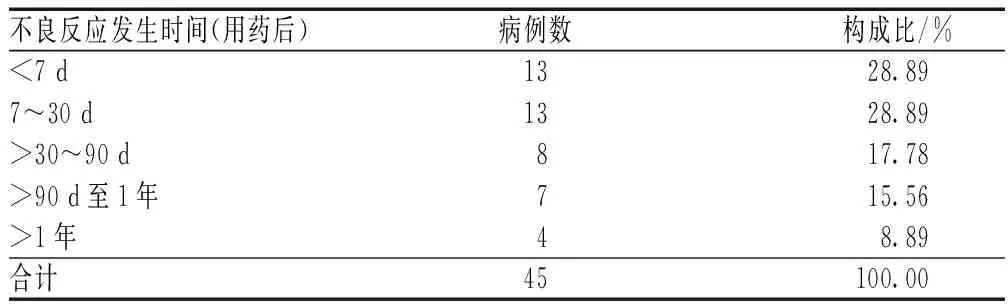
表3 他克莫司致神经系统不良反应的发生时间分布Tab 3 Distribution of occurrence time of nervous system adverse drug reactions induced by tacrolimus
2.5 联合用药情况
2.6 发生神经系统不良反应时他克莫司血药浓度分布及临床症状
45例患者中,有4例未记录发生神经系统不良反应发生时的他克莫司血药浓度;41例记录了他克莫司血药浓度的患者中,他克莫司血药谷浓度为1.9~53.0 ng/mL,具体他克莫司血药浓度分布见表4。45例患者中,临床表现为他克莫司导致后部可逆性白质脑病(PRES)25例,癫痫8例,精神障碍2例,视神经改变3例,神经系统异常2例,构音障碍2例,耳聋1例,双下肢疼痛综合征1例,躁狂症1例。有43例对头部磁共振成像检查结果进行了详细描述,其中35例异常,8例无异常。
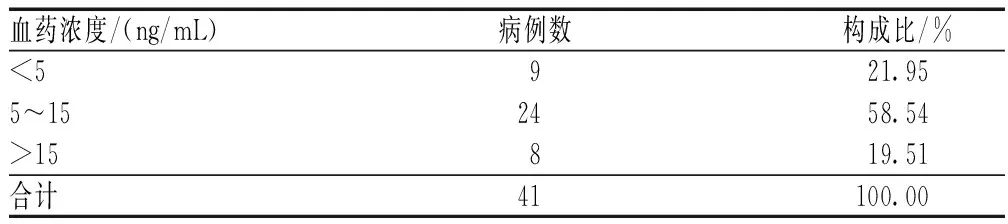
表4 他克莫司致神经系统不良反应患者的他克莫司血药浓度分布Tab 4 Distribution of blood drug concentration of patients with nervous system adverse drug reactions induced by tacrolimus
2.7 他克莫司致神经系统不良反应的处理及转归
45例患者发生神经系统不良反应后,27例停用他克莫司;12例他克莫司减量后仍继续应用;4例先减量,再次出现严重不良反应后停用;2例未进行任何处理。27例报告调整了免疫治疗方案,其中4例他克莫司减量加用西罗莫司/依维莫司,14例换用环孢素,4例换用西罗莫司,4例换用吗替麦考酚酯+环孢素,1例换用贝拉西普。21例描述了对症处理方式,加用左乙拉西坦或丙戊酸钠对症处理。出现神经系统不良反应后,经相应治疗,有1例患者死亡;4例患者神经系统不良反应症状仍持续存在,未得到缓解;其余40例患者症状消失。
3 讨论
3.1 他克莫司致神经系统不良反应的特点
3.1.1 与患者性别、年龄的关系:本研究结果显示,他克莫司导致神经系统不良反应可发生于各年龄段,最小14个月[3],最大65岁[4],以≤50岁患者居多,平均年龄为(36.07±18.71)岁,性别无明显差异。但是本研究发现,有9例为青少年或儿童,应当引起临床重视。相关研究结果表明,口服相同剂量的他克莫司时,儿童患者的血药浓度相对偏高,可能因为他克莫司的代谢酶肝药酶CYP的表达水平不同所致[5]。
3.1.2 与他克莫司血药浓度的关系:描述了他克莫司血药浓度的有41例,他克莫司血药谷浓度最低为1.9 ng/mL[6],最高达53 ng/mL[4];其中≤15 ng/mL的为33例(占80.49%),>15 ng/mL的为8例(占19.51%),表明80.49%的患者发生神经系统不良反应时他克莫司血药浓度≤15 ng/mL,提示在治疗浓度范围内的患者也可能发生神经系统不良反应。文献报道,肝移植后神经系统不良反应的发生率高达43%,神经系统症状的发生与原发病灶或免疫抑制剂的浓度没有明确的关系[7]。本研究结果与上述文献报道相一致。在心脏或肾脏等实体器官移植领域,所用的免疫抑制剂与肝移植大体是相同的。因此可以认为,在肝移植中出现的神经系统不良反应,可能会在其他实体器官移植中出现。
但是一项针对大鼠的研究发现,触发神经毒性事件的大鼠他克莫司血药浓度为20 ng/mL[8]。Lyson等[9]研究发现,他克莫司结合蛋白,钙调蛋白和亲环蛋白大多数分布在脑组织中,并进一步证实他克莫司诱导的交感神经激活与钙调磷酸酶介导的T细胞信号转导抑制有关。研究结果表明,他克莫司血药浓度高与神经系统不良反应发生有关,血药浓度>20 ng/mL,神经系统不良反应发生率较高[10]。
本研究中,明确报道神经系统不良反应与他克莫司浓度相关的有9例。其中8例患者发生神经系统不良反应时的他克莫司血药浓度>15 ng/mL,1例患者他克莫司血药浓度为12.7 ng/mL(<15 ng/mL)[11]。因样本量小,仅对文献报道的案例进行整理,虽研究未明确神经系统不良反应与他克莫司血药浓度相关,但临床应用过程中仍需关注他克莫司血药浓度过高可能导致的头晕、头痛、视觉、意识改变、癫痫、昏迷等神经系统不良反应,并进行血药浓度监测。
3.1.3 他克莫司致神经系统不良反应的发生时间:本研究结果表明,他克莫司导致神经系统不良反应发生时间最短为用药后3 d[12],最长为用药后11年[4];主要发生在用药后1个月内,这与出现高血钾等其他不良反应的时间相似[13-14]。本研究纳入的45例患者中,仅1例为膜性肾病,4例造血干细胞移植,其余40例均为实体器官移植。25例患者确诊为PRES,药物所致PRES是最常报告的不良事件,发生在移植后不久(平均31 d)[15]。本研究结果与文献报道相一致。服药早期的神经系统不良反应可能是由于他克莫司个体差异较大、药物相互作用等,移植术后早期抗感染、抑制胃酸保护胃黏膜(质子泵抑制剂)等药物均可能与他克莫司产生相互作用。肝脏、肾脏、心脏、小肠等器官移植后,他克莫司的代谢和消除受到较大影响,这可能是用药1个月后神经系统不良反应高发的主要原因。因此,临床应早期监测患者生化指标,密切关注患者病情变化。
3.1.4 他克莫司致神经系统不良反应的临床症状:文献报道,他克莫司常见的神经系统不良反应临床症状包括震颤、脑病、头痛和癫痫发作[16],最严重的神经系统不良反应为PRES,与皮层下和深部白质改变有关[17]。轻度神经系统症状包括震颤、失眠、噩梦、头痛、眩晕、感觉迟钝、畏光和情绪障碍。严重的神经系统表现包括行动不便的缄默症、癫痫发作、视神经损伤、精神病和脑病[18]。本研究结果显示,45例他克莫司相关神经系统不良反应患者中,临床症状为PRES的有25例,癫痫8例,精神障碍2例,视神经改变3例,神经系统异常2例,构音障碍2例,耳聋1例,双下肢疼痛综合征1例,躁狂症1例,与文献报道基本一致。
3.1.5 不良反应的处理及转归:本研究结果显示,发生神经系统不良反应后的处理包括换用其他免疫抑制剂替代他克莫司,换用西罗莫司、依维莫司、霉酚酸酯或泼尼松,他克莫司减量,以及停用他克莫司。然而,经过免疫治疗方案调整和相应对症治疗后,仍有1例死亡,死亡原因可能是感染与严重的神经系统不良反应,神经系统症状表现为癫痫发作和脑水肿[19]。4例患者的神经系统不良反应症状未得到缓解,且后期随访仍持续存在。未缓解的神经系统症状包括构音障碍[20]、脑内和蛛网膜下腔出血[21]、左侧肢体肌无力[22]、周边视力丧失[4]。说明他克莫司导致神经系统不良反应经过停用或者减量大都能够缓解,但仍需注意一些严重的头晕、头痛、癫痫发作等神经系统症状。
3.2 他克莫司导致神经系统不良反应的发生机制
他克莫司是一种钙调磷酸酶抑制剂。钙调磷酸酶是一种钙调蛋白结合磷酸酶,参与广泛的细胞过程和钙依赖性信号转导途径,包括 T细胞活化,诱导下游阻断白细胞介素2信号,最终干扰T细胞活化、增殖和分化。钙调磷酸酶在中枢神经系统中高度表达,特别是在缺血性和创伤性损伤的神经元中。他克莫司在生理状态下不容易穿过血脑屏障(BBB),可能会诱导脑毛细血管内皮细胞凋亡并抑制P糖蛋白功能,从而改变BBB通透性[23]。通过BBB扩散后,他克莫司可能对神经胶质细胞和少突胶质细胞产生选择性毒性作用[24]。他克莫司也可能直接改变线粒体功能,增加神经胶质细胞的氧化应激[25]。除对神经细胞的直接影响外,他克莫司还可能导致主要血管收缩系统(即肾素-血管紧张素和内皮素系统)的激活,并增加交感神经系统的活动。此外,他克莫司能够抑制一氧化氮合成和一氧化氮介导的血管扩张。总之,这些过程会导致血管收缩和内皮功能障碍,从而导致全身性高血压、局部缺血和脑水肿,而脑部血管源性水肿可以在磁共振成像中检测到[26]。本研究中,具体描述了头部磁共振成像检查情况的有43例,其中35例有异常。他克莫司导致神经系统不良反应可能与脑部血管水肿有关,具体机制尚需进一步研究。
综上所述,他克莫司在器官移植或者免疫系统疾病治疗中是一个长期用药过程,神经系统不良反应发生时间在用药后数日乃至数年,虽然该不良反应的病理生理学尚未完全阐明,但通过减少他克莫司剂量或停止用药后,大部分患者的不良反应好转。本研究总结了45例他克莫司致神经系统不良反应患者的病例资料,希望能够引起临床重视,以期有益于处理该不良反应。临床医师应了解钙调磷酸酶抑制剂毒性相关的潜在神经系统不良反应,建议尽早进行头部磁共振成像检查,调整免疫治疗方案。

