HPLC法同时测定双载药复合物中伊立替康和姜黄素的载药量
赵 柔,王 姗,崔婷婷,王圆圆,韩晓燕,张 毅
(天津中医药大学中药学院,天津 300193)
伊立替康(Irinotecan, ICA)为半合成喜树碱衍生物,是DNA拓扑异构酶Ⅰ抑制剂,通过体内的羧酸酯酶转化为活性代谢产物SN38,进而发挥抗肿瘤活性。在酸性环境中,ICA以内酯环形式存在,抗肿瘤作用较强[1]。ICA的抗癌谱较广,对肺癌、宫颈癌、结肠癌等均有一定疗效。姜黄素(curcumin,CUR)是从姜科姜黄属(Curcumal)植物姜黄、莪术、郁金等的根茎中提取的一种多酚类化合物。CUR几乎不溶于水,不稳定,易降解,在体内吸收差。研究显示,CUR对乳腺癌、前列腺癌、结肠癌等[2]均有抑制作用。多种抗肿瘤药物联用是减少药物毒副作用、克服药物耐药性、发挥药物协同作用、提高药物抗肿瘤效果的最有效方法之一。伊立替康与姜黄素联用时,通过调节肿瘤细胞内相关通路或进一步诱导肿瘤细胞凋亡而大大提高其抗肿瘤活性[3-4]。
金属有机框架(metal organic frameworks,MOFs)是由金属离子或团簇与有机配体通过配位键自组装形成的具有多孔晶体的有机-无机杂化材料[5]。MOFs材料因孔隙率高、比表面积大及表面易功能化等特点成为微纳米制剂的新型药物载体之一。MOFs作为药物载体递送药物,具有缓控释性、靶向性等优点[6-8],可以提高药物的生物利用度。其中MIL-100(Fe)具有较好的生物相容性和安全性,能通过辅助诱导铁死亡等方式直接发挥抗肿瘤功效[9-10],在药物递送领域应用广泛。
在此,作者以ICA和CUR为模型药物,以MIL-100(Fe)为药物载体,采用浸渍吸附法制备双载药复合物ICA/CUR@MIL-100(Fe),建立同时测定ICA/CUR@MIL-100(Fe)中ICA、CUR载药量的HPLC法,并进行方法学验证,拟为ICA/CUR@MIL-100(Fe)的后续研究奠定基础。
1 实验
1.1 试剂与仪器
MIL-100(Fe),自制;甲醇(色谱纯)、三氯甲烷,天津渤化化学试剂有限公司;伊立替康,天津易生源生物技术有限公司;姜黄素,北京百灵威科技有限公司;乙腈(色谱纯)、乙醇,天津康科德科技有限公司;十二烷基硫酸钠、磷酸氢二钠,天津大茂化学试剂厂;去离子水,Smart2 Pure Pro智能超纯水系统。
RCT B S025型集热式恒温加热磁力搅拌器,德国IKA;ME104E型电子天平、高效液相色谱仪,日本岛津公司;H1650型台式高速离心机,长沙湘仪离心机仪器有限公司;5424R型高速冷冻离心机,德国Eppendorf;IVOS-30A型真空干燥箱,施都凯仪器设备有限公司;电热鼓风干燥箱,天津中环电炉股份有限公司;XO-5200DTS型超声波清洗机,南京先欧仪器制造有限公司;Varian 640型傅立叶变换红外光谱仪,南昌捷岛科学仪器有限公司;Horiba型粒径电位仪,日本Horiba公司。
1.2 ICA/CUR@MIL-100(Fe)的制备
精密称取5 mg经150 ℃ 活化3 h的MIL-100 (Fe),在避光条件下加入5 mL ICA和CUR的4%甲醇-氯仿混合溶液(浓度均为4 mg·mL-1),置于磁力搅拌器上,室温搅拌36 h,12 000 r·min-1离心10 min,收集上清液和沉淀,上清液即为供试溶液,沉淀即为双载药复合物ICA/CUR@MIL-100(Fe)。
不加ICA和CUR,同法操作,收集上清液和沉淀,上清液即为空白对照溶液,沉淀即为MIL-100(Fe)。
1.3 溶液的制备
对照储备液的制备:精密称取ICA、CUR对照品适量,分别置于10 mL棕色容量瓶中,加入乙腈,分别制成1.01 mg·mL-1的ICA对照储备液、1.022 mg·mL-1的CUR对照储备液。
混合对照储备液的制备:精密称取ICA、CUR对照品适量,置于10 mL棕色容量瓶中,加入乙腈,制成含1.01 mg·mL-1ICA、1.022 mg·mL-1CUR的混合对照储备液。
1.4 ICA/CUR@MIL-100(Fe)的载药量测定
1.4.1 色谱条件
Agilent C18色谱柱(150 mm×4.6 mm,5 μm);柱温25 ℃;流动相为乙腈-水溶液(含8%冰醋酸、0.08 mol·L-1十二烷基硫酸钠、0.002 mol·L-1磷酸氢二钠)(48∶52,体积比,下同);流速1.0 mL·min-1;检测波长376 nm;进样量20 μL。
1.4.2 载药量的计算
按1.2方法平行制备3份双载药复合物ICA/CUR@MIL-100(Fe),分别精密移取200 μL载药上清液和载药原液(未加载体的药物溶液)于10 mL容量瓶中,加流动相至刻度,摇匀,经0.45 μm微孔滤膜过滤,进样,记录峰面积,按下式计算载药量:

式中:m0为加入的药物质量,mg;m1为载药后上清液中游离的药物质量,mg;m为MIL-100(Fe)的加入质量,mg。
2 结果与讨论
2.1 ICA/CUR@MIL-100(Fe)的表征
2.1.1 红外光谱分析
采用KBr压片法,在400~4 000 cm-1范围内分别对ICA、CUR、MIL-100(Fe)和ICA/CUR@MIL-100(Fe)进行扫描,结果见图1。
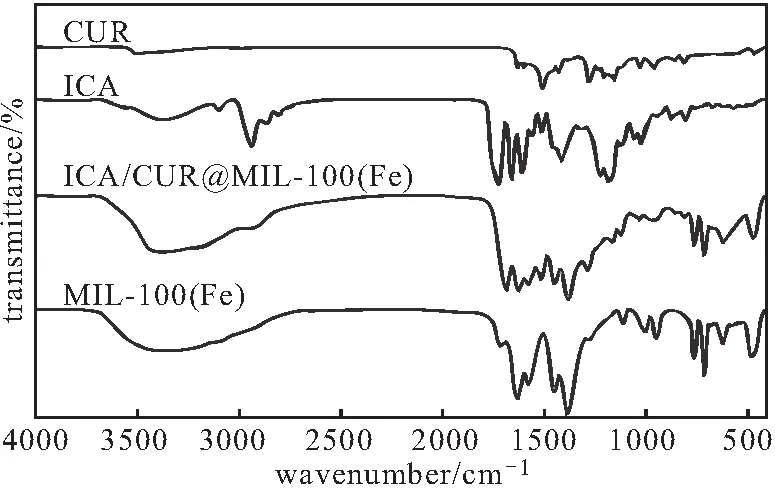
图1 ICA、CUR、MIL-100(Fe)和ICA/CUR@MIL-100(Fe)的红外光谱Fig.1 FTIR spectra of ICA,CUR,MIL-100(Fe),and ICA/CUR@MIL-100(Fe)
由图1可知,对于MIL-100(Fe)的红外光谱曲线,486 cm-1、619 cm-1处分别为Fe-O和Fe-O-Fe的伸缩振动峰;941 cm-1处为Fe-O的四边形和八边形几何结构的伸缩和弯曲振动峰;1 454 cm-1、1 379 cm-1、760 cm-1、712 cm-1处的中强吸收峰为MIL-100(Fe)的特征峰;1 633 cm-1处为C=O振动峰;1 108 cm-1处为苯环中羧酸根的C-H弯曲振动峰;3 425 cm-1处为水分子的典型伸缩振动峰,与文献[11]报道相似。对于ICA/CUR@MIL-100(Fe)的红外光谱曲线,MIL-100(Fe)的特征峰基本完全保留,而ICA的C=O伸缩振动峰(1 718 cm-1处)红移到1 686 cm-1处,这是由于,ICA与MIL-100(Fe)中苯环的共轭作用使π电子的离域增大,减小了C=O键的键级;另外,可以明显看到1 510 cm-1处ICA和CUR的C=C骨架振动峰及1 278 cm-1处CUR的酮基振动峰,证明ICA和CUR成功负载于MIL-100(Fe)中。
2.1.2 Zeta电位分析
取稀释适当倍数后的MIL-100(Fe)和ICA/CUR@MIL-100(Fe)分散液适量,用粒径电位仪分别测定MIL-100(Fe)和ICA/CUR@MIL-100(Fe)的Zeta电位,平行测定3次,结果见图2。
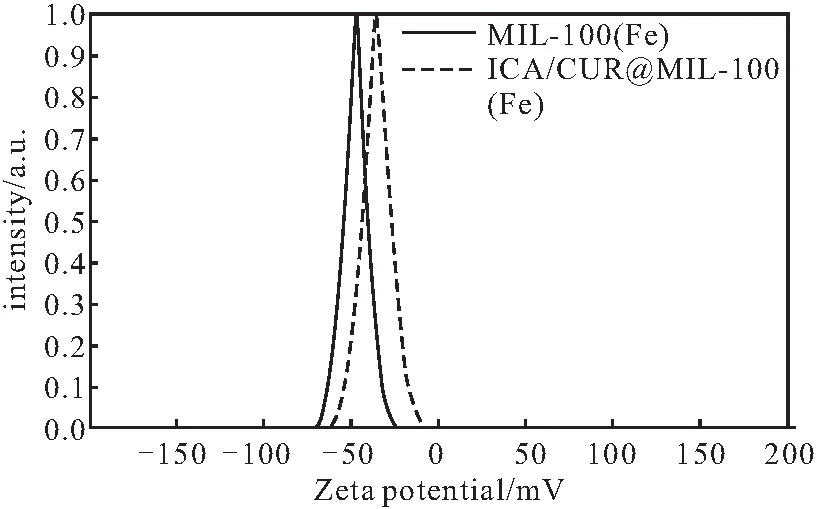
图2 MIL-100(Fe)和ICA/CUR@MIL-100(Fe)的Zeta电位Fig.2 Zeta potentials of MIL-100(Fe) and ICA/CUR@MIL-100(Fe)
由图2可知,MIL-100(Fe)、ICA/CUR@MIL-100(Fe)的Zeta电位分别为(-47.1±3.5) mV、(-36.6±2.0) mV,载药前后的Zeta电位相差较大,进一步证明ICA和CUR成功负载于MIL-100(Fe)中。
2.2 方法学验证
2.2.1 专属性
取空白对照溶液和供试溶液,按1.4.1色谱条件进样分析,结果见图3。
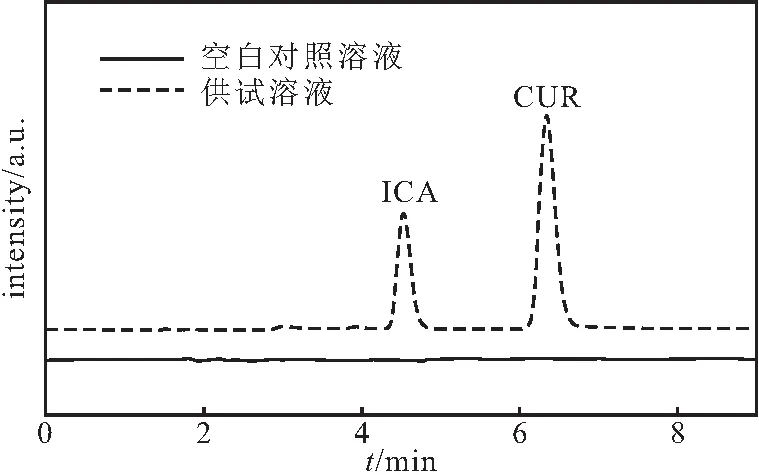
图3 空白对照溶液和供试溶液的HPLC图谱Fig.3 HPLC spectra of blank control solution and test solution
由图3可知,MIL-100(Fe)对ICA、CUR出峰没有干扰,ICA和CUR的保留时间分别为4.53 min和6.34 min,分离度较好,达到1.5以上,专属性强。
2.2.2 线性关系
在避光条件下,分别精密吸取0.05 mL、0.1 mL、0.3 mL、0.6 mL、0.8 mL、1.0 mL混合对照储备液于10 mL容量瓶中,用流动相定容至刻度,得系列浓度(ICA:5.05、10.10、30.30、60.60、80.80、101.00,μg·mL-1;CUR:5.11、10.22、30.66、61.32、81.76、102.20,μg·mL-1)的混合对照溶液,经0.45 μm微孔滤膜过滤,进样,记录峰面积。以进样量(μg·mL-1)为横坐标、峰面积为纵坐标绘制标准曲线。ICA标准曲线的线性回归方程为y1=23107x1+11542,R2=0.9999,在5.05~101.00 μg·mL-1范围内线性关系良好;CUR标准曲线的线性回归方程为y2=28467x2+16145,R2=0.9999,在5.11~102.20 μg·mL-1范围内线性关系良好。
2.2.3 精密度
在避光条件下,精密吸取经0.45 μm微孔滤膜过滤后的混合对照储备液,连续进样测定6次,记录峰面积。结果显示,ICA峰面积的RSD值为0.39%,CUR峰面积的RSD值为1.41%,均小于2%,说明仪器精密度良好。
2.2.4 重复性
在避光条件下,精密吸取6份相同条件下制备的供试溶液于10 mL容量瓶中,用流动相定容至10 mL,经0.45 μm微孔滤膜过滤,进样,记录峰面积。结果显示,ICA峰面积的RSD值为0.58%,CUR峰面积的RSD值为1.28%,均小于2%,说明该方法的重复性较好。
2.2.5 稳定性
在避光条件下,取同一份供试溶液,经0.45 μm微孔滤膜过滤,分别于0 h、1 h、3 h、5 h、7 h、9 h、12 h 进样,记录峰面积。结果显示,ICA峰面积的RSD值为0.96%,CUR峰面积的RSD值为1.92%,均小于2%,说明供试溶液在12 h内稳定性较好。
2.2.6 加标回收率
在避光条件下,在3份等体积的已知浓度的供试溶液中分别加入浓度为80%、100%和120%的ICA和CUR混合对照储备液,用流动相定容至10 mL,经0.45 μm微孔滤膜过滤,进样,记录峰面积,平行测定3次,结果见表1。

表1 加标回收率结果
由表1可知,ICA、CUR的平均加标回收率分别为100.06%±0.81%、101.07%±1.59%,RSD值分别为0.81%、1.57%,均小于2%,表明该方法的准确度较高。
2.3 载药量的测定(表2)

表2 ICA/CUR@MIL-100(Fe)的载药量
由表2可知,ICA、CUR的平均载药量分别为12.33%±0.66%、26.97%±1.59%。
2.4 讨论
2.4.1 流动相的选择
以乙腈-水溶液(含4%冰醋酸、0.08 mol·L-1十二烷基硫酸钠、0.002 mol·L-1磷酸氢二钠)(50∶50)为流动相时,ICA色谱峰峰形良好,但CUR色谱峰拖尾现象较严重。发现,通过改变冰醋酸含量及乙腈比例可以改善CUR的拖尾现象,当以乙腈-水溶液(含8%冰醋酸、0.08 mol·L-1十二烷基硫酸钠、0.002 mol·L-1磷酸氢二钠)(48∶52)为流动相时,ICA和CUR峰型均较好,且ICA和CUR色谱峰的对称因子、理论塔板数及分离度均达到要求。故选择流动相为乙腈-水溶液(含8%冰醋酸、0.08 mol·L-1十二烷基硫酸钠、0.002 mol·L-1磷酸氢二钠)(48∶52)。
2.4.2 检测波长的选择
在200~600 nm范围内分别对ICA对照溶液和CUR对照溶液进行紫外可见扫描,结果见图4。
由图4可知,ICA对照溶液在220 nm、256 nm处有最大紫外吸收,CUR在420 nm处有最大紫外吸收,且ICA和CUR的紫外可见吸收光谱在376 nm处存在重叠。为在同一波长下能同时测定ICA和CUR含量,选择376 nm为检测波长。
3 结论
以ICA和CUR为模型药物,以MIL-100(Fe)为药物载体,采用浸渍吸附法制备了双载药复合物ICA/CUR@MIL-100(Fe),建立了同时测定ICA/CUR@MIL-100(Fe)中ICA、CUR载药量的HPLC法。结果表明,在确定的色谱条件下,ICA和CUR的色谱峰分离度达到1.5以上,分离效果较好,且MIL-100(Fe)对ICA和CUR的测定无干扰,该方法的精密度、重复性、稳定性和加标回收率的RSD值均小于2%,符合制剂含量测定要求。ICA和CUR的平均载药量分别为12.33%±0.66%、26.97%±1.59%。该研究为新型药物制剂的研究奠定了基础。

