UPLC 法同时测定五味子糖浆中7 种成分
赵 硕,张金朋,赵志远,陈玉凤,郭晓帆,刘媛媛
[山东第一医科大学(山东省医学科学院) 药学院,山东 泰安 271016]
五味子糖浆是五味子经浸渍、渗漉等过程制成的中药制剂[1],具有补气生津、补肾安神功效[2],常用于治疗慢性咳嗽、气短、心悸、失眠等症状[3-4],2020 年版《中国药典》 一部“含量测定”项下以五味子醇甲为定量指标[5],不能全面反映该制剂整体质量,在临床应用方面存在很大局限性。前期报道,五味子产地、采收期、加工方式不同可能会导致相关制剂的质量或安全问题[6-7],故加强药材质量控制十分重要。迄今为止,关于五味子糖浆的含量测定已有文献[8-13] 报道,但尚未采用UPLC 法同时测定五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素的含量,故本实验对其进行研究,以期为该制剂质量控制、临床应用提供依据。
1 材料
1.1 仪器 超高效液相色谱仪(日本岛津公司,型号Nexera X2); 德安特电子分析天平(0.1 mg,天津德安特传感技术有限公司,型号ES-E120A);高速冷冻离心机[赛默飞世尔科技(中国) 有限公司,型号Fresco 21]; 数控超声波清洗器(昆山市超声仪器有限公司,型号KQ-600DB); 纯水机(德国默克公司,型号Direct-Q®8UV-R)。
1.2 试剂与药物 五味子醇甲(批号D1827017,纯度≥98%)、五味子醇乙(批号F1508140,纯度≥98%)、五味子甲素 (批号D1911039,纯度≥98%) 对照品(上海阿拉丁生化科技股份有限公司); 戈米辛J (批号G99633663,纯度≥98%)、当归酰戈米辛H (批号A43133661,纯度≥98%)对照品(上海吉至生化科技有限公司); 当归酰戈米辛Q 对照品(北京中科质检生物技术有限公司,批号PCS-210329,纯度≥98%); 五味子酚对照品(上海麦克林生化科技有限公司,批号C12256480,纯度≥98%)。五味子糖浆(湖北端正药业股份有限公司,批号211101、210102、201102、220501、220301、201501)。甲醇为色谱纯(天津市科密欧化学试剂有限公司,批号20210331); 乙腈为色谱纯(安徽天地高纯溶剂有限公司,批号19115052);甲酸为质谱纯[赛默飞世尔科技(中国) 有限公司,批号214053]。
2 方法与结果
2.1 色谱条件 Ultimate ® UHPLC XB-C18色谱柱(2.1 mm×100 mm,1.8 μm); 流动相水(含0.1%甲酸) (A) -乙腈(含0.1%甲酸) (B),梯度洗脱(0~1.2 min,45% ~53%B; 1.2~3 min,53% ~53.5%B; 3~10 min,53.5% ~55%B; 10 ~13 min,55% ~95% B; 13 ~15 min,95% ~95% B; 15 ~17 min,95% ~45%B; 17~21 min,45% ~45%B); 体积流量0.3 mL/min; 柱温40 ℃; 检测波长267 nm; 进样量3 μL。
2.2 溶液制备
2.2.1 对照品溶液 精密称取五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素对照品适量,置于10 mL 量瓶中,甲醇定容至刻度,摇匀,得到质量浓度分别为1 252、154、375、259、258、102、375 μg/mL 的贮备液,分别精密吸取1 mL,置于10 mL 量瓶中,甲醇定容至刻度,摇匀,即得(各成分质量浓度分别为五味子醇甲125.20 μg/mL、戈米辛J 15.40 μg/mL、五味子醇乙37.50 μg/mL、当归酰戈米辛H 25.90 μg/mL、当归酰戈米辛Q 25.80 μg/mL、五味子酚10.02 μg/mL、五味子甲素37.50 μg/mL),置于4 ℃冰箱中保存。
2.2.2 供试品溶液 精密吸取2 mL 本品,置于15 mL 离心管中,4 倍量80%甲醇稀释,超声(功率540 W) 提取20 min,80% 甲醇补足减失的质量,12 000 r/min 离心5 min,取上清液,过0.22 μm 微孔滤膜,即得。
2.2.3 阴性样品溶液 按照处方工艺,制成缺五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素的阴性样品,按“2.2.2” 项下方法制备,即得。
2.3 方法学考察
2.3.1 专属性试验 取“2.2” 项下对照品、供试品、阴性样品溶液适量,在“2.1” 项色谱条件下进样测定,结果见图1。由此可知,供试品溶液中各成分保留时间与对照品溶液中的一致,分别为3.867、4.332、4.600、5.971、6.622、9.435、13.186 min,而且相邻峰之间的分离度均大于1.5,表明该方法专属性良好。

图1 各成分UPLC 色谱图Fig.1 UPLC chromatograms of various constituents
2.3.2 线性关系考察 精密吸取“2.2.1” 项下对照品溶液适量,甲醇依次稀释1.25、2、5、50、500 倍,在“2.1” 项色谱条件下进样测定。以对照品质量浓度为横坐标 (X),峰面积为纵坐标(Y) 进行回归,结果见表1,可知各成分在各自范围线性关系良好。

表1 各成分线性关系Tab.1 Linear relationships of various constituents
2.3.3 精密度试验 精密吸取“2.3.2” 项下对照品溶液(含五味子醇甲25.04 μg/mL、戈米辛J 3.08 μg/mL、五味子醇乙7.50 μg/mL、当归酰戈米辛H 5.18 μg/mL、当归酰戈米辛Q 5.16 μg/mL、五味子酚2.04 μg/mL、五味子甲素7.50 μg/mL)适量,在“2.1” 项色谱条件下进样测定6 次,测得五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素峰面积RSD 分别为0.41%、1.15%、0.34%、0.54%、1.32%、1.17%、0.36%,表明仪器精密度良好。
2.3.4 重复性试验 精密吸取同一份本品(批号211101),按“2.2.2” 项下方法平行制备6 份供试品溶液,在“2.1” 项色谱条件下进样测定,测得五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素含量RSD 分别为1.61%、1.21%、1.21%、1.25%、1.73%、1.88%、1.14%,表明该方法重复性良好。
2.3.5 稳定性试验 精密吸取同一份供试品溶液,于0、2、4、8、12、24 h 在“2.1” 项色谱条件下进样测定,测得五味子醇甲、戈米辛J、五味子醇乙、当归戈米辛H、当归戈米辛Q、五味子酚、五味子甲素峰面积RSD 分别为0.59%、1.51%、0.89%、1.69%、1.98%、1.78%、1.11%,表明溶液在24 h内稳定性良好。
2.3.6 加样回收率试验 精密吸取各成分含量已知的本品(批号211101) 9 份,每份1 mL,分为低、中、高剂量组,每组3 份,分别按50%、100%、150%水平加入对照品溶液,按 “2.2.2”项下方法制备供试品溶液,在“2.1” 项色谱条件下进样测定,计算回收率。结果,五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素平均加样回收率分别 为 99.96%、99.41%、100.26%、100.51%、99.68%、99.18%、99.83%,RSD 分别为0.48%、0.68%、1.93%、0.76%、1.01%、1.07%、0.82%。
2.3.7 样品含量测定 精密吸取6 批样品,每批2 mL,按“2.2.2” 项下方法制备供试品溶液,在“2.1” 项色谱条件下各进样测定3 次,计算含量,结果见表2。
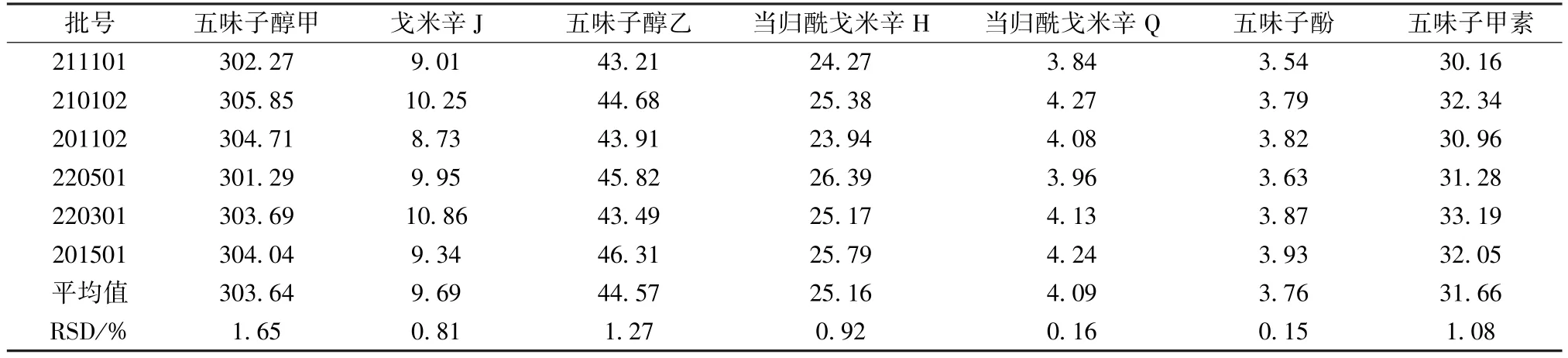
表2 各成分含量测定结果(μg/mL,n=3)Tab.2 Results of content determination of various constituents (μg/mL,n=3)
3 讨论
3.1 提取条件选择 前期报道,不同料液比、溶剂对成分含量测定具有一定影响[14]。本实验采用单因素试验分别对料液比(1 ∶1、1 ∶4、1 ∶9)、甲醇体积分数 (70%、80%、100%)、提取时间(10、20、30 min) 进行考察,结合提取率等指标,最终发现料液比1 ∶4 的80%甲醇超声提取20 min效果最好。
3.2 色谱条件选择 对于流动相的选择,考虑到五味子味酸,故本实验考察了水-乙腈、0.1%甲酸-0.1%乙腈体系[15-17],发现前者洗脱时基线较稳定,但峰形有拖尾现象,故在上述两相中加入0.1%甲酸,此时峰形得到很好的改善,分离度也有所提高。
3.3 含量分析 表2 显示,五味子醇甲含量最高,在中药质量控制评价模式中,该成分作为五味子糖浆质量控制标准符合2020 年版《中国药典》 规定;五味子醇乙、五味子甲素、当归酰戈米辛H 含量次之,药理活性较强[18-19],也可作为检测指标。
4 结论
本实验建立UPLC 法同时测定五味子糖浆中五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素的含量,该方法简便快速,稳定可靠,可用于该制剂全面质量控制和评价。

