1例RhCE抗原缺失型个体的分子机制研究
李小薇 赵明明 雷慧芬 李翠莹
空军军医大学空军特色医学中心输血科,北京 100142
Rh血型系统是人类血型系统中最复杂且最具多态性的血型系统,其临床意义仅次于ABO血型系统[1-3]。ISBT目前确认的Rh血型系统抗原达56个,其中D、C、c、E和e抗原均具有很强的免疫原性,是临床上产生同种免疫性抗体最常见的5种抗原。迄今为止,ISBT已经确认了超过160种RHCE等位基因,这些等位基因可导致抗原弱表达、部分表达等变异体产生[4]。Rh缺失型D--是非常罕见的,即红细胞上D抗原表达正常,但C/c、E/e抗原表达均缺失,其分子遗传基础多种多样,包括基因插入、缺失、重排等。血型基因检测方法能够克服血型血清学检测局限,结果判断更加客观,逐渐成为准确判断疑难血型必不可少的重要辅助手段[5-7]。本研究对Rh缺失型D--患者及其父亲血型采用血清学及RHCE基因外显子测序研究,首次分析发现由于第8外显子缺失导致RhCE血型抗原不表达,现报告如下。
材料与方法
1 研究对象
2023年3月就诊于本中心儿科患者1名,男性,12岁,诊断为特应性皮炎,既往无输血史,送输血科进行血型和不规则抗体筛查。
2 仪器与试剂
ABO血型反定细胞A1细胞、B细胞(批号:202302006,江苏力博医药生物技术股份有限公司);红细胞不规则抗体筛查细胞(批号:202302001,江苏力博医药生物技术股份有限公司);IgM抗-C、抗-c、抗-E和抗-e单克隆抗体试剂(批号:2150031,BIOSCOT);ABO及RHD血型鉴定凝胶卡(批号:202302006,江苏力博医药生物技术股份有限公司),Rh分型鉴定凝胶卡(批号:202211007,江苏力博医药生物技术股份有限公司);核酸提取或纯化试剂(批号:21072810T148,西安天隆科技有限公司);核酸提取仪NP968-C(西安天隆科技有限公司),基因扩增仪LifeECO(杭州博日科技有限公司),通用型电泳仪JY300C(北京君意东方电泳设备有限公司),测序仪ABI 3130xl(美国ABI公司)。
3 方法
3.1 ABO及Rh血型血清学鉴定
采用微柱凝集法鉴定患者及其父亲ABO及RhD血型,采用盐水法和微柱凝集法鉴定患者Rh血型C、c、E和e表型,具体操作方法参照试剂说明书。
3.2 红细胞不规则抗体筛查
采用微柱凝集法筛查患者红细胞不规则抗体情况,具体操作方法参照试剂说明书。
3.3 DNA提取
按照试剂盒说明书提取患者及其父亲血液标本DNA,采用微量紫外核酸分析仪测定DNA浓度和纯度,调整DNA浓度至30 ng/μL,A260/A280为1.6~2.0。
3.4RH基因测序
患者及其父亲样本分别进行RHCE基因第1~10外显子测序,确定基因型特征。采用Sanger测序法,将目的片段扩增后,测序仪进行RHCE基因第1~10外显子测序,并读取结果及分析。根据ISBT网站提供的RH(ISBT 004)Blood Group Alleles:RHCE(004RHCEalleles v4. 0_20180208),以及BLAST序列比对(标准序列BN000065.1以及RHCE*CeMN091966.1),确定是否存在基因突变及其所在基因位置,本研究设计测序引物与扩增引物一致(表1),测序反应送公司完成(天津市秀鹏生物技术开发有限公司)。

表1 RHCE扩增(测序)引物序列
按照以下反应体系对RHCE基因第1~10外显子进行扩增:dNTP-Buffer工作液43.5 μL,Taq酶(5 units/μL)0.5 μL,特异性引物对(300 nM)1.0 μL,DNA 5 μL,总体积50 μL。
反应程序如下:96℃ 2 min,1组循环;96℃20 s,68℃ 60 s,5组循环;96℃ 20 s,64℃ 50 s,72℃ 90 s,10组循环;96℃ 20 s,61℃ 50 sec,72℃ 90 s,25组循环;72℃ 5 min,1组循环。扩增产物使用2.5%琼脂糖凝胶进行分离,确定产物条带均一且亮度足够后,进行测序。使用chromespro软件以及DNAMAN8.0软件进行比对分析。
结 果
1 ABO及Rh血型血清学鉴定
微柱凝集法显示患者及其父亲红细胞ABO血型均为O型,微柱凝集法及盐水法显示患者红细胞与抗-D凝集强度为4+,与抗-C、抗-c、抗-E 和抗-e凝集强度均为0,Rh血型为Rh缺失型D--;父亲红细胞与抗-D、抗-c、抗-E凝集强度为4+,与抗-C、抗-e凝集强度为0,Rh血型为RhccDEE(表2)。
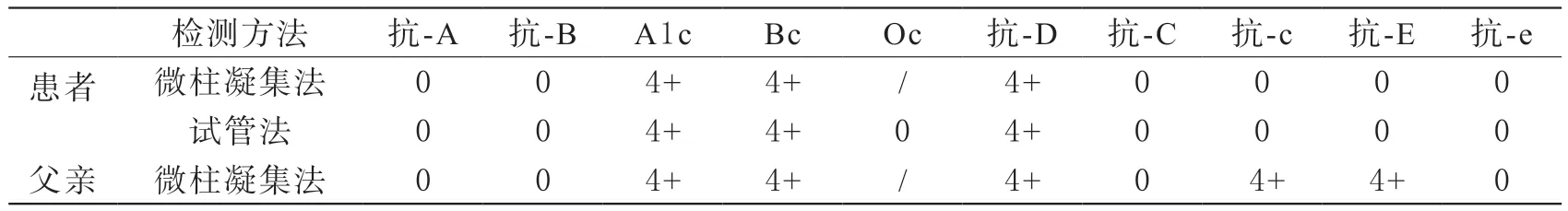
表2 患者及其父亲ABO及Rh血型血清学结果
红细胞不规则抗体显示患者血浆与红细胞不规则抗体筛查3细胞凝集强度均为0,自身对照及直接抗人球蛋白试验均为阴性。
2 RHCE基因测序扩增凝胶图分析
RHCE*c和RHCE*C通常在第2外显子上通过特异点进行区分(表3),但因为RHD和RHCE*C的第2外显子上基因无区别点,故本例患者(RHD基因阳性)RHD基因第2外显子干扰RHCE*C的检出,本研究通过第12孔(RHCE*C在非外显子区域内含子2中表达剪切点位置区分于RHCE*c和RHD的特异性点[8])检测RHCE*C基因的存在。患者及其父亲均检测到RHCE*C(第12孔阳性)(图1),证明均存在RHCE*C等位基因。扩增图第2孔(CE-Exon2)检测的是RHCE*c等位基因的第2外显子,患者第2外显子为阴性,故RHCE*c等位基因缺失;患者的父亲第2外显子为阳性,故RHCE*c等位基因存在。

图1 患者及其父亲RHCE基因第1~10外显子测序扩增凝胶图

表3 RHCE(ISBT 004)血型等位基因分布
3 RHCE基因测序分析
患者及其父亲第2外显子测序结果提示第2外显子突变点是RHCE*C的突变点,进一步证明患者及其父亲均存在RHCE*C等位基因(表3)。患者第2外显子的突变均为纯合,第1外显子上存在48G>C杂合突变,提示存在RHCE*c等位基因,在第5外显子上未发现RHCE*E突变点(676G),并且第8外显子为纯合缺失,提示存在RHCE*Ccee等位基因但序列不完整,导致其抗原表达为RhD--,第3-7,9-10外显子均未检测到突变(图2)。患者的父亲第2外显子的突变均为杂合,第1外显子上存在48G>C杂合突变,提示存在RHCE*c等位基因,在第5外显子上发现RHCE*E突变点(676G>C),提示其存在RHCE*CcEe等位基因;第3,4,6,7,8,9,10外显子未检测到突变,且根据患者第8外显子为纯合缺失,推测患者的父亲为第8外显子杂合缺失,缺失的单倍体为RHCE*Ce,导致其未能正确表达RhCe抗原,故患者的父亲血清学表现为RhccDEE(图3,表2)。因此,可以判断患者RHCE基因型为RHCE*Ccee,但由于第8外显子发生纯合缺失,导致RhCe抗原不表达。患者的父亲RHCE基因型为RHCE*CcEe,存在第8外显子杂合缺失,且该变异的RHCE*Ce等位基因遗传给了患者。

图2 患者RHCE基因第1,2外显子测序结果

图3 患者的父亲RHCE基因第1,2,5外显子测序结果
讨 论
Rh血型系统属于复杂多变的血型系统,Rh抗原部分或者完全缺失是十分罕见的表型。日本研究人员在6万多名献血者中,研究发现Rh缺失型D--仅7例,频率约为0.01%[9]。国内针对Rh缺失型D--分布频率的相关研究多为D--个案报道,尚未见Rh缺失型D--人群分布研究。目前血型的判断仍然主要依据血清学结果,但在血型检测过程中往往出现一些疑难样本,结合血型基因检测方法进行基因结构分析和解读,不仅可以准确鉴定患者血型,而且对于安全输血具有重要的参考价值。
RH血型基因是由RHD与RHCE2个基因串联排列组成的。RHD基因编码D抗原,RHCE基因编码C/c和E/e抗原,2个基因均由10个外显子和9个内含子组成,编码417个氨基酸[10]。在Rh血型系统中,编码RhC和Rhc抗原的RHCE等位基因有6个核苷酸不同,而编码RhE和Rhe抗原的RHCE等位基因仅有1个核苷酸的差异,RHD和RHCE基因具有93.8%同源性,且紧密连锁,因此2个基因之间易发生基因置换、基因杂交、基因重排等现象,引起RH基因变异[11-12]。Rh抗原缺失的血清学表现虽然为对应的D、C、c、E、e抗原的缺失,但是其产生的分子机制却不尽相同;即使是表型相同的Rh缺失型D--,其发生的分子机制也不一样。张秀铮等[13]发现1例Rh缺失型D--的RHCE基因第1、10 外显子检出RHCE基因的特异性序列,而第2、3、6、7、8、9外显子则全为RHD基因序列;伍伟健等[14]分析1例Rh缺失型D--,未检出RHCE基因的特异性序列;左琴琴等[15]分析2例Rh缺失型D--,基因型分别为RHCE-D(3-7)-CE、RHCE-D(3-8)-CE,其发生与RHCE基因和RHD基因之间的基因重组相关;Flatt等[16]分析2例Rh缺失型D--,基因型分别为RHCE-D(2-8)-CE、RHCE-D(4-9)-CE;Pham等[10]研究发现RHCE基因剪接位点突变导致剪接模式的改变和缺失会引起mRNA转录本异常,影响RhC/c、E/e抗原表达。本文对Rh缺失型D--表型患者的分子遗传背景研究发现,存在RHCE基因第8外显子纯合缺失导致RhCE血型抗原不表达。
Rh缺失型D--表型个体比较罕见,但因其RhC/c、E/e抗原均不表达,导致D--个体受到输血或妊娠等免疫刺激后,很容易产生针对C/c、E/e位点的特异性抗体,即抗-Hro联合抗体。抗-Hro抗体为针对Rh血型系统的高频抗原联合抗体,采用吸收放散试验很难将其分离并进行抗体特异性鉴定,其与普通Rh血型红细胞均可发生凝集反应,仅与Rhnull、Rhmod及RhD--红细胞不发生凝集反应[17-18]。因此,Rh缺失型D--个体受到免疫刺激产生抗-Hro抗体后,很难找到相合的血液与之匹配。此外,Rh缺失型D--育龄期女性一旦产生抗-Hro抗体,常常会导致习惯性流产、死胎及胎儿新生儿溶血病等严重后果[19-21]。Rh缺失型D--个体血液极其稀有,临床输血时可选择自体输血或在家系成员中筛选配合型血液;孕妇存在胎儿新生儿溶血病时,可采用血浆置换,也可对新生儿进行提早分娩、静脉注射免疫球蛋白、蓝光照射等综合治疗方式,以取得满意的疗效。本文Rh缺失型D--表型患者为男性,既往无输血史,红细胞不规则抗体筛查阴性,已告知家属患者为稀有血型,临床输血时选择自体输血或筛选亲属间配合型血液。
综上所述,临床患者的血型检测联合应用血清学和分子生物学技术,对于亚型、稀有血型、弱抗原或抗体等疑难血型的准确鉴定具有重要意义。本研究首次发现第8外显子缺失造成RhCE血型抗原不表达,丰富了Rh抗原缺失变异造成血清学改变的情况,为解决患者安全输血提供参考。本研究未能获取患者母亲的样本,故患者另一条缺失第8外显子的单倍体中其他外显子的基因序列情况尚不清楚,后续研究希望通过单链测序等手段进行单倍体确认,以明确外显子缺失和碱基突变对血型的影响。
利益冲突所有作者均声明不存在利益冲突。

