Ni2+浓度变化对厌氧污泥胞外聚合物的影响
王悦静,袁胜煜
(1.山东省烟台生态环境监测中心,山东烟台 264000;2.中国石油管道局工程有限公司,河北廊坊 065000;3.辽宁大学环境学院,辽宁沈阳 110036)
由于化工行业的快速发展,污水处理系统中重金属污染现象日益严峻。Ni2+作为镍合金、电池、涂料等工业产品的原材料,广泛存在于工业废水中[1]。Ni2+超过一定浓度范围时,微生物的新陈代谢会受到抑制作用[2],这会对污水生物处理工艺产生严重的影响。与传统污水处理工艺相比,厌氧污泥处理工艺具有耐冲击负荷、耗能低、处理效率高等优势[3],在复杂污水处理领域受到了学者们的关注。胞外聚合物(EPS)是厌氧污泥的重要组成物质,由微生物代谢以及细胞自溶产生的有机多聚物而形成,主要由蛋白(PN)、多糖(PS)以及少量的腐植酸、核酸等物质组成,可分为内层紧密结合型EPS(TB-EPS)和外层松散结合型EPS(LB-EPS)。EPS对细胞的能量传递、微生物的理化性质以及污泥絮体结构的稳定性等方面具有重要的作用[4]。污水中的重金属离子Ni2+会诱导微生物产生应激反应,造成EPS的组分和结构功能发生变化,进而影响污水生物处理工艺的处理效率[5-6]。因此,研究Ni2+对EPS的影响是有必要的。
关于污水中重金属离子浓度变化对EPS组分和含量的影响已经引起了学者们的关注。胡学伟等[7]研究发现,在Cu2+进水质量浓度由0增加至10mg/L的过程中,EPS中PS和PN含量分别降低了83.64%和43.19%。宋浩亮等[5]研究发现,活性污泥LB-EPS和TB-EPS的含量随Ni2+进水浓度增加而增加,在Ni2+进水质量浓度由0增加至50mg/L的过程中,LB-EPS和TB-EPS含量分别增加了26.09%和47.17%,PN/PS由1.27增加至1.99。Wang等[8]研究发现,在Cr6+质量浓度由0增加至30mg/L的过程中,LB-EPS和TB-EPS中PN/PS分别由6.90和6.75增加至7.69和8.32。学者们开展了许多关于重金属离子对EPS的组分及含量影响的研究,然而关于Ni2+浓度变化对厌氧污泥EPS含量与组成的影响,特别是Ni2+浓度增加对厌氧污泥理化性质与EPS间关系的影响研究较少。
本文采用升流式厌氧污泥流化床(UASB)厌氧污泥处理工艺,研究厌氧污泥LB-EPS和TB-EPS中PN和PS的含量受到进水Ni2+浓度增加的影响,对厌氧污泥LB-EPS和TB-EPS进行三维荧光光谱(3D-EEM)分析,并研究了厌氧污泥沉降性能与LB-EPS和TB-EPS含量变化相互间的关系。
1 材料与方法
1.1 试验装置
UASB反应器的主要材质为有机玻璃,反应器上部分为沉淀区域,下部分为反应区域。沉淀区域有效容积为2 L,内径为15 cm,有效高度为15 cm;反应区域有效容积为4 L,内径为8 cm,有效高度为80 cm。UASB反应器的总有效容积为6 L,总有效高度为100 cm。UASB反应器通过电磁蠕动泵控制进水,进水流量控制在0.45 L/h,水力停留时间为24 h,反应器在室温下稳定运行,通过曝气循环装置使污泥与污水混匀。
1.2 接种污泥与模拟进水
接种污泥取自沈阳市北部污水处理厂厌氧池的活性污泥,混合液挥发性悬浮固体质量浓度(MLVSS)为4.25 g/L。采用模拟有机废水作为试验用水,主要成分包括:葡萄糖1 524mg/L、NH4Cl 160mg/L,KH2PO478mg/L,Ni2+进水质量浓度分别为0、10、15、20、25mg/L。进水pH值控制在7.5左右。
1.3 分析方法
1.3.1 常规水质测定方法

1.3.2 EPS的提取与测定
厌氧污泥EPS的提取方法参照肖倩等[10]的方法。具体操作方法如下:量取UASB反应器中50 mL污泥样品,置于离心管中在5 000g下离心8 min,移除上清液,加入0.5%的NaCl溶液至50 mL,于5 000g下离心15 min,将上清液移除;向移除上清液的离心管中加入0.5%的NaCl溶液至50 mL,混匀后置于8 000g下离心15 min,将提取到的上清液经0.22 μm滤膜过滤即为LB-EPS;将剩余的浓缩污泥置于离心管中,向其中加入0.5%的NaCl溶液至50 mL,放置于水浴箱中在70 ℃下加热20 min后,充分混匀置于20 000g下离心20 min,将提取到的上清液经0.22 μm滤膜过滤即为TB-EPS。LB-EPS和TB-EPS中PN的测定以牛蛋白血清为基准,具体测定方法参照Lowry等[11]的方法;PS的测定以葡萄糖为基准,具体测定方法参照Dubois等[12]的方法。将测定出的LB-EPS(或TB-EPS)中PN和PS含量求和即为LB-EPS(或TB-EPS)的总量。
1.3.3 3D-EEM分析
厌氧污泥LB-EPS和TB-EPS置于荧光分光仪(Hitachi,F-5000)进行3D-EEM分析,详细的设置参数如下:发射波长(Em)的设置为200~500 nm,激发波长(Ex)的设置为200~400 nm,Em和Ex的扫描增量均设置为10 nm;激发光与发射光的扫描速度均设置为12 μm/min,狭缝均设置为5 nm。3D-EEM的数据处理使用Origin 8.0软件。
2 结果与分析
2.1 Ni2+浓度变化对UASB工艺CODCr和氮去除效果的影响

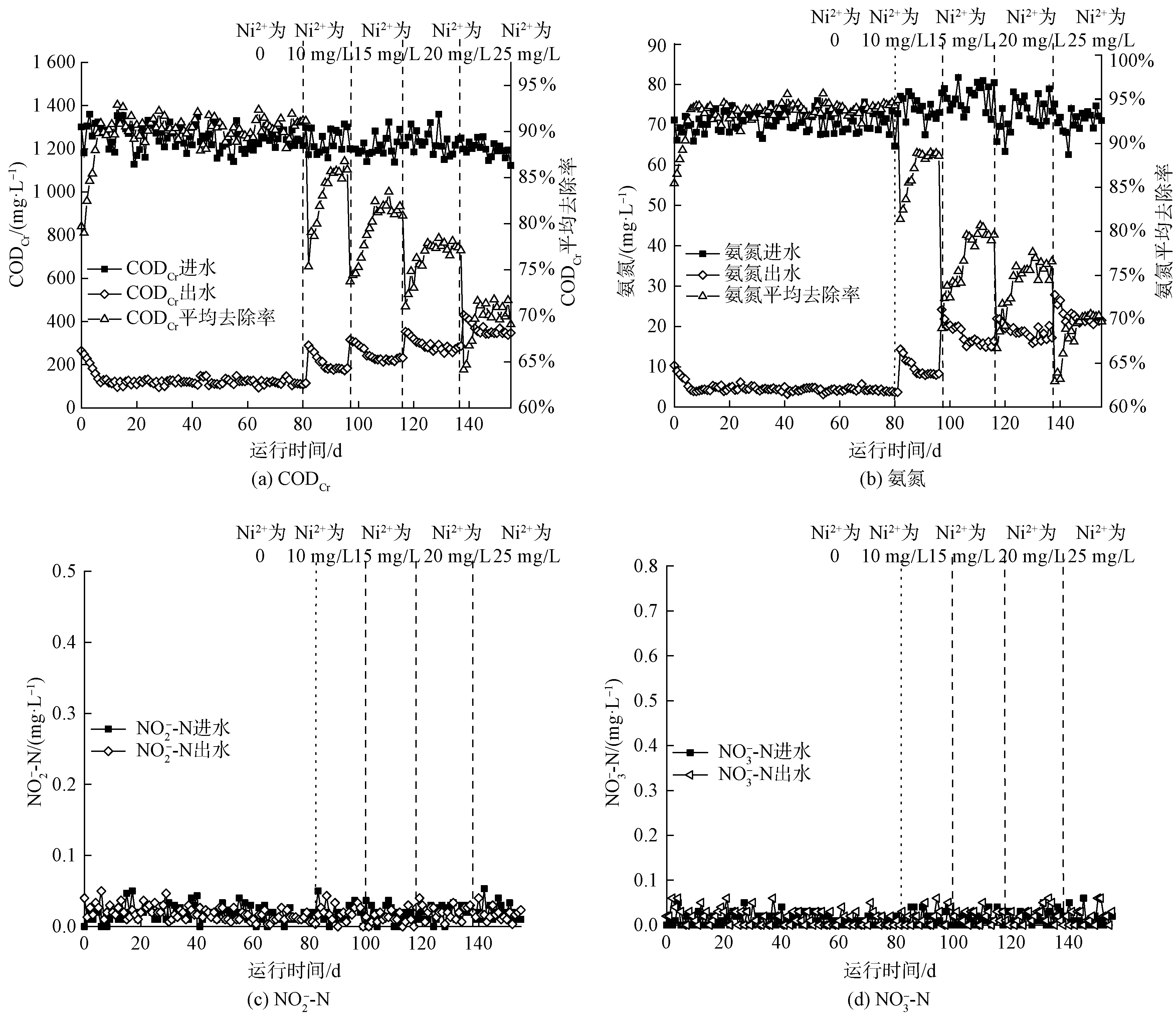
图1 不同Ni2+浓度下的UASB工艺CODCr和氮去除的变化
2.2 Ni2+浓度变化对LB-EPS和TB-EPS中PN和PS含量的影响
不同Ni2+浓度下厌氧污泥LB-EPS和TB-EPS中PN和PS含量变化如图2(a)和图2(b)所示。随着Ni2+进水质量浓度由0增加至25mg/L,LB-EPS中PN和PS质量分数分别由7.18 mg/g和2.16 mg/g(以MLVSS计)增加至45.12 mg/g和17.79 mg/g(以MLVSS计),TB-EPS中PN和PS含量分别由18.27 mg/g和4.94 mg/g(以MLVSS计)增加至54.32 mg/g和17.83 mg/g(以MLVSS计)。在不同进水Ni2+浓度下,LB-EPS和TB-EPS中PN含量始终高于PS含量,这表明,与PS相比,PN是EPS中的主要组成物质。这与Liu等[15]的报道相一致,厌氧污泥EPS中以PN为主要成分,并且由胞外酶引起的EPS分解是造成LB-EPS和TB-EPS中PN含量始终高于PS含量的原因之一[5]。随着进水Ni2+浓度的增加,LB-EPS和TB-EPS中PN和PS含量的增加表明厌氧污泥在Ni2+的刺激下分泌了更多EPS来抵御Ni2+的毒性作用。李姗姗等[16]认为,高浓度的金属离子通过干扰微生物的新陈代谢对污泥产生毒害影响,而微生物通过分泌EPS的方式以减轻金属离子的毒性效应。有学者[5]报道了相似的结论,随着Ni2+质量浓度由0增加至50mg/L,生物膜EPS分泌量由248.8 mg/g增加至338.9 mg/g,其中LB-EPS和TB-EPS分别增加了26.09%和47.17%。图2(c)描述了不同Ni2+进水浓度下的厌氧污泥LB-EPS和TB-EPS中PN/PS的变化情况。随着Ni2+进水质量浓度由0增加至25mg/L,LB-EPS和TB-EPS中PN/PS分别由3.32和3.70降至2.54和3.05,结果表明,由进水Ni2+浓度的增加引起的EPS中PS含量增加较PN更显著。这一变化与金属离子易促进PS合成酶的产生有关[6],并且PS分子上的羧基官能团可直接与金属离子相结合[17],这可能也是导致上述变化的原因之一。关于Ni2+浓度增加对EPS中PN/PS影响的报道并不一致,宋浩亮等[5]的研究显示,Ni2+浓度的增加导致生物膜EPS中PN/PS随之增加,这可能与微生物的种类和生存条件有关。

图2 不同Ni2+浓度下厌氧污泥LB-EPS和TB-EPS中PN和PS含量变化
2.3 不同Ni2+浓度下厌氧污泥LB-EPS和TB-EPS的3D-EEM
对不同Ni2+浓度下的厌氧污泥LB-EPS和TB-EPS进行3D-EEM分析,分析结果如图3所示。y轴和x轴分别表示荧光光谱的Ex和Em。荧光峰A(220 nm/300~340 nm)为类蛋白荧光,与芳香类蛋白物质有关;荧光峰B(270~280 nm/300~310 nm)为类蛋白荧光,与色氨酸类蛋白有关[18]。在进水Ni2+浓度为0时,峰A和峰B在厌氧污泥TB-EPS中被检测到,这表明芳香类蛋白和色氨酸类蛋白是TB-EPS的组成物质;而LB-EPS中只检测到峰A,未检测到峰B,这可能与LB-EPS中色氨酸类蛋白物质含量较低有关。进水Ni2+质量浓度为25mg/L时,厌氧污泥LB-EPS和TB-EPS中均检测到峰A和峰B,表明在25mg/L进水Ni2+浓度下,LB-EPS中生成了色氨酸类蛋白,芳香类蛋白和色氨酸类蛋白是LB-EPS和TB-EPS的重要响应物质。

图3 不同Ni2+浓度下厌氧污泥LB-EPS和TB-EPS的3D-EEM
厌氧污泥LB-EPS和TB-EPS三维荧光峰的具体峰位及峰强度参数随Ni2+浓度增加的变化情况如表1所示。进水Ni2+质量浓度为25mg/L时的荧光峰位与进水Ni2+浓度为0相比,LB-EPS中荧光峰A的荧光峰位未发生变化,TB-EPS中荧光峰A沿Em方向发生40 nm的蓝移(向短波长移动),荧光峰B沿Ex和Em方向各自发生10 nm蓝移。荧光峰峰位的移动与EPS中各组分的变化密切相关,荧光峰的蓝移与荧光基团中芳香环数、胺基、羟基、羰基以及共轭键数量的减少有关[19],大分子物质的裂解是造成荧光峰峰位蓝移的重要原因[20]。龚喜平等[21]报道了相似的结论,颗粒污泥EPS中代表芳香类物质的荧光峰蓝移与芳香环数和共轭键数丰度的减少有关。Zeng等[20]报道了相似的研究结果,芳香类物质的减少与荧光峰的蓝移相关。张倩等[22]研究认为荧光峰峰位的蓝移意味着LB-EPS和TB-EPS中芳香酯基、胺基、羰基和羟基数量的减少。与进水Ni2+浓度为0时的TB-EPS荧光峰的峰强度相比,荧光峰A和峰B的荧光强度均发生显著增强,表明在25mg/L进水Ni2+质量浓度下,TB-EPS中生成了更多的芳香蛋白以及色氨酸物质。荧光峰峰强度的变化和峰位的移动反映了进水Ni2+浓度增加导致厌氧污泥LB-EPS和TB-EPS中芳香蛋白和色氨酸蛋白物质的含量变化情况,造成这些变化的机理及相关规律需要进一步探讨。
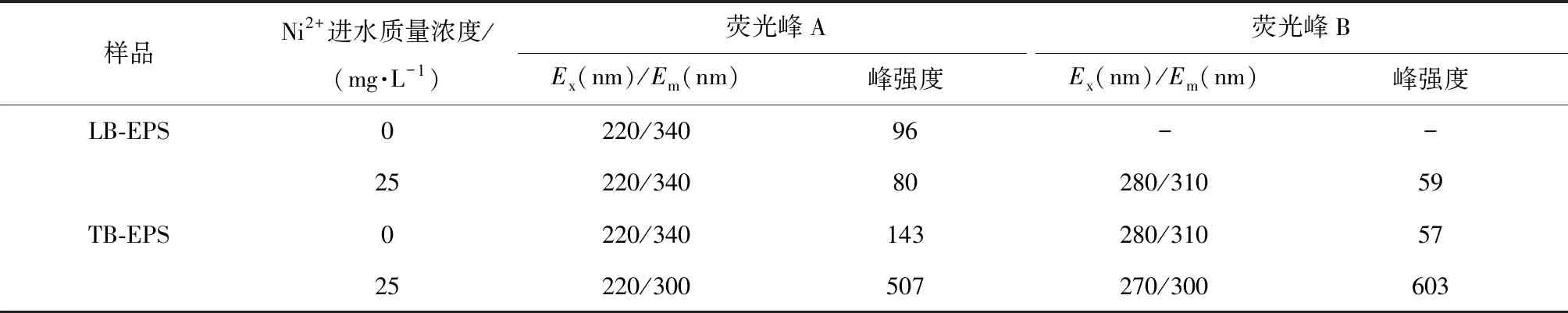
表1 不同Ni2+浓度下厌氧污泥LB-EPS和TB-EPS的荧光峰特征
2.4 Ni2+浓度变化对厌氧污泥LB-EPS和TB-EPS含量与沉降性能关系的影响
在进水Ni2+质量浓度分别为0、10、15、20mg/L和25mg/L条件下,UASB工艺出水水质稳定后,取不同进水Ni2+浓度下的厌氧污泥的SVI、LB-EPS和TB-EPS进行测定分析,分析结果如图4(a)所示。随着进水Ni2+质量浓度由0增加至25mg/L,厌氧污泥LB-EPS和TB-EPS质量分数分别由9.34 mg/g和23.20 mg/g(以MLVSS计)增加至62.91 mg/g和72.15 mg/g(以MLVSS计),LB-EPS和TB-EPS含量的增长情况与进水Ni2+浓度增加的线性关系显著,R2分别为0.908(TB-EPS)和0.966(LB-EPS)。上述结果显示,与TB-EPS相比,LB-EPS含量的变化与进水Ni2+浓度的增加关系更为显著。LB-EPS无明显边缘的黏液层,可向周围环境扩散,而TB-EPS的结构较LB-EPS更为稳定,与细胞壁结合紧密,这可能是造成LB-EPS含量更容易受到进水Ni2+浓度增加而变化的原因之一。在进水Ni2+质量浓度由0增加至25mg/L的过程中,厌氧污泥SVI由91.53 mL/g降至77.31 mL/g,SVI的变化情况与进水Ni2+浓度增加的线性关系显著,R2为0.991。厌氧污泥SVI随进水Ni2+浓度的增加而逐渐下降,表明厌氧污泥的沉降性随进水Ni2+浓度的增加而逐渐提升。为了进一步理解厌氧污泥SVI受到进水Ni2+浓度增加的影响,对不同进水Ni2+浓度下LB-EPS和TB-EPS与SVI的关系进行分析,分析结果如图4(b)所示。在进水Ni2+质量浓度由0增加至25mg/L的过程中,厌氧污泥LB-EPS和TB-EPS含量的变化情况与SVI的变化关系均表现出良好的相关性,R2分别为0.930(LB-EPS)和0.981(TB-EPS)。有学者[20]研究发现,活性污泥TB-EPS含量的变化与SVI的线性关系不明显,而LB-EPS含量的变化与SVI线性关系显著。也有学者[21]报道了不同的研究结果,LB-EPS含量变化与SVI呈现负相关,而TB-EPS含量的变化与SVI呈现正相关。这一变化可能与LB-EPS和TB-EPS的结构与含量组成有关[22-25],详细机理需要进一步探讨研究。
3 结论
(1)Ni2+浓度增加导致厌氧污泥LB-EPS和TB-EPS中PN和PS含量增加,PN/PS降低。
(2)在进水Ni2+质量浓度为25mg/L下,厌氧污泥LB-EPS和TB-EPS中芳香类蛋白和色氨酸类蛋白是重要的响应物质。
(3)厌氧污泥LB-EPS和TB-EPS含量的增加促进了厌氧污泥的沉降性能。