急性脑梗死后继发血管性认知损害风险预警模型构建与验证
倪芳琴 唐志仙 王佳敏
(绍兴市第七人民医院老年二科,浙江 绍兴 312000)
急性脑梗死(acute cerebral infarct,ACI)是目前常见的脑血管疾病,具有高致残、高死亡率的特点,是由大脑血液供应突然中断导致的脑组织软化、坏死[1]。据统计[2]发现,1990-2019年国内ACI的发病率、死亡率、伤残调整寿命年均显著增加,疾病负担加重。血管性认知损害(vascular cognitive impairment,VCI)是由脑血管疾病及其危险因素引起单一或多个认知域受损的认知障碍综合征,表现为语言、记忆、计算和执行能力等方面障碍[3]。认知损害是脑梗死的常见并发症之一,即使神经功能缺损程度较低的患者也可能出现VCI;约30%以上的脑梗死患者会出现VCI,梗死后VCI患病率甚至高达80%,严重影响了患者生活质量及家庭负担[4]。有研究[5]指出,发现脑梗死后通过调控危险因素可预防认知障碍的发生。因此,及早识别继发VCI风险高的ACI患者具有重大意义。本研究以本院收治的ACI患者为研究对象,通过对患者相关临床资料的收集,以患者治疗3个月后复诊的诊断情况进行分组,通过相关影响因素,以此构建风险预测模型并行验证,旨在为临床预防VCI提供相应参考,现报道如下。
1 资料与方法
1.1一般资料 回顾性选取我院2018年1月-2020年12月收治146例ACI患者纳入建模组样本。纳入标准:参照指南[6]中的ACI的诊断标准,经头颅影像学确诊;年龄≥18岁;临床资料完整;患者发病至入院时间≤4.5 h,并接受静脉溶栓治疗或血管内治疗;入院后接受脑梗死一般处理和特异性治疗,依从性好;治疗3个月后复诊。排除标准:既往有颅脑肿瘤、严重颅脑创伤史;脑出血或其他脑血管病者;既往有阿尔茨海默病、帕金森病史者;溶栓期间发生出血等不良事件;未按时复诊患者。本研究中共采用15个变量,参照样本量计算方法[7],样本量为变量的5~10倍,即本研究可纳入研究对象75~150例,另考虑无效率及实际情况,最终选择纳入146例患者作为建模组。建模组患者中,男性81例,女性65例;年龄52~76岁,平均年龄(64.34±8.27)岁;平均BMI为(23.13±2.46);发病至入院时间1.25~4.33 h。另选取2021年1月-2022年6月于我院收治的符合上述标准的62例ACI患者纳入验证组,其中男性35例,女性27例;年龄48~72岁,平均年龄(65.88±9.76)岁;平均BMI为(23.65±2.80);发病至入院时间1.30~4.30 h。2组患者一般资料差异无统计学意义(P>0.05),见表1。本研究为回顾性研究,对患者治疗方案未做任何干预措施。
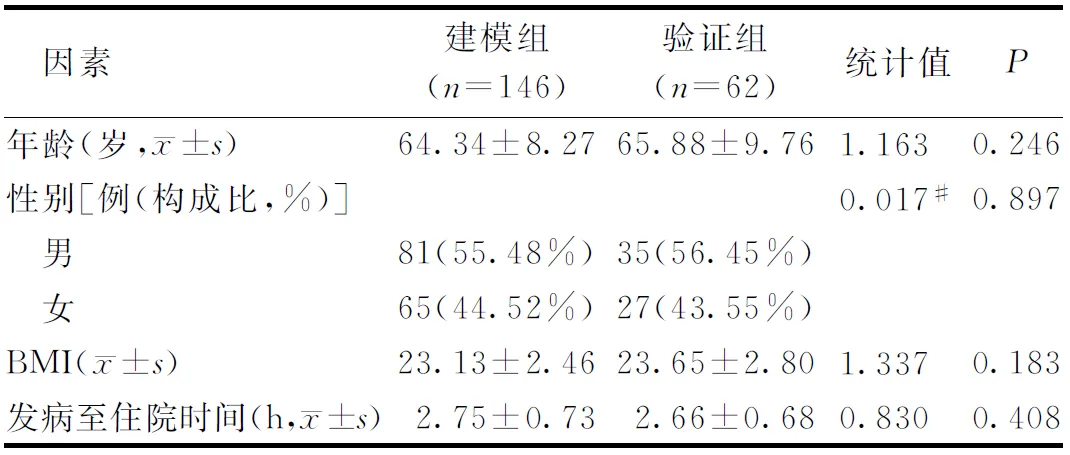
表1 建模组及验证组患者的一般资料对比分析(n=208)
1.2方法
1.2.1资料收集与分组方法 根据阅读相关文献,查阅医院信息系统,收集2组患者的相关资料,包括年龄、性别、BMI、受教育程度、吸烟史、饮酒史、高血压史、糖尿病史、高脂血症史、美国国立卫生研究院卒中量表(national institute of health stroke scale,NIHSS)评分、Fazakas评分、既往脑梗病史、梗死部位、梗死面积(Adams分类法)、同型半胱氨酸(hyc)水平。治疗3个月后复诊,参考共识[8]推荐的诊断标准,根据患者的临床评估、蒙特利尔认知评估计表(montreal cognitive assessment,MoCA)得分<22分、影像学评估情况分为VCI组或无VCI组。
1.2.2相关评估标准 (1)梗死面积[9]:脑梗死灶最大层面直径<1.5 cm为小面积,直径为1.5~5.0 cm为中面积,直径>5.0 cm 为大面积。(2)Fazekas评分[10]:评估白质病变严重程度的视觉评分量表,分开评估脑室旁和深部白质,总分为0~6分,分数越高,白质病变严重程度越高,Cronbach′s α系数0.806(P<0.001)。(3)NIHSS评估患者的神经功能[11]:一共由11项测试组成,评分为0~42分,评分越高提示神经功能损害越严重,Cronbach′s α系数0.858(P<0.001)。
2 结果
2.1建模组患者的相关资料及继发VCI的单因素分析 选取的建模组样本中,146例ACI患者共有72例后续继发VCI,继发VCI发生率为49.32%。单因素分析结果显示,患者的年龄、高血压史、多发脑梗病史、梗死面积、hyc水平、NIHSS评分、Fazakas 评分在是否发生VCI患者间差异有统计学意义(P<0.05);而患者的性别、BMI、受教育程度、吸烟史、饮酒史、糖尿病史、高脂血症史、梗死部位差异无统计学意义(P>0.05),见表2。
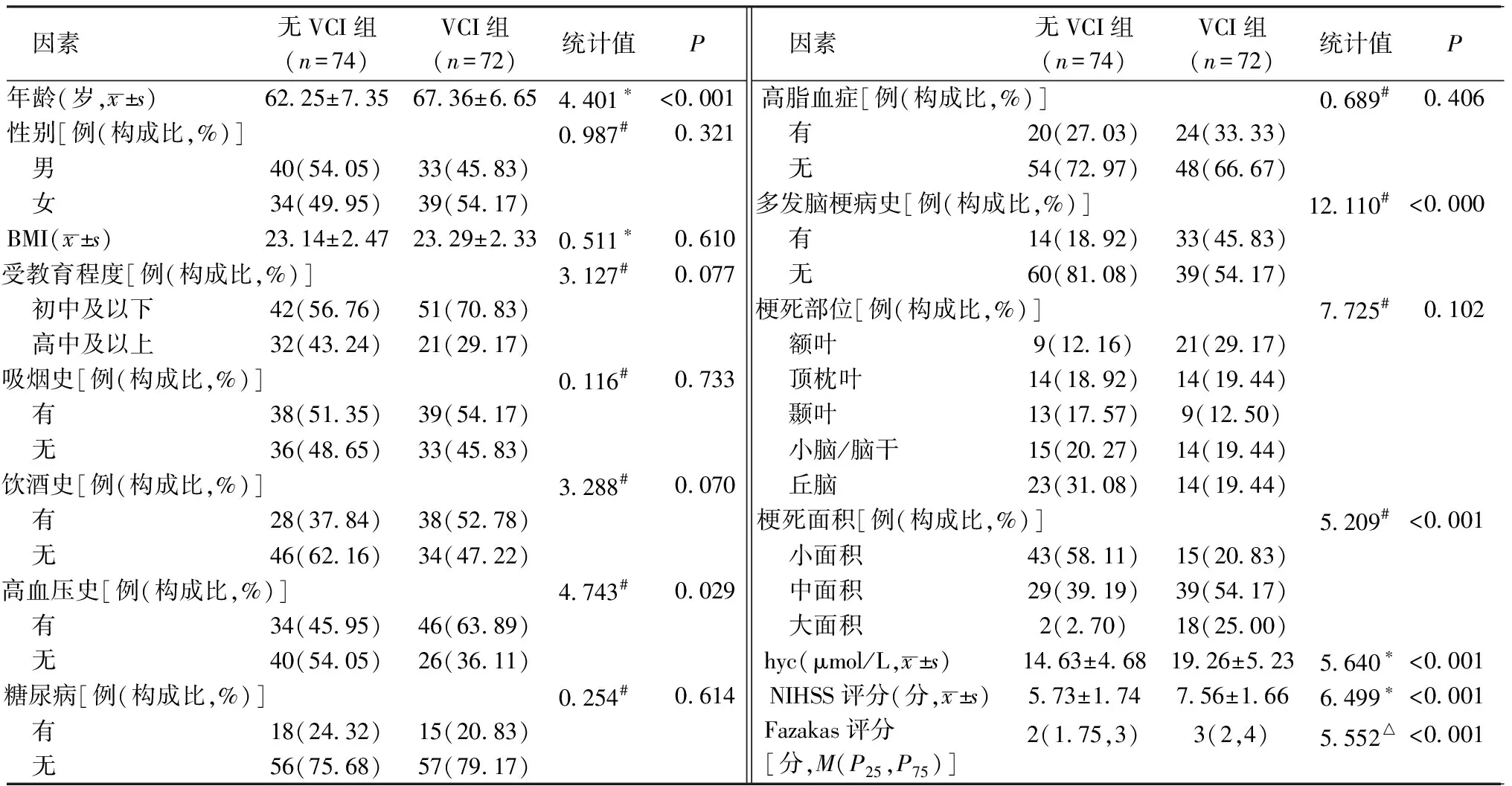
表2 建模组患者的相关资料及继发VCI的单因素分析(n=146)
2.2影响ACI患者继发VCI的多因素分析 将单因素分析中具有显著差异的相关因素代入多因素logistic回归分析,对因素变量进行赋值,见表3。多因素分析结果显示,年龄、高血压、既往梗死病史、梗死面积、NIHSS评分、Fazakas评分、hyc水平均是影响ACI患者继发VCI的独立危险因素(P<0.05),见表4。

表3 因素赋值表
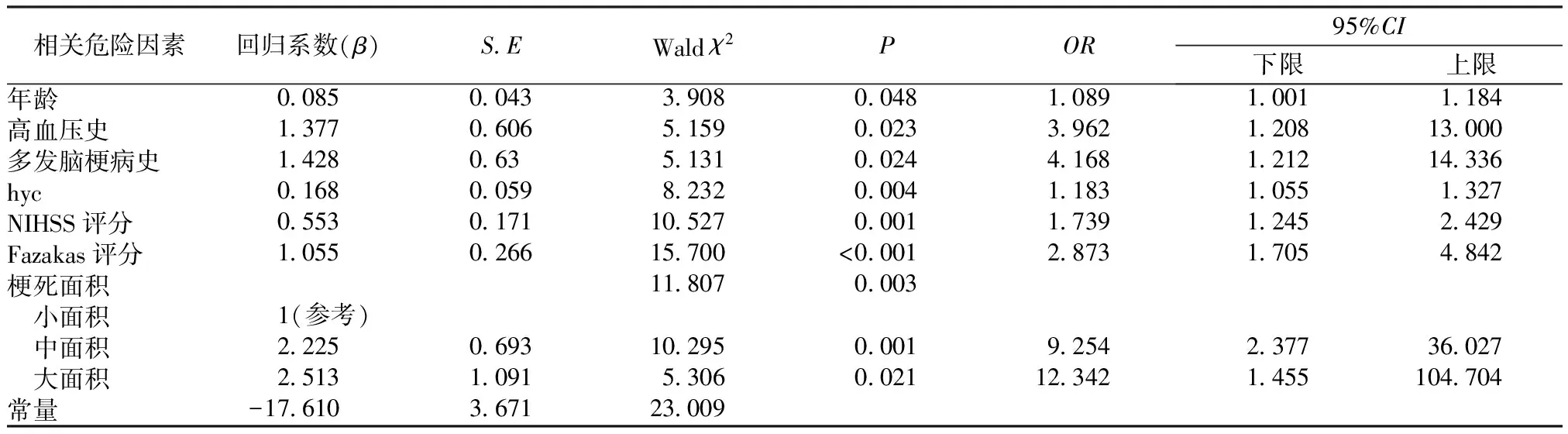
表4 影响ACI患者继发VCI的多因素分析
2.3风险预警模型的构建与ROC曲线分析预警模型的效能 选取上述结果中差异有统计学意义指标纳入构建模型,Logit(P)=-17.610+0.085×年龄+1.377×高血压史+1.428×多发脑梗病史+0.168×hyc+(1×小面积梗死或2.225×中面积梗死或2.513大面积梗死)+0.553×NIHSS评分+1.055×Fazakas评分。通过RCO曲线分析预警模型的区分度,以Youden指数作为最佳临界值,构建预警模型的ROC曲线下面积(AUC)为 0.901(95%CI:0.849~0.954),P<0.001。最大Youden指数为0.755,以最大Youden指数选取截断值(即0.562),灵敏度为83.8%,特异度为 91.7%,见图1。经 Hosmer-Lemeshow 拟合优度检验结果显示χ2=9.446,P=0.306,提示该模型预测ACI后继发VCI的概率与实际概率比较,差异无统计学意义(P>0.05),拟合度较好,预测价值高。
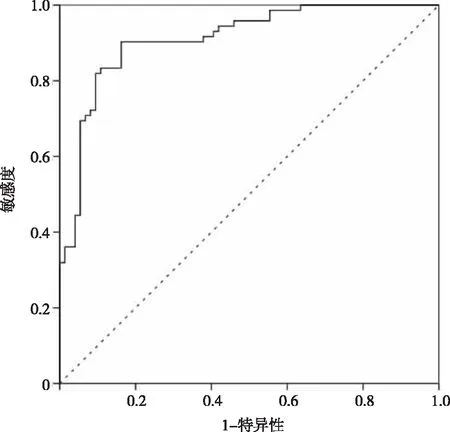
图1 ACI后继发VCI预警模型的ROC曲线
2.4风险预警模型的验证 将验证组患者(62例)各因素代入风险预测模型进行外部验证,根据预测模型的截断值,即Logit(P)≥0.562时,可认为ACI患者会继发VCI,验证组中患者实际继发VCI为30例,预测模型判断患者会继发VCI为25例,灵敏度76.66%(23/30),特异度93.75%(30/32),阳性预测值92%(23/25),阴性预测值81.1%(30/37),总准确率为85.5%(53/62)。
3 讨论
3.1构建ACI后继发VCI风险预警模型对VCI的预防具有重要意义 VCI目前被认为是继阿尔茨海默病之后痴呆症的第二大原因,VCI不仅影响患者生活、社会功能,还增加了患者的病死率[12]。脑组织缺血缺氧缺血、血脑屏障破坏、脑血管潜在危险因素、脑血光疾病损伤等都可能是引起VCI的病因[13]。伴随ACI治疗的进展,患者死亡风险下降,而ACI发病后继发VCI的人数却持续增加,临床上应重视ACI后可能继发VCI的高危人群,及早给予针对性预防。故探索影响ACI继发VCI的相关危险因素、构建相应的预测模型对疾病的预防具有重要意义。
3.2危险因素分析 本研究中,建模组ACI患者继发VCI的概率为49.32%,验证组为48.38%,与尹立勇等[14]研究结果相近。本研究中多因素分析结果显示,年龄、高血压、既往梗死病史、梗死面积、NIHSS评分、Fazakas 评分、hyc水平均为影响ACI患者继发VCI的独立危险因素。年龄因素可能与患者暴露于各种脑血管危险因素的时长有关,是导致认知功能变化的潜在因素,即便是非脑梗患者也会出现认知功能减退[15]。高血压是心脑血管终点事件的高危因素,患者升高的血压变异性会导致脑皮质中的神经纤维缠绕沉积,引发脑小血管病(白质病变、脑损伤、微出血),导致脑循环失调,认知功能受损[16]。反复发作脑梗和中、大面积梗死的患者相对脑组织的损伤更大,缺血缺氧相对严重,可进展为脑萎缩,因此继发VCI的概率更高,与李冰鹤等[17]研究结果相似。NIHSS评分为反映患者神经功能损伤程度的评估指标,ACI的发生导致多区域的神经细胞变形或死亡,进而导致患者接受外界信息能力减弱,认知功能下降。hyc已被证实可通过改变血管活性介质的释放导致血管内皮功能障碍,高水平的hyc还能通过阻滞细胞甲基化过程,损伤神经元,致使认知功能受损[18]。据向慧等[19]研究显示,NIHSS评分升高、hyc水平升高是继发认知障碍的危险因素,与本研究相符。Fazakas 评分为评估脑白质病变严重程度的工具,研究[20]报道,脑白质病变的患者可能存在延迟回忆、执行力减退等认知领域的受损。
3.3ACI后继发VCI风险预警模型的实用性及可靠性 目前,关于ACI患者VCI继发率差异大,存在认知功能评估不足等问题,罕有公认的针对ACI患者继发VCI的风险评估体系[21]。Lim等[22]采用NINDS-CSN量表预测卒中后3个月的重度VCI,AUC为0.74;截断值为6或7分,敏感度和特异度分别为0.82和0.67;Kandiah等[23]根据患者资料和神经影像学特征构建SIGNAL2风险评分模型,包括年龄、教育程度、急性皮质梗死、慢性腔隙数量、皮质萎缩程度和颅内大血管狭窄等因素,模型AUC为0.829,预测短期发生VCI的敏感度和特异度分别为82.1%和68.0%。本研究基于上述危险因素构建风险预警模型,模型经ROC曲线分析,结果显示其AUC为0.901(95%CI:0.849~0.954),灵敏度为83.8%,特异度为91.7%,拟合程度良好,且经外部验证发现其具有良好的风险评估效能,预警价值高,优于上述研究预测模型,或可作为ACI患者发病后的VCI风险评估工具。同时,该模型也存在不足,如模型通过单中心和回顾性的研究资料构建,模型是否适用于其他医院的患者尚未明确,且在进行单因素分析时可纳入的指标受限,这可能造成相关危险因素的遗漏。因此,后续仍需多中心、大样本量的前瞻性研究对本研究结果加以证明,以提高模型的实用性及可靠性。
综上所述,年龄、高血压、既往梗死病史、梗死面积、NIHSS评分、Fazakas 评分、hyc水平均为影响ACI患者继发VCI的独立危险因素。本研究构建风险预警模型的预测效能较为良好。但本研究为回顾性研究,存在一定的局限,对目前研究可能与VCI有关的部分生物学标记物纳入不全(如脑脊液内淀粉样蛋白、载脂蛋白H等),后续待进一步研究。

