联碱碳化塔“挂硫”除铁的可行性分析
赵沁乐,田宏伟
(重庆湘渝盐化有限责任公司,重庆 万州 404000)
纯碱产品含铁量高,导致产品出现“色碱”的质量问题,一直困扰建厂早、设备投运时间长的纯碱生产企业,在不更换碳钢设备的前提下,稳定、持续产出高质量的纯碱产品,是市场的需求也是经济效益的保证。目前联碱生产中传统的除铁理论认为,通过加硫能在碳化塔内壁与铁生成Fe离子薄膜,以保护碳化塔内壁不受腐蚀,我厂在下段气中通入H2S气体拟替代加入Na2S的方法,该方法反而加剧了产品含铁,因此,有必要对传统“挂硫”除铁方法的可行性进行进一步分析论证。
1 联碱体系中铁杂质的来源
联碱生产中母液系统不可避免地会含有一定量的铁,其来源有四种:1)作为原料的盐中夹带铁;2)铸铁设备内壁发生电化学腐蚀析出铁;3)固体颗粒与设备内壁发生磨蚀脱落细小铁;4)碳钢设备腐蚀脱落微粒铁。以上来源中,第2、3、4种原因可以通过更换碳钢设备从根本上解决产品含铁的问题,但此方法不经济也不可行;第1种来源,即使对原盐进行精制除铁,也面临不能根除后续工序混入铁的问题,必须通过其他手段降低纯碱产品中的铁含量。
对反应体系与设备内壁的反应作进一步区分,在正常生产中,联碱母液中的铁主要来源于盐水(原盐)精制、吸氨、碳化三个工段,而各工段进入联碱母液的铁含量也有所不同。在盐水(原盐)精制工段中,饱和盐水中的氧含量较低,设备内壁的盐沉积也起到了保护作用,因而带入铁较少;在吸氨工段中,由于大量吸氨溶液的氧含量也较低,同时联碱母液中的Ca、Mg杂质在碱性条件下沉积在内壁,带入的铁杂质也较少。而在碳化工段中,由于联碱母液pH降低加剧酸腐蚀、体系反应温度升高会加快反应速率、气液接触频繁剧烈扰动增大接触面积,加之参与碳化反应的碳化塔数量多,所以纯碱产品中的铁应该有75%~80%来自该工序。
因此要降低产品的铁含量,应重点关注碳化塔中的碳化反应过程。
2 碳化工序中相关副反应
2.1 铁进入碳化液的反应
铸铁设备内壁的铁单质与碳化液接触,由单质铁变为二价铁离子:
Fe-2e-=Fe2+
生成的二价铁离子很不稳定,很快会被溶解氧氧化为三价铁离子。多余的电子积累在与碳化液接触的设备内壁上,形成双电层结构,碳化液中的溶解氧在铸铁设备内壁上发生去极化反应:
O2+4e-+2H2O=4OH-
上述两反应构成原电池,当碳化塔清洗停车时,曝空导致溶解氧含量增加,加剧上述反应。因此电化学腐蚀在碳化塔中长期存在并不断在进行,铁源源不断地进入碳化液。
2.2 原料气中硫化氢与铁的反应
由于碳化塔中的温度与标准状态偏离不大,高压又有利于吸收气体的反应,故计算中用标准状态下的平衡常数近似评估实际反应进行的程度。下列计算过程中所用数据列于表1中。

表1 相关物质的各类常数
硫化氢在碳化塔中可能发生如下反应:
①与碳酸氢根发生质子传递
该反应的标准平衡常数计算为:
②与游离氨发生酸碱中和反应
两反应的标准平衡常数分别计算为:
③与二价铁离子生成硫化亚铁沉淀
Fe2++H2S+2OH-=2H2O+FeS↓
该反应的平衡常数为:
④与三价铁离子发生氧化还原反应

由碱性条件下的标准电极电势,根据能斯特方程计算该反应的平衡常数为:
由于K4>K2>K1>K5>K3,绝大部分硫化氢进入碳化液后会与亚铁离子结合产生FeS。
其中:Ka(H2S)1为H2S的一级电离平衡常数;
Ka(H2S)2为H2S的二级电离平衡常数;
Ka(H2CO3)1为H2CO3的一级电离平衡常数;
Kb(NH3)为NH3的电离平衡常数;
Kw为水的离子积常数(55 ℃);
Ksp(FeS)为FeS的溶度积;
n为反应转移电子数;
EΘ为反应的标准电势,为反应正、负极标准电极电势之差。
2.3 母液中的硫离子与铁的反应
硫离子在碳化塔中可能发生如下反应:
①与碳酸氢根发生质子传递
其反应标准平衡常数计算为:
②与亚铁离子生成沉淀

查标准溶度积常数表可知该反应的平衡常数为:
由于K7>K6,绝大部分硫离子进入碳化液后会与亚铁离子结合产生FeS。
第2.2节与第2.3节的计算结果表明,以H2S或是S2-的形式向碳化塔中引入硫均会生成FeS,但不能确定其存在形式:既可能是保护膜,也可能是沉淀。
3 碳化塔中FeS及其他保护膜的存在状态分析
传统的碳化理论认为加硫的意义是在碳化塔内壁形成FeS薄膜,起到阻止进一步腐蚀的发生。然而在长期的实际生产中观察到,即使向碳化塔中加硫也无法阻止纯碱产品发红,向碳化塔中配入硫化氢气体反而使产品中铁含量进一步增加。因此,有必要对FeS是否在碳化塔中形成薄膜、FeS是否能在碳化塔中稳定存在重新进行研究。
3.1 向CO2气中配入H2S的试验结果分析
我厂通过在CO2气中配入H2S的方式探究该理论的合理性。图1为生产稳定的条件下CO2气中H2S含量和轻灰产品铁离子含量随时间的变化情况。
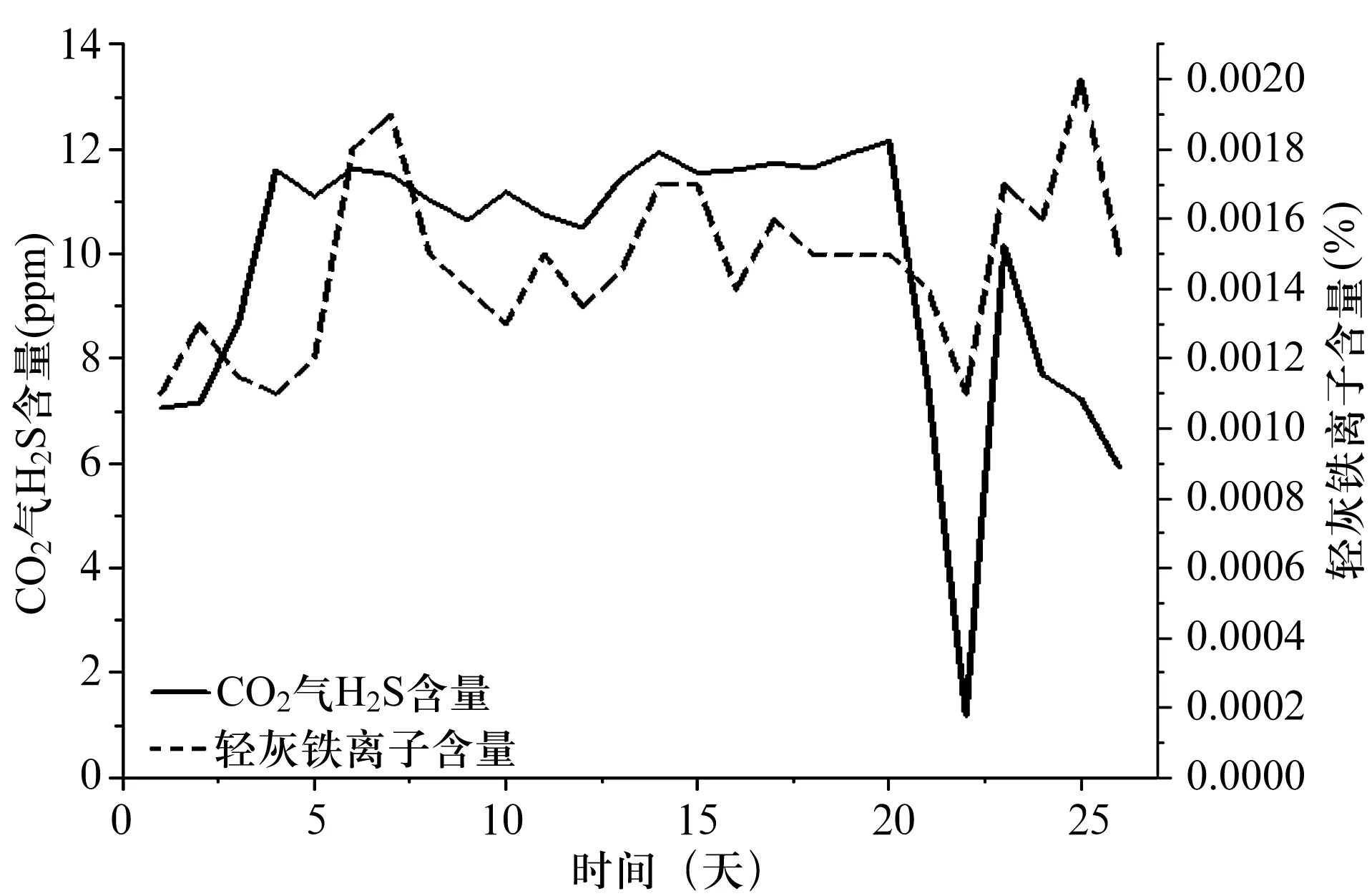
图1 CO2气中H2S含量和轻灰产品铁离子含量变化图
若碳化塔设备内壁能生成FeS薄膜,则配入H2S含量的增加有利于保护膜的生成,应当使得轻灰产品中的铁含量降低。然而图中CO2气中H2S含量和轻灰产品铁离子含量的变化趋势大体一致, 即配入H2S含量增加,产品中铁含量也增加,这一事实表明配入的H2S并没有形成有效的保护膜,反而加重了碳化塔中的腐蚀情况和产品中的铁含量。
同时,还对联碱生产中相关液体中的铁、硫离子含量进行了追踪,如图2所示。

AⅡ母液 清洗AⅡ母液
可见各类液体中的铁含量变化趋势均与CO2气中H2S含量变化趋势一致,由于沉淀溶解平衡,S2-含量变化趋势与之相反。另外,进入碳化塔的清洗AⅡ中的铁含量是最高的,原因是联碱生产中绝大部分电化学腐蚀都发生在碳化工段,而碳化塔洗塔时需要将塔壁结疤冲刷除去,不仅反应条件更剧烈,还增大了设备内壁与清洗液的接触面积,因此腐蚀情况最为严重。各类液体和产品中较高的Fe含量也表明,通入H2S并不能将体系中的铁有效去除。
3.2 碳化塔中不存在FeS薄膜
事实上,FeS薄膜在实验室中制备的要求较高,通常需要制备均匀的前驱体溶液和特定的基底,在严格的反应条件下处理、沉积得到。在反应剧烈、物料组成复杂的碳化塔中,仅通过添加S2-是不能得到稳定且具有抗腐蚀性的FeS薄膜的。
另外,若加硫能在碳化塔中生成FeS薄膜(即“挂硫”),则由于气相在整个碳化塔内分布更均匀、更充分,通入气相H2S的“挂硫”效果应当优于加入Na2S水溶液的效果,然而事实证明随着H2S浓度的升高,产品中铁含量也随之上升,这表明H2S并没有起到在设备内壁生成FeS的作用,反而使得游离状态的Fe2+生成沉淀,与产品一同被取出。
由表1可知,H2CO3的一级电离酸性强于H2S的二级电离酸性,在碳化塔中H2CO3的浓度又很大,因此可以推动碳化液中发生下述反应:

由于Fe(HCO3)2会迅速发生双水解生成氢氧化亚铁和碳酸,随后氢氧化亚铁迅速被氧化为氢氧化铁,其溶度积常数难以获取,因此无法从数值上计算平衡常数;但基于反应物的高浓度以及生成物能不断被移走的事实,可以判断平衡具有正向进行的推动力,即生成的FeS会被碳化液不断溶解再转化为沉淀,自然也就无从谈起由FeS薄膜保护设备内壁了。
此外,传统的“挂硫”理论存在矛盾:对碳化塔与母液接触的内壁而言,由于生产中产生碳酸氢钠结疤,即使存在内壁保护膜也会被覆盖而不能长时间起保护作用;对碳化塔不与母液接触的内壁而言,由于并不发生电化学腐蚀和磨蚀,也就没有形成保护膜的必要了。
3.3 向碳化塔内加硫的弊端
溶液中的FeS是一种絮状沉淀,一部分在碳化塔底部生成的H2S还未被完全溶解就包裹在碳酸氢钠结晶上被同一取出,阻止结晶生长、恶化晶体形态,随碳酸氢钠进入滤碱机后还会恶化滤饼透气性和透水性、堵塞滤布孔,进而造成母液损失。
因此在碳化塔中直接产生FeS对生产极其不利,实际生产中需要同时控制Fe与S2-的浓度处于较低水平。当溶液中的离子浓度满足c(Fe2+)c(S2-) 有文献提到向母液中添加MgCl2以在碳化塔内壁形成结疤的方式对碳化塔内壁进行保护,但这种方式仍然存在一些弊端,现讨论如下: 1)无法准确控制结疤位置与厚度。碳化塔内是一个复杂的反应体系,反应较为激烈,很难控制结疤在生产需要的位置产生适当的厚度。 2)结疤对碳化塔生产不利。由于无法准确控制结疤,加上低温更有利于产生沉淀,可见结疤会无法避免地产生在冷却段,与碳酸氢钠结晶共同结疤,导致生产效率降低、碳酸氢钠结晶变细、碳化塔工作周期缩短。 3)碳化塔在生产中频繁清洗。洗塔的目的是除去碳酸氢钠结疤,因此无法保证镁疤能在该过程中得以保存。 4)降低了产品纯度。加入的MgCl2生成沉淀混入碳酸氢钠晶体中,反而造成产品镁含量偏高,主含量降低。 考虑到碳化塔内的反应条件与洗塔的需求,虽然通过直接向母液中添加试剂以期生成保护膜的方式是不现实的,但碳化塔生产中产生的碳酸氢钠结疤在一定程度上起到了保护冷却段碳化塔内壁的作用,且无需额外加入其他物质(如MgCl2),避免了影响产品纯度。因此,对传统的索尔维塔应当控制清洗条件,避免过度清洗导致塔内结疤全部脱落而暴露碳化塔内壁;同时控制碳化塔负荷,避免负荷过高放热增加加快腐蚀速率,以及塔内压力过高使母液接触到未被结疤覆盖的部分加重腐蚀。 清洗程度在实际生产中很难控制,若清洗不足反而会缩短碳化塔工作周期,因此该方案只作为长期运行的设备的备选方案。对于新建的设备,要彻底控制产品铁含量,应当从改良碳化塔内壁材质和覆盖防腐涂层两方面入手。 联碱的碳化工段不仅是电化学腐蚀最严重的工段,也是初步得到纯碱产品的工段,同时又不能直接在碳化塔中除铁,在这一点上存在一定的矛盾。由于碳化塔后的设备内壁也会产生电化学腐蚀,联碱生产的母液又处于循环中,若不进行除铁将导致铁离子不断积累;同时较高的铁离子含量也更易导致FeS的析出,对生产造成不利影响。 综合考虑上述因素,最适合除铁的位置应在母液进入碳化塔之前,将一轮循环积累的铁尽可能除去,让处理后的母液通过最少的设备进入碳化塔。由于联碱生产设计在AⅡ桶前往往设有澄清桶,FeS作为絮状沉淀需要较长的时间完全沉淀或被反应除去,因此可利用澄清桶完成充分的除铁工作,实际生产中往往也在澄清桶中加入Na2S,只是加入的S2-的作用并非随母液进入碳化塔形成保护膜,而是直接在澄清桶中将铁沉淀除去。此方法应该是联碱除铁的最重要手段,而非碳化塔的“挂硫”操作。但是AⅡ桶需定期排放的“AⅡ泥”的处理令联碱生产企业非常头痛。 当CO2中H2S含量较高时,可利用这部分H2S进行除铁,即在碳化塔前设置“预碳化”工段,将CO2通入AⅡ液中提高碳化度的同时令FeS沉淀。这样不仅利用了CO2中的有害成分,还降低了脱硫和除铁的成本。 要从根源上解决纯碱产品含铁高的问题,则需彻底更换碳化塔内部材料,使用高强度有机材料内衬或防腐涂层等杜绝碳化液在碳化过程中与铁质内壁的接触。近年来侯氏制碱法的碳化塔开始改用碳钢制造,并内衬防腐蚀层;冷却小管用不锈钢或钛材制造,以尽可能减少腐蚀。 目前针对碳化塔内防腐已开发了多种材质,包括将不锈钢和钛材钝化再结合牺牲阳极的电化学保护法,以及新的碳钢—不锈钢复合材质,塔内件采用不锈钢或钛材质,耐蚀性好,使用寿命长,平时不需维修,运行中不必加Na2S,设备制造周期短,产品白度高,可以大型化。设备材质虽然升级但重量轻,大型化后设备数量减少,相应费用下降,其总投资不会比采用铸铁塔高。 碳化塔内壁涂料包括环氧玻璃鳞片衬里、阳离子氯丁胶乳水泥砂浆、钝化金属层等;还有一些全新结构的碳化塔正在开发中。碳化塔的防腐改造途径已经十分完备,虽然一次投资成本较高,但能从根源上解决产品含铁的问题,还避免了化学除铁存在的环保问题,因此是最为经济合理的处理方法。 纯碱产品出现含铁高的现象时,应严格控制原料气中H2S含量,向碳化塔中直接引入任何形式的硫不仅不能生成FeS保护膜,还会使产品中铁含量进一步升高。另外,传统采取的加硫措施不能从根源上解决纯碱产品铁含量高的问题,应对碳化塔内壁采取防腐措施,新建碳化塔应选择抗腐蚀性更好的非碳钢材料;对于已经投产的碳化塔,可采取控制清洗程度和负荷的方法,利用结疤保护碳化塔内壁。本文结合我厂实际生产中的情况提出以上一些建议,供各位同行参考。3.4 结疤保护层在碳化塔内的工作情况
4 联碱生产中除铁方案的选择
4.1 化学除铁位置的选择
4.2 碳化塔新材料的选择
5 结 语

