临床药师参与化脓性脑膜炎肥胖患儿个体化治疗分析
刘晓玲,吕萌,王营,陶兴茹,张胜男*
郑州大学附属儿童医院,1药学部,2神经内科,郑州 450018
化脓性脑膜炎也叫细菌性脑膜炎,是由各种化脓性细菌引起的以脑膜炎症为主的中枢神经系统感染性疾病[1]。该病致残率高,神经系统后遗症发生率占存活儿的1/3,是小儿严重感染性疾病之一[2],具有起病急、发展快、病情重等特点,治疗关键是及时合理应用抗菌药物。临床药师作为药物治疗团队的一员,越来越多地参与到化脓性脑膜炎患者的用药管理中,协助医生改善患者治疗效果,保障患者用药安全,减少患者经济负担,提高用药依从性[3-5]。本研究报道了1例化脓性脑膜炎肥胖患儿治疗病例,深入探讨临床药师在药物选择、剂量调整、不良反应处理等方面的作用,以期为医生和临床药师对此类患者的共同管理提供参考。
1 病例资料
患儿,女,8岁,身高141cm,实际体重(total body weight,TBW)53.8kg,理想体重(ideal body weight,IBW)[6]32.8kg。主因发热2周余,间断头痛、呕吐12天,于2022年5月31日收入该院神经内科。患儿有左耳中耳炎病史,行耳道冲洗和口服抗菌药物缓解。2022年5月16日出现发热伴左耳痛、流脓,先后至诊所、县医院对症治疗,但治疗效果较差,并出现剧烈头痛、呕吐等表现。5月20日于当地妇幼保健院住院治疗,诊断为:化脓性脑膜炎、左耳中耳炎。5月20~30日,均给予注射用头孢曲松钠(2g,q12h),注射用万古霉素(0.75g,q6h)抗感染治疗,治疗后患儿仍有间断发热。入院查体:体温37℃,呼吸21次/min,心率92次/min,血压100/60mmHg,体格检查无异常。辅助检查:5月20日血常规示:白细胞计数(white blood cell count,WBC)12.78×109/L,中性粒细胞百分率(NEUT%)94.5%,C反应蛋白(C reactive protein,CRP)定量测定152.74mg/L;5月21日脑脊液常规示:WBC 1680×106/L,多核细胞91%;脑脊液生化示:糖2.04mmol/L、蛋白771.9mg/L;5月23日脑脊液宏基因二代测序技术(metagenomics next-generation sequencing,mNGS):中间链球菌(序列数272),生痰二氧化碳噬纤维菌(序列数156),具核梭杆菌(序列数60),直肠弯曲菌(序列数19);5月26日WBC 13.76×109/L,NEUT% 70.4 %,CRP 17.16mg/L;5月27日脑脊液常规示:WBC 89×106/L,多核细胞78%;脑脊液生化示:糖1.48mmol/L、蛋白936.4mg/L。
2 治疗过程
入院后,医生电话联系临床药师协商患儿抗感染治疗方案,考虑该患儿院外已规范治疗10天,脑脊液细胞数下降,生化指标好转不理想,临床仍有发热、呕吐、精神差等表现。临床药师建议给予美罗培南联合万古霉素抗感染治疗。药物剂量方面,因患儿肥胖,查阅相关文献后,建议美罗培南依据IBW给予,万古霉素依据TBW给予,总用量超成人量时按成人量计,医生采纳临床药师建议。
入院后患儿体温正常,第2天(6月1日)晨查房发现患儿面部、前胸、后背散在红色皮疹,压之不褪色。请皮肤科会诊,考虑为紫癜。给予维生素C注射液(瑞阳制药股份有限公司,国药准字H37022063,规格2ml∶0.5g)1g临时静脉滴注、糠酸莫米松乳膏(湖北恒安芙林药业股份有限公司,国药准字H20074173,规格10mg∶10g)0.1g 外用对症支持治疗。药师考虑该患儿院外已高剂量静脉应用头孢曲松联合万古霉素10天,有皮疹。需警惕药疹的可能,建议密切监护患儿皮疹情况,必要时调整用药。
入院第4天(6月3日):患儿头晕较前减轻,未再呕吐,面部、前胸、后背皮疹较前明显消退。双耳内镜检查未见明显异常,纯音听阈示患儿左耳高频听阈损伤。医生担心万古霉素会加重患儿听力损伤,更换为利奈唑胺葡萄糖注射液(Pfizer AS,国药准字HJ20160301,规格300ml∶利奈唑胺0.6g与葡萄糖15.0g)0.5g,q8h静脉滴注。
入院第11天(6月10日):患儿治疗顺利,临床症状好转,复查脑脊液指标较前好转:有核细胞计数67×106/L,多核细胞5.9%,葡萄糖2.41 mmol/L,脑脊液蛋白532.0mg/L。
入院第14天(6月13日):患儿一般情况可,用药方案调整:利奈唑胺葡萄糖注射液改为利奈唑胺片(Pfizer Pharmaceuticals LLC,国药准字H20181089,规格600mg)0.5g,q8h,po。WBC 2.87×109/L,NEUT% 43.7%,中性粒细胞计数(NEUT#)1.25×109/L。患儿WBC、NEUT#减少,临床药师考虑为利奈唑胺引起的血液系统不良反应,建议送检利奈唑胺血药浓度(Cmin),以便调整剂量,医生采纳建议。
入院第15天(6月14日):利奈唑胺Cmin17.1mg/L,临床药师建议调整利奈唑胺用法用量为0.3g,q8h,po,2天后复查利奈唑胺Cmin,医生采纳建议。
入院第17天(6月16日):停用美罗培南,查利奈唑胺Cmin7.0mg/L;WBC 3.33×109/L,NEUT%44.5%,NEUT# 1.48×109/L。利奈唑胺Cmin下降,血常规好转,临床药师建议继续目前用量应用,并密切监测血常规。
入院第18天(6月17日):患儿准予出院,出院带药:利奈唑胺片0.3g,q8h,po;利可君片20mg,tid,po。临床药师对患儿及家属进行用药教育。
临床药师于6月21日电话联系患者家属,询问当地检查结果,血常规示:WBC 5.32×109/L,NEUT#3.05×109/L,基本正常,患儿回家后无不适表现,预后良好。本次入院主要治疗及药物情况见表1。
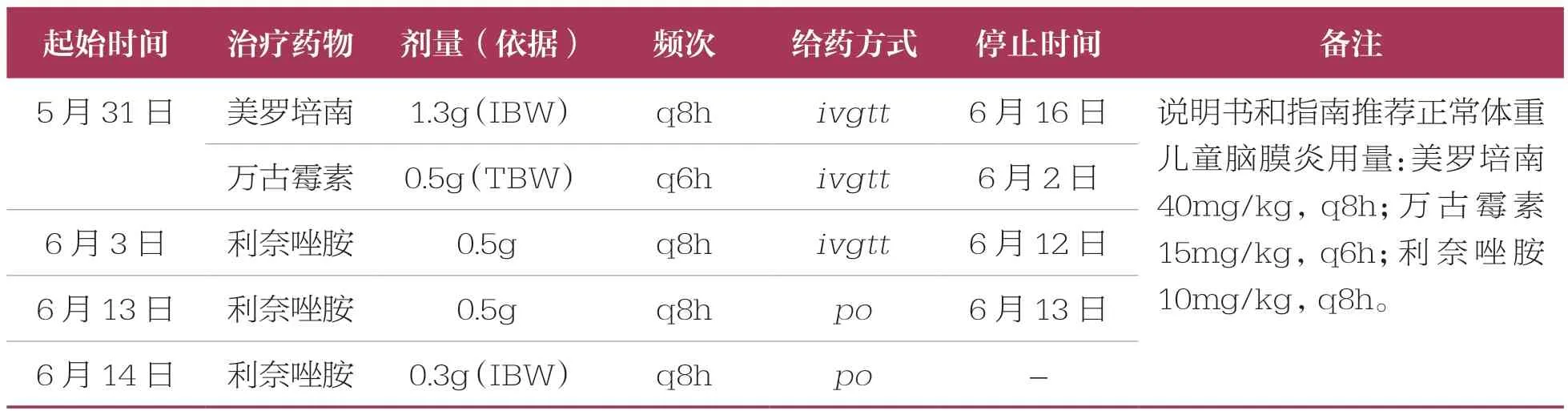
表1 主要治疗及药物情况
3 用药分析
3.1 初始抗感染用药分析
本研究为1例化脓性脑膜炎肥胖患儿病例,主要治疗手段为抗感染治疗。根据国内外细菌性脑膜炎相关诊疗指南和共识[7-10],该病强调早期足量足疗程应用合适的抗菌药物。初始经验性治疗时,需结合患儿年龄、细菌入颅途径、颅外感染灶、该地区脑膜炎常见细菌谱及细菌耐药情况等几个方面进行综合判断,选择合适抗菌药物。我国肺炎链球菌多见,该菌脑膜炎型菌株耐药率高,可将三代头孢(头孢曲松/头孢噻肟)联合万古霉素作为初始经验治疗方案[10]。针对病原菌明确的患者[7-12],目标治疗需选择对病原菌敏感且能较高浓度透过血脑屏障的药物。本病例患儿为8岁女童,疫苗接种史正常,社区发病,左耳有中耳炎病史,考虑可能的致病菌为肺炎链球菌、流感嗜血杆菌等,5月20日于外院经验性给予头孢曲松联合万古霉素抗感染治疗,5月23日脑脊液mNGS示中间链球菌(序列数272),生痰二氧化碳噬纤维菌(序列数156),具核梭杆菌(序列数60),直肠弯曲菌(序列数19)。临床未予调整用药,继续前方案抗感染治疗。转至该院,针对脑脊液mNGS所检出细菌,药师查阅文献获知,上述细菌是人类口腔和胃肠道正常菌群的成员,主要存在于口腔,为条件致病性兼性或专性厌氧菌,可引起口腔颌面部感染、头颈部感染、血流感染、中枢神经系统感染等[13-15],通常对β内酰胺类抗菌药物敏感,但对于产β内酰胺酶类的菌株,不宜选择青霉素和头孢菌素类抗菌药物[16]。中间链球菌属于米勒链球菌群的一个菌种,该菌群的主要特征是容易形成感染部位脓肿[13,17],询问患儿病史并查体,未获得口腔、胃肠道感染相关病史和体征,无牙周脓肿、腹泻等临床表现。文献报道中间链球菌多引起需氧菌厌氧菌混合感染[16],结合患儿病史和院外治疗情况,药师考虑无法排除肺炎链球菌、流感嗜血杆菌等感染可能,入院后抗感染用药方案建议美罗培南联合万古霉素治疗,医生采纳临床药师建议。
3.2 肥胖儿药物剂量分析
儿童用药剂量非常重要,计算方法依据体重、年龄和体表面积[18],大多数抗感染药物儿童给药剂量依据体重计算。本病例患儿TBW 53.8kg,体重 指 数(body mass index, BMI)27.06kg/m2,IBW 32.8kg,过量的脂肪组织会改变药物的分布、代谢和清除[6],主要体现在药物的表观分布容积(apparent volume of distribution,Vd)、清除率(clearance,CL)和蛋白结合率等参数的改变,而给药剂量受上述指标的影响,因此如何给予肥胖患儿一个安全有效的合理剂量,是该患儿的治疗重点。
抗菌药物依据其亲水疏水基团分为亲水性药物和亲脂性药物[19],理论上,对于水溶性抗菌药物,由于其难以进入脂肪组织,若使用TBW计算给药剂量,Vd易被高估,导致体内Cmin偏高,所以通常使用IBW或校正体重(adjusted body weight,ABW)来推算。针对亲水性抗菌药物,如头孢吡肟、头孢他啶、美罗培南、哌拉西林他唑巴坦等,在肥胖人群给药剂量的研究数据均来自成人,剂量依据ABW计算[20-21]。因ABW适用于成人,而IBW更适用于儿童[6],故对于本病例患儿临床药师建议美罗培南剂量根据IBW给予。亲水性药物万古霉素的药动学研究较为成熟,儿童研究的数据表示,肥胖儿童Vd基本不变,半衰期增加,CL显著增加[22-23];对于肥胖儿童,相关指南建议以TBW计算药物剂量,并进行治疗药物监测(therspeutic drug monitoring ,TDM)[24]。故临床药师建议本病例患儿万古霉素剂量依据TBW计算,考虑用药安全性,总量超过成人剂量时,按成人量算。利奈唑胺属于中度亲脂性抗菌药物,其进入脂肪组织的能力较强,可以按照TBW给药。成人研究数据表明[25],对于总体重150kg以下人群,推荐600mg,q12h固定剂量,不需要调整。本病例患儿利奈唑胺的初始用药剂量,医生根据说明书推荐剂量按TBW给予0.5g,q8h静脉滴注,临床药师未干预。
4 讨论
4.1 不良反应分析
患儿6月1日查血常规基本正常;6月3日开始使用利奈唑胺0.5g,q8h,ivgtt;6月13日复查血常规示WBC减少(2.87×109/L)、NEUT#减少(1.25×109/L);查利奈唑胺Cmin偏高;6月14日利奈唑胺用法用量调整为0.3g,q8h,po;6月16日血常规示WBC 3.33×109/L,NEUT# 1.48×109/L;6月21日当地复查血常规示WBC 5.32×109/L,NEUT# 3.05×109/L。利奈唑胺上市后的临床应用中,儿童和成人均有引起骨髓抑制的报道,发生频率归类为少见(≥1/1000至<1/100),主要出现在用药时间超过28天的患者,但在用药时间较短的患者中也有报道。该患儿出现粒系细胞减少与利奈唑胺应用有合理的时间关系,且减量后该反应减轻,无法用原患疾病或合并用药来解释,不良反应报告评价为很可能。
4.2 利奈唑胺TDM
本病例患儿利奈唑胺初始剂量依据TBW给予0.5g,q8h静脉输注,后续发生骨髓抑制,查Cmin17.1mg/L偏高,超正常范围2~8mg/L,即过高的药物浓度和血液系统相关不良反应的发生呈正相关[26-28]。提示利奈唑胺在肥胖患儿中的给药剂量不应依据TBW,原因可能是肥胖重症患儿的药动学数据受多种病理生理因素影响而发生变化[29-30]。临床药师根据Cmin推算体内剂量,并依据IBW,调整利奈唑胺用法用量为0.3g,q8h,po,查Cmin7.0mg/L,该剂量下监测WBC、NEUT#逐渐恢复正常。因此,由Cmin指导的利奈唑胺个体化给药,在临床实践中很有必要,尤其对于儿童危重患者。目前暂无肥胖儿童使用利奈唑胺的药动学相关数据,迫切需要开展肥胖儿童群体药动学及药效学相关研究,指导过重或肥胖儿童用药。
综上所述,临床药师参与1例化脓性脑膜炎肥胖患儿的治疗过程,通过查阅相关指南和文献,与医生共同制定抗感染治疗方案,确定化脓性脑膜炎肥胖儿药物治疗剂量,及时发现利奈唑胺引起的血液毒性,开展利奈唑胺TDM,通过调整药物剂量来减轻该反应,最终使患儿有较好的临床获益。临床药师参与化脓性脑膜炎肥胖患儿的药物治疗,可协助医生优化治疗方案,保障患者用药安全,提高药物治疗水平。

