醋酸亮丙瑞林对不同BMI中枢性性早熟女童的治疗效果
林清栋,陈宇,吴思进
作者单位: 352100 福建省宁德市妇幼保健院
中枢性性早熟(CPP)是由于下丘脑—垂体—性腺轴(HPGA)功能过早启动,促性腺激素释放激素(GnRH)脉冲分泌增强所致,导致女童在7.5岁前、男童在9岁前即出现内外生殖器官快速发育及第二性征,或女童在10岁前即出现月经初潮。据报道,我国女童CPP发病率占总发病率的80%~90%[1]。CPP病情呈进行性发展,直至生殖系统发育成熟,其中CPP女童出现乳房发育及月经初潮提前,极易导致其出现自卑、焦虑等心理问题,不利于身心健康[2]。临床治疗此病主要原则为抑制性激素过度分泌,国际广泛使用促性腺激素释放激素类似物(GnRHa)[3]。醋酸亮丙瑞林是一种GnRHa,可有效抑制垂体分泌促性腺激素,减少性激素的合成及分泌,促使患儿第二性征消退[4]。但临床发现,不同体质指数(BMI)的CPP女童经醋酸亮丙瑞林治疗后,其卵巢、子宫容积的改善程度不同,认为BMI可能会影响治疗效果。本研究观察醋酸亮丙瑞林对不同BMI CPP女童卵巢及子宫体积的影响,现报道如下。
1 资料与方法
1.1 临床资料 选取2021年2月—2022年2月宁德市妇幼保健院收治的CPP女童80例,根据BMI分为正常组(BMI<85百分位)、超重组(BMI≥85百分位),每组40例。正常组年龄4~10(7.00±1.22)岁;病程6~24(15.00±2.23)个月;生长发育程度Tanner分期:乳房B3期9例,乳房B4期13例,PH2期10例,PH3期8例。超重组年龄3~10(6.50±1.25)岁;病程6~25(15.50±2.25)个月;生长发育程度Tanner分期:乳房B3期8例,乳房B4期13例,PH2期11例,PH3期8例。2组临床资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会审核批准。
1.2 病例选择标准 纳入标准:(1)符合《中枢性性早熟诊断与治疗专家共识(2022)》[5]中的CPP诊断标准;(2)女童,有乳房发育、月经初潮等表现;(3)年龄<11岁,骨龄比实际年龄大1岁及以上;(4)腹部超声检查显示卵巢容积为>1 ml,子宫容积>3 ml,且有多个直径≥4 mm的卵泡;(5)既往无醋酸亮丙瑞林治疗史。排除标准:(1)合并严重血液性疾病者;(2)存在先天代谢性、内分泌疾病者;(3)并甲状腺功能减退症、营养不良等影响人体生长发育的疾病者;(4)家族遗传性矮小症者;(5)治疗依从性差者。
1.3 治疗方法 患儿均采用注射用醋酸亮丙瑞林缓释微球(北京博恩特药业有限公司生产,规格:含醋酸亮丙瑞林3.75 mg/瓶)首次剂量为80~100 μg/kg皮下注射,每28 d用药1次,每次最大注射剂量不超过3.75 mg,持续治疗1年。
1.4 观察指标与方法 (1)卵巢容积、子宫容积、卵泡直径:于治疗前及治疗1年后采用彩色多普勒超声诊断仪检测患儿卵巢容积、子宫容积及卵泡直径。(2)性激素指标:于治疗前及治疗1年后,抽取患儿清晨空腹静脉血,以3 000 r/min转速离心10 min,取血清置于-20 ℃冰箱中保存待测。以化学发光法检测血清雌二醇(E2)、黄体生成素(LH)、卵泡刺激素(FSH)水平。(3)骨代谢指标:于治疗前及治疗1年后,取上述待测血清,以电化学发光免疫分析法检测血清I型前胶原氨基端肽(PⅠNP)、β-胶原降解产物(β-CTX)、骨钙素N端中分子片段(N-MID)水平。PⅠNP参考范围:570.4~785.9 μg/L;β-CTX参考范围:1 230.2~2 138.0 ng/L;N-MID参考范围:13.4~16.6 μg/L。(4)不良反应:包括发热、恶心、呕吐、体质量增加。
1.5 疗效判定标准 于患儿治疗1年后参考《诸福棠实用儿科学》[6]评估疗效,临床控制:患儿乳房缩小至青春前期,阴道分泌物消失、阴毛停止生长,骨龄与实际年龄相符,性激素改善至参考范围;好转:患儿乳房缩小,阴道分泌物消失、阴毛生长减缓,骨龄增长速度降低,性激素水平有一定改善;未愈:上述症状均未发生改善,卵巢、子宫继续增长。总有效率=(临床控制+好转)/总例数×100%。

2 结 果
2.1 临床疗效比较 超重组患儿治疗总有效率与正常组比较,差异无统计学意义(87.50% vs. 90.00%,P=1.000),见表1。
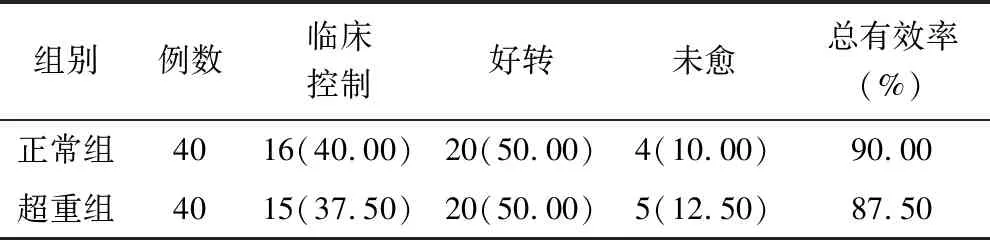
表1 正常组与超重组临床疗效比较 [例(%)]
2.2 卵巢容积、子宫容积、卵泡直径比较 治疗前及治疗1年后,2组患儿卵巢容积、子宫容积、卵泡直径比较,差异无统计学意义(P>0.05);治疗1年后,2组患儿卵巢容积、子宫容积及卵泡直径小于治疗前(P<0.01),见表2。

表2 正常组与超重组治疗前后卵巢容积、子宫容积、卵泡直径比较
2.3 性激素水平比较 治疗前及治疗1年后,2组患儿血清E2、LH、FSH水平比较,差异无统计学意义(P>0.05);治疗1年后,2组患儿血清E2、LH、FSH水平低于治疗前(P<0.01),见表3。

表3 正常组与超重组治疗前后血清性激素水平比较
2.4 骨代谢指标比较 治疗前及治疗1年后,2组患儿血清PⅠNP、β-CTX、N-MID水平比较,差异无统计学意义(P>0.05);治疗1年后,2组患儿血清PⅠNP、β-CTX、N-MID水平低于治疗前(P<0.05或P<0.01),见表4。

表4 正常组与超重组治疗前后骨代谢指标比较
2.5 不良反应比较 超重组与正常组患儿不良反应总发生率比较差异无统计学意义(10.00% vs. 7.50%,P=1.000),见表5。
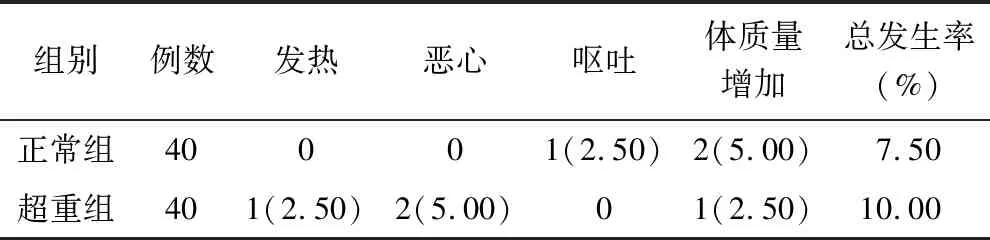
表5 正常组与超重组不良反应比较 [例(%)]
3 讨 论
CPP主要是由于下丘脑—垂体—性腺轴功能提前启动所引起的性早熟。近年来,CPP发病率越来越高,其中以女童最为多见[7]。目前,关于CPP的具体发病机制尚未明确。倪娜等[8]认为,儿童对环境内分泌干扰物的暴露程度与性早熟发病率密切相关。Bigambo等[9]指出,环境因素与CPP的发生有密切关系。CPP会导致骨骼加速生长,骨骺融合提前,影响最终成年身高,且第二性征的提前出现还会使患儿出现自卑、焦虑等心理障碍疾病,严重危害患儿的身心健康[10]。因此,早期有效、安全的治疗CPP尤为重要。近30年来,临床治疗CPP患儿常采用GnRHa,其中醋酸亮丙瑞林较常用,此药可有效阻滞患儿青春期的进展,延缓骨成熟,改善患儿病情[11]。但对于不同BMI的CPP女童应用醋酸亮丙瑞林的治疗效果差异需进一步探讨。
石星磊[12]发现,亮丙瑞林对CPP患儿具有较高的治疗效果及安全性,但该学者并未探讨此药对不同BMI患儿的效果差异。本研究结果显示,正常组与超重组治疗总有效率、不良反应总发生率均无明显差异,且治疗1年后,2组患儿卵巢容积、子宫容积、卵泡直径较治疗前均有改善,进一步证实了醋酸亮丙瑞林对于正常及超重的CPP女童均有明显疗效,且安全性较高。分析原因为:醋酸亮丙瑞林与垂体促性腺激素受体竞争性结合,可发挥激素调节的作用,有效抑制垂体性腺激素的分泌,从而延缓骨骺发育与融合,达到延迟月经及改善最终成年身高的效果[13]。
王喜平等[14]认为,青春期儿童主要特点为GnRH脉冲释放幅度、频率增加,垂体分泌FSH、LH,激活性腺能力。本研究结果显示,治疗1年后,正常组与超重组血清E2、LH、FSH水平较治疗前降低,提示醋酸亮丙瑞林治疗不同BMI的CPP女童均可明显降低其性激素水平。醋酸亮丙瑞林可有效调控垂体分泌功能,从而阻滞垂体分泌E2、LH、FSH,且与LH的亲和力高,可根据负反馈机制,抑制垂体—性腺系统功能,减少促性腺激素的分泌,降低患儿性激素水平[15]。
PⅠNP主要是由骨胶原合成、释放的产物,可有效反映骨细胞骨胶原合成活性;β-CTX主要反映机体的骨吸收水平;N-MID可有效反映骨细胞活性、骨形成水平。付晓宁等[16]发现,与健康女童的N-MID(14.4±1.3)μg/L、PⅠNP(745.2±77.30)μg/L比较,CPP女童的N-MID、PⅠNP分别为(16.6±1.9)μg/L、(849.3±88.6)μg/L,明显高于健康女童,表明CPP女童的骨代谢速度明显高于同龄健康女童。本研究结果显示,治疗1年后正常组与超重组患儿PⅠNP、β-CTX、N-MID水平较治疗前均明显降低,提示不同BMI的CPP女童接受醋酸亮丙瑞林治疗均可减缓骨代谢速度,减慢骨骼生长速度。但目前关于醋酸亮丙瑞林对CPP患儿骨代谢指标的药理机制尚未见明确报道,有待今后临床进行多中心研究。
综上所述,正常及超重CPP女童采用醋酸亮丙瑞林治疗的效果均较好,均可显著减小卵巢、子宫容积及卵泡直径,改善性激素水平,还可减缓骨代谢速度,且治疗安全性高。
利益冲突:所有作者声明无利益冲突。

