长春西汀注射剂小粒径不溶性微粒倍增现象及风险分析
贾丽华,李佳奇,2,郭欢迎
(1.陕西省食品药品检验研究院,陕西 西安 710065;2.陕西中医药大学药学院,陕西 咸阳 712046)
长春西汀(vinpocetine)是从夹竹桃科植物提取的一种生物碱,为长春胺的衍生物,可选择性地抑制脑血管平滑肌钙离子依赖性磷酸二酯酶,增加脑中cGMP 和cAMP 的水平,使脑血管扩张,继而增加脑血流量,改善脑循环[1]。临床上常与胞磷胆碱、川芎嗪、丹红注射液以及抗生素等联合用药,用于急性缺血性脑血管病、非急性缺血性脑血管病、脑小血管病与认知功能障碍、神经系统症状的治疗和改善[2-5]。但近年来,由于长春西汀注射剂存在临床使用不合理、不良反应数量较多等问题,2019 年,国家卫生健康委会同国家中医药局印发《第一批国家重点监控合理用药药品目录(化药及生物制品)》,对该品种进行限制使用和重点监控[6]。长春西汀不良反应主要涉及全身性损害、皮肤及其附件损害、心血管系统损害、神经系统损害、免疫功能紊乱和感染。本研究将对长春西汀注射剂的不溶性微粒进行分析,特别是对粒径在10 μm 以下的小微粒进行分析,重点探讨不同pH 值、不同溶媒及不同配伍用药对长春西汀注射液不溶性微粒的影响,为长春西汀注射剂不良反应情况分析和临床合理用药提供研究思路和数据支撑。
1 材料与方法
1.1 仪器 S210 型酸度计(瑞士梅特勒公司);GWJ-8型微粒分析仪(天津天大天发科技有限公司)。
1.2 试药 长春西汀注射液(河南润弘药业有限公司,批号1909232);氯化钠注射液(西安京西双鹤药业有限公司,批号200624 2A);葡萄糖注射液(西安京西双鹤药业有限公司,批号200203 6AD);葡萄糖氯化钠注射液(西安京西双鹤药业有限公司,批号200303 6AD);碳酸氢钠林格注射液(西安万隆制药股份有限公司,批号R190701);复方电解质葡萄糖注射液(西安万隆制药股份有限公司,批号B190502);右旋糖酐40 氯化钠注射液(四川科伦药业股份有限公司,批号L19111202);RPMI Medium Modified 培养基(HyClone,批号AF29246308);维生素C 注射液(西安利君制药有限责任公司,批号1911201);胞磷胆碱钠注射液(陕西顿斯制药有限公司,批号19100403);盐酸川芎嗪注射液(西安汉丰药业有限责任公司,批号2005121);丹参川芎嗪注射液(吉林四长制药有限公司,批号20170211);丹参注射液(正大青春宝药业有限公司,批号1901183);丹红注射液(山东丹红制药有限公司,批号19031017);肾康注射液(西安世纪盛康药业有限公司,批号191105);注射用氨苄西林钠(山东鲁抗医药股份有限公司,批号181209);注射用酒石酸吉他霉素(哈药集团制药总厂,批号B1812006-2);注射用青霉素钠(山东鲁抗医药股份有限公司,批号181025);注射用头孢他啶(哈药集团制药总厂,批号1910701-1);注射用阿奇霉素(西安利君制药有限责任公司,批号200302-1);克林霉素磷酸酯注射液(山东方明药业股份有限公司,批号19111881);注射用头孢美唑钠(四川合信药业有限责任公司,批号19032107)。
1.3 方法
1.3.1 pH 变化对不溶性微粒的影响 ①样品溶液的制备:ⓐ氯化钠注射液:取氯化钠注射液1 瓶,用水将容器外壁洗净,小心翻转20 次,使溶液混合均匀,小心开启容器,静置脱气,备用;ⓑ长春西汀氯化钠溶液:取长春西汀注射液1 支,用水将容器外壁洗净,小心翻转20 次,使溶液混合均匀,小心开启容器,将注射液完全冲洗至500 ml 氯化钠注射液中,混合均匀,静置脱气,备用;ⓒRPMI 培养基:取RPMI 培养基,用水将容器外壁洗净,小心翻转20次,使溶液混合均匀,小心开启容器,静置脱气,备用;ⓓ0.1 mol/L NaOH 溶液:采用不溶性微粒检查用水配制,0.22 μm 微孔滤膜过滤,备用。②测定方法:打开仪器,用微粒检查用水冲洗仪器通道,备用。微粒检查用水按《中国药典2020 年版四部》通则0903 的要求进行检测,符合使用要求。分别取氯化钠注射液和长春西汀氯化钠溶液适量,置不溶性微粒测定仪取样器中,由仪器直接抽取适量溶液(以不吸入气泡为限),测定并记录2~5、5~10、10~25、≥25 μm 微粒数据,另计算每毫升含不同粒径微粒数量。取长春西汀氯化钠溶液适量,逐滴加入0.1 mol/L NaOH 溶液,调节pH 值,按照以上方法,测定不同pH 值条件下混合溶液中每毫升含不同粒径微粒数量,同法测定氯化钠注射液在不同pH 条件下的不溶性微粒数。取长春西汀氯化钠溶液和RPMI 培养基各50 ml,小心混匀,静置脱气,按照以上方法,测定不同粒径微粒数,并计算每毫升含微粒数量,同法测定RPMI 培养基每毫升含不同粒径微粒数量。
1.3.2 不同溶媒的影响 ①样品溶液的制备:ⓐ溶媒溶液:取氯化钠注射液、葡萄糖注射液、葡萄糖氯化钠注射液、碳酸氢钠林格注射液、复方电解质葡萄糖注射液各1 瓶,用水将容器外壁洗净,小心翻转20次,使溶液混合均匀,小心开启容器,静置脱气,备用;ⓑ长春西汀溶媒样品溶液:取长春西汀注射液1 支,用水将容器外壁洗净,小心翻转20 次,使溶液混合均匀,小心开启容器,将注射液完全冲洗至500 ml 以上溶媒溶液中,混合均匀,静置脱气,备用。②测定方法:分别取溶媒溶液和长春西汀溶媒样品溶液适量,置不溶性微粒测定仪取样器中,由仪器直接抽取适量溶液(以不吸入气泡为限),测定并记录2~5、5~10、10~25、≥25 μm 微粒数据,并计算每毫升含不同粒径微粒数量。
1.3.3 不同样品配伍的影响 ①样品溶液的制备:ⓐ配伍样品溶液:取维生素C 注射液等配伍用样品各1 瓶,用水将容器外壁洗净,小心翻转20 次,使溶液混合均匀,小心开启容器,将注射液完全冲洗至100 ml 氯化钠注射液中静置脱气,备用;ⓑ长春西汀样品溶液:取长春西汀注射液1 支,用水将容器外壁洗净,小心翻转20 次,使溶液混合均匀,小心开启容器,将注射液完全冲洗至500 ml 氯化钠注射液中,混合均匀,静置脱气,备用。②测定方法:取配伍样品和长春西汀溶媒样品适量,分别置不溶性微粒测定仪取样器中,由仪器直接抽取适量溶液,测定并记录2~5、5~10、10~25、≥25 μm 微粒数据,并计算每毫升含不同粒径微粒数量。取配伍样品和长春西汀溶媒样品各100 ml,小心混匀,静置脱气,按以上方法测定每毫升含不同粒径微粒数量。
2 结果
2.1 pH 变化对不溶性微粒的影响 采用0.1 mol/L NaOH 溶液溶液调节0.9%氯化钠注射液的pH 值,其不溶性微粒数变化不大,见表1。为此,研究中采用RPMI 培养基模拟长春西汀注射液滴注至人体环境后不溶性微粒的变化,结果显示长春西汀氯化钠溶液与模拟人体液的培养基混合以后,产生了大量的不溶性微粒,2~5 μm 的颗粒数增加至原来的200多倍,5~10 μm 的颗粒数增加至原来的60 倍,10~25 μm 的颗粒数变化不是很明显,见表2。
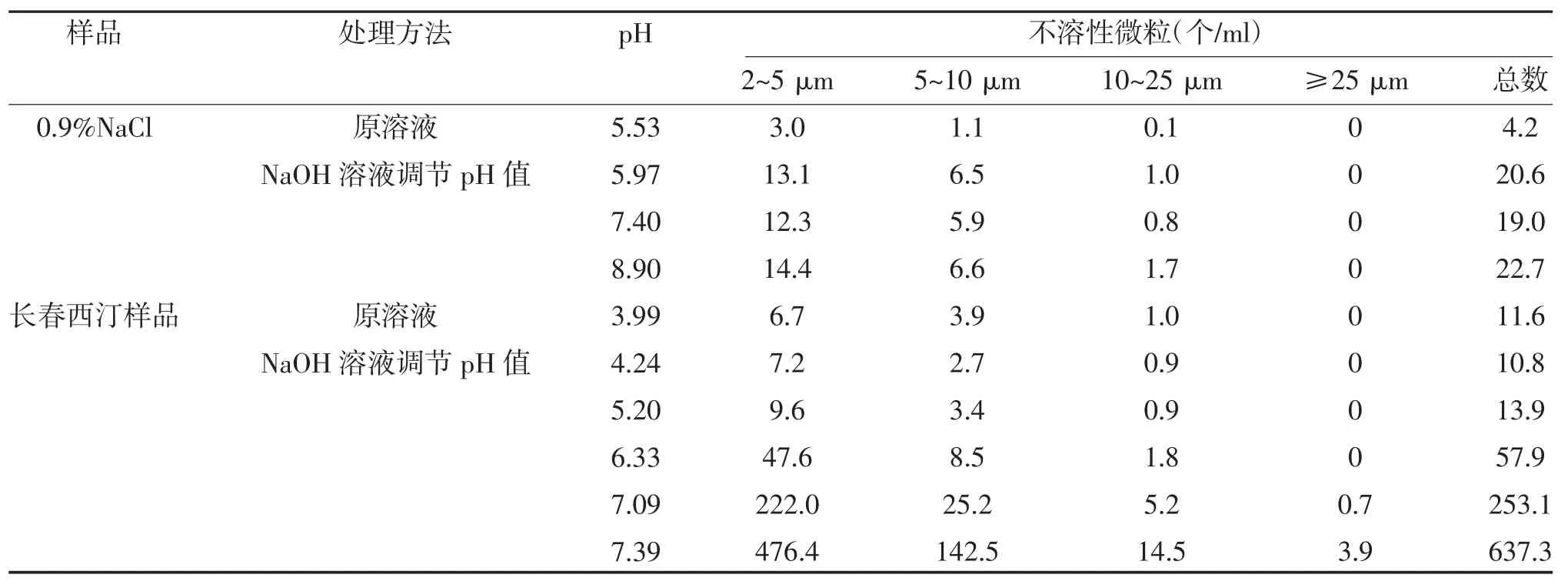
表1 不同pH 值条件下长春西汀溶液的不溶性微粒测定结果(n=3)

表2 细胞培养基对长春西汀溶液的不溶性微粒的影响(n=3)
2.2 不同溶媒对不溶性微粒的影响 长春西汀在不同溶媒中的不溶性微粒差异较大,以氯化钠注射液和葡萄糖注射液为溶媒,不溶性微粒差异不大,但溶媒成分越复杂,不溶性微粒数量有所增加,特别是在右旋糖酐40 氯化钠注射液、碳酸氢钠林格注射液中的不溶性微粒是氯化钠注射液中的150 倍左右,见表3。
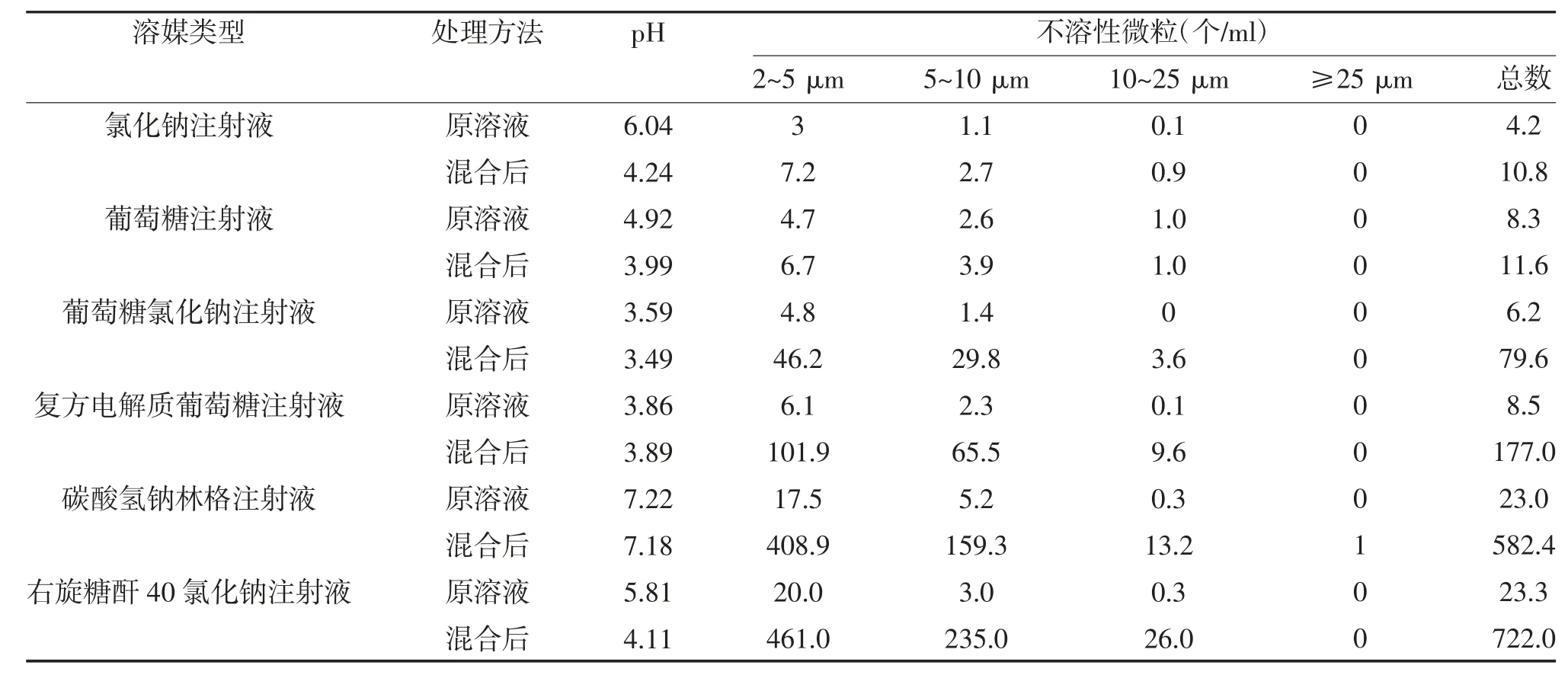
表3 不同溶媒中长春西汀的不溶性微粒测定结果(n=3)
2.3 不同样品配伍对不溶性微粒的的影响 长春西汀注射液与维生素C 注射液、盐酸川芎嗪注射液、注射用酒石酸吉他霉素等酸性注射剂配伍后,不同粒径不溶性微粒变化不大,见表4。
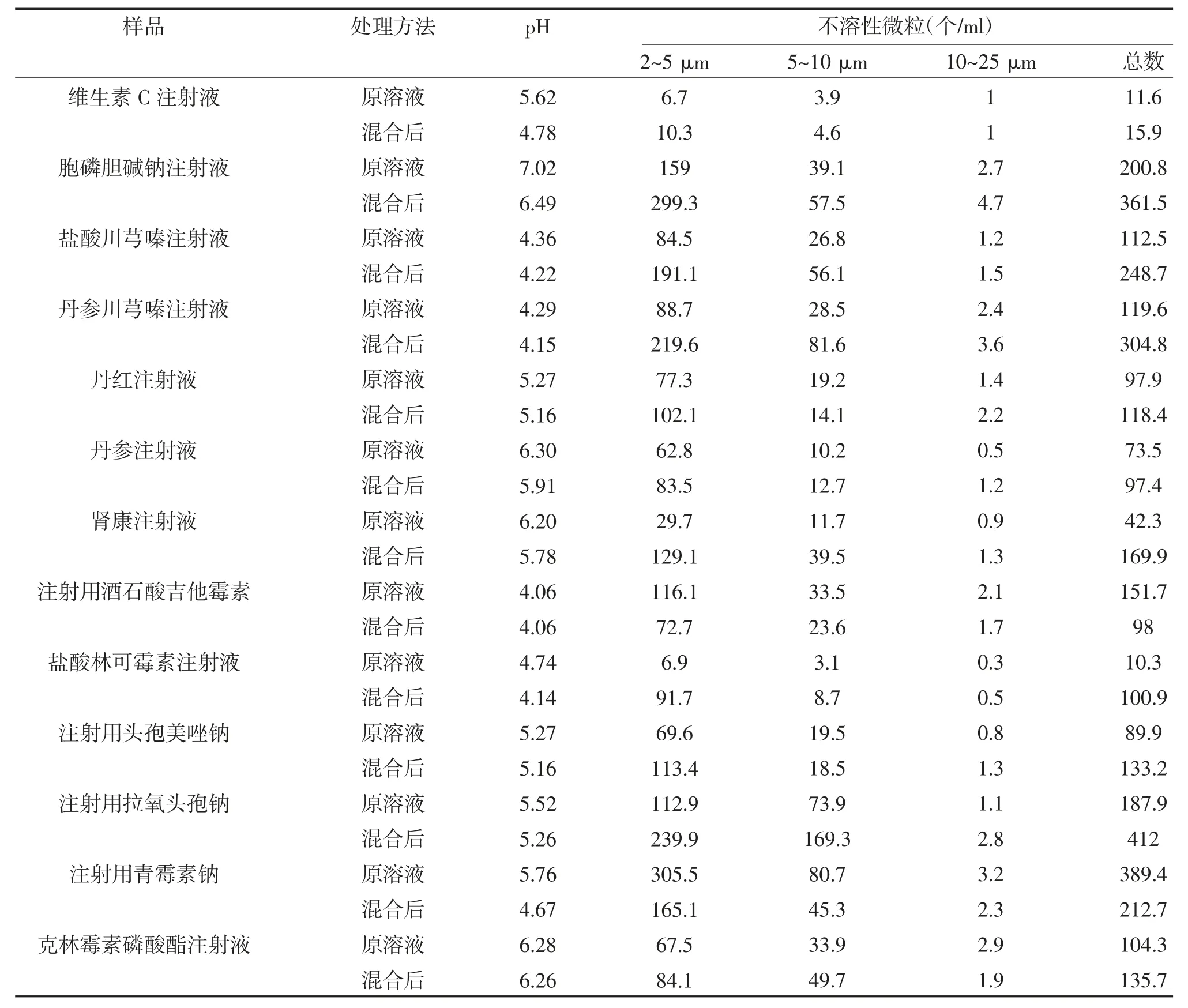
表4 不同药物配伍后长春西汀注射液的不溶性微粒测定结果(n=3)
3 讨论
3.1 现象分析 临床不良反应的发生与药品本身特点、临床使用方法等因素密切相关,如不溶性微粒增加、pH 敏感、稳定性差等问题[7,8]。长春西汀是弱碱性(pKa=7.31)药物,几乎不溶于水,在酸性条件下易溶,中性或碱性条件下会析出白色结晶或颗粒,因此长春西汀注射剂多为偏酸性(pH 约在4 左右)。有文献报道[6,8,9],长春西汀注射剂与多种药物存在配伍禁忌,多数表现在两种药物混合后出现白色、乳白色或絮状浑浊,其主要原因是配伍以后改变了长春西汀注射剂pH 值,在中性或偏碱性环境中长春西汀析出所致。但现有文献中关于对长春西汀注射剂不溶性微粒,特别是小粒径不溶性微粒产生的具体情况进行分析的研究较少。《中国药典》对注射剂中不溶性微粒的控制仅限于粒径大于10 μm 和25 μm的微粒数,对于粒径小于10 μm 的微粒数未作规定[10]。目前医院常用的一次性输液器孔径多为15 μm 规格和5 μm 规格,个别品种采用1.2 μm 规格,这样的输液器对于大粒径微粒(≥10 μm)截留效果较好,对于小粒径微粒(2~10 μm)截留效果较差。实际上,人体最小的毛细血管内径仅有4~7 μm,婴、幼儿的毛细血管更细,只有粒径2 μm 以下的微粒才可能通过肾交换被排出体外,而粒径为2~10 μm 的微粒无法被排出。据报道[11-13],静脉滴注含微粒输液可致兔体温增高,并且微粒可致抗原性刺激、微血管梗塞及机械性损伤。微粒进入体内造成危害的部位一般多在肺、脑、肾、眼等处,较大的微粒会直接造成局部循环障碍,引起血管栓塞或导致肉芽肿,且有短期内可见的特点。因此,粒径为2~10 μm 的微粒则可能造成潜伏性的更大危害,是导致输液不良反应之一“热原样反应”的重要原因[14-16]。
3.2 pH 值风险分析 将长春西汀注射液配制成临床应用的大输液以后,随着溶液pH 值的增加,不溶性微粒数迅速增加,其中倍增最多的是2~5 μm和5~10 μm 的微粒数,分别增加了约70 和50 倍。本研究中长春西汀大输液样品配置的浓度约为0.04 mg/ml,试验过程中未发生大粒径(≥25 μm)微粒倍增的现象。弱碱性药物在酸性条件下易溶,在中性或碱性条件下易析出结晶,这类注射液在使用和配伍过程中的不溶性微粒变化应引起重视。
此外,长春西汀氯化钠溶液与模拟人血液的培养基混合以后,产生了大量的不溶性微粒,2~5 μm 的颗粒数增加至原来的200 多倍,5~10 μm 的颗粒数增加至原来的60 倍,该结果与pH 值对长春西汀氯化钠溶液的不溶性微粒的影响是一致的。人体血液的pH 值在7.35~7.45 间,推测长春西汀注射液在进入人体血液后,随着pH 值的改变,不溶性微粒数特别是小粒径微粒会大量增加,由此带来的安全风险值得关注。
3.3 溶媒风险分析 长春西汀在不同溶媒中的不溶性微粒差异较大,以氯化钠注射液和葡萄糖注射液为溶媒,不溶性微粒差异不大,但是溶媒成分越复杂,不溶性微粒数量有所增加,特别是在右旋糖酐40 氯化钠注射液、碳酸氢钠林格注射液中的不溶性微粒是氯化钠注射液中的145 倍。因此,建议临床上长春西汀注射剂应选择氯化钠注射液和葡萄糖注射液为溶媒。
3.4 配伍风险分析 长春西汀注射液与中性(如胞磷胆碱钠注射液、注射用阿奇霉素)或碱性样品(如注射用阿莫西林钠舒巴坦钠、注射用氨苄西林钠)配伍以后,不溶性微粒数显著增加,倍增数量较大的是粒径为2~5 μm 和5~10 μm 的不溶性微粒。因微粒所致热原样反应和抗原样反应的可能性是存在的。因此临床应注意长春西汀注射液使用过程中的配伍问题。
4 总结
长春西汀注射液在临床用药过程中应注意用法、用量和输液中的配伍问题,如采用选择氯化钠注射液和葡萄糖注射液为溶媒,浓度不得过0.06 mg/ml,输液速度不得大于80 滴/min,不得与其他药物配伍使用,且用使用前后均应冲洗输液管道。

