甲烷选择性氧化制含氧化合物催化剂研究进展
余海杰,李 潇,冉建速,丁大千,王健健
(1.重庆大学 化学化工学院,前沿交叉学科研究院,煤矿灾害动力学与控制全国重点实验室,跨尺度多孔材料研究中心,重庆 401331;2.内蒙古工业大学 化工学院,内蒙古 呼和浩特 010051)
化石能源日益枯竭,原油价格剧烈波动,贮藏量丰富的天然气作为重要的燃料和化工原料的来源越来越受到人们关注。甲烷是天然气、页岩气等气体资源的主要成分,储量丰富,是一种洁净的优质能源。然而天然气、页岩气等资源大多位于人口稀少的偏远地区,由于缺乏储存和运输的基础设施,提高了其使用成本。此外,煤矿行业中排放的瓦斯气体也含有一定量的甲烷,这部分瓦斯气体往往被直接燃烧处理,造成了资源浪费,还会加剧温室效应[1-4]。工业化利用甲烷的过程中,多采用蒸汽重整先将甲烷转化为合成气(H2+ CO),随后通过费托合成转化为目标产物。但是,甲烷蒸汽重整通常在高温和高压条件下进行,步骤繁琐、工艺复杂、成本较高[5-7]。因此,开发一种将甲烷直接转化为高附加值产品的方法具有重要意义。甲醇、甲醛、甲酸和乙酸是一类基本的低碳含氧化工原料,广泛用于烯烃、芳烃、高分子、树脂、农药、医药、燃料和食品等领域。就地将甲烷选择性地转化为这些产品,既避免了产生天然气运输成本,又减少了温室气体排放,有利于提高天然气利用率和优化能源结构。
甲烷选择性氧化制含氧化物过程存在两大挑战:一是甲烷C—H键的活化,因为甲烷分子具有高度对称的空间四面体构型,该结构中的C—H 键难以极化,同时甲烷的高HOMO(最高占有分子轨道)-LUMO(最低未占分子轨道)间隙(9.91 eV)和高电离电势(12.61 eV)使其难以在催化循环中得失电子[8-10];二是甲烷选择性氧化反应产物的调控,甲烷C—H键的解离能为440 kJ/mol,反应生成的含氧化合物的C—H键能通常比甲烷更低(如甲醇C—H键的解离能为388.4 kJ/mol),生成的含氧化合物相对于甲烷更加活泼,容易被进一步转化为CO2,导致产物选择性降低[11-14]。因此,实现甲烷C—H键的高效活化和定向转化是甲烷选择性氧化制含氧化合物的关键。
自然界中,甲烷单加氧酶(MMO)在好氧条件下可以高效催化甲烷选择性氧化为甲醇。MMO存在两种形式,即可溶性甲烷单加氧酶(sMMO)和颗粒型甲烷单加氧酶(pMMO),其中sMMO的活性中心包含双核Fe 中心,而pMMO 则以Cu 为活性中心[15-16]。而在甲烷工业氧化中,温度、压力和溶剂耐受性等因素大大限制了酶的应用。为了应对上述挑战,保留高活性和高选择性,研究者们尝试合成多相催化剂来模拟sMMO和pMMO对甲烷的活化。受生物酶活性中心结构启发,具有类似限域空间的分子筛材料和金属有机框架(MOF)材料被用于制备仿酶甲烷活化催化剂。其中,Fe 基分子筛催化剂[17-18]、Cu 基分子筛催化剂[19-21]和MOF 催化剂[22-24]等,在甲烷C—H 键的高效活化和定向转化中展现出了优异性能。
本文总结近十年来甲烷转化为甲醇[25-26]、甲醛[27]、甲酸[18]和乙酸[28]等含氧化合物的研究进展,包括金属修饰的分子筛催化剂、MOF 催化剂及其他类型催化剂(表1),综述反应过程中催化剂活性中心、活性中间体的演变过程和反应机理,并对甲烷选择性氧化的发展前景进行展望,旨在为设计与开发高活性、高选择性的甲烷选择性氧化催化剂提供理论指导。
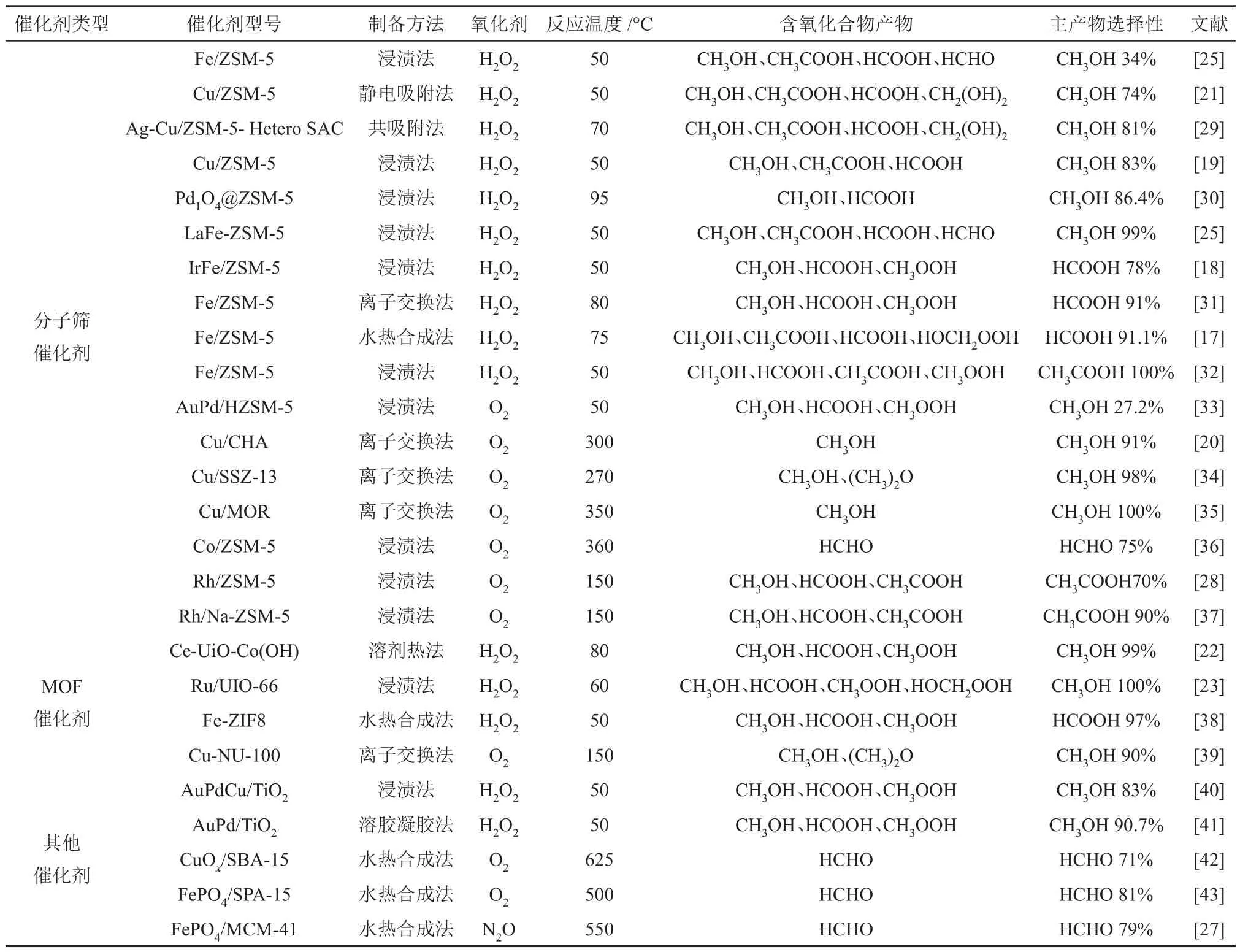
表1 甲烷选择性氧化制含氧化合物催化剂的对比Table 1 Comparison of catalysts for selective oxidation of methane to oxygenated compounds
1 甲烷选择性氧化制甲醇
实现甲烷选择性氧化制甲醇,催化剂起到至关重要的作用。如表1 所示,目前报道的催化剂主要包括分子筛催化剂[25]、MOF 催化剂[23],以及其他催化剂[41],反应过程中使用的氧化剂包括H2O2和O2。
1.1 分子筛催化剂
1.1.1 Fe基分子筛催化剂
分子筛具有较大的比表面积、规则的微孔通道、良好的水热稳定性和可控的酸性等特点,可作为催化剂载体。经担载过渡金属组分Fe 后制成Fe基分子筛催化剂,用于甲烷选择性氧化制甲醇反应中。HUTCHⅠNGS 团队发现采用Fe/ZSM-5 为催化剂时,以H2O2为氧化剂,50 °C 下经过30 min 反应后,产物甲醇的选择性只有34%,当向催化剂结构中引入La后,抑制了H2O2消耗速率,从而将产物甲醇的选择性提高至99%[25]。在选择性氧化甲烷制甲醇中,上述催化剂显示出良好的活性,但当时对催化活性位点的精确结构尚未完全了解。
2021 年,YU 等[44]通过电子顺磁共振(EPR)和1H/13C-核磁共振(NMR)等表征证明了稳定在ZSM-5骨架外的单核Fe3+物种是甲烷氧化的活性位点。2023年,HAN的团队也证明了单核Fe3+物种是甲烷选择性氧化的活性位点,并模拟出单核铁位点的结构(图1)[17]。如图1 所示,Fe/ZSM-5 催化剂中的单核Fe 物种以[(H2O)2—Fe(Ⅲ)—OH]2+的形式存在,并与沸石分子筛骨架上的3 个氧原子(Of)相连接。该反应机理包含4个过程:Fe/ZSM-5催化剂结构中的单核Fe(ⅠⅠⅠ)物种在双氧水作用下生成Fe(ⅠV)==O物种和•OH自由基;甲烷吸附在Fe(ⅠV)==O物种上,经过均裂方式断开甲烷结构中的1个C—H键,生成Fe(ⅠⅠⅠ)—OH 物种和•CH3自由基;产生的•CH3自由基在溶液中与•OOH 自由基和•OH 自由基反应生成CH3COOH 和CH3OH;H2O2进一步氧化生成的Fe(ⅠⅠⅠ)—OH物种,将其重新转变为Fe(ⅠV)==O物种。
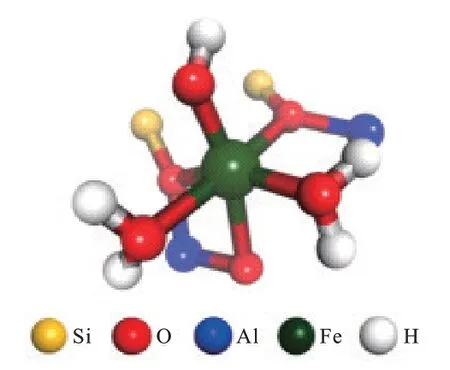
图1 Fe/ZSM-5催化剂中单核铁位点模型[17]Fig.1 Mononuclear iron site model in Fe/ZSM-5 catalyst[17]
双核铁位点也是Fe 基分子筛催化剂的活性中心。例如,MLEKODAJ 等[45]指出Fe 基分子筛催化剂中稳定的双核Fe2+活性物质,诱导氧裂解形成活性氧物种α-氧,然后α-氧进一步将甲烷氧化为甲醇。HE 等[46]发现甲烷选择性氧化制甲醇途径分为甲烷的C—H 键活化和甲醇生成两个步骤,两个步骤均在4 种双核铁位点上完成(图2)。由此可以看出,单核铁物种和双核铁物种均是Fe基分子筛催化剂的活性物种,活性物种结构取决于Fe基分子筛催化剂的骨架结构和合成方法。
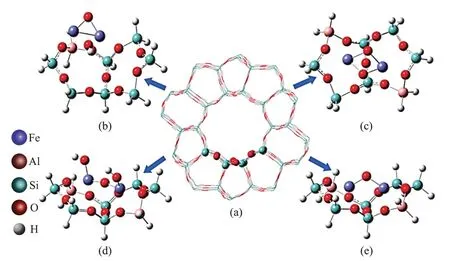
图2 Fe/ZSM-5催化剂中4种双核铁位点计算模型[46]Fig.2 Four binuclear iron site computational models in Fe/ZSM-5 catalyst[46]
理论计算有助于深入研究Fe 基分子筛催化剂上的甲烷活化机理,为研究甲烷选择性氧化制甲醇提供理论指导。SZECSENYⅠ等[47]通过密度泛函理论(DFT)计算,系统地研究了Fe/ZSM-5催化剂双核铁位点上H2O2氧化甲烷的机理,发现甲烷选择性氧化存在3 种不同的反应路径:异裂解、均裂解和OH自由基(•OH)为催化物种的芬顿(Fenton)型反应(图3)。如图3所示,Fe在与H2O2反应时,形成不同的Fe(ⅠⅠⅠ)和Fe(ⅠV)团簇,其中Fe(ⅠⅠⅠ)物种催化异裂解和Fenton 型活化,而Fe(ⅠV)物种促进甲烷的均裂解活化。Fe(ⅠⅠⅠ)物种被过氧配体氧化后,CH3和OH基团组合形成甲醇。在均裂解和Fenton型机制下,首先会形成一个甲基自由基(•CH3),这些甲基自由基可以通过回弹机制进一步转化为甲醇,或者与O2反应,并从活性位点上夺取氢原子从而转化为CH3OOH。Fe(ⅠV)位点是催化甲烷均裂解和H2O2分解为O2和[H+]离子的活性中心。
总的来说,单核铁物种和双核铁物种均是Fe基分子筛催化剂的活性物种,调节活性位点的位置、调控载体的酸性和引入助剂等方式均能够促进活性中心的生成,从而提升催化剂的性能、减少H2O2的消耗。Fe 基分子筛催化剂中甲烷氧化的反应路径较为复杂,仍需进一步探索。
1.1.2 Cu基分子筛催化剂
铜氧化物是pMMO 的活性位点[16],因此Cu 基分子筛催化剂可作为模拟pMMO 活化的材料用于甲烷选择性氧化制甲醇反应中。研究发现,Cu 基分子筛催化剂中单核铜物种、双核铜物种和多核铜物种均可作为甲烷选择性氧化制甲醇的活性位点。例如,KNORPP 等[48]通过反常X 射线衍射(AXPD)和X 射线吸收光谱(XAS),证实了ω分子筛骨架中稳定的成对[CuOH]+单体有助于提高催化性能。HEYER 等[49]结合紫外-可见分光光度法(UV-Vis)、电子顺磁共振(EPR)和XAS 表征结果,发现Cu 基丝光沸石分子筛(Cu-MOR)催化剂中的双核[Cu2O]2+位点反应性显著高于单核[CuOH]+位点。DⅠNH等[34]通过原位XAS 光谱证明了Cu-SSZ-13 催化剂中[Cu—O—Cu]2+物种是甲烷选择性氧化的主要活性位点,当反应温度为270 °C时,以O2为氧化剂,Cu-SSZ-13对甲醇的选择性为98%。SUSHKEVⅠCH 等[50]通过实验和表征结果发现,Cu-MOR中的Cu—O—Cu是甲烷选择性氧化为甲醇的活性位点。除单、双铜核位点外,三核铜氧团簇([Cu3(μ-O)3]2+)也被认为是Cu基分子筛结构中的催化位点。GRUNDNER等[12]利用原位XAS 技术揭示了三核铜氧团簇([Cu3(μ-O)3]2+)是Cu-MOR 催化剂中唯一的活性位点,其结构见图4。如图4 所示,三核铜氧团簇锚定在MOR 的8-MR 侧袋中,并与MOR 中两个骨架铝原子相连。
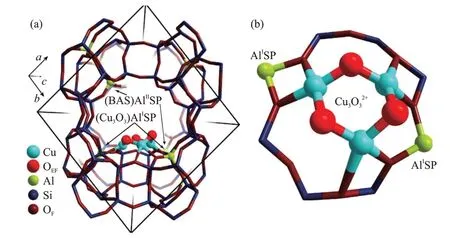
图4 DFT计算中Cu-MOR催化剂中三核铜氧团簇[Cu3(µ-O)3]2+的位置(a)和结构(b)[12]Fig.4 Location (a) and structure (b) of trinuclear copper oxo cluster [Cu3(µ-O)3]2+ in Cu-MOR catalyst, as calculated by DFT[12]
同一种催化剂的结构中,也会同时出现存在双核和三核铜物种的现象,两种活性催化位点共同催化甲烷选择性氧化。LⅠ等[51]发现双核[Cu(µ-O)Cu]2+和三核[Cu3(µ-O)3]2+物种都存在于Cu/ZSM-5 催化剂结构中(图5),两个物种能通过不同的反应路径实现甲烷选择性氧化。在焙烧条件下,三核铜氧团簇位点是Cu/ZSM-5 催化剂结构中最稳定的团簇。
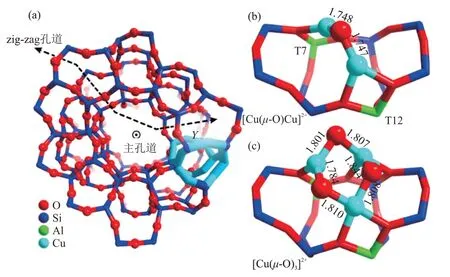
图5 Cu/ZSM-5 催化剂中双核和三核铜氧团簇的位置(a)和局部优化结构((b)~(c))[51]Fig.5 Location of binuclear and trinuclear cationic copper oxo clusters in Cu/ZSM-5 catalyst (a) and their local optimized structures ((b)~(c))[51]
通过调控Cu 基分子筛催化剂中不同Cu 物种的数量,可以控制甲醇的生成。例如,PARK 等[20]通过离子交换法制备了一系列Cu 基分子筛催化剂,结果发现Cu-MAZ 分子筛催化剂结构中的八元环通道中形成的铜氧活性物种最多,因此表现出最高的甲醇产率(86 mmol/g,1 g 催化剂的甲醇产率为86 mmol)。MARKOVⅠTS 等[52]发现Cu-H-ZSM-5上多核铜氧物种的形成受MFⅠ分子筛中Al浓度的限制,较高的Al浓度会抑制多核铜氧物种的形成,从而降低了甲醇的生成量。YU等[29]合成了锚定在ZSM-5上原子分散的银铜双单原子(Ag-Cu/ZSM-5-Hetero SAC)用于催化甲烷直接选择性氧化,在70 °C下,以H2O2作为氧化剂,甲醇的选择性为81%,同时甲醇的产率达到40.2 mmol/(g·h)(1 g催化剂在1 h内的甲醇产率为40.2 mmol)。表征结果表明,锚定在分子筛孔道内的银和铜原子之间的单/双核动态切换,促进形成了高活性的表面羟基物种(OH*),从而活化甲烷中C—H键。LⅠ等[53]报道了一种Cu-CHA催化剂,其表现出543 mmol/(mol·h)(1 mol Cu-CHA催化剂在1 h内的甲醇产率为543 mmol)的优异甲醇产率和高达91%的甲醇选择性。DFT计算结果表明,Cu-CHA催化剂结构中的单核Cu物种和双核Cu物种均能促进甲烷选择性氧化,且两类Cu 物种之间可以发生相互转化[53-54]。JEONG 等[35]对比了Cu-H-MOR 和Cu-Na-MOR 的甲烷氧化性能,发现Cu-H-MOR对甲醇的选择性为85%,远远高于Cu-Na-MOR(65%),这表明Brønsted酸性位的存在也有利于Cu-MOR上的甲烷选择性氧化制甲醇反应。
催化剂结构中形成的Cu 物种能抑制甲醇向甲酸过氧化,从而促进甲醇的生成。HAMMOND等[19]发现Cu2+物种可以促进甲醇的生成,并抑制甲醇过度氧化为其他含氧化合物。YU 等[55]同样发现,Cu物种通过与H2O2产生•OH 而不是•OOH,从而促进甲醇的生成,并抑制形成甲酸(图6)。而DⅠNH等[34]认为,Cu 物种通过控制•OH 自由基的数量,抑制甲醇进一步氧化为甲酸。
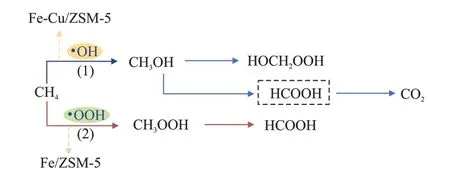
图6 Fe-ZSM-5 与Fe-Cu-ZSM-5 催化剂上甲烷氧化的反应路径[55]Fig.6 Reaction pathways for methane oxidation on Fe-ZSM-5 and Fe-Cu-ZSM-5 catalysts[55]
WU 等[56]通过EPR 和NMR 表征手段探索了Cu/Na-ZSM-5 催化剂上甲烷选择性氧化为甲醇的反应路径,结果见图7。如图7 所示,甲烷在Cu/Na-ZSM-5 催化剂的活化转化主要包含以下3个步骤:甲烷在Cu-Na-ZSM-5 催化剂的[Cu2O]2+核上活化生成甲醇,Cu2+还原为Cu+;吸附的甲醇在Cu+上进一步活化,形成铜甲氧基(—Cu—O—CH3)和—Al—OH 基;通过铜甲氧基的水合作用和吸附甲醇的置换作用形成游离甲醇。
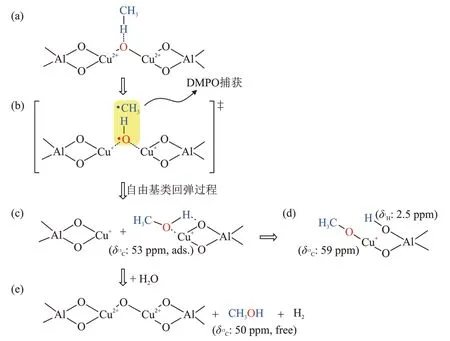
图7 Cu-ZSM-5催化剂上甲烷转化为甲醇的机理[56]Fig.7 Mechanism of methane conversion to methanol on Cu-ZSM-5 catalyst[56]
Cu 基分子筛催化剂催化甲烷选择性氧化制甲醇过程中会产生不同的甲氧基类活性物种。KOLGANOV等[57]结合NMR和DFT计算结果,发现Cu-ZSM-5 催化剂活化甲烷时产生3 种不同的表面甲氧基类物质(O—CH3),包括:两个相邻铜位点Cu—(HOCH3)—Cu 吸附的甲醇;吸附在Brønsted 酸位点的甲醇;晶格结合的甲氧基。Cu-ZSM-5 分子筛中Cu 的负载量影响反应过程中甲氧基类中间体的种类和含量。
此外,Cu2+-Cu+-Cu2+氧化还原循环也会影响Cu基分子筛催化剂的催化性能。SUN 等[53]通过紫外-可见-近红外分光光度计(UV-Vis-NⅠR)、原位傅立叶红外光谱仪(FTⅠR)和DFT 计算对Cu-SSZ-13 催化剂上甲烷选择性氧化反应路线进行了研究,结果见图8。如图8 所示,Cu-SSZ-13 中CuOH 单体和二聚体均能通过Cu2+-Cu+-Cu2+快速氧化还原的循环,有效地催化甲烷选择性氧化制甲醇,Cu—OOH 是关键反应中间体。同时,该反应条件下单核Cu物种与双核Cu物种可相互转化。
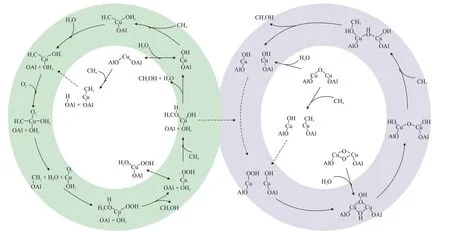
图8 Cu-SSZ-13催化剂上甲烷选择性氧化制甲醇机理[53]Fig.8 Mechanism of methane selective oxidation to methanol on Cu-SSZ-13 catalyst[53]
概括来说,Cu基分子筛催化剂结构中单核铜物种、双核铜物种和多核铜物种均是甲烷选择性氧化的活性位点。通过调控Cu 基分子筛催化剂中活性物种的数量和分布,从而能促使催化剂展现优异的催化性能。然而,Cu基分子筛上的反应机理和甲烷活化机理复杂,尚未有统一的结论,因此仍需进一步探索。
1.1.3 贵金属分子筛催化剂
贵金属修饰的分子筛催化剂在甲烷选择性氧化制甲醇反应中也显示出不错的催化性能。HUANG等[30]采用浸渍法制备了一种Pd1O4@ZSM-5催化剂,单位点Pd 锚定于分子筛内表面上,所制得的催化剂在95 °C下,以H2O2为氧化剂时,产物甲醇的选择性可以达到86.4%。理论计算表明,相对于甲基过氧化氢的生成来说,Pd1O4@ZSM-5催化剂在热力学上更加有利于甲醇的生成。此外,将采用限域的AuPd 作为活性中心时,通入的氢气和氧气可以直接发生反应原位生成H2O2,从而也能催化甲烷选择性转化为甲醇[33]。
1.2 MOF催化剂
MOF材料具有结构多样性和可调节性,能提供明确的限域空间和配位环境,可用于封装或锚定过渡金属活性组分,从而用于化学选择性活化甲烷结构中的C—H键。基于此,设计和合成MOF催化剂用于选择性氧化甲烷制甲醇引起了广泛的关注。例如,OSADCHⅠⅠ等[58]成功将原子分散的Fe 活性位点锚定到MⅠL-53的晶体骨架中,该模型模拟了酶催化碳氢活化生成甲醇的行为,并证明这种反应的关键是形成孤立的氧桥铁单元。XU 等[59]设计合成了AuPd@ZⅠF-8催化剂,在H2O2和O2的存在下,甲醇的产率为21.7 mmol/(g·h),选择性为21.9%。ZHENG等[39]通过阳离子交换法,成功将Cu-oxo 二聚体锚定在NU-1000 的氧化锆节点上,实现甲烷选择性氧化制甲醇,其选择性为90%。FANG 等[23]开发了一种高效的MOF 负载的单原子Ru 催化剂(Ru1/UiO-66),使甲烷能够以约100%的选择性和185.4 h-1的优异转化频率(TOF)转化为甲醇。表征结果和DFT计算结果表明,Ru1/UiO-66材料中UiO-66的缺电子Ru1位点和富电子Zr-氧合节点之间存在强的协同作用。其中,Ru1位点负责通过产生的Ru1==O*物种活化甲烷,而Zr-氧合节点负责形成含氧自由基物种以产生含氧物。同时,Ru1修饰的Zr-oxo 节点将过量的H2O2转化为非活性的O2,而不是•OH 物种,有助于抑制含氧化合物的过度氧化。ANTⅠL等[22]成功设计和合成了Ce-UiO-Co(OH)催化剂,在80 °C 下,以H2O2为氧化剂,甲醇的选择性和产率分别高达99%和2166 mmol/g。通过扩展X 射线吸收精细结构谱(EXAFS)、X射线光电子能谱(XPS)、EPR等表征手段探究了Ce-UiO-Co(OH)催化甲烷转化为甲醇的反应机理,结果见图9。Ce4+-oxo节点和氧配体的亲电性质使Ce-UiO-Co(OH)的Co(Ⅲ)中心高度缺电子,通过σ键复分解过程从而促进了甲烷的活化。
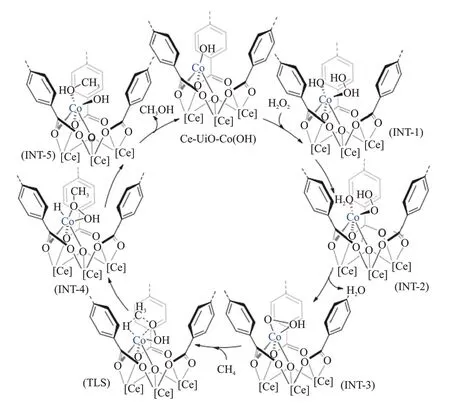
图9 Ce-UiO-Co(OH)催化剂催化甲烷转化为甲醇的机理[22]Fig.9 Mechanism of methane conversion to methanol on Ce-UiO-Co(OH) catalyst[22]
将金属活性物种封装或锚定在MOF材料中,提升金属活性位点与MOF 材料中金属节点的协同作用,有助于活化甲烷结构中的C—H键,并产生更多的活性中间体,从而使MOF催化剂展现出优异的催化活性和甲醇选择性。
1.3 其他催化剂
除了分子筛催化剂和MOF催化剂外,过渡金属修饰的二氧化钛催化剂也可用于甲烷选择性氧化制甲醇的反应中。例如,RAHⅠM等[40]将Cu与Au/Pd一起沉积在TiO2表面,三金属AuPdCu/TiO2催化剂在50 °C下,以H2O2为氧化剂,产物甲醇的选择性高达83%。WⅠLLⅠAMS 等[41]报道了通过调节纳米颗粒尺寸、金属负载量和金属氧化态,优化了AuPd/TiO2催化剂的活性,甲醇选择性达到90.7%。ZHONG等[60]采用硼氢化钠还原方法制备了合金PdxAuy纳米线用于选择性氧化甲烷。结果表明,合金PdxAuy纳米线中特殊的一维结构具备优异的甲烷吸附能力和电子协同效应,因此所制备的催化剂表现出超过90%的甲醇选择性。
综上所述,可以看出Fe基分子筛催化剂、Cu基分子筛催化剂、MOF 催化剂,以及金属修饰的二氧化钛催化剂均在甲烷选择性氧化制甲醇反应中显示出优良的催化性能。其中,以Fe 基和Cu 基分子筛为催化剂时,催化剂结构中单核金属物种、双核金属物种和多核金属物种的形成是甲烷活化生成甲醇的活性位点。调控Fe基和Cu基分子筛催化剂中活性位点的位置,强化金属活性中心和载体之间的协同作用,有助于活化甲烷结构中的C—H键,使催化剂展现出优异的催化性能。
2 甲烷选择性氧化制甲醛
2.1 分子筛催化剂
如表1 所示,过渡金属修饰的分子筛催化剂可用于甲烷选择性氧化制甲醛,反应过程中的氧化剂为O2。LUCAS 等[61]采用氨水对Mo/ZSM-5 催化剂进行处理,以调控活性Mo 物种在分子筛孔道中的分布,在600 °C 下,以O2为氧化剂,甲醛选择性为10.6%。BEZNⅠS等[36]探讨了酸处理对Co-ZSM-5催化剂产物选择性的影响。研究发现,Co-ZSM-5 材料经酸处理后,分子筛通道中高度分散Co2+物种的含量增加,产物甲醛的选择性达到75%。
2.2 介孔氧化物催化剂
除了分子筛载体外,介孔SBA-15和MCM-41材料近年来也引起了人们的广泛关注。例如,LⅠ等[62]通过水热合成法制备了一系列CuOx/SBA-15 催化剂,探究了其在甲烷选择性氧化制甲醛反应中的催化活性。结果表明,当Si/Cu 物质的量之比为13200 时,CuOx/SBA-15 催化剂活性最佳,甲醛形成的速率为5.6 mol/(mol·s)(CuOx/SBA-15 催化剂中1 mol Cu 在1 s 内的甲醛产率为5.6 mmol)。如图10(a)所示,反应过程中产生的CuⅠ位点促使O2分子形成活性氧,活性氧选择性地将甲烷氧化为甲醛;与CuⅡ物种相连的晶格氧与甲烷反应生成CO和CO2,CuⅡ物种被还原为CuⅠ位点;进一步,还原的CuⅠ位点被活化为Cum+—O*簇,最终与甲烷反应选择性生成甲醛。AN 等[42]探究了不同制备方法对CuOx/SBA-15 催化剂催化活性的影响,与浸渍法制备的CuOx/SBA-15 催化剂相比,通过接枝方法制备的CuOx/SBA-15 催化剂具有更多分离的Cu2+,见图10(b)。如图10(b)所示,分离的Cu2+在反应过程中部分被还原为Cu+位点,Cu+位点活化O2生成Cum+—O*活性氧物种,活性氧物种进一步实现甲烷选择性氧化为甲醛。因此,接枝方法制备的CuOx/SBA-15催化剂具有更佳的甲醛选择性(71%)。WANG等[27]研究了FePO4负载量对FePO4/MCM-41 催化剂的甲烷选择性氧化性能的影响,发现当FePO4负载量(质量分数)低于40%时,磷酸铁团簇高度分散在介孔材料MCM-41 表面;而当FePO4负载量较高时,磷酸铁的结晶相主要呈鳞片状,其中FePO4负载量为40%的FePO4/MCM-41 催化剂性能最佳,甲醛的选择性达到79%。进一步,WANG 等[43]对比了不同载体(SBA-15 和MCM-41)负载FePO4后的甲烷氧化活性。结果表明,与FePO4/MCM-41 催化剂相比,FePO4/SBA-15催化剂表现出更佳的甲醛选择性(81%)。
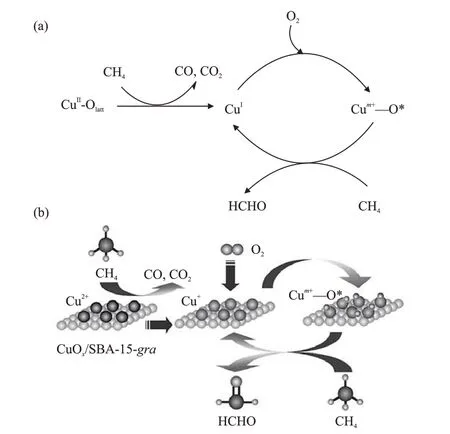
图10 CuOx/SBA-15 催化剂上甲烷选择性氧化为甲醛的反应机理Fig.10 Reaction mechanism of selective oxidation of methane to formaldehyde on CuOx/SBA-15 catalyst
综上所述,分子筛和介孔氧化物可用作载体制备相应催化剂,应用于甲烷选择性氧化制甲醛反应中。氧化反应过程中,调控中间价态金属位点的形成,进而活化O2生成Mm+—O*活性氧物种,生成的活性氧物种有利于进一步选择性氧化为甲醛。值得注意的是,甲烷选择性氧化生成甲醛的反应温度远高于生成甲醇、甲酸和乙酸。甲醛的选择性和产率,以及反应温度和压力的控制是甲烷选择性氧化制甲醛需要克服的难题,未来的研究方向应侧重于优化反应条件,提高催化剂的性能和稳定性,探索反应机理。
3 甲烷选择性氧化制甲酸
3.1 分子筛催化剂
如表1 所示,过渡金属修饰的分子筛催化剂可用于甲烷选择性氧化制甲酸。含铁分子筛被认为是甲烷选择性氧化制甲酸的潜在催化剂[17,38,63],反应过程中的氧化剂为H2O2。例如,YU 等[18]研究了甲烷在Fe/ZSM-5 催化剂上的选择性氧化性能。在50 °C下,以H2O2为氧化剂时,产物甲酸的选择性为54%;当向Fe/ZSM-5 催化剂结构中引入Ⅰr 后,甲酸的选择性从54.0%提高到了71.3%。X 射线吸收精细结构谱(XAFS)表征结果表明,Ⅰr 的引入促使了Fe/ZSM-5催化剂中Fe—O—Ⅰr结构的形成(图11)。如图11 所示,H2O2在Fe—O—Ⅰr 位点上被活化为自由基•OOH和•OH,CH4被•OH氧化为自由基•CH3。因此,形成的•CH3将与•OOH 和•OH 反应,生成甲醇和乙酸,后被进一步氧化为甲酸。ZHU等[31]通过离子交换法制备了Fe/ZSM-5催化剂用于甲烷选择性氧化制甲酸的反应中。结果表明,以0.03% Fe/ZSM-5(66)为催化剂时,甲酸的产率为383.2 mmol/(g·h),同时其选择性达到91%。
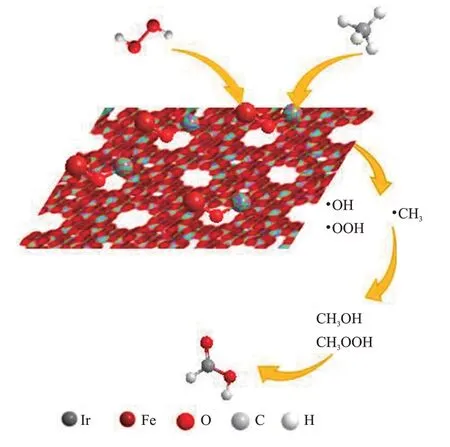
图11 以H2O2为氧化剂在IrFe/ZSM-5催化剂上甲烷选择氧化制甲酸的机理[18]Fig.11 Mechanism of selective oxidation of methane to formic acid on IrFe/ZSM-5 catalyst using H2O2 as oxidant[18]
CHENG等[17]报道了通过无模板法合成Fe-ZSM-5催化剂(Fe-HZ5-TF),活性位点是传统Fe-ZSM-5的3 倍多。在75 °C 下,用H2O2选择性氧化甲烷时,产物甲酸的选择性达到91.1%。光谱表征和DFT计算结果表明,不同于传统Fe-ZSM-5 中以双核Fe 作为活性位点,Fe-HZ5-TF 中的活性位点为单核Fe 物种,其以[(H2O)2—Fe(ⅠⅠⅠ)—OH]2+的形式与分子筛骨架中的Al 对结合(图12)。如图12 所示,在反应过程中,[(H2O)2—Fe(ⅠⅠⅠ)—OH]2+首先被H2O2氧化 为[(H2O)3—Fe(V)==O]2+,进而作为催化中心活化CH4并促进其氧化转化,最终以高选择性产生甲酸。YANG等[64]使用球磨方法将Fe/ZSM-5中游离的Fe3+转化为骨架外的高活性Fe物种,0.03% Fe/ZSM-5经球磨后显示出高催化活性,在70 °C 时甲酸选择性达到96%。TARAN等[63]通过草酸活化Fe-MFⅠ催化剂,增加了催化剂的总酸度,促使催化剂中分离的铁的阳离子从四面体骨架氧周围迁移到八面体骨架外氧周围,同时形成具有催化活性的低聚铁氧簇,从而提高了生产甲酸的性能。
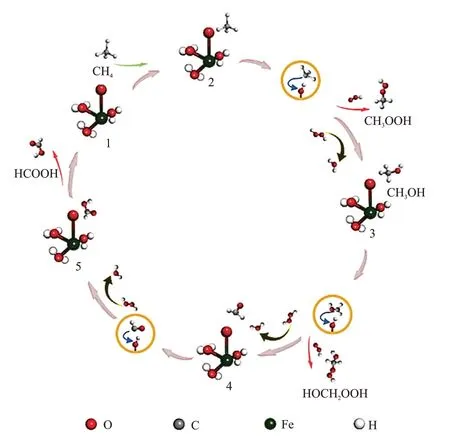
图12 甲烷在单核Fe物种上选择性氧化的自由基驱动途径[17]Fig.12 Free radical-driven pathway for selective oxidation of methane on mononuclear Fe active species[17]
在甲烷选择性氧化制甲酸过程中,甲醇被认为是中间产物。例如,HAMMOND等[19]发现在过氧化氢和催化剂的存在下,甲烷反应后生成的主要中间产物为CH3OOH,生成的CH3OOH 被进一步分解或反应形成甲醇,然后甲醇和•OH自由基反应形成甲酸。YU 等[44]发现ZSM-5 相邻的Brønsted 酸位点有利于甲烷的活化,甲烷首先被氧化为乙酸和甲醇,然后转化为HOCH2OOH,最后转化为甲酸。SHAHAMⅠ等[65]还报道了强酸活性位的存在有利于甲烷选择性生成甲酸。
3.2 MOF催化剂
除了分子筛催化剂外,MOF催化剂也在甲烷选择性氧化制甲酸反应中显示出良好的催化性能。LⅠN 等[38]报道了ZⅠF-8 限域的高度分散Fe 物种,用于在50 °C下,以H2O2作为氧化剂,将甲烷直接氧化转化为甲酸。结果表明,Fe-ZⅠF-8 显示出优异的催化性能,产物甲酸的选择性高达97%。XPS、XAS和紫外-可见漫反射光谱(UV-Vis DRS)等表征结果表明,Fe-ZⅠF-8 催化剂结构中六配位的单核Fe3+物种是甲烷转化的活性位点。
综上所述,可以看出分子筛催化剂和MOF催化剂均在甲烷选择性氧化制甲酸反应中显示出优良的催化性能。甲醇被认为是甲烷选择性氧化制甲酸反应中的中间产物,改变催化剂的酸性或者向催化剂结构中引入其他金属组分,抑制甲醇的过氧化反应,从而能够提高甲酸的产量。因此,如何控制副反应和其他产物的产生是甲烷选择性氧化制甲酸的关键问题。
4 甲烷选择性氧化制乙酸
4.1 分子筛催化剂
如表1 所示,过渡金属(贵金属和非贵金属)修饰的分子筛催化剂可用于甲烷选择性氧化制乙酸,反应过程中的氧化剂包括H2O2和O2。例如,TANG 等[28]制备了Rh/ZSM-5 催化剂用于甲烷选择性氧化。结果表明,锚定在分子筛中的Rh1O5位点表现出了最佳的催化活性,产物乙酸的选择性达到70%,是游离Rh3+活性的1000 倍以上。通过同位素研究得出的反应途径见图13(a)。如图13(a)所示,Rh1O5活性位点活化甲烷结构中的第一个C—H键,在Rh 上形成CH3基团和OH 基团;紧接着,CO 分子插入Rh—O—H物种结构中的Rh—O键,从而在Rh位点上形成COOH 基团;然后,生成的COOH 基团与甲基基团偶联生成乙酸,剩余的Rh—O oxo 物种开始活化第二个甲烷分子结构中的C—H 键,进而在Rh 原子上又重新形成了CH3基团和OH 基团,使得催化循环持续进行。SHAN等[37]探究了酸性位点的数量对Rh-ZSM-5 甲烷氧化性能的影响,含有少量Brønsted 酸位点的Rh@Na-ZSM-5 催化剂使甲烷选择性地转化为甲醇,而具有更多Brønsted 酸位点的Rh@H-ZSM-5催化剂使甲烷定向生成乙酸,此时乙酸的选择性达到90%。通过DFT 计算和同位素标记测量等表征手段,揭示了甲烷直接转化为含氧化合物的反应途径,结果见图13(b)。如图13(b)所示,甲烷首先在活性位点生成Rh—CH3物种,并通过活性氧进一步转化为Rh—OCH3物种,然后水解生成甲醇,或者通过CO插入反应生成Rh—COCH3物种,并最终水解生成乙酸。
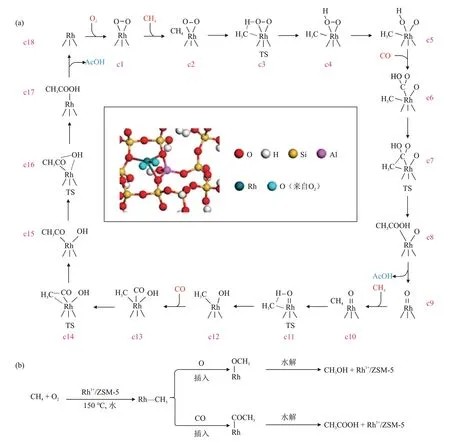
图13 甲烷、CO和O2在Rh/ZSM-5催化剂上生成乙酸的反应途径(a)[28]和甲烷在Rh/ZSM-5催化剂上转化为甲醇和乙酸的可能反应途径(b)[37]Fig.13 Reaction pathway for formation of acetic acid from methane, CO, and O2 on Rh/ZSM-5 catalyst (a)[28] and possible reaction pathways for methane conversion to methanol and acetic acid on Rh/ZSM-5 catalyst (b)[37]
在甲烷选择性氧化制乙酸反应中,非贵金属修饰的分子筛催化剂也显示出良好的催化性能。NARSⅠMHAN 等[66]研究了在Cu-H-MOR 催化剂上甲烷氧化为乙酸的催化活性,发现Cu-H-MOR中的Brønsted 酸位点和CuxOy位点在甲烷活化生成甲氧基,以及在甲氧基羰基化的过程中起到了重要作用,固定在Cu-H-MOR 上的Cu 簇氧原子将甲烷氧化为甲氧基,然后甲氧基被CO羧化生成乙酸。WU等[32]制备了具有双核Fe 位点的Fe/ZSM-5 催化剂,该催化剂具有[Fe(ⅠⅠⅠ)—(mO)2—Fe(ⅠⅠⅠ)—(OH)2]活性位,反应中显示出100%的乙酸选择性。FANG 等[24]报道了Fe-MOR催化剂中的单核铁和二聚体铁物种促进生成了活性—OH 和—OOH 物种,从而也促进了乙酸形成。
4.2 MOF催化剂
除了分子筛催化剂,MOF催化剂同样具备用于选择性氧化甲烷制乙酸的潜力。例如,ANTⅠL等[67]报道了在温和条件下,以分子氧作为氧化剂,在多孔铈金属-有机框架(Ce-UiO-Cu(OH))的单铜羟基位点上,甲烷一步转化为乙酸,在115 °C的水中,乙酸的选择性和产率分别为96%和335 mmol/g。
综上所述,分子筛催化剂和MOF催化剂均在甲烷选择性氧化制乙酸反应中显示出了良好的催化性能。当催化剂结构中存在更多Brønsted 酸位点时,催化剂能够促使甲烷定向生成乙酸。然而,目前所报道的实验结果距离工业化应用仍有较大距离,在反应条件的优化、催化剂的活性和稳定性,以及产物的选择性和产率方面仍然需要进一步探索。
5 结语与展望
金属修饰的分子筛催化剂及MOF 催化剂广泛用于甲烷选择性氧化反应中。Fe 基催化剂主要用于甲烷选择性氧化制备甲酸和乙酸,Cu基催化剂或者改性的Fe 基催化剂主要用于制备甲醇。催化剂的组成成分及结构特性对催化剂的催化性能有着重要的影响。Fe基和Cu基分子筛上形成的单核金属物种、双核金属物种或多核金属物种是甲烷活化生成甲醇的活性位点,调控活性位点的位置、强化活性金属中心和载体之间的协同作用,有助于活化甲烷C—H 键,促进催化剂的催化性能。调控中间价态金属位点的形成,进而活化氧气生成Mn+—O*活性氧物种,选择性氧化活性氧物种生成甲醛,该过程反应温度远高于生成甲醇、甲酸和乙酸。分析认为甲醇是甲烷选择性氧化制备甲酸反应的中间产物,改变催化剂的酸性或者向催化剂结构中引入其他金属组分,可以抑制甲醇过氧化反应,从而提高甲酸的生成量。当催化剂结构中存在更多的Brønsted 酸位点时,催化剂能够促使甲烷定向生成乙酸。此外,在甲烷选择性氧化反应中,相比于O2、N2O,使用H2O2作为氧化剂,反应所需温度更低,产物选择性更高。
基于目前的研究现状,可以从以下5 个方面对甲烷选择性氧化反应过程及催化剂研制开展进一步探索:(1)结合原位实验和理论计算,分析反应官能团变化过程,明晰活性中间体演变规律,深入认识甲烷活化机理。(2)利用原位表征技术,研究催化剂活性中心在甲烷选择性氧化过程中的变化过程,确定有效的反应活性中心。(3)调控活性中心的空间分布,进而精确活化甲烷结构中的C—H键,抑制过氧化反应的发生,高选择性生成含氧化合物。(4)优化催化剂结构,提高催化剂的稳定性。(5)优化甲烷选择性氧化反应条件,提高甲烷转化率和含氧化合物的选择性,助力甲烷选择性氧化工业化进程的推进。

