功能核酸侧流层析传感器及其食品安全快速检测应用
汪德颖 齐小花 盛万里 裴佳欢 邹明强*
(1.中国检验检疫科学研究院& 国家市场监管重点实验室(食品质量与安全) 北京 100176;2.北京工业大学环境与生命学部;3.呼和浩特海关技术中心)
0 引言
据世界卫生组织统计,全球约有6 亿人在食用受污染的食物后健康状况不佳,每年超42 000 人死亡[1-2]。 传统的测试分析方法包括色谱法、质谱法和实时荧光定量PCR、酶联免疫吸附测定,虽然这些方法在检测食品污染方面成熟可靠, 但耗时长、成本高、操作复杂,这些弊端严重制约了从农田到餐桌有效防线的及时建立。 功能核酸侧流层析传感器作为一项快速检测技术,不受环境制约,可以现场检测食品污染,能够更可靠、更快速地检出危害,确保食品安全。
1 功能核酸侧流层析传感器概述
功能核酸是一种具有特殊功能的核酸序列,可以特异性结合目标物质或催化反应,具有特异性高、稳定性好、体积小、成本低、易于化学修饰、靶标范围广泛、 从金属离子到全细胞等优点, 包括核酸适配体、三链核酸、G-四链核酸、切割核酸酶、反义寡核苷酸、异种核酸(XNAs)、金属碱基对DNA 和点击化学键核酸等丰富的形态结构[3-5]。
功能核酸侧流层析传感器 (Functional nucleic acids lateral flow biosensor,FNA-LFB) 集成了功能纳米技术和功能核酸技术[6],能够克服免疫侧流层析传感器靶标范围局限、抗体蛋白热稳定性较差[7]、抗体不可避免的批次差异、突破抗体进行荧光标记、酶标记或结构可变性设计时复杂的修饰、纯化瓶颈[8]。
2 功能核酸侧流层析传感器构建
功能核酸侧流层析传感器通过“检测形式”“靶标识别技术”“信号转导技术”“靶标放大技术”“定量分析系统”5 个环节构建,检测形式主要分为“极简型” 单重检测形式、“多线型” 多重检测形式、“多条型”多重检测形式、“多点型”多重检测形式以及“密闭性”集成检测形式。 FNAs 在侧流层析传感器的样品预处理、捕获探针固定、目标识别、信号放大和信号转导都表现出多种功能,如图1 所示[3]。
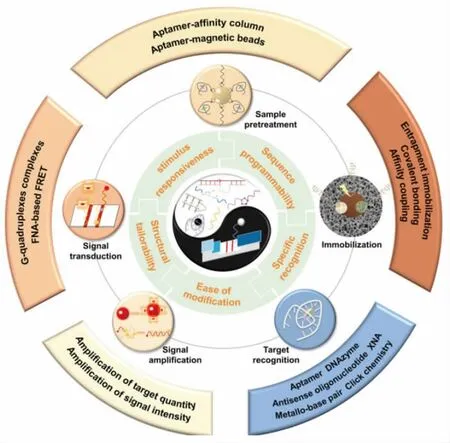
图1 FNAs 参与构建LFB 示意图Fig.1 Schematic of FNAs involved in constructing the LFB
LFB 由样品垫、共轭垫、硝化纤维素膜(NC 膜)、吸收垫和粘性背卡组成,如图2 所示[9]。
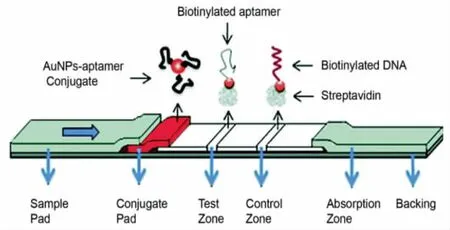
图2 侧流层析传感器组成示意图Fig.2 Schematic diagram of the lateral flow chromatographic sensor composition
2.1 样品预处理
检测食品样品前,通常要进行提取、纯化和浓缩目标物的预处理, 以提高后续LFB 检测的灵敏度、准确度和可重复性。 适配体功能化磁珠(AFMBs)和适体功能化亲和柱(AFACs)可用于样品靶标的提取和富集,样品垫可控制样品释放,消除了不同样品之间组分差异,并作为样品基质的过滤器。
2.2 NC 膜涂装方法
不能简单地通过空气干燥将核酸涂布在NC 膜上, 因为它们可能会被毛细管力驱动的流动样品液冲走。 适当的涂覆方法包括亲和偶联、共价结合、诱捕固定用来确保FNAs 在NC 膜上稳定分布, 以保持其亲和力或催化活性。
2.3 靶标识别
核酸侧流层析传感器的靶标识别技术分为“核酸类靶物质”和“非核酸类靶物质”,其识别原理取决于不同FNAs 和靶标各自的特征, 这些因素显著影响检测性能。
2.3.1 基于适配体的LFB
三明治夹心反应形式通常用于检测大分子靶标,例如蛋白质、病原体和病毒。 它具有多个结合位点, 可以同时与一对适配体或适配体和抗体组合结合,形成三明治状结构。 通常,三明治格式的LFB 表现出“开启”信号,主要识别元件作为捕获探针固定在T 线上,次要识别元件与信号报告器耦合作为检测探针。 目标物存在情况下,形成“检测探针-目标物-捕获探针”三明治复合物,在T 线上表现出可检测的信号[10]。
竞争性反应形式通常用于检测只有一个结合位点或一种可用适体的小分子,如霉菌毒素、抗生素、农药和生物化合物。当与特定的适配体探针结合时,靶标和竞争物之间会发生竞争,产生“关闭”信号[11]。为获得最高的竞争反应灵敏度, 需要调整竞争物的结构和序列,同时优化适配体和竞争物浓度比。
2.3.2 基于DNAzyme 核酶的LFB
DNAzyme 核酶,尤其是RNA 切割DNAzyme 核酶, 以其显著的结合亲和力和特异性被广泛用于金属传感。 在基于RNA 切割DNAzyme 核酶的LFB中,酶链通过靶标识别和结合被激活, 以切割底物链上的RNA 并释放ssDNA,ssDNA 可以直接捕获在条带上,或扩增以进行扩增子捕获产生可检测的信号[12]。
2.3.3 基于反义寡核苷酸的LFB
基于反义寡核苷酸的LFB 通常根据Watson-Crick 碱基配对原理用于基因组样品测试。反义寡核苷酸探针(DNA/RNA)与靶核酸序列互补,通过杂交实现特异性和准确识别捕获靶标。 传统的基于杂交的LFB 采取竞争性[13]和夹心[14]反应形式进行核酸检测。 此外,重组酶聚合酶扩增(RPA)[15]和催化发夹组装(CHA)[16]等靶标扩增策略也已集成到基于杂交的LFB 中,作为影响后续检测的关键步骤。
传统LFB 直接检测基因扩增产物,由于引物二聚体的形成,会产生假阳性信号。簇状规则间隔短回文重复序列(CRISPR)/Cas 系统,由于其优异的ds-DNA 识别能力,包含CRISPR/Cas9 和CRISPR/Cas12系统, 已被整合到LFB 中。 在基于CRISPR/Cas9 的LFB 中,具有特殊设计的锚定位点的扩增子Cas9/sgRNA 复合物通过形成夹心结构在试纸上捕获, 产生“开启”信号[17-18]。CRISPR/Cas12 系统在dsDNA 识别后显示出反式切割活性,切割的ssDNA 报告基因不能继续在试纸上捕获,产生“关闭”信号[19]。YANG 等[20]设计Leptotrichia wadei(Lwa)Cas13a,与电化学方法相结合,检测到阿托摩尔浓度的SARS-CoV-2 基因组,无需靶标预扩增,LwaCas13a 酶具有增强的侧支活性,可随时集成到其他基于Cas13a 的平台用于核酸的超灵敏检测。
2.3.4 基于XNA 的LFB
XNA 是化学合成的具有修饰的糖磷酸骨架或碱基核酸类似物,如肽核酸(PNA)、磷酸二胺吗啉基低聚物(PMO)、苏糖核酸(TNA)和己醇核酸(HNA)。基于XNA 的LFB 遵循Watson-Crick 碱基配对原理,但由于其引进了修饰的组分,因此在XNA-DNA杂交过程中表现出比传统DNA-DNA 杂交更高的亲和力、稳定性和选择性。
2.3.5 基于金属碱基对的LFB
金属碱基对DNA 代表具有特定核碱基的核酸,这些核碱基可以通过配位键选择性地与金属离子结合,形成强烈的金属-核碱基错配。 富含T/C 的DNA可以选择性结合Hg2+/Ag+形成T-Hg2+-T 和C-Ag+-C错配[21]。 通过使用靶标识别诱导的核碱基错配启动核酸扩增产生的扩增子随后参与基于杂交的LFB。
2.3.6 基于点击化学的LFB
点击化学连接核酸结合了铜催化叠氮化物/炔烃环加成(CuAAC)的高选择性和催化活性优点以及核酸的多功能性[22]。CuAAC 反应与核酸结合触发核酸的构象变化,扩增或杂交[23],有助于更稳定和灵敏地检测铜离子。在基于点击化学的LFB 中,2 个寡核苷酸分别用叠氮化物和炔基团修饰,Cu+的存在促进了2 个修饰片段的连接,偶联的ssDNA 在T 线上进一步捕获,通过互补杂交或SA-生物素键形成夹心复合物。
2.4 信号放大
核酸侧流层析传感器的信号转导模式分为比色信号、荧光信号、磷光信号、电化学信号和化学发光信号等[24],每种信号都基于相应的纳米颗粒或基团作为信号元件。当检测的靶标物质浓度较低时,往往需要靶标放大技术与核酸侧流层析传感器联用。FNA-LFB 中通常使用核酸扩增方法增强靶标,通过富集或改进信号分子进行信号探针放大。
2.4.1 变温放大方法
PCR 是一种经典且广泛使用的核酸扩增方法。基于半保守复制原理,在DNA 聚合酶和dNTP 引物存在下,通过“变性-退火-延伸”循环,对DNA 模板进行扩增产生dsDNA 扩增子。 标记的DNA 扩增子通常与LFB 一起使用,使用标记的引物进行进一步分析。 许多升级PCR 版本,如比例竞争定量PCR(PCQPCR),对流PCR(cPCR),双超级PCR(DSPCR)和超快光子PCR(UPPCR),已经构建以实现更精准和易于使用的核酸扩增[25]。
2.4.2 等温扩增方法
FNA-LFB 中采用了酶催化法和无酶法2 类等温扩增方法。酶催化等温扩增方法,将具有独特活性和具有特定序列和结构的引物/模板与靶核酸在恒定的最佳反应温度下孵育, 产生许多单链或双链扩增子连接到许多化学分子如生物素、罗丹明、地高辛。环介导等温扩增(LAMP),RPA, 指数放大反应(EXPAR)和Exo III 介导的等温放大已被集成到LFB中以进行信号放大。 无酶等温扩增方法使用靶标结合诱导的构象变化和立足点原理将CHA 和发夹触发的DNA 酶切割整合到FNA-LFB 中[26]。
2.4.3 信号分子富集
信号分子可以通过核酸杂交、 扩增子的生物素化dUTP、介孔二氧化硅和FNA-LFB 中的病毒纳米颗粒富集。 单个AuNP 探针在LFB 中的灵敏度有限, 因此, 已经用修饰的互补寡核苷酸合成了双AuNP 探针,并分别分配在2 个共轭垫上。 样品溶液流过,通过互补杂交重新水化和偶联2 种AuNPs,在检测区域产生更深的红色信号[27]。
2.4.4 信号分子增强
信号分子增强可以通过酶催化的显色反应来实现。 具有G4 结构的DNAzymes 核酶显示出过氧化物酶样活性,因为更简单,稳定性更好,成本相对较低优于HRP 等蛋白质酶。 CHENG 等[28]设计了一种DNAzymes 核酶催化扩增方法来增强AuNP 信号,有效地提高了FNA-LFB 检测灵敏度,单个AuNP 可以加载数百个DNAzymes 核酶。
2.5 信号转导
信号转导使用各种可检测信号包括比色信号、荧光信号、表面增强拉曼光谱、热信号和电化学信号量化不可见的反应。FNA-LFB 的传统信号转导方法通常采用化学分子或纳米材料进行信号传导,例如:AuNPs、纳米酶、荧光染料、染料掺杂纳米颗粒和荧光纳米颗粒[29-30]。
3 食品安全快速检测应用
核酸侧流层析传感器已广泛应用于食品安全快速检测中(图3)[31]。 靶标物质涉及食源性致病微生物、生物毒素、农兽药残留、重金属离子、非法添加、肉类掺假以及生物技术食品等。
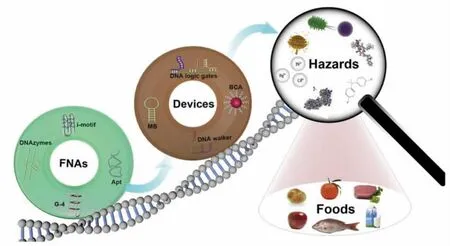
图3 核酸侧流层析传感器在食品安全检测中的应用Fig.3Application in the rapid detection of food safety
3.1 食源性致病微生物检测
大肠杆菌O157:H7、沙门氏菌、单核细胞增生李斯特菌和金黄色葡萄球菌是导致大多数食源性暴发的主要病原体。 TASBASI 等[32]设计了一种基于适配体门控和TMB 负载介孔二氧化硅纳米颗粒的LFB 检测鸡肉中的单核细胞增生李斯特菌,LOD 为53 cell/mL。 GAO 等[33]将等温链交换扩增(SEA)和LFB 结合,以10 CFU/mL 的目视检测限准确测定婴幼儿配方奶粉中的克罗诺杆菌属。 QU 等[34]将HCR多连体 (mHCR) 与食源性沙门氏菌16S rRNA 偶联,可检测到低至53.65 CFU/mL 的沙门氏菌。
3.2 生物毒素检测
生物毒素是在活细胞或生物体内产生的有害物质,包括霉菌毒素、植物毒素、细菌毒素和海洋毒素。 ZHU 等[35]设计了一种靶适配体抗原和靶适配体互补链双竞争LFB,用于食品和饲料中的黄曲霉毒素(AFB1)检测,其LOD 为0.1 ng/mL。 WU 等[36]采用同源适配体组合与β-凝集素和Fe3O4@Au 核壳纳米颗粒结合,通过磁富集策略和酶信号扩增开发了一种超灵敏的LFB,用于痕量β-凝集素检测。LOD 为8fM,比没有磁聚焦的类似测定低1 000 倍。
3.3 农兽药残留检测
滥用抗生素和杀虫剂严重影响着自然环境和人类健康,采用基于适配体的LFB 可以确保农产品的安全性。 以适体修饰的AuNPs 作为报告探针,寡核苷酸DNA1 修饰的AgNPs 作为信号放大元件,LIU等[37]开发了一种快速、廉价的LFB,用于现场检测蜂蜜、牛奶和奶粉中的卡那霉素。DNA1 与固定在T 系上的核酸适配体和DNA2 部分互补,形成AgNP-DNA1-apt-AuNPs 复合物并捕获在试纸上, 显示出比传统的基于AuNP 的LFB 更深的红色条带,视觉检出限为35 nM, 扫描读数仪最低检出限为0.077 8 nM。CHENG 等[38]构建了荧光适配体apta-LFB,用于同时检测毒死蜱、二嗪磷和马拉硫磷,该方法集成了更高特异性和稳定性的荧光apta-LFB 和零背景信号读出智能手机光谱阅读器,用于现场定量多种农药。
3.4 金属离子检测
人造DNA 酶和适配体可选择性地与金属离子结合,导致结构和功能发生变化,通过分析设备能够转换为可测量的信号[41]。 ZHOU 等[39]设计了1 个DNA序列和2 个发夹探针,通过核酸外切酶(Exo III)辅助级联信号放大,Hg2+存在下,DNA 序列与发夹探针结合,产生的富G 序列通过与N-甲基间卟啉IX(NMM)结合形成G-四链体结构作为信号传感器, 检测限为10 fM。 LI 等[40]采用无荧光标记单链DNA 和SYBR Green I 快速检测Hg2+,LOD 为3 nM,SYBR Green I仅当存在Hg2+情况下嵌入双螺旋结构的凹槽中,产生强烈的荧光。
3.5 掺假检测
掺假经常发生在食品工业中,威胁人类健康,通常使用物种特异性基因进行食品真实性检测。 QIN等[41]整合多种聚合酶链扩增(mPCR)和LFB 来检测牛肉中的多种掺假成分。 掺假组分的引物组具有不同的核酸标签(NAT),使扩增子能够在2 个相反的末端具有特定的摆动序列。该方法能够同时从牛肉中准确识别鸡肉、 鸭肉和猪肉掺假成分,LOD 低至0.01%(wt%)。WANG 等[15]开发了一种基于快速等温重组聚合酶扩增(RPA)的LFB 用于牦牛奶检测,可在40 min 内检测低至5%的牦牛奶。 ZHANG 等[42]使用标签标记多重环介导等温扩增(TM-LAMP)和三叉戟状LFB 建立了智能生物传感器,用于马和驴产品的真伪检测,提供了一个高通量和现场识别平台。
3.6 转基因食品检测
由于存在多种性状, 准确和现场检测堆叠的转基因生物是当下难题。LI 等[43]构建了通用FNA 侧流磁试纸条(MTS),将转基因玉米MON810 作为生物传感器的双链模型靶标,以磁性纳米颗粒(MNPs)为信号输出元件与阻断超PCR(BS-PCR)相结合,指数PCR 扩增和磁性增敏技术提高了MON810 对单个拷贝的检测灵敏度。CHENG 等[44]结合事件特异性标签标记的多重LAMP 技术检测转基因大豆的内参基因和两段侧翼序列, 实现了堆积转基因大豆快速、高灵敏检测,检测限为0.1%(w/w)。
4 展望
近年来, 核酸侧流层析传感器在开发固定化FNAs 和提高其功能、多样和有效信号读出等领域取得了快速进展。然而,大多数已发表的功能核酸侧流层析传感器无法满足WHO 为生物传感器规定的理想“ASSURE”标准:价格合理、灵敏、特异性、用户友好、快速、坚固、无需设备且可交付给最终用户;其次,大多数应用涉及单靶点检测,很少有研究充分利用核酸结构来开发多重检测方法。因此,未来需要提高FNAs 筛选效率,开发更有效的分区方法、简单的实时监控策略和自动选择设备; 将FNAs 与其他有益的识别元件(如受体、MIP 等)相结合,开发高性能FNAs-LFB;重点将反应模块集成到单个可以处理原始样品并产生易于解释的准确读数的侧流层析传感器中,如PGM 和PST,发展远程数据收集和传输;高通量检测是FNAs-LFB 发展的共性需求,需要开发更强大的检测模式, 以及相应的多通道和便携式读出设备。

