右美托咪定、甲苯磺酸瑞马唑仑与丙泊酚对脑出血手术患者麻醉效果及血清神经损伤标志物和神经功能的影响
黄菲,陈婷婷,贺红侠,刘军武,胥磊
(四川大学华西医院眉山医院麻醉科,四川 眉山 620010)
脑出血手术是一种对患者身体和心理都有很大影响的创伤性手术,对麻醉控制的要求较高。一方面,需要充分麻醉保证手术过程的安全性和有效性;另一方面,为了减少麻醉对患者神经系统的损伤,需要尽可能地选择对神经系统影响较小的麻醉药物。麻醉药物的选择与使用,是影响手术成功与否的重要因素,针对脑出血手术患者的麻醉药物选择,传统上常用的是丙泊酚等静脉麻醉药物。近年来,右美托咪定、甲苯磺酸瑞马唑仑等药物的应用越来越广泛。右美托咪定是一种新型的α2肾上腺素能受体激动剂,具有镇静、催眠和镇痛等作用,常用于麻醉诱导和维持;甲苯磺酸瑞马唑仑是一种短效、快速作用的苯二氮类药物,具有快速诱导麻醉、减轻焦虑和镇痛等特点[1-2]。这些麻醉药物具有不同的作用机制和药理特点,但对于脑出血手术患者的麻醉效果和对神经功能的影响仍需进一步研究和探讨。本研究旨在比较右美托咪定、甲苯磺酸瑞马唑仑和丙泊酚对脑出血手术患者的麻醉效果及其对血清神经标志物和神经功能的影响。
1 资料与方法
1.1 一般资料
选取2020年6月至2022年10月四川大学华西医院眉山医院收治的120例脑出血手术患者为研究对象,根据麻醉药物不同分为右美托咪定组、甲苯磺酸瑞马唑仑组和丙泊酚组,每组各40例。本研究经院伦理委员会审核批准,患者及家属知情同意,各组患者性别、年龄、发病至接受治疗时间、入院时格拉斯哥昏迷评分(GCS)、ASA分级等一般资料比较,差异无统计学意义(P>0.05)。见表1。

表1 各组患者一般资料比较
纳入标准:(1)年龄18~60岁;(2)既往有高血压病史;(3)符合脑出血诊断标准[3]并经头颅CT检查证实;(4)出血量<40 mL;(5)美国麻醉师学会(ASA)分级[4]Ⅱ或Ⅲ级;(5)临床资料完整。排除标准:(1)创伤引起的脑出血患者;(2)患血友病、白血病等严重的血液系统疾病者;(3)原发性脑室出血或蛛网膜下腔出血者;(4)存在面罩通气困难风险者;(5)因不良反应中断治疗或不接受定期随访、随访失联的患者。
1.2 方法
患者入手术室后立即面罩吸氧,监测生命体征。右美托咪定组:予以1 μg/kg的右美托咪定,10 min泵完,随后予以舒芬太尼0.8 μg/kg、罗库溴铵1 mg/kg进行麻醉诱导,待脑电双频指数(BIS)<40、肌松充分后进行气管插管,术中泵注0.5 μg·kg-1·h-1,静脉输注瑞芬太尼0.05~0.2 μg·kg-1·h-1,间断静脉注射罗库溴铵,术中维持BIS值45~55,必要时追加舒芬太尼或者血管活性药,维持生命体征稳定。甲苯磺酸瑞马唑仑组:静脉注射甲苯磺酸瑞马唑仑0.4 mg/kg、舒芬太尼0.8 μg/kg、罗库溴铵1 mg/kg麻醉诱导,待BIS<40、肌松充分进行气管插管,术中静脉泵注甲苯磺酸瑞马唑仑0.5~1.0 mg·kg-1·h-1,静脉输注瑞芬太尼0.05~0.2 μg·kg-1·h-1,间断静脉注射罗库溴铵,术中维持BIS值45~55,必要时追加舒芬太尼或者血管活性药,维持生命体征稳定。丙泊酚组:静脉注射丙泊酚2 mg/kg、舒芬太尼0.8 μg/kg、罗库溴铵1 mg/kg进行麻醉诱导,待BIS<40、肌松充分进行气管插管,术中静脉泵注丙泊酚4~12 mg·kg-1·h-1,静脉输注瑞芬太尼0.05~0.2 μg·kg-1·h-1,间断静脉注射罗库溴铵,术中维持BIS值45~55,必要时追加舒芬太尼或者血管活性药,维持生命体征稳定。
1.3 观察指标
(1)血流动力学指标:包括患者入手术室时(T0)、气管插管即刻(T1)、血肿清除时(T2)及手术结束时(T3)的心率(HR)、收缩压(SBP)和舒张压(DBP)。(2)CSI值:术中采用脑状态指数麻醉深度监护仪监测T0、T1、T2、T3时CSI值。(3)神经损伤标志物:术前、术后24 h、术后1周采集患者外周静脉血,离心分离血清,采用酶联免疫吸附法测定血清神经元特异性烯醇化酶(NSE)、胶质纤维酸性蛋白(GFAP)、中枢神经特异蛋白(S100β)水平。(4)神经功能:术前、术后1个月、术后6个月,采用美国国立卫生研究院卒中量表(NIHSS)评分[5]评估,总分为42分,分值越高表明神经功能受损越严重。(5)不良反应发生情况:包括呼吸抑制、躁动、恶心呕吐、心动过缓等。
1.4 统计学分析

2 结果
2.1 各组患者血流动力学指标比较
T1时,各组患者HR、SBP、DBP均低于T0、T2、T3时(P>0.05),但组间各时间点HR、SBP、DBP比较,差异无统计学意义(P>0.05)。见表2。
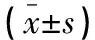
表2 各组患者血流动力学指标比较
2.2 各组患者CSI值比较
T1、T2时,各组患者CSI值均低于T0、T3时(P<0.05),但组间各时间点CSI值无统计学差异(P>0.05)。见表3。
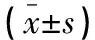
表3 各组患者CSI值比较
2.3 各组患者神经损伤标志物比较
术前,各组患者血清NSE、GFAP、S100β水平差异无统计学意义(P>0.05)。术后24 h,各组患者血清NSE、GFAP、S100β水平均升高(P<0.05),且右美托咪定组高于甲苯磺酸瑞马唑仑组及丙泊酚组(P<0.05);术后1周,各组患者血清NSE、GFAP、S100β水平均低于术前(P<0.05),但甲苯磺酸瑞马唑仑组及丙泊酚组低于右美托咪定组(P<0.05)。见表4。
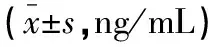
表4 各组患者神经损伤标志物比较
2.4 各组患者神经功能比较
术前,各组患者NIHSS评分比较,差异无统计学意义(P>0.05)。术后1个月,各组患者NIHSS评分均降低(P<0.05),且术后6个月进一步降低(P<0.05),甲苯磺酸瑞马唑仑组及丙泊酚组均低于右美托咪定组(P<0.05)。见表5。
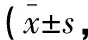
表5 各组患者神经功能比较分)
2.5 各组患者不良反应发生情况比较
右美托咪定组出现躁动2例,心动过缓1例,术后恶心呕吐1例;甲苯磺酸瑞马唑仑组出现躁动1例,心动过缓2例,术后恶心呕吐3例;丙泊酚组躁动3例,心动过缓3例,术后恶心呕吐3例,经对症干预后均有效缓解。各组患者不良反应总发生率比较,差异无统计学意义(χ2=2.290,P=0.318)。
3 讨论
脑出血本身及手术创伤均会导致大量神经细胞死亡和脑组织破坏。研究[6]显示,脑出血幸存患者中,半数以上合并中重度神经功能缺陷。脑出血手术过程中需要深度麻醉控制,除了保证手术安全和患者的舒适度之外,还应尽可能地减少对神经系统的影响,避免更多的神经细胞死亡和脑组织破坏[7]。
麻醉药物可通过抑制脑内兴奋性神经递质来达到控制神经功能的目的,但同时也会对脑细胞代谢、脑血流量产生一定影响[8]。因此如何通过合理的麻醉管理,减少麻醉对神经功能的损伤,提高手术成功率,是脑出血手术中的一个重要课题。本研究结果显示,T0、T1、T2、T3各时间点,各组HR、SBP、DBP、CSI及CSI值比较,差异均无统计学意义,提示丙泊酚、甲苯磺酸瑞马唑仑和右美托咪定在脑出血中均有理想的麻醉效果。研究[9-10]表明,脑出血后神经元和胶质细胞会受到细胞死亡、炎症反应和氧化应激等多种损伤,进而释放大量神经标志物,如NSE、GFAP和S100β等,这些标志物可作为反映神经元损伤程度和预测患者预后的生物指标。NSE主要存在于神经元和神经内分泌细胞中,当脑组织发生损伤时,NSE大量释放进入血液循环中,可在血清中检测到其水平异常升高,因此在脑出血等脑损伤情况下,NSE浓度可作为反映脑组织损伤程度的重要指标[11]。GFAP是主要分布在星形胶质细胞中的一种胶质纤维酸性蛋白,当脑组织受损时,星形胶质细胞活性增加,导致GFAP的表达增加,其浓度可反映星形胶质细胞的活性和胶质纤维的破坏程度[12]。S100β是主要分布于胶质细胞的一种神经胶质细胞特异性钙结合蛋白,在脑出血等脑部损伤情况下,其浓度可反映胶质细胞损伤程度[13]。脑出血可引起脑组织的神经元和星形胶质细胞损伤,导致NSE、GFAP和S100β水平增加。本研究结果显示,各组术后24 h血清NSE、GFAP、S100β水平高于术前,提示术后短时间内神经功能损伤加剧。
本研究中,甲苯磺酸瑞马唑仑组、丙泊酚组术后24 h血清NSE、GFAP、S100β水平变化幅度均小于右美托咪定组,而各组术后1周血清NSE、GFAP、S100β水平均低于术前,且甲苯磺酸瑞马唑仑组、丙泊酚组均低于右美托咪定组,提示甲苯磺酸瑞马唑仑与丙泊酚的神经保护作用更优。右美托咪定是一种选择性α2肾上腺素能受体激动剂,主要通过抑制交感神经系统来减少应激反应,同时也可能抑制神经元代谢,增加血脑屏障通透性[14]。甲苯磺酸瑞马唑仑是一种苯二氮类药物,主要作用是增强γ氨基丁酸受体基因簇(GABAa)受体的抑制性传导,抑制神经元的兴奋性,丙泊酚是一种GABAa受体激动剂,作用机制与甲苯磺酸瑞马唑仑类似,均可通过抑制神经元兴奋性来实现麻醉效果。本研究结果显示,甲苯磺酸瑞马唑仑组、丙泊酚组术后早期的神经保护作用较强,对血清神经标志物的水平有较好的调节作用,同时能有效降低术后1个月和6个月的NIHSS评分,考虑与二者增强GABAa受体的作用有关。脑出血患术后脑组织的损伤和神经元的大量死亡与中枢神经系统炎症反应、星形胶质细胞活度的异常激活以及神经炎症等机制有关[15]。一方面,三种麻醉药物均能够抑制神经元的兴奋性,减少神经元的能量消耗和代谢负担,保护神经元免受细胞内外环境的不良影响,从而减轻术后早期神经元的损伤;另一方面,它们还能促进突触前和突触后神经元的相互作用,改善神经递质的释放和神经传递过程,从而调节神经元的功能和结构,减轻术后晚期的神经功能障碍;此外,甲苯磺酸瑞马唑仑和丙泊酚还具有血脑屏障保护作用,可减少血液中毒性物质进入脑内,抑制星形胶质细胞的异常激活,减少细胞因子和炎症介质的释放,从而保护神经细胞免受损伤。另外,三种麻醉药物在不良反应发生率上无显著差异,故三者在手术中的耐受性、安全性相似。
综上,右美托咪定、甲苯磺酸瑞马唑仑与丙泊酚在脑出血手术中的麻醉效果相当,但甲苯磺酸瑞马唑仑与丙泊酚对于神经功能的保护作用更优,二者可能通过激活GABAa受体发挥神经保护作用。

