铁及其化合物考点剖析
吴凯明
(浙江省义乌中学)
铁在地壳中的含量极其丰富,是人类最早使用的金属之一.铁元素有+2 价和+3 价,可以形成+2、+3价化合物,还可形成+2 价和+3 价结合的化合物,铁及其化合物是考试的热点和难点.
1 铁在日常生产、生活中的应用考查
铁的化学性质较为活泼,铁及其合金在工农业生产中有广泛的应用.例如,铁粉在食品包装中常用作脱氧剂;航母甲板高强度钢材是一种铁碳合金;氧化铁用作油漆、涂料;四氧化三铁用于制备激光打印墨粉;K2FeO4既可用于自来水的消毒杀菌又可除去水中的悬浮杂质;用FeCl3溶液腐蚀铜板;FeSO4作补血剂.
例1下列有关铁及其化合物的说法错误的是( ).
A.生铁比纯铁易生锈
B.不锈钢是铁合金,只含金属元素
C.常温下可以用铁制或铝制容器盛装浓硫酸
D.稀土元素被称为“冶金工业的维生素”,其加入钢中后可增加钢的韧性、抗氧化性
2 铁的化合物的性质考查
铁常见的化合价有+2、+3 价.+2 价的铁主要体现还原性,同时兼有氧化性;+3价的铁主要体现氧化性,同时兼有还原性(高中阶段只考虑氧化性).Fe2+通常用铁氰化钾或酸性KMnO4或KSCN 和氯水检验;Fe3+用KSCN 检验.
例2下列实验对应的现象和结论都正确的是( ).
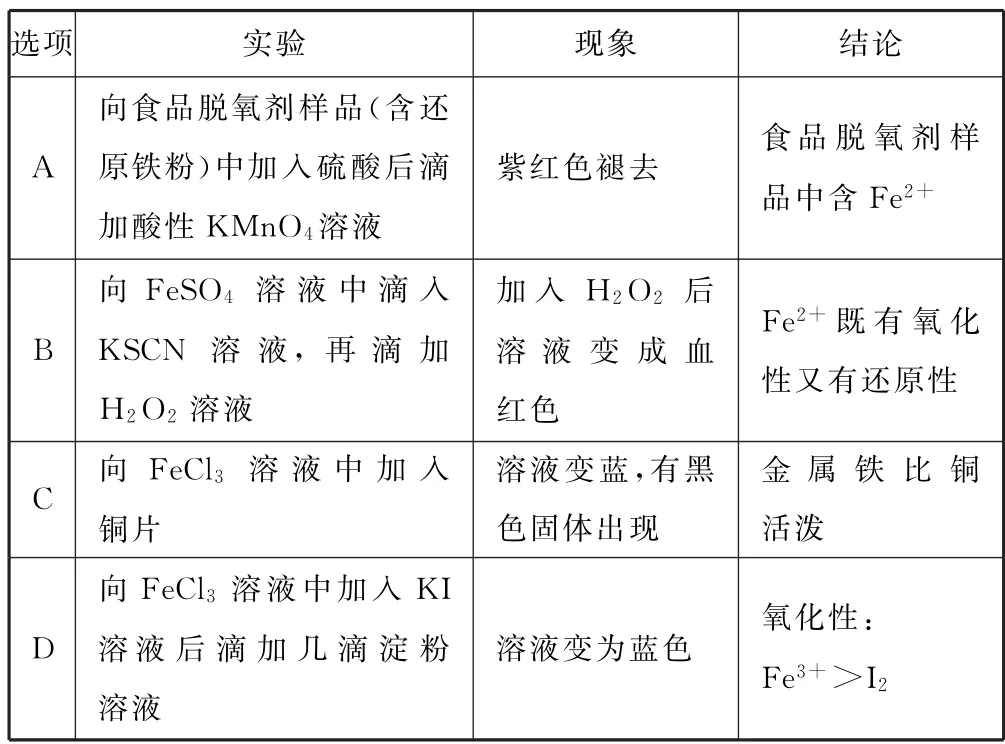
3 化工流程题中铁及其化合物的考查
铁在自然界中广泛存在,自然界的矿石中大多含有铁,提炼铁及其化合物成为考试的重点和热点.化工流程题中大多包括铁及其化合物的转化.
例3煤化学链技术具有成本低、能耗低的CO2捕集特性.以铁矿石(主要含铁物质为Fe2O3)为载氧体的煤化学链制氢工艺如图1所示.测定反应前后不同价态铁的含量,对工艺优化和运行监测具有重要意义.
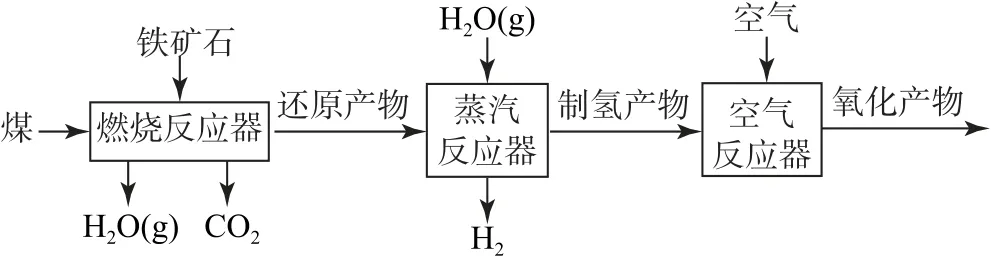
图1
(1)进入燃烧反应器前,铁矿石需要粉碎,煤需要烘干研磨,其目的是________.
(2)分离燃烧反应器中产生的H2O(g)和CO2,可进行 CO2高纯捕集和封存,其分离方法是_________.
(3)测定铁矿石中全部铁元素的含量.
ⅰ.配制铁矿石待测液:铁矿石加酸溶解,向其中滴加氯化亚锡(SnCl2)溶液.
ⅱ.用重铬酸钾(K2Cr2O7)标准液滴定可测定样品中的全部铁元素的含量.配制铁矿石待测液时SnCl2溶液过量会对测定结果产生影响,分析影响结果及其原因_________.
(4)测定燃烧反应后产物中单质铁的含量:取ag样品,用FeCl3溶液充分浸取(FeO 不溶于该溶液),向分离出的浸取液中滴加bmol·L—1K2Cr2O7标准液,消耗K2Cr2O7标准液VmL.已知K2Cr2O7被还原为Cr3+,样品中单质铁的质量分数为_________.
(5)工艺中不同价态铁元素的含量测定结果如图2所示.
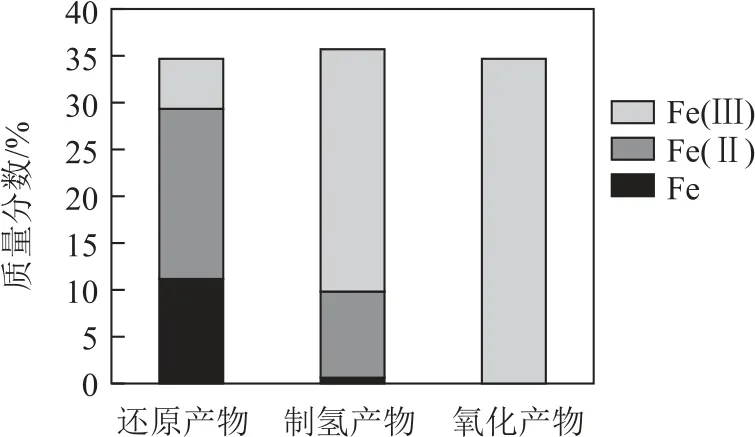
图2
①制氢产物主要为Fe3O4,写出蒸汽反应器中发生反应的化学方程式________.
②工艺中可循环使用的物质是________(填化学式).
(1)进入燃烧反应器前,铁矿石需要粉碎,煤需要烘干研磨,其目的是增大接触面积,提高化学反应速率.
(2)分离燃烧反应器中产生的H2O(g)和CO2,可进行CO2高纯捕集和封存,其分离方法是冷凝,因为经过冷凝后气态水转化为液态水.
(3)配制铁矿石待测液时SnCl2溶液过量会对测定结果产生影响,因为过量的SnCl2能与K2Cr2O7反应,导致测定结果(铁元素含量)偏高.
(4)已知K2Cr2O7被还原为Cr3+,关系式为
样品中单质铁的质量
(5)①制氢产物主要为Fe3O4,蒸汽反应器中发生反应的化学方程式为
②根据分析可知,工艺中可循环使用的物质是H2O(g).
总之,铁及其化合物在日常生活或工业生产中有广泛的应用.由于存在可变化合价,Fe2+和Fe3+的转化及检验成为化学实验的热点,地壳中铁的含量成为化工流程中的必考点.不管是铁的除杂还是铁的化合物的制备,都是高考常考的知识点.
(完)

