富马酸伏诺拉生片联合亮菌口服溶液对慢性萎缩性胃炎的疗效观察*
尤 伟,张 梅,鲁大林,陈 燕,王 欣,方宜正
1.芜湖市第五人民医院 消化内科(芜湖 241000);2.安徽医科大学第一附属医院 中西医结合肿瘤科(合肥 230000)
慢性萎缩性胃炎(chronic atrophic gastritis,CAG)是消化系统常见的一种疾病,临床症状表现为上腹胀痛、反酸、嗳气、恶心等。CAG内镜下图像特点为黏膜颜色红白相间,以白色为主,黏膜皱襞变平或消失,部分出现黏膜菲薄、血管显露等情况;胃黏膜上皮、固有腺体萎缩,细胞数目减少和体积缩小可诱发胃功能异常和胃蛋白酶原(pepsinogen,PG)(Ⅰ、Ⅱ)等激素分泌异常[1-2]。从CAG的发病机制上来看,CAG的抑酸治疗效果显著。富马酸伏诺拉生片是一种新型抑酸药物,临床广泛用于反流性食管炎治疗,对于CAG治疗研究较少;而亮菌口服溶液已广泛用于CAG的临床治疗。因此,本研究拟探索富马酸伏诺拉生片联合亮菌口服溶液方案对CAG患者的临床疗效,为CAG的治疗提供一种新探索,现报道如下。
1 资料与方法
1.1 临床资料
选取2021年9月至2022年3月在芜湖市第五人民医院消化内科就诊的60 例CAG患者为研究对象,随机分为对照组与试验组,每组30 例。对照组男22 例,女8 例,年龄48~70(60.90±6.73)岁;试验组男19 例,女11 例,年龄37~70(56.13±9.42)岁。纳入标准:1)年龄18~70 岁,有自主行为能力;2)符合《中国慢性胃炎共识意见》[3](2017 版)CAG诊断标准,均有病理诊断支持;3)知晓本研究并签署知情同意书。排除标准:1)无自主行为能力或拒绝本研究者;2)有严重器官功能障碍,如严重肝功能异常、凝血功能障碍等;3)胃镜提示存在胃溃疡或消化道出血者;4)胃黏膜表现癌变或高级别上皮内瘤变。本研究通过芜湖市第五人民医院伦理委员会审核批准(审批号:皖康20210020)。
1.2 药品与试剂
亮菌口服溶液(生产厂家:合肥诚志生物制药有限公司,批准文号:国药准字H34020002);富马酸伏诺拉生片(生产厂家:武田制药株式会社,批准文号:国药准字J20200011);抗细胞增殖核抗原(proliferative cell nuclear antigen,PCNA)单克隆抗体(武汉博士德生物工程有限公司,货号:BM3888);PGⅠ、Ⅱ检测试剂(安徽伊普诺康生物技术股份有限公司,产品技术编号:皖械注准20172400180)。
1.3 方法
对照组服用亮菌口服溶液(10 mL/次,3 次/d),连续服用6周;试验组在服用亮菌口服溶液基础上加用富马酸伏诺拉生片(20 mg/次 ,1 次/d)治疗,两组均服药6周。
1.4 观察指标
1.4.1 血清PGⅠ、Ⅱ含量 在治疗前1 d及治疗6 周后留取两组患者空腹静脉血5 mL送检,离心后血清标本经乳胶增强免疫比浊法测定PGⅠ、Ⅱ含量并计算PG比值(pepsinogen ratio,PGR)。
1.4.2 内镜积分 在治疗前后两组患者均行胃镜检查,参照李鹏等[4]萎缩性胃炎标准评估内镜积分,内镜下黏膜特征每下降1 个数量级计1 分,0 分为治疗前后胃黏膜无变化,3 分为胃黏膜痊愈。
1.4.3 病理积分 在治疗前后两组胃黏膜组织均行苏木精伊红(hematoxylin-eosin staining,HE)染色,参考孙利红等[5]方法制定病理积分:0 分为胃黏膜无改变;1 分为胃黏膜异细胞增生恢复达2 个级别;2 分为胃黏膜异细胞增生恢复达1 个级别但未达2 个级别;3 分为胃黏膜异细胞增生恢复未达1 个级别。
1.4.4 PCNA阳性率 根据课题组前期研究[6]方法,留取治疗前后两组胃黏膜组织进行免疫组织化学染色,检测PCNA阳性表达,核染色是棕黄色或棕褐色为阳性,选5 个非重叠阳性细胞视野,高倍镜下计数200 个细胞,统计阳性细胞率。
1.4.5 临床疗效 治疗6 周后,分析两组治疗效果,总有效率=(症状消失+明显改善+轻度改善)人数/总人数×100%。
1.5 统计学方法
采用SPSS20.0 统计软件进行数据分析,服从正态分布的定量资料采用()表示,两组间比较采用t检验;不服从正态分布的定量资料采用M(P25,P75)表示,采用秩和检验;定性资料采用例数(%)表示,组间比较采用χ2检验。检验水准α除特别说明外均设定为0.05。
2 结果
2.1 两组基线资料比较
两组性别、年龄基线资料比较,差异无统计学意义(P<0.05)(表1)。
表1 两组基线资料比较[n(%),,n=30]
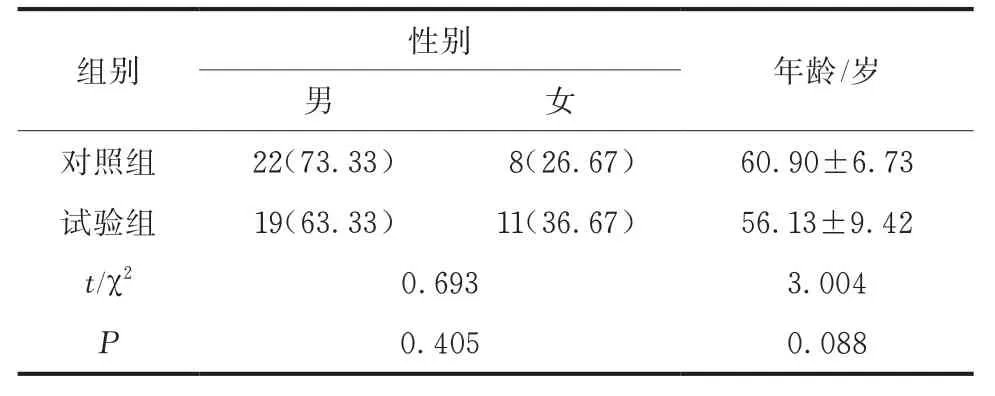
表1 两组基线资料比较[n(%),,n=30]
?
2.2 两组PGⅠ、Ⅱ含量及PGR 比较
与治疗前比较,两组PGⅠ含量、PGR均上升,且试验组PGⅡ下降更明显,差异有统计学意义(P<0.05)。与对照组比较,治疗后试验组PGⅠ含量、PGR明显上升,PGⅡ含量明显下降,差异有统计学意义(P<0.05)(表2)。
表2 两组PGⅠ、Ⅱ及PGR比较(,n=30)
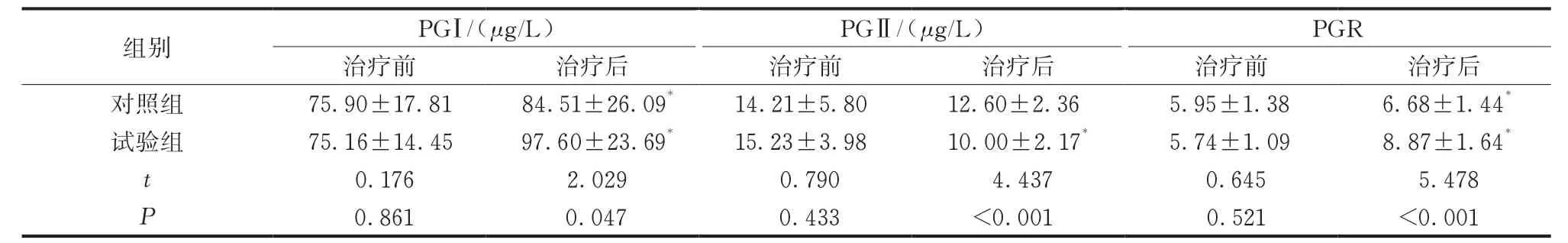
表2 两组PGⅠ、Ⅱ及PGR比较(,n=30)
注:与同组治疗前比较,*P<0.05。
?
2.3 两组内镜、病理积分及PCNA 阳性率比较
与对照组比较,治疗后试验组内镜积分增多,病理积分下降,差异有统计学意义(P<0.05)。与治疗前比较,两组PCNA阳性率均明显下降,且试验组低于对照组,差异有统计学意义(P<0.05)(表3、图1~2)。
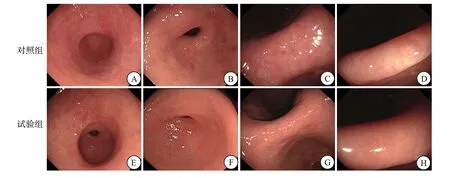
图1 两组治疗前后内镜下图像比较

图2 两组胃黏膜组织的病理图像比较
表3 两组内镜、病理积分及PCNA阳性率比较[M(P25,P75),,n=30]
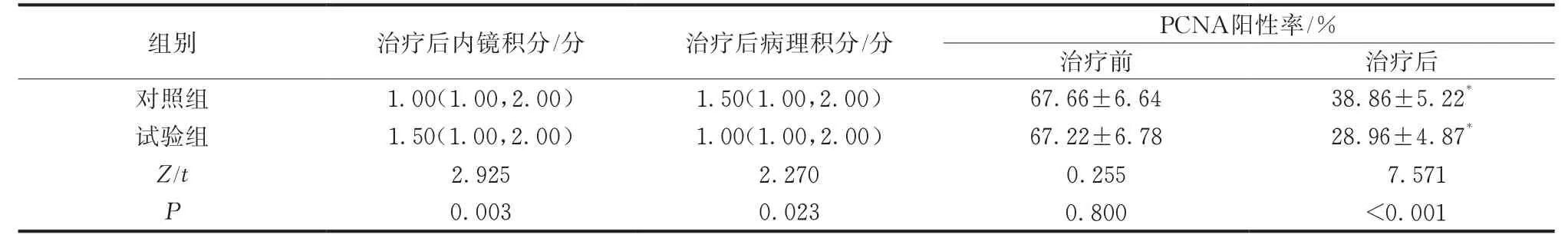
表3 两组内镜、病理积分及PCNA阳性率比较[M(P25,P75),,n=30]
注:与同组治疗前比较,*P<0.05。
?
2.4 两组临床总有效率比较
治疗后试验组临床总有效率(90.00%)高于对照组(73.33%),差异有统计学意义(P<0.05)(表4)。

表4 两组临床总有效率比较[n(%),n =30 ]
3 讨论
CAG是指胃黏膜受到长期的炎症刺激,导致胃黏膜细胞和胃腺萎缩,有0.10%~0.25%的概率进展为癌[7]。目前CAG临床上常采用抗菌药物、胃酸抑制剂、营养支持、胃肠动力药物、中成药及微生物调节等治疗方式[8-9]。有研究[10-11]证实,亮菌口服溶液有效成分为亮菌多糖、多肽,治疗萎缩性胃炎效果较好。伏诺拉生片是一种新型钾离子竞争性酸阻滞剂(potassium-competitive acid blockers,P-CAB),与传统质子泵抑制剂相比,其发挥作用不依靠强酸活化,可直接与H+/K+-ATP酶的结构蛋白靶点Glu795 特异性结合,起效更迅速、持续时间更久;与常见的奥美拉唑、凯普拉生等质子泵抑制剂、P-CAB制剂相比,伏诺拉生片是目前最有效的抑酸药物之一[12]。有研究[13]证实,富马酸伏诺拉生片对抗幽门螺杆菌感染更有效,这与其抑酸效果有关,因此本研究主要通过富马酸伏诺拉生片联合亮菌口服溶液联合方案治疗CAG,观察其临床疗效。
PCNA是一种DNA合成的辅酶,能准确反映细胞的生长速度和状态。有研究[14-16]证实,患者胃黏膜萎缩、化生、感染等情况越重,其PCNA阳性率则越高,PCNA可用于胃黏膜损伤的监测,为检测CAG的有效生物学指标。PGⅠ、Ⅱ为胃蛋白酶前体,常用于监测胃黏膜损伤和功能变化。相关研究[17-18]进一步证实,胃黏膜萎缩与PGⅠ、PGR呈负相关,而PGⅡ与胃黏膜萎缩呈正相关。本研究显示,富马酸伏诺拉生片联合亮菌口服溶液方案可使PGⅠ上升、PGⅡ下降且PGR增加更明显,表明该联合方案可改善CAG患者胃黏膜功能。本研究还显示,与对照组比较,试验组治疗后HE染色中胃黏膜萎缩、化生的范围或程度较小,同时PCNA阳性率更低,表明该联合方案能减轻CAG患者胃黏膜萎缩、化生等情况。本研究发现,富马酸伏诺拉生片联合亮菌口服溶液对于CAG患者治疗有效且优于单纯亮菌口服溶液,推断可能与该联合方案能更有效控制炎症有关。本研究试验组在使用富马酸伏诺拉生片联合亮菌口服溶液后临床症状改善与内镜积分变化趋势一致,这点从HE染色变化中也得到证实,故从微观角度上也证实该联合方案对CAG的治疗效果优于单纯亮菌口服溶液。生理状态下前列腺素E2 可加速胃黏膜微循环流动,保护胃黏膜,亮菌口服溶液联合兰索拉唑可通过调节前列腺素E2增强这一作用[19-21]。此外亮菌口服溶液的有效成分主要为亮菌多糖、多肽。有研究[22]认为,兰索拉唑可抑制NF-κb的表达来保护乙醇诱导小鼠胃黏膜损伤;而P-CAB药物即使在静息状态下也可与K+结合阻碍H+/K+-ATP酶结合;而传统质子泵抑制剂则必须在活化状态下才能起到抑酸作用;推断P-CAB药物可能通过某些类似途径起到抗黏膜损伤作用且作用更强。
综上所述,富马酸伏诺拉生片联合亮菌口服溶液可改善CAG患者胃黏膜,提高其临床疗效。本研究试验样本较少且研究时间较短,试验组未能设置不同服药周期,对于不同服药周期是否存在PCNA表达上的差异未能明确,同时对于CAG的治疗详细机制未能进行探究,拟后续试验进一步探究。

