监测血清HBV RNA水平变化对于NAs治疗CHB停药复发的预测价值
刘虹 王鹏雁 刘友德
1烟台市奇山医院肝病一科,济宁 264000;2烟台市奇山医院肝病二科,济宁 264000
慢性乙型肝炎(chronic hepatitis B,CHB)是由乙型肝炎病毒(hepatitis B virus,HBV)感染所致的传染性疾病,随着病情进展,可导致肝硬化、肝细胞癌。积极的抗病毒治疗是CHB的治疗基石,核苷(酸)药物[nucleoside (acid) drugs,NAs]是其常用的抗病毒药物,可有效抑制病毒复制,延缓肝硬化进程,降低肝癌的发生风险[1]。但CHB抗病毒治疗停药后的复发是影响患者预后的危险因素,寻找停用口服抗病毒药物后复发的预测因子有助于改善CHB的治疗效果,是目前临床研究的热点[2]。共价闭合环状DNA(covalent closed circular DNA,cccDNA)持续存在是导致HBV感染慢性化、停药后复发的主要原因。但cccDNA检测需要肝穿刺活组织检查,具有有创性,且cccDNA在肝脏中的分布不均,穿刺时易发生漏诊[3]。基础研究认为,在乙型肝炎病毒e抗原(hepatitis B virus e antigen,HBeAg)阳性的慢性HBV感染者中,血清乙型肝炎病毒核糖核酸(hepatitis B virus RNA,HBV RNA)水平与肝组织内cccDNA水平呈正相关,而血清标志物易获得、可重复取样[4]。本研究探讨血清HBV RNA水平在预测NAs抗病毒治疗CHB停药复发的价值,现报道如下。
资料与方法
1.一般资料
回顾性选取2017年1月至2021年1月在烟台市奇山医院治疗的CHB患者160例为研究对象,其中男105例、女55例,年龄27~61(43.32±8.81)岁。纳入标准:(1)CHB诊断符合《慢性乙型肝炎防治指南(2015年更新版)》[5]中的标准;(2)接受NAs抗病毒治疗,且达到停药标准;(3)初治患者;(4)依从性高,能配合治疗随访者;(5)患者及家属知情同意,并签署知情同意书。排除标准:(1)有酒精性、药物性、免疫性及其他病毒性肝脏疾病;(2)合并有恶性肿瘤、慢性阻塞性肺疾病、甲状腺疾病等其他严重疾病;(3)合并有结核、艾滋病病毒(HIV)等感染者。
本研究经烟台市奇山医院伦理委员会审批通过(201603012)。
2.治疗方法
所有患者均接受NAs抗病毒治疗,口服恩替卡韦分散片(正大天晴药业集团股份有限公司,国药准字H20100019,规格0.5 mg)0.5 mg/次,1次/d,或口服富马酸替诺福韦二吡呋酯片(齐鲁制药有限公司,国药准字H20173185,规格0.3 g)0.3 mg/次,1次/d,或口服替比夫定片(北京诺华制药有限公司,国药准字H20070028,规格600 mg)600 mg/次,1次/d。达到停药标准,随访患者停药复发情况。
3.检查方法
于治疗前(基线)、治疗24周、治疗48周、治疗72周、停药时抽取患者空腹状态下静脉血标本6 ml,分装于两支真空采血管。一支以转速2 500 r/min离心10 min,离心半径12.5 cm,取血清采用日本日立7180型全自动生化分析仪及其配套试剂检测肝功能指标丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST);采用化学发光法检测HBeAg。另一支采用荧光定量PCR法定量检测乙型肝炎病毒脱氧核糖核酸(hepatitis B virus DNA,HBV DNA)、HBV RNA。HBV DNA试剂盒为罗氏诊断产品(上海)有限公司产品,HBV RNA试剂盒为上海任度科技有限公司产品。
4.评判标准
(1)停药标准:HBeAg阳性患者治疗后ALT正常,HBV DNA转阴,且HBeAg转阴至少1年以上;HBeAg阴性患者治疗后ALT正常,HBV DNA转阴,巩固治疗至少2年以上。(2)复发判断标准:满足以下标准之一,①最低检出限以下的HBV DNA再次复现增高;②已阴转的HBeAg有复阳;③已正常的ALT、AST再次增高。
5.统计学处理
统计分析采用SPSS 22.0软件,符合正态分布的计量资料采用()表示,组间比较采用独立样本t检验;计数资料采用例(%)表示,行χ2检验;多因素分析采用logistic回归分析;预测价值采用受试者工作特征曲线(ROC)分析。以P<0.05为差异有统计学意义。
结果
1.停药复发情况
截止2023年2月,160例患者中,停药复发患者46例,停药复发率28.75%。
2.停药复发和未复发患者临床资料比较(表1)

表1 慢性乙型肝炎患者停药复发和未复发的临床资料比较
停药复发患者年龄、合并糖尿病比例、基线HBV DNA、基线HBV RNA和停药时HBV RNA均明显高于停药未复发患者,差异均有统计学意义(均P<0.05);停药复发和未复发患者性别、体质量指数、高血压、高脂血症等比较,差异均无统计学意义(均P>0.05)。
3.停药复发危险因素的多因素分析(表2)
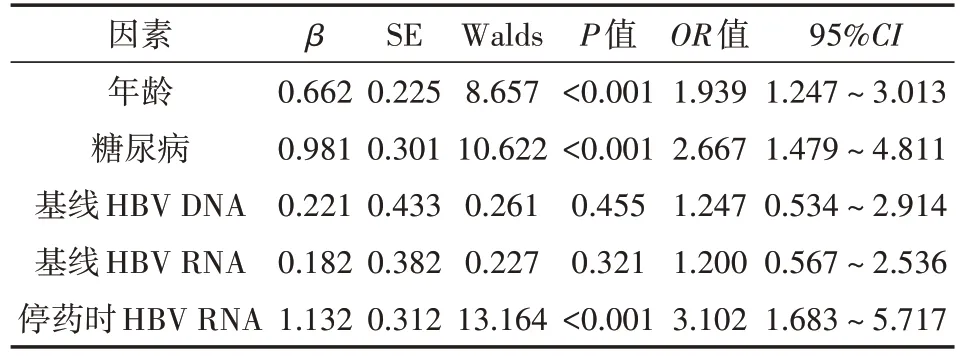
表2 160例慢性乙型肝炎患者停药复发危险因素的多因素分析
将年龄、是否合并糖尿病、基线HBV DNA、基线HBVRNA和停药时HBV RNA作为自变量,是否发生停药复发作为因变量进行logistic回归分析,结果显示,年龄、合并糖尿病、停药时HBV RNA是患者停药复发的影响因素(均P<0.05)。
4.停药时HBV RNA预测停药复发的价值(图1)

图1 160例慢性乙型肝炎患者停药时乙型肝炎病毒核糖核酸(HBV RNA)预测停药复发的受试者工作特征曲线
停药时HBV RNA预测患者停药复发的ROC曲线下面积为0.777(95%CI0.706~0.849),P<0.05,截断值为1.61 log copies/ml,灵敏度和特异度分别为88.50%、54.80%。
5.HBeAg阳性患者HBeAg、HBV DNA和HBV RNA转阴情况(表3)
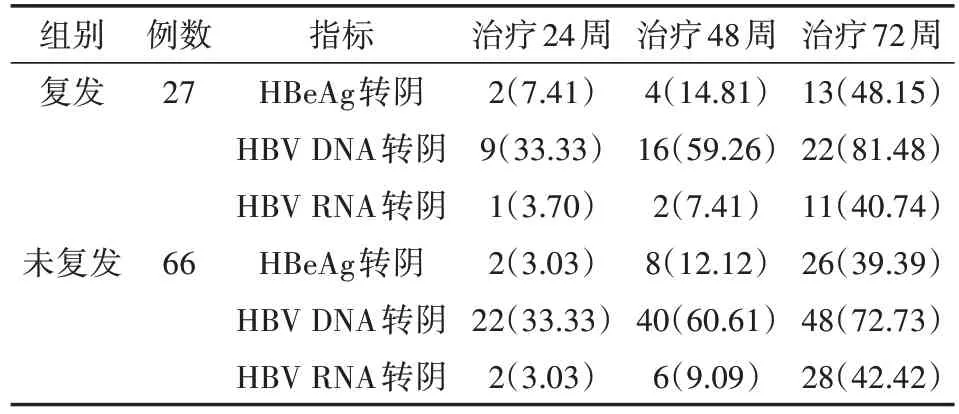
表3 HBeAg阳性患者HBeAg、HBV DNA和HBV RNA转阴情况[例(%)]
HBeAg阳性停药复发和未复发患者治疗24周、48周、72周HBeAg转阴、HBV DNA转阴、HBV RNA转阴率比较,差异均无统计学意义(均P>0.05);HBV DNA转归较快,而HBeAg和HBV RNA转归较慢,且较同步。
讨论
流行病学研究发现,目前全球HBV感染患者人数已超过2亿,其中约4 000万患者已进展至肝硬化、肝功能失代偿或原发性肝癌阶段,预后较差[6]。NAs是目前临床治疗HBV感染的基础性用药,常用品种包括拉米夫定、恩替卡韦、阿德福韦酯、替比夫定、替诺福韦等[7]。NAs可有效抑制HBV的复制活性,延缓病情进展,改善CHB患者的生活质量。目前,临床对于HBV的治疗目标为HBsAg阴转,长期抑制病毒复制,延缓肝硬化进程,防止肝衰竭、肝癌,最大限度改善患者生活质量[8]。NAs的停药时机为HBeAg阳性者HBeAg血清转阴后3年;HBeAg阴性者,HBsAg转阴后至少12个月。但仍有相当一部分患者停药后复发[9]。
HBV RNA是携带病毒遗传信息的第一道传递者,在病毒复制活性、疗效评估方面具有重要意义[10]。严景全等[11]研究发现,血清HBV RNA可精确反映肝细胞中cccDNA的表达,可为CHB患者体内病毒复制活跃程度提供直接证据。本研究发现,截止2023年2月,停药复发患者46例,停药复发率28.75%,这提示CHB患者NAs停药后复发率较高。本研究还发现,停药复发患者年龄、糖尿病、基线HBV DNA、基线HBV RNA和停药时HBV RNA均明显高于停药未复发患者。停药复发和未复发患者性别、体质量指数、高血压、高脂血症等比较差异均无统计学意义(均P>0.05),这提示高龄、合并糖尿病、基线HBV DNA、基线HBV RNA和停药时HBV RNA较高者更易出现停药后复发现象。这是由于高龄患者机体免疫功能相对较差,感染HBV的病程相对较长,停药后机体免疫功能往往不能较好抑制HBV病毒复制[12]。合并糖尿病患者体内的高糖环境有利于病原体的增殖、复制,且糖尿病患者机体往往处于免疫紊乱状态,不能对HBV产生有效的免疫应答,因此停药后更易复发[13]。基线HBV DNA、基线HBV RNA和停药时HBV RNA水平较高提示肝细胞中cccDNA高表达,患者体内病毒复制活跃程度更高,因此停药后更易复发[14-15]。
本研究将年龄、是否合并糖尿病、基线HBV DNA、基线HBV RNA和停药时HBV RNA作为自变量,是否发生停药复发作为因变量进行logistic回归分析,结果显示年龄、糖尿病、停药时HBV RNA是患者停药复发的影响因素。停药时HBV RNA预测患者停药复发的ROC曲线下面积为0.777,截断值为1.61 log copies/ml,灵敏度和特异度分别为88.50%、54.80%。上述结果提示,年龄、糖尿病、停药时HBV RNA水平与CHB患者NAs停药复发有关,停药时HBV RNA在预测停药复发方面有一定应用价值,其预测灵敏度较好,而特异度相对较差。在今后的临床工作中,应将高龄、合并糖尿病、停药时HBV RNA水平高的CHB患者作为NAs停药复发的高危人群,在停药后加强随访和实验室检测,以便及时发现CHB复发,及时给予有效的抗病毒治疗干预,以防病情恶化。本研究还发现,HBeAg阳性停药复发和未复发患者治疗24周、48周、72周HBeAg转阴、HBV DNA转阴、HBV RNA转阴率比较,差异均无统计学意义(均P>0.05);HBV DNA转归较快,而HBeAg和HBV RNA转归较慢,且较同步。上述结果提示,HBeAg阳性患者治疗期间的HBeAg、HBV DNA、HBV RNA转阴并不会影响停药复发风险。在今后的临床工作中,可考虑将HBeAg和HBV RNA转归作为停药的指征,可有助于降低复发风险。但该方案是否可行,还需要进一步的深入研究。
综上所述,停药时HBV RNA水平与CHB患者NAs停药复发有关,在预测停药复发方面有一定应用价值。
利益冲突所有作者均声明不存在利益冲突
作者贡献声明刘虹、刘友德:研究实施,数据整理,论文撰写,统计学分析,研究指导,论文修改,经费支持;王鹏雁:研究实施,数据整理,论文撰写,研究指导,论文修改,经费支持

