老年脓毒症相关性脑病患者血清外泌体LncNEAT1、LncSOX2OT表达及对临床预后评价
李雪莲,冷凌涵,张丽涓,向相,宋家志,陈陶江,韩强,王平
脓毒症相关性脑病(sepsis-associated encephalopathy,SAE)是继发于中枢神经系统以外的感染引起的弥漫性脑功能损伤,病死率较高[1-2]。寻找能够评估SAE预后的生物标志物具有重要临床意义。外泌体是直径为30~150 nm小囊泡,包含蛋白、脂质及RNA等[3]。长链非编码RNA核富含丰富的转录本1(long noncoding RNA nuclear-enriched abundant transcript 1,lncNEAT1)能够调节神经元棘突密度,参与SAE的疾病进展[4-5]。长链非编码RNA SRY盒转录因子2重叠转录本(long noncoding RNA SOX2 overlapping transcript,LncSOX2OT) 是调节性别决定区Y框蛋白2(sex determining region Y-box2,SOX2)的非编码RNA,可导致脓毒症患者心肌细胞线粒体功能障碍的发生[6]。目前SAE患者血清外泌体LncNEAT1、LncSOX2OT表达尚不清楚,本研究通过检测SAE患者血清外泌体LncNEAT1、LncSOX2OT的表达,分析两者与生存预后的关系,报道如下。
1 资料与方法
1.1 临床资料 选取2020年2月—2022年2月就诊于成都中医药大学附属第五人民医院重症医学科的老年SAE患者96例为SAE组,男51例,女45例,年龄 (71.95±6.04)岁;体质量指数(21.07±2.76)kg/m2;受教育年限(4.61±1.85)年;合并症:高血压史31例,糖尿病史17例;感染部位:肺部感染42例,尿路感染19例,血液感染22例,腹腔感染13例;根据SAE患者28 d内生存状态将SAE组再分为生存亚组(n=50)和死亡亚组(n=46)。以同期诊治的无SAE的脓毒症患者60例为非SAE组,男33例,女27例,年龄(70.78±5.96)岁;体质量指数(21.18±2.72)kg/m2;受教育年限 (4.69±1.91)年;合并症:高血压20例,糖尿病10例;感染部位:肺部感染30例,尿路感染13例,血液感染10例,腹腔感染7例。SAE组和非SAE组患者性别、年龄、体质量指数、受教育年限、高血压史、糖尿病史及感染部位比较差异均无统计学意义(P>0.05)。本研究经医院伦理委员会审核通过(2019SF-106),患者或家属知情同意并签署知情同意书。
1.2 病例选择标准 (1)纳入标准:①脓毒症诊断符合脓毒症3.0诊断标准[7];②SAE诊断排除药物效应、电解质紊乱、代谢紊乱及脑膜炎、脑炎等原发性中枢神经系统病理状态及非感染性全身炎性反应等引起的认知功能障碍,表现为谵妄,注意力,定向力障碍和书写能力等受损;③临床资料完整。(2)排除标准:①合并颅脑感染、脑血管疾病、脑占位性疾病、阿尔茨海默病及癫痫等颅内病变;②肝性脑病、肺性脑病、肾性脑病等其他器官功能障碍继发的意识障碍;③甲状腺危象,甲状腺功能减退及糖尿病并发症等能够引起意识障碍的内分泌与代谢性疾病;④水电解质紊乱、精神疾病及药物中毒等引起的意识障碍;⑤妊娠、哺乳期女性。
1.3 观测指标与方法
1.3.1 血清外泌体LncNEAT1、LncSOX2OT的相对表达量检测:患者入院后次日留取清晨空腹肘静脉血5 ml,室温静置1 h,2 500 r/min离心10min,留取上层血清。利用外泌体RNA分离提取试剂盒(购自北京百奥莱博公司,货号BTN180807)提取血清外泌体,取血清0.5 ml加入外泌体分离试剂0.1 ml,4℃室温孵育30 min,离心去上清,加入缓冲液0.2 ml重悬。加入外泌体核酸提取溶液A 0.6 ml,混匀后静置3 min,加入溶液B 0.7 ml,混匀后离心加入溶液C 1 ml,离心取上清后加入无酶水重悬外泌体总RNA 0.2 ml。逆转录为cDNA后,采用荧光定量PCR仪(美国ABI公司,型号ABI7500)检测血清外泌体LncNEAT1、LncSOX2OT的相对表达量,实时荧光定量PCR试剂盒购自北京索莱宝公司,货号SR1110。引物由华大公司设计合成。PCR总反应体系20 μl:模板 0.5 μl,2×SYBR Green Premix 10 μl,正反向引物各1 μl,无酶水7.5 μl。反应程序:94℃ 预变性5 min、95℃变性30 s、62℃退火30 s、70℃延伸30 s,变性退火延伸共35个循环。引物序列:LncNEAT1正向序列5'-ACGGGCACACATCAAGCATA-3'、反向序列5'-AGCCTCAGCCCCCTATACAA-3',LncSOX2OT正向序列5'-GGGCTCTGTGGTCAAGTCCG-3'、反向序列5'-CGCTCTGGTAGTGCTGGGC-3';GAPDH正向序列5'-TGAGGCCGGTGCTGAGTATGTCG-3',反向序列:5'-CCACAGTCTTCTGGGTGGCAGTG-3'。2-ΔΔCt法对血清外泌体LncNEAT1、LncSOX2OT的相对表达量进行定量分析。
1.3.2 SAE严重程度评估:对96例SAE患者应用急性生理学与慢性健康状况评价Ⅱ (acute physiology and chronic health evaluationⅡ,APACHEⅡ)进行评分,范围0~72分,分值越高,病情越重。根据入院24 h内呼吸系统、血液系统、肝脏系统等6个系统的相应参数,进行序贯器官衰竭评分(sequential organ failure assessment,SOFA评分),范围0~24分,分值越高,病情越重。

2 结 果
2.1 2亚组临床资料比较 死亡亚组SAE患者C反应蛋白(CRP)、降钙素原(PCT)、神经元特异性烯醇化酶(NSE)、APACHEⅡ评分、SOFA评分高于生存亚组(P均<0.01),其他资料比较差异无统计学意义(P>0.05),见表1。

表1 生存亚组与死亡亚组SAE患者临床资料比较
2.2 SAE组和非SAE组血清外泌体LncNEAT1、LncSOX2OT表达比较 SAE组血清外泌体LncNEAT1、LncSOX2OT相对表达量分别为(2.45±0.65)、(3.02±0.74),明显高于非SAE组的(0.93±0.34)、(0.85±0.27)(t=16.726、21.803,P均<0.001)。
2.3 2亚组血清外泌体LncNEAT1、LncSOX2OT表达比较 生存亚组血清外泌体LncNEAT1、LncSOX2OT相对表达量分别为(1.82±0.59)、(2.52±0.69 ),明显低于死亡亚组 (3.13±0.71 )、( 3.56±0.78)(t=9.861、6.931,P均<0.001)。
2.4 血清外泌体LncNEAT1、LncSOX2OT表达与APACHEⅡ评分、SOFA评分相关性分析 Pearson相关系数分析结果显示,SAE患者血清外泌体LncNEAT1、LncSOX2OT与APACHEⅡ评分、SOFA评分呈明显正相关(r=0.812,0.761,0.833,0.598,P均<0.001)。
2.5 SAE患者28 d生存预后的多因素Logistic回归分析 以SAE患者28 d生存预后为因变量(死亡=1,生存=0),以上述结果中P<0.05项目为自变量进行多因素Logistic回归分析,结果显示,降钙素原高、C反应蛋白高、神经元特异性烯醇化酶高、APACHEⅡ评分高、SOFA评分高、LncNEAT1高及LncSOX2OT高是影响SAE患者28 d生存预后的独立危险因素(P<0.01),见表2。
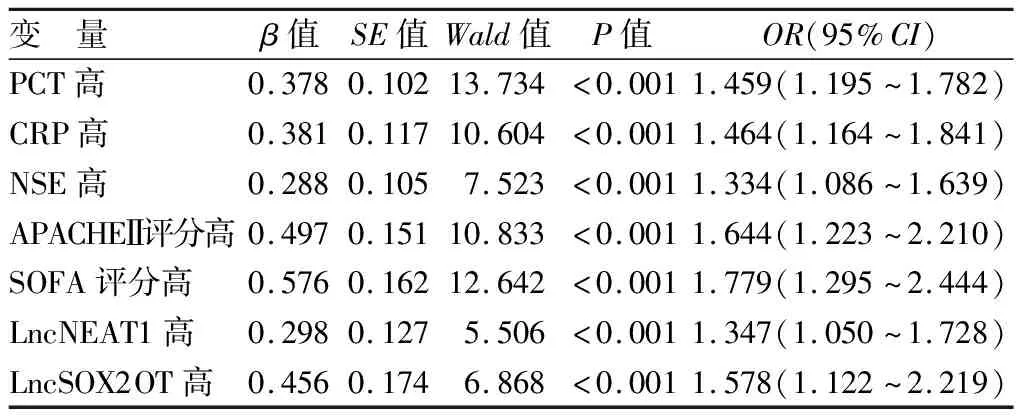
表2 影响SAE患者28 d生存预后的多因素Logistic回归分析
2.6 血清外泌体LncNEAT1、LncSOX2OT对SAE患者28 d生存预后的评估价值 绘制血清外泌体LncNEAT1、LncSOX2OT对SAE患者28 d生存预后的评估价值的ROC曲线,并计算曲线下面积(AUC),结果显示,血清外泌体LncNEAT1、LncSOX2OT及二者联合对SAE患者28 d生存预后诊断的AUC分别为0.846、0.834、0.914,二者联合高于单项指标检测 (Z=3.864、3.915,P均<0.001),见表3、图1。

图1 血清外泌体LncNEAT1、LncSOX2OT及联合对SAE患者28 d生存预后的评估价值ROC曲线

表3 血清外泌体LncNEAT1、LncSOX2OT对SAE患者28 d生存预后的评估价值
3 讨 论
SAE是脓毒症常见的并发症,患者致残率、致死率较高[8]。SAE缺乏典型的临床表现,目前无特异性生物标志物及影像学改变,其诊断过程仍为排除性诊断。目前认为SAE的发生与神经炎性反应、血脑屏障功能障碍及氨基酸和神经递质异常有关[9]。虽然炎性反应及中枢神经系统损伤标志物如降钙素原、神经元特异性烯醇化酶等标志物一定程度上能够反映SAE患者病情程度,但在评估SAE患者预后方面仍存在敏感度及特异度不高等缺点,临床应用价值有限[10]。深入研究SAE疾病机制,寻找能够评估SAE预后的生物标志物,有利于SAE的早期诊治,降低SAE死亡率。
外泌体是细胞释放的直径在几十纳米到几百纳米不等的磷脂双分子层细胞外囊泡,能够使核酸、蛋白等分子进行细胞间通讯[3]。近年来发现,脓毒症患者血清外泌体中的核酸及蛋白等内容物可通过促进细胞死亡,参与SAE疾病的发生发展,是潜在的生物标志物[4]。LncNEAT1是近年来发现的新的非编码RNA,其能够加重脓毒症患者炎性反应感染程度,导致多器官功能衰竭,是新的预后相关生物标志物[11]。本研究中,SAE患者血清外泌体LncNEAT1水平升高,与SAE病情程度有关,提示LncNEAT1参与脓毒症患者SAE的疾病发生和发展。SAE患者血清外泌体LncNEAT1升高与患者机体炎性反应程度较重有关。研究表明,肿瘤坏死因子α、白介素1β等促炎细胞因子能够诱导单核巨噬细胞中LncNEAT1的表达上调,LncNEAT1能够以外泌体形式分泌到细胞外,进一步发挥促炎的生物学效应[11]。此外,LncNEAT1的水平升高能够使神经细胞和脑微血管内皮细胞功能出现障碍,加重SAE患者病情严重程度。研究发现,脓毒症小鼠血清外泌体中LncNEAT1表达升高,其作为分子海绵结合微小RNA-9-5p,上调转铁蛋白受体基因的表达,促进脑微血管内皮细胞株bEnd.3细胞的铁死亡的发生,导致SAE疾病的发生发展[12]。尚有研究表明,脓毒症小鼠神经细胞中lncNEAT1表达明显增加,lncNEAT1能够直接与血红蛋白β亚单位相互作用,抑制突触后密度蛋白95,降低神经元树突棘密度,导致神经元功能障碍[5]。本研究中,血清外泌体LncNEAT1升高是SAE患者不良生存预后的独立危险因素,提示检测SAE患者血清外泌体LncNEAT1水平有助于评估患者临床预后。分析其原因,一方面可能是LncNEAT1的表达能够加重患者机体炎性反应程度,促进SAE患者病情进展。研究发现,在脂多糖诱导的脓毒症小鼠模型中,LncNEAT1的表达上调能够激活微小RNA-31-5p/POU结构域2类转录因子1通路,促进小鼠腹腔巨噬细胞RAW264.7释放大量白介素1β、肿瘤坏死因子α等促炎细胞因子,加重脓毒症疾病严重程度[13]。另一方面,LncNEAT1还能够通过激活心肌细胞中Toll样受体2/核因子κB信号通路,促进脂多糖诱导的脓毒症小鼠心肌细胞凋亡,增加脓毒症小鼠死亡率[14]。
LncSOX2OT编码基因位于人类3号染色体,表达于发育中大脑皮质,参与调节神经干细胞的增殖和分化,与恶性肿瘤、中枢神经系统疾病的发生发展有关[15-16]。近年来发现,LncSOX2OT的异常表达上调能够抑制细胞间黏附分子1的表达,促进人心肌细胞AC16的氧化应激反应和炎性反应损伤,促进心肌细胞凋亡[17]。本研究中,SAE患者血清外泌体LncSOX2OT升高,与病情程度呈正相关,表明LncSOX2OT促进SAE的疾病进展。LncSOX2OT的表达升高可能与rs9839776位点的单核苷酸多态性有关,rs9839776位点CC等位基因人群脓毒症发生率显著高于TT等位基因[18]。研究发现,脂多糖诱导的脓毒症动物模型中,LncSOX2OT的表达上调能够抑制SOX2的表达,促进线粒体分裂蛋白Drp1的表达升高,引起线粒体功能障碍,过度氧化应激及炎性反应导致认知功能障碍及SAE的发生[6,19]。本研究证实,血清外泌体LncSOX2OT水平能够评估SAE患者的生存预后。其原因可能是LncSOX2OT能加重SAE患者病情严重程度,导致患者不良预后。有学者利用盲肠结扎穿孔术建立C57BL/6J雄性小鼠脓毒症模型中发现,LncSOX2OT基因敲除可通过下调SOX2表达抑制脓毒症诱导的小鼠海马神经元凋亡,改善小鼠认知功能的损伤,抑制LncSOX2OT/SOX2信号通路可能是治疗或预防脓毒症相关性脑病神经退行性变的有效方法[20]。笔者进一步绘制ROC曲线,发现血清外泌体LncNEAT1、LncSOX2OT联合检测对SAE患者生存预后具有较高的评估价值,诊断的敏感度和特异度分别为0.904,0.813。临床医生可根据血清外泌体LncNEAT1、LncSOX2OT水平对SAE患者的预后进行评估,及早进行干预治疗,从而改善SAE患者的预后。
综上所述,老年SAE患者血清外泌体LncNEAT1、LncSOX2OT水平升高,两者表达与APACHEⅡ评分、SOFA评分呈正相关,均参与SAE的疾病进展。血清外泌体LncNEAT1、LncSOX2OT水平升高是影响SAE患者28 d生存预后的独立危险因素,两项联合对SAE患者28 d生存预后具有较高的预测价值。本研究也存在不足,本研究随访时间有限,未能对血清外泌体LncNEAT1、LncSOX2OT水平在评估SAE患者长期认知功能障碍中的临床价值进行深入研究,有待今后设计前瞻性多中心临床试验进一步研究。
利益冲突:所有作者声明无利益冲突
作者贡献声明
李雪莲:设计研究方案,实施研究过程,论文撰写;冷凌涵:实施研究过程,资料搜集整理;张丽涓:进行统计学分析;向相:课题设计,论文撰写;宋家志:核对、整理资料,检查数据;陈陶江:论文审核,论文修改;韩强:参与研究设计和试验过程;王平:提出研究思路,分析试验数据

