全子宫切除术后阴道残端血管平滑肌瘤一例
丁懿,高峻,李文燕,叶丹,马振琴,何荣霞
血管平滑肌瘤(angioleiomyoma)是一种罕见的良性肿瘤,起源于平滑肌细胞。血管平滑肌瘤可发生于全身各处,但更常发生于下肢、头颈部及躯干[1],女性生殖系统少见,子宫切除术后血管平滑肌瘤更是罕见。本文报道2023 年5 月于兰州大学第二医院妇科就诊的因子宫肌瘤行全子宫切除术后再发阴道残端血管平滑肌瘤1 例,并复习既往文献,对该类疾病特点及诊治做一总结。
1 病例报告
患者 女,49 岁,因阴道不规则出血约5 个月,于2023 年5 月10 日收住我院妇科。患者系围绝经期妇女,孕2 产2。2015 年因子宫平滑肌瘤于当地医院行全子宫切除术,术后病理检查提示:子宫平滑肌瘤(具体不详),未规律随访。患者自述约5 个月前无明显诱因出现阴道不规则出血,持续3~10 d不等,间断时间不明,量少,呈鲜红色或稍淡红色,反复至今,无明显加重及缓解因素,无腹痛、腹胀,无头晕、乏力,无尿频、尿急,无恶心、呕吐。于当地医院就诊,磁共振成像(magnetic resonance imaging,MRI)提示:子宫切除术后8 年复查,盆腔内多发团块状占位,并周围受侵,瘤内出血;盆腔内及双侧腹股沟区多发淋巴结。B 超提示盆腔实性占位(85 mm×68 mm),建议上级医院就诊。患者为求进一步诊治就诊于我院,以盆腔肿物收住入院。患者自发病以来,精神状况一般,饮食睡眠一般,大小便正常,体质量未见明显增减。
入院查体:体温36.3 ℃,脉搏78 次/min,心率20 次/min,血压100/85 mmHg(1 mmHg=0.133 kPa),头颈胸部发育正常,心肺查体未见明显异常,肝脾未触及肿大。腹软,无压痛及反跳痛,下腹部一长约7 cm 纵向陈旧性手术瘢痕,愈合良好。妇科查体:外阴发育正常,阴道通畅,阴道残端愈合良好,未见异常,盆腔偏右侧触及一大小约12 cm×10 cm 包块,质韧,活动度欠佳,压痛阳性。三合诊:包块偏向右侧,致宫旁间隙变窄。入院后我院盆腔MRI 示:子宫切除术后,盆腔多发团块状混杂信号影(部分病变囊变坏死出血)考虑恶性肿瘤,请结合临床;左侧附件区囊性灶(见图1)。全腹CT 增强示:盆腔多发占位,右侧髂静脉多发癌栓形成,卵巢来源的恶性肿瘤多考虑;右肺钙化灶。肿瘤标志物:人附睾蛋白4(human epididymis protein 4,HE4)438.6 pmol/L,糖类抗原125(carbohydrate antigen 125,CA125)、CA19-9、癌胚抗原(carcinoembryonic antigen,CEA)、鳞状细胞癌抗原(squamous cell carcinoma antigen,SCC)等未见明显异常。血常规、传染病八项、凝血四项、肝肾功能等均未见明显异常。根据患者症状、体征及辅助检查诊断为:盆腔肿物,右侧卵巢来源多考虑。
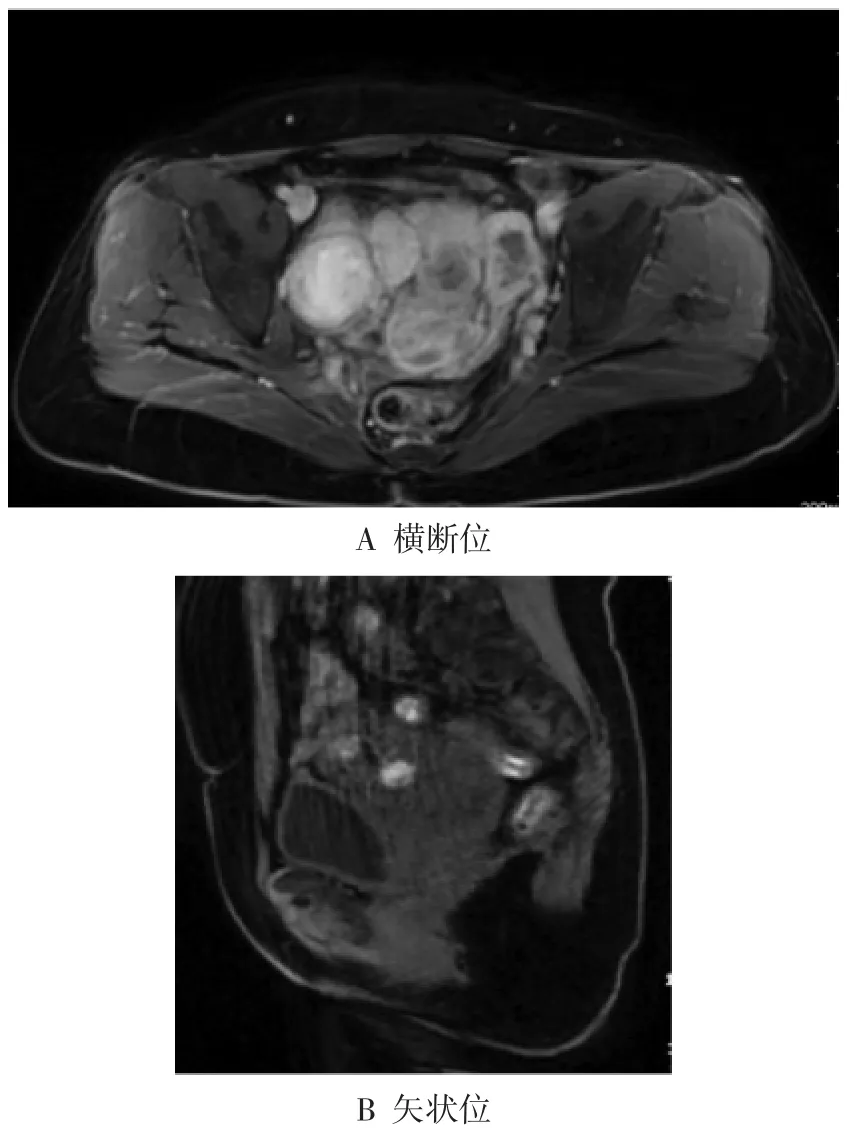
图1 盆腔MRI 图
遂于2023 年5 月16 日在全身麻醉下行开腹探查术,术中见:子宫缺如,盆腔内见一大小约10 cm×8 cm×7 cm 形态不规则肿物,包膜完整,色灰白,质地韧,探查该肿物由阴道残端发出,向前侵及膀胱,向后封闭直肠子宫陷凹,双侧附件包裹粘连于侧盆壁及阴道残端肿物。遂行阴道残端肿物切除术+双侧附件切除术+盆腔粘连松解术,切除过程中见肿物内黄色及褐色黏稠组织流出。术中冰冻病理回报:(盆腔)恶性潜能未定或良性肿瘤,具体分型待石蜡及免疫组织化学染色。将肿物剥除,可吸收线缝合。术后病理检查回报:(盆腔肿物)血管平滑肌瘤,大小约7 cm×4 cm×3 cm,伴出血、水肿、变形,部分区域生长密集,请定期复查;镜下见:组织内以梭形细胞为主,细胞排列疏密不均,瘤细胞核无异型性,其间散在较多血管,血管壁薄厚不均,见图2。免疫组织化学检测结果:广谱细胞角蛋白(pCK,-),平滑肌肌动蛋白(SMA,+),HMB45(-),重型钙调蛋白结合蛋白(h-caldesmon,+),结蛋白(desmin,+),分化抗原34(CD34,血管+),信号转导及转录激活因子6(STAT6,-),CD117(-),S100(-),SOX-10(-),Bcl-2(+),Ki-67(2%+)。
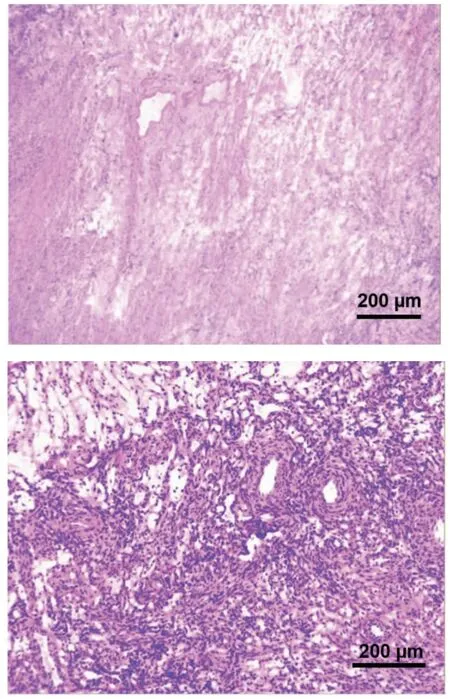
图2 术后病理图(HE 染色×40)
术后给予补液预防感染、调节电解质等对症支持治疗,患者恢复良好,于2023 年5 月24 日出院。出院后1 个月复查,阴道残端愈合良好,腹部切口愈合良好,妇科B 超提示子宫及双侧附件切除术后,少量盆腔积液,余未见明显异常。
2 讨论
2.1 发病特点与发病机制血管平滑肌瘤是一种罕见的间叶源性肿瘤,由平滑肌细胞和厚壁血管组成。该类肿瘤多发于40~60 岁,通常发生在下肢、躯干和头颈部[1],女性生殖系统少见。在现有的研究报道中,女性生殖系统的血管平滑肌瘤多发生于子宫,也可发生于卵巢、阴道壁、宫颈及阔韧带等。阴道残端的血管平滑肌瘤尚少有明确病例报道。目前女性生殖系统血管平滑肌瘤的发病机制尚不清楚,有研究认为其起源于轻微创伤、慢性静脉阻塞或性激素刺激[2]。Gupta 等[3]认为血管平滑肌瘤起源于血管平滑肌细胞,也有研究认为这些肿瘤来源于动静脉吻合[4]。本病例于8 年前行全子宫切除术,血管平滑肌瘤发生于阴道残端,可能印证了以上观点,但目前对于女性生殖系统血管平滑肌瘤的病因尚无统一定论。
2.2 临床表现与诊断血管平滑肌瘤术前往往难以诊断。子宫血管平滑肌瘤患者通常主诉为严重痛经、腹痛不适、阴道出血或可触及的腹部肿块[1],起源于卵巢的血管平滑肌瘤患者则常表现为盆腔肿物和下腹部不适[5]。也有少数病例临床症状并不典型,Thomas等[6]报道了1 例以CA125 水平升高和伪Meigs 综合征(卵巢纤维瘤常并发腹水与胸水)为临床表现的病例,Handler 等[7]报道了1 例血管平滑肌瘤继发的消耗性凝血功能障碍。本例患者表现为间断阴道出血。在既往病例中,肿瘤标志物检查有CA125、CA72-4的升高[5-6],本例患者表现为HE4 的升高,但均缺乏特异性。影像学检查包括超声、CT 及MRI,通常可用于术前评估,若CT 扫描显示子宫软组织肿块中存在明显的弯曲血管样增强结构,则应考虑血管平滑肌瘤[4],但确诊多依靠术后病理检查结果。标本从肉眼看,血管平滑肌瘤大小不等,常为灰白色,质韧,大多数肿瘤呈实性,偶有坏死、出血和囊性变;在显微镜下可分为3 种组织学类型:①毛细血管狭窄与厚平滑肌束交错的毛细血管型;②厚血管与平滑肌束交错的静脉型;③海绵状血管加宽,平滑肌较少的海绵状血管型[4]。免疫组织化学结果显示,肿瘤细胞SMA、肌肉特异性肌动蛋白(muscle-specific actin,MSA)和钙调理蛋白(calponin)呈弥漫性阳性,h-caldesmon和desmin 呈不同程度阳性,S-100 蛋白和HMB45的免疫染色通常为阴性[8]。本例患者MRI 提示部分病变囊变坏死出血,免疫组织化学结果SMA(+),h-caldesmon(+),desmin(+),CD34(血管+),S100(-),HMB45(-),与文献报道相一致。
2.3 治疗与预后目前对于女性生殖系统血管平滑肌瘤的治疗方式较为统一,即首选手术治疗[9],手术根据患者的年龄及生育需求选择不同的切除范围。若为有生育需求的患者,在保证生育要求的情况下尽量将瘤体切除,包括切除边缘和整个囊[1];对于无生育要求的患者,应行全子宫切除术,治疗可选择全子宫切除术联合或不联合双侧附件切除。根据患者瘤体大小及位置、年龄、体质量、基础疾病等选择手术方式,腹腔镜不会增加未完全切除血管平滑肌瘤的发生风险[10],现有报道中开腹手术应用较多。本例患者49 岁,已切除子宫,卵巢萎缩,功能下降,且术中冰冻性质不明,综合评估后行开腹阴道残端血管平滑肌瘤+双侧附件切除术。手术作为首选治疗方式,一是血管平滑肌瘤在术前难以确诊,二是预后较好。有学者研究了国外34 例子宫血管平滑肌瘤病例,无论行子宫血管平滑肌瘤切除术、全子宫切除,还是全子宫加双侧附件切除,均未见复发[11]。
综上,女性生殖系统血管平滑肌瘤少见,阴道残端血管平滑肌瘤更是十分罕见,现未见临床报道。其发病机制不明,临床症状主要表现为阴道出血、腹部包块,腹部CT、盆腔MRI 可判断肿瘤的大小、占位及性质,但确诊依据手术后病理及免疫组织化学检查。治疗以手术完整切除肿瘤为主,预后良好。

