自拟抗早衰汤联合针刺治疗肝郁肾虚型早发性卵巢功能不全患者的临床效果▲
梁 欢 曾凡慧 李 玲 谭姣姣 杨 静
(恩施土家族苗族自治州中心医院中医部妇产科,湖北省恩施市 445000)
早发性卵巢功能不全(premature ovarian insufficiency,POI)是由多种病因所致卵巢功能衰退的异质性综合征,常见于40岁以下女性,主要临床表现为闭经或月经稀发,伴随促性腺激素水平升高和雌激素水平降低,可增加骨质疏松性骨折、心脑血管疾病的发生风险,严重影响女性身心健康和生活质量[1]。目前西医治疗POI以雌孕激素序贯疗法为主,虽然该方法能改善临床症状,恢复正常月经,但药物治疗可产生胃肠道不适、溶血性贫血、抑郁等毒副作用,且其存在较多使用禁忌证,如对于不明原因子宫出血、乳腺恶性肿瘤病史、心脑血管梗死病史等患者,整体疗效并不理想[2]。POI归属于中医学的血枯、闭经、不孕等范畴,与肾虚、肝郁及痰湿血瘀等有关,因肾气-天癸-冲任-胞宫功能轴紊乱而发病,应以滋阴补肾、疏肝解郁、祛痰化湿为治疗原则[3]。近年来,中药联合针刺疗法逐渐成为治疗POI的主流方法。自拟抗早衰汤是在归肾丸和逍遥丸的基础上加减而成,具有疏肝健脾、补肾养血等功效[4]。针刺是中医内病外治的独特疗法,通过作者主要经络、穴位进行辨证治施,促使整体气血经络得到疏通[5]。目前关于中药汤剂联合针刺治疗POI的临床研究报告较少,鉴于此,本研究探讨自拟抗早衰汤联合针刺治疗肝郁肾虚型POI患者的临床效果。
1 资料与方法
1.1 临床资料 选取2021年5月至2022年6月在恩施土家族苗族自治州中心医院就诊的70例肝郁肾虚型POI患者作为研究对象。纳入标准:(1)符合《早发性卵巢功能不全的临床诊疗中国专家共识》[6]中POI的诊断标准,即年龄<40岁,月经稀发或停经≥4个月,且至少连续2次检测血清促卵泡激素(follicle stimulating hormone,FSH)>25 IU/L(检测间隔时间>4周)。(2)符合《中医妇科学》[7]中肝郁肾虚型POI的诊断标准。肝郁肾虚证主症为闭经或经期错后,量少,色暗淡;次症为腰骶酸痛,头晕耳鸣,倦怠乏力,性欲下降,潮热汗出,胸胁胀痛,经行不畅夹有血块,小腹胀痛,善太息,心烦易怒;舌脉为舌淡红,苔薄白,脉弦细数。以上主症必备,次症具备1~2项,结合舌脉即可确诊。(3)所有患者对本研究的治疗均可耐受。(4)患者均知情本研究内容并签署知情同意书。排除标准:(1)伴有多囊卵巢综合征、子宫损伤及其他原因导致的闭经;(2)合并精神异常、恶性肿瘤;(3)近3个月内接受其他药物治疗;(4)合并宫腔粘连;(5)合并心肝肾及造血系统等严重疾病。按随机数字表法将患者分为观察组和对照组,每组35例。对照组年龄20~39(30.36±5.27)岁,POI病程6~25(18.48±3.24)个月。观察组年龄21~39(30.75±5.42)岁,POI病程7~24(18.72±3.46)个月。两组患者的年龄、POI病程差异无统计学意义(P>0.05),具有可比性。本研究经恩施土家族苗族自治州中心医院医学伦理委员会审核批准(批号:2023-071-001)。
1.2 治疗方法
1.2.1 对照组:给予对照组患者雌孕激素序贯治疗。于月经周期[对于有月经来潮患者以月经第1天为月经周期第1天,无月经来潮患者则在服用药物(达英-35,即炔雌醇环丙孕酮片)后出现撤退性出血的第1天为月经周期第1天]第5天开始口服复方戊酸雌二醇片(浙江仙琚制药股份有限公司,国药准字H20020299,每片含戊酸雌二醇2 mg+炔诺酮0.7 mg),1片/次,1次/d,连续服用21 d;于月经周期第12天加用黄体酮胶囊(浙江仙琚制药股份有限公司,国药准字H20041902,50 mg/粒)治疗,100 mg/次,2次/d,连用10 d后停药。若服药后月经按时来潮,于月经周期第5天继续开始下一疗程;若服药后7 d内仍无月经来潮,则于停药第7天继续开始下一疗程。持续治疗3个疗程。
1.2.2 观察组:给予观察组患者自拟抗早衰汤配合针刺治疗。(1)自拟抗早衰汤配方为菟丝子、女贞子、枸杞子各20 g,白芍、当归、杜仲、茯苓各15 g,熟地、山茱萸、山药、香附、川芎、路路通各10 g,柴胡6 g,甘草3 g。加水煎至400 mL,每日1剂,分2次温服,均为饭前服药,经期停服,连续服用3个月(3个疗程)。(2)针刺治疗。穴组1为百会穴、本神穴(双侧)、神庭穴、中脘穴、天枢穴(双侧)、关元穴、子宫穴(双侧)、大赫穴(双侧)、三阴交穴(双侧)、足三里穴(双侧)、太溪穴(双侧)、太冲穴(双侧)。穴组2为肾俞穴(双侧)、次髎穴(双侧)。选用一次性使用无菌针灸针(苏州东邦医疗器械有限公司,规格:0.25 mm×25 mm、0.25 mm×40 mm、0.25 mm×75 mm)与脉冲针灸电针仪(青岛鑫升实业有限公司,型号:G6805-IB)。交替针刺穴组1与穴组2。首先针刺穴组1,患者取仰卧位,常规消毒,平刺百会穴、神庭穴、本神穴0.5~1.0寸,仅捻转,直刺其余穴位1.0~1.5寸,均提插捻转,平补平泻。然后,针刺穴组2,调整患者至俯卧位,常规消毒,直刺肾俞穴0.5~1.0寸,向内下斜刺次髎穴2.5~3.0寸,提插捻转,平补平泻,得气后连接脉冲针灸电针仪,采用疏密波治疗,电流强度以患者耐受为宜,留针30 min。每周治疗2次,经期暂停治疗,连续治疗3个月(3个疗程)。
1.3 观察指标
1.3.1 中医证候积分:分别于治疗前、治疗3个月后评价两组患者的中医证候积分。共8个中医证候,包括经少或闭经、经量或色质、腰骶酸痛、头晕耳鸣、潮热汗出、性欲下降、胸胁胀痛、心烦易怒,每个中医证候以无、轻、中、重依次记0、2、4、6分,总积分范围0~48分,评分越低表示临床症状越轻。
1.3.2 卵巢功能和子宫内膜厚度:分别于治疗前、治疗3个月后检测两组患者的阴道超声参数。应用阴道超声仪(徐州市凯尔医学仪器有限公司,型号:KR-E80),于月经周期第10~12天测量患者子宫内膜厚度,于月经周期第2~4天监测卵巢体积、窦卵泡数,若未监测到优势卵泡则每2 d监测1次,若监测到优势卵泡则每日监测1次,探查直径>10 mm的优势卵泡至排卵或黄素化,记录排卵周期。卵巢体积=(长径×横径×前后径×3.14)/6。
1.3.3 血清性激素、抗苗勒管激素及炎症因子水平:分别于治疗前、治疗3个月后,在月经周期第2~4天内抽取患者晨起空腹静脉血3 mL,4 ℃下3 500 r/min离心10 min后分离血清,应用ELISA测定血清FSH、黄体生成素(luteinizing hormone,LH)、雌二醇、抗缪勒管激素(anti-Müllerian hormone,AMH)、肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、γ干扰素水平,试剂盒购自武汉明德生物科技股份有限公司(批号分别为201228、170503、190522、191196、180931、171094)。
1.3.4 临床疗效:治疗3个疗程后,评价两组的临床疗效。痊愈为排卵周期恢复正常,其他症状基本消失,且疗效指数[疗效指数=(治疗前中医证候总积分-治疗后中医证候总积分)/治疗前中医证候总积分×100%]≥95%;显效为排卵周期显著缩短,停药后能维持≥3个月,其他症状明显减轻,70%≤疗效指数<95%;有效为排卵周期有所缩短,但停药后维持时间<3个月,其他症状减轻,30%≤疗效指数<70%;无效为排卵周期未见缩短,其他症状无改善,且疗效指数<30%[8]。总有效率=(痊愈+显效+有效)例数/总例数×100%。
1.3.5 不良反应发生情况:3个疗程治疗结束后,统计两组治疗期间不良反应的发生情况,包括头痛、胃肠道反应、肝功能异常及乳房胀痛等。
1.4 统计学分析 采用SPSS 22.0软件进行统计学分析。计量资料以(x±s)表示,组间比较采用两独立样本t检验,组内比较采用配对t检验;计数资料以例数(百分比)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 治疗前后两组患者中医证候积分的比较 治疗前,两组患者的各中医证候积分及总积分差异无统计学意义(P>0.05)。治疗后,两组患者的各中医证候积分及总积分较治疗前降低,且观察组的上述积分低于对照组(P<0.05),见表1。
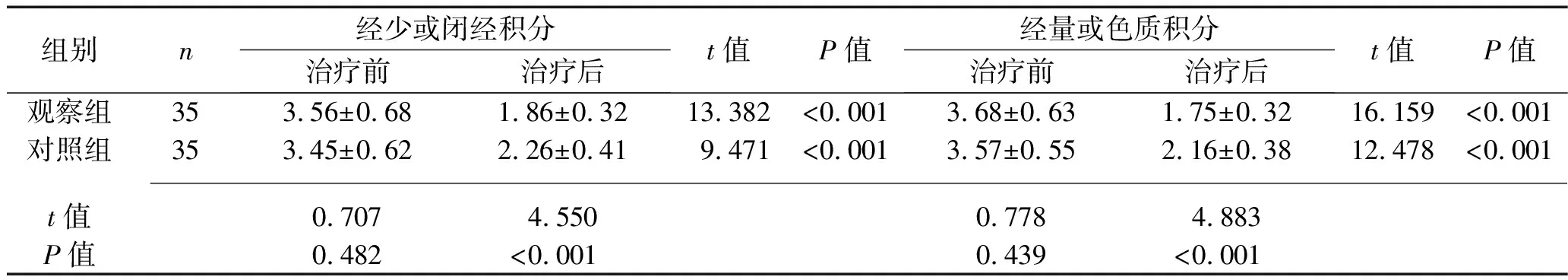
表1 治疗前后两组患者中医证候积分的比较(x±s,分)
2.2 治疗前后两组患者卵巢功能和子宫内膜厚度的比较 治疗前,两组患者的卵巢体积、窦卵泡数、子宫内膜厚度及排卵周期差异无统计学意义(P>0.05);治疗后,两组患者的卵巢体积、窦卵泡数和子宫内膜厚度较治疗前增加,排卵周期较治疗前缩短,且观察组上述指标优于对照组(P<0.05),见表2。

表2 治疗前后两组患者卵巢功能和子宫内膜厚度的比较(x±s)
2.3 治疗前后两组患者血清性激素和AMH水平的比较 治疗前,两组患者血清FSH、LH、雌二醇、AMH水平差异无统计学意义(P>0.05);治疗后,两组患者血清FSH、LH水平较治疗前降低,血清雌二醇、AMH水平较治疗前升高,且观察组上述指标优于对照组(P<0.05),见表3。

表3 治疗前后两组患者血清性激素和AMH水平比较(x±s)
2.4 治疗前后两组患者血清炎症因子水平的比较 治疗前,两组患者血清TNF-α、γ干扰素水平差异无统计学意义(P>0.05);治疗后,两组患者血清TNF-α、γ干扰素水平较治疗前降低,且观察组上述指标低于对照组(P<0.05),见表4。
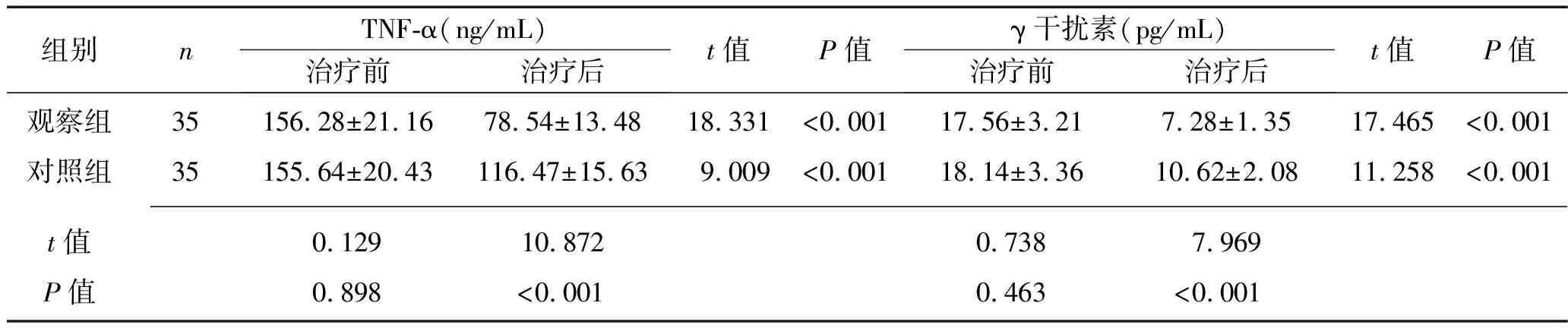
表4 治疗前后两组患者血清炎症因子水平的比较(x±s)
2.5 两组患者临床疗效的比较 观察组的总有效率高于对照组(χ2=6.437,P=0.023),见表5。
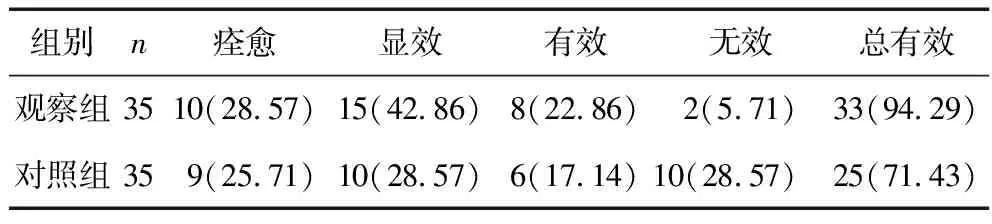
表5 两组患者临床疗效的比较[n(%)]
2.6 两组患者治疗期间不良反应发生率的比较 观察组治疗期间出现胃肠道反应2例,肝功能异常1例,其不良反应发生率为8.57%(3/35);对照组治疗期间出现胃肠道反应1例,头痛1例,乳房胀痛2例,其不良反应发生率为11.43%(4/35)。两组患者治疗期间不良反应发生率差异无统计学意义(χ2=0.159,P=0.690)。
3 讨 论
POI是一种慢性内分泌紊乱性疾病,其病因可能与遗传、自身免疫、环境及病毒感染等因素有关,若未及时治疗,可导致女性闭经或不孕[9]。近年来,随着现代社会生活节奏的加快,女性承受来自工作和生活的压力越来越大,促使POI的发病率不断升高,且发病人群趋于年轻化,严重影响女性生殖健康[10]。目前西医治疗POI主要采用口服药物治疗,包括戊酸雌二醇、黄体酮等激素类药物,这些药物虽短期疗效显著,但长期应用会增加卵巢癌、血栓形成及肝功能损害等的发生风险,临床应用受限[11]。因此,探寻一种安全有效的POI治疗方法是临床亟须解决的难题。
中医学认为,POI以肾虚为病理基础,以肝郁、脾虚、痰湿为病机,该病多因妇女肾气虚久导致精血亏虚,肾精衰竭、冲任虚衰则胞宫失于濡养,加之女子性忧郁,肾虚伤肝,肝郁耗阴、肝血不足导致损伤阴津,使经血乏源,冲任乏养,致经血变少甚至闭经,故治疗原则应以疏肝解郁、活血化瘀、祛痰化湿为主[12]。本研究应用自拟抗早衰汤联合针刺治疗肝郁肾虚型POI患者。配方中的菟丝子可益髓固精、调经助卵,女贞子、枸杞子可补益肝肾,熟地可平补肝血、滋肾填精,山茱萸、杜仲能补益肝肾、收涩固脱,山药可生津健脾、补肾固精,当归补血通经、调理冲任,联合白芍共获养血平肝、缓中止痛之效,香附、川芎可行气开郁、行气活血,路路通能活络通经,茯苓可燥湿利水,柴胡能调达肝郁,路路通、茯苓、柴胡三者合用增强疏肝行气解郁之功,甘草可补虚调和诸药,全方共奏补肾活血、疏肝解郁及调经止痛之功[13-14]。针刺穴位选用百会穴、本神穴、神庭穴,发挥益气安神、定志之效,配合太冲穴,可疏肝解郁;肾俞穴、三阴交穴、太溪穴有调肝补气、培元固肾之功;关元穴、子宫穴、大赫穴可调理冲任、补气益精血;中脘穴、天枢穴、足三里穴有生化气血、调经理气之功;次髎穴补益下焦、活血调经、畅通气机。诸穴合用共奏疏通经脉、补益肝肾及通调气血之效[15-16]。本研究结果显示,治疗后两组患者的中医证候积分较治疗前降低,卵巢体积、窦卵泡数、子宫内膜厚度和排卵周期较治疗前改善,且观察组上述指标优于对照组,治疗总有效率高于对照组(P<0.05),提示采用自拟抗早衰汤联合针刺和雌孕激素序贯疗法治疗肝郁肾虚型POI患者均有一定效果,且自拟抗早衰汤联合针刺方案的治疗效果更优,能更有效地改善患者中医证候和围绝经期症状,增加子宫内膜厚度,改善卵巢功能,原因可能是自拟抗早衰汤联合针刺治疗可协同发挥疏肝、补肾、调和气血的作用,促进卵巢储备功能恢复,增强治疗效果。
FSH、LH、AMH是评估卵巢储备功能的重要血清学指标。其中,FSH、LH具有促进卵泡生长发育、雌激素分泌及排卵等作用,二者表达水平及比值变化可反映卵巢功能情况;AMH通过抑制LH受体及黄体酮的合成途径来延缓颗粒细胞的凋亡进度,发挥调节卵子发育过程的作用,且与窦卵泡数量呈正相关[17-18]。雌二醇可促进女性性器官及第二性征发育,影响排卵和卵泡的发育,调节体内激素分泌水平,雌激素缺乏可导致卵巢排卵能力下降。研究显示,TNF-α、γ干扰素的表达上调可诱导黄体细胞抗原表达,破坏卵泡与颗粒细胞,导致卵巢储备功能异常,从而抑制排卵[19]。本研究结果显示,治疗后两组患者血清雌二醇、AMH水平较治疗前升高,FSH、LH、TNF-α、γ干扰素水平较治疗前降低,且观察组上述指标优于对照组(P<0.05),提示采用自拟抗早衰汤联合针刺治疗肝郁肾虚型POI,能调节患者机体内激素水平,改善卵巢功能,抑制炎症反应。现代药理学表明,菟丝子、山茱萸可调节激素的合成与分泌,加速卵泡发育成熟,增加子宫内膜蛋白和脂类含量,改善卵巢储备功能和子宫内膜厚度[20-21];白芍苷能促进造血干细胞增殖,增强骨髓造血能力,还具有调节免疫功能、抑制炎症反应的作用[22]。现代解剖学研究显示,多种穴位与其对应部位受相同神经节段支配,针刺穴位能有效地刺激交感神经和调节神经内分泌系统,从而改善生殖功能障碍[23]。针刺天枢穴可改善卵巢血液循环,同时调节颗粒细胞的新陈代谢,从而改善卵巢功能[24];针刺次髎穴可通过促进中枢内啡肽的产生和分泌,来调节下丘脑-垂体-性腺轴的功能,从而下调血清FSH、LH水平[25]。此外,两组患者治疗期间不良反应发生率差异无统计学意义(P>0.05),提示采用自拟抗早衰汤联合针刺治疗肝郁肾虚型POI患者是安全的。
综上所述,自拟抗早衰汤联合针刺治疗肝郁肾虚型POI患者疗效确切,能改善临床症状,增加子宫内膜厚度,提高卵巢功能,调节性激素水平,抑制炎症反应,效果优于雌孕激素序贯治疗,且具有较好的安全性。

