基于FAERS 数据库的周期蛋白依赖性激酶4/6 抑制剂相关颌骨坏死不良事件信号挖掘与重构*
郎晓琴,枉 前,刘 通
(1. 中国人民解放军陆军军医大学第一附属医院,重庆 400038; 2. 中国人民解放军陆军第九五八医院,重庆 400020)
周期蛋白依赖性激酶(CDK)4/6 抑制剂可通过抑制激酶活性,阻断细胞周期从G1期到S 期的进展,进而阻碍癌细胞生长[1]。目前,经美国食品和药物管理局(FDA)批准的3种CDK4/6抑制剂包括哌柏西利(2015年)、瑞博西利(2017年)、阿贝西利(2018年)。一系列高质量循证医学证据表明,CDK4/6抑制剂联合内分泌治疗能显著延长晚期乳腺癌患者无进展生存期,以及激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)晚期乳腺癌患者的总生存期[2-3],但部分患者使用哌柏西利、阿贝西利后出现颌骨坏死(ONJ)[4]。ONJ 不仅加大了乳腺癌的治疗难度,影响治疗进程,还会引起严重的疼痛,降低患者的生活质量[5]。由于ONJ的罕见性,以及受限于临床试验的纳入与排除标准、有限的病例数量及随访时间,对评估CKD4/ 6 抑制剂与ONJ 的相关性造成一定困扰。本研究中基于美国食品和药物管理局不良事件报告系统(FAERS),通过OpenVigil 2.1 药物警戒分析工具中比例失衡分析方法评价3 种CDK4/ 6抑制剂与ONJ 的关联性,并利用布尔代数函数去除混杂因素(并用药品)后,进一步评估该信号作为假阳性的可能,为CDK4/ 6 抑制剂上市后的安全评估提供客观证据。现报道如下。
1 资料与方法
1.1 数据收集与处理
本研究中使用OpenVigil 2.1 药物警戒分析工具[6]的比例失衡分析法中报告比值比(ROR)法、比例报告比(PRR)法,挖掘FAERS数据库中2004年1月至2022年9 月的CDK4/ 6 抑制剂与ONJ 的关联性信号。以3 种CDK4/6抑制剂哌柏西利、瑞博西利和阿贝西利作为药物检索词;根据国际医学词典(MedDRA)24.0版的首选术语(PT),以“Osteonecrosis of jaw”作为不良事件检索词,提取“Raw_data”中患者的基本信息,包括“ISR”“Case_ID”“Drug name”“Event”“Outcome”“Indication”“Gender”“Reporter country”“Age_in_Report”“Role_Code”“Date received”。提取“Raw_data”数据后,根据FDA推荐的方法进行去重处理,若具有相同的“Case_ID”则选择最新的“FDA_DT”;“Case_ID”“FDA_DT”相同时,选择较大的“ISR”[7];提取“Frequentist_methods”中“PRR”“Chi_squared”“ROR”“ROR_lower_bound”“ROR_upper_bound”。
1.2 信号重构
针对1.1 项下筛选的CDK4/ 6 抑制剂与ONJ 阳性信号,使用OpenVigil 2.1 药物警戒分析工具中的药物组合检索功能,利用布尔代数函数(AND,OR,NOT)[8],将3种CDK4/6抑制剂哌柏西利、瑞博西利和阿贝西利与伴随药物中可能导致ONJ的7种双膦酸盐类药物(唑来膦酸盐、唑来膦酸、帕米膦酸盐、阿仑膦酸盐、阿仑膦酸、伊班膦酸盐、利塞膦酸盐)[9]及地诺单抗组成不同的组合,分别提取不同药物组合与ONJ 关联性信号进行信号重构,以确定消除合并用药混杂因素后CDK4/ 6抑制剂与ONJ 的关联性信号强度。与ONJ 相关不良事件的药物组合:1)CDK4/6抑制剂去除含有地诺单抗后报告;2)CDK4/ 6 抑制剂去除含有7 种双膦酸盐后报告;3)CDK4/6 抑制剂去除含有7 种双膦酸盐和地诺单抗后报告;4)7种双膦酸盐与ONJ相关报告;5)7种双膦酸盐去除含有CDK4/ 6 抑制剂后报告;6)地诺单抗与ONJ相关报告;7)地诺单抗去除含有CDK4/6抑制剂后报告。
1.3 数据统计与分析
ROR 及PRR 计算方法均基于比例失衡测量法四格表[10-11],计算公式与判断标准见表1。其中,95%CI为95%置信区间,N为同时出现的次数。ROR 和PRR 中两项检测结果均为阳性时,判定为可疑不良事件信号。ROR 和PRR 值越大,信号关联度越高[10-11]。采用Graphpad Prism 9.4.1 软件绘制CDK 4/ 6 抑制剂及去除含有伴随药物报告后与ONJ的关联性信号。

表1 CDK4/6抑制剂与ONJ关联性评估的计算公式与判断标准Tab.1 Formulas and judgement criteria for association assessment of CDK4/6 inhibitor with ONJ
2 结果
2.1 CDK4/6 抑制剂相关ONJ 临床特征与关联性分析
2.1.1 临床特征
FAERS 数据库共筛选出ONJ 相关报告12 645 份,其中地诺单抗5 409 份,7 种双膦酸盐类药物6 748 份,CDK4/ 6 抑制剂225 份,其他药物263 份。2015 年哌柏西利批准用于临床,2015 年至2022 年CDK4/6 抑制剂相关ONJ 的年报告数分别为1,9,23,23,29,15,57,68份,呈逐年上升趋势。CDK4/6 抑制剂导致ONJ 的药物主要为哌柏西利(70.67%),其次为瑞博西利(24.00%)、阿贝西利(5.33%)。255 例患者中女性居多(90.22%);年龄大于70 岁占比较高(25.33%),平均(66.21±9.73)岁,中位年龄为69.50(41~89)岁;适应证主要为乳腺肿瘤(70.67%);死亡4例,危及生命1例,致残2例,住院48例。详见表2。

表2 CDK4/6抑制剂相关ONJ不良事件报告的临床特征(n=225)Tab.2 Characteristics of CDK4/6 inhibitor-associated ONJ adverse event reports(n=225)
2.1.2 CDK4/6 抑制剂与ONJ 关联性分析
在关联性分析中,哌柏西利[ROR= 2.47,95%CI(2.11,2.89);PRR= 2.46,χ2= 135.24]和瑞博西利[ROR= 3.80,95%CI(2.90,4.96);PRR= 3.78,χ2=107.48]与ONJ 均存在显著相关性;阿贝西利[ROR=1.63,95%CI(0.93,2.88);PRR= 1.63,χ2= 2.35]未检测到阳性信号。详见图1 和表3。

图1 哌柏西利、瑞博西利相关ONJ去除含有地诺单抗和双膦酸盐报告前后信号分析森林图Note:* refers to the positive signals(for Fig.1 and Tab.3 - 4).Fig.1 Forest plot of piperacillin and reboxetine-associated ONJ before and after removal of denosumab and bisphosphonates
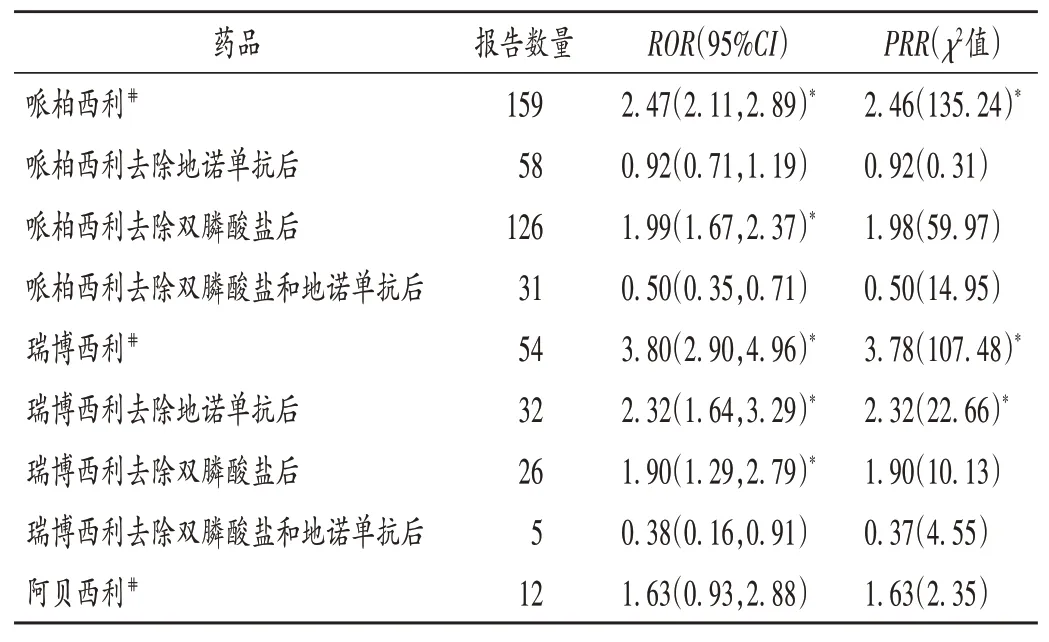
表3 CDK4/6抑制剂相关ONJ去除含有地诺单抗和双膦酸盐报告前后信号强度Tab.3 Signal intensity of CDK4/6 inhibitors-associated ONJ adverse event reports before and after the removal of denosumab and bisphosphonates
2.2 信号重构
2.2.1 哌柏西利
去除含有双膦酸盐和地诺单抗报告后,哌柏西利与ONJ 相关报告数量由159 例降至31 例。哌柏西利与ONJ相关报告中,去除含有双膦酸盐报告后与ONJ相关的PRR 关联信号由阳性转为阴性(PRR= 1.98,χ2=59.97);去除含有地诺单抗报告后,与ONJ 相关的ROR及RPP 信号均由阳性转为阴性[ROR= 0.92,95%CI(0.71,1.19);PRR=0.92,χ2=0.31];去除含有双膦酸盐和地诺单抗报告后,与ONJ 相关的ROR 及RPP 信号强度进一步降至检测阈值以下[ROR= 0.50,95%CI(0.35,0.71);PRR= 0.50,χ2= 14.95]。详见图1和表3。
2.2.2 瑞博西利
去除含有双膦酸盐和地诺单抗报告后,瑞博西利与ONJ相关报告数量由54例降至5例。瑞博西利与ONJ相关报告中,去除含有地诺单抗报告后信号强度仍高于检测阈值[ROR= 2.32,95%CI(1.64,3.29);PRR=2.32,χ2=22.66];去除含有双膦酸盐报告后,与ONJ相关的ROR 关联信号仍高于检测阈值,但PRR 关联信号由阳性转为阴性[ROR= 1.90,95%CI(1.29,2.79);PRR= 1.90,χ2= 10.13];去除含有双膦酸盐和地诺单抗后,与ONJ 相关的ROR 及PRR 信号强度均低于检测阈值[ROR= 0.38,95%CI(0.16,0.91);PRR= 0.37,χ2=4.55]。详见图1和表3。
2.3 伴随药物双膦酸盐与地诺单抗
地诺单抗[ROR= 65.79,95%CI(63.49,68.18);PRR=62.95,χ2=188 891.53]和双膦酸盐[ROR=99.73,95%CI(96.26,103.33);PRR=94.43,χ2=291 223.16]与ONJ 均具有显著关联性。去除含有CDK4/ 6 抑制剂报告后,双膦酸盐及地诺单抗与ONJ 关联性信号均无显著变化。详见表4。
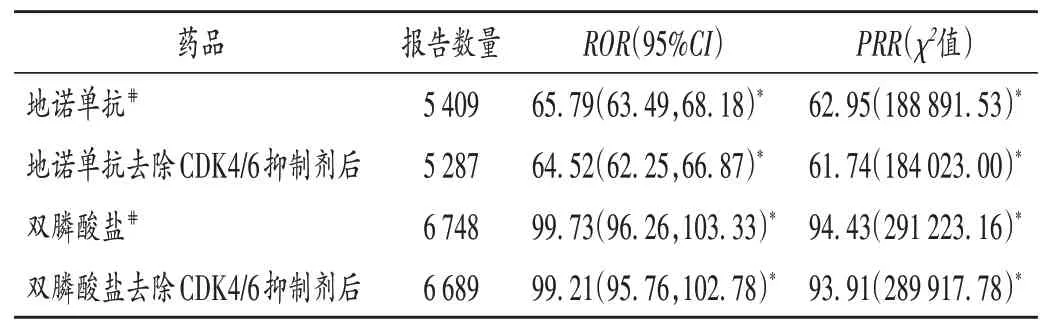
表4 地诺单抗及双膦酸盐去除含有CDK4/6抑制剂报告前后与ONJ的信号强度Tab.4 Signal intensity of denosumab and bisphosphonates with ONJ before and after removal of CDK4/6 inhibitors
3 讨论
有研究显示,2.09%的乳腺癌患者发生药物相关ONJ,队列研究中药物相关ONJ患者中近50%患有乳腺癌[7]。FDA批准CDK4/6抑制剂为晚期乳腺癌的一线及二线治疗药物[12],临床试验中30%使用哌柏西利、15%使用阿贝西利、12%使用瑞博西利治疗的患者发生口腔炎[13-14]。一项回顾性研究报道,5 例使用哌柏西利及1 例使用阿贝西利治疗的患者出现ONJ,推测ONJ 的发生可能与CDK4/ 6 抑制剂引发口腔及黏膜炎,导致口腔黏膜层破裂和底层骨暴露于细菌有关[4,15-16]。
本研究中初步信号检测结果显示,CDK4/6抑制剂中除阿贝西利外,哌柏西利及瑞博西利均显示与ONJ相关的阳性信号。根据FAERS 数据库中CDK4/ 6 抑制剂相关ONJ不良事件报告信息,CDK4/6抑制剂主要用于乳腺肿瘤(70.67%)的治疗,常见的伴随药物中双膦酸盐和地诺单抗有更高引起ONJ的倾向[5]。去除含有双膦酸盐和地诺单抗报告后,哌柏西利及瑞博西利与ONJ相关的信号强度均降低至ROR 和PRR 检测阈值以下,而双膦酸盐和地诺单抗在去除含有CDK4/6 抑制剂报告后信号强度并无明显变化。可见,联用药物双膦酸盐和地诺单抗增强了CDK4/6 抑制剂与ONJ 的关联性信号,从而导致假阳性信号的产生。
有研究表明,对于大多数药物,假阳性信号的比例可能高达50%[17],如氯卡色林与体质量增加的PRR为5.47,高于检测阈值,表明药物与不良事件有显著关联性,但结果表明该信号为假阳性[17]。对于假阳性信号的产生,除了FAERS 数据库本身的局限性,如漏报、报告不精确、数据缺失等情况外[8],另一主要原因是数据挖掘方法如ROR、PRR、贝叶斯法等评价标准仅基于检测阈值,无法回避混杂因素如并用药物、年龄、性别、适应证等因素的影响[7]。本研究中基于FAERS 数据库,使用OpenVigil 2.1 药物警戒分析工具中的药物组合检索功能,利用布尔代数函数(AND,OR,NOT),去除本研究中混杂因素并用药物的影响。
研究发现,年龄增长、女性、共病因素(贫血、自身免疫性疾病和糖尿病)、口腔卫生不良、药物(如双膦酸盐、地诺单抗、类固醇类药物)等是引发药物相关ONJ的危险因素[5,18]。本研究中,CDK4/ 6 抑制剂相关ONJ患者主要为女性(90.22%);发病中位年龄较高(69.50岁),上述2 项因素可能对CDK4/ 6 抑制剂与ONJ 关联性结果产生影响。研究表明,1.3%使用双膦酸盐及1.1%使用地诺单抗治疗患者发生ONJ[19]。接受唑来膦酸钠治疗发生ONJ 的风险为接受安慰剂治疗癌症患者的50~100 倍[4,18]。双膦酸盐可通过抑制法尼基焦磷酸合酶,破坏破骨细胞介导的骨吸收来降低破骨细胞的活性,加速细胞凋亡而减少破骨细胞数量。此外,双膦酸盐还可直接抑制内皮细胞血管生成,以上共同介导了ONJ的发生[20-21];地诺单抗可抑制核因子-κB受体活化因子配体(RANKL)与核因子-κB 受体活化因子(RANK)受体的结合,抑制破骨细胞的功能从而抑制骨吸收,破坏骨重塑,进而引发ONJ[19]。本研究中,双膦酸盐与地诺单抗均显示出与ONJ 显著的关联性信号,在去除含有CDK4/6 抑制剂的报告后,信号强度均无显著变化。而CDK4/6 抑制剂目前仍缺乏明确的作用机制来解释与ONJ的关联性。虽在FAERS 数据库中哌柏西利、瑞博西利与ONJ 初步关联性信号高于检测阈值,但在去除含有双膦酸盐和地诺单抗的报告后,关联性信号均显著降低至检测阈值以下。故认为FAERS 数据库中CDK4/6 抑制剂与ONJ 相关的阳性信号不排除为假阳性的可能。
本研究中基于FAERS 数据库,故受到数据库本身局限性的影响。首先,数据库由各种职业人员自发呈报,可能存在漏报,以及不完整、不准确和不精确的报告[8,22-23];其次,目前数据挖掘方法(如ROR、PRR、贝叶斯法等)的判断标准仅基于检测阈值,无法排除混杂因素如并用药物、年龄、性别、适应证等因素的影响。利用比例失衡分析法评价CDK4/6 抑制剂与ONJ 的关联性,并利用布尔代数函数去除本研究中主要混杂因素(伴随药物)的影响,对关联性信号进行重构,进一步分析CDK4/6 抑制剂与ONJ 关联性信号作为假阳性的可能性,此类分析方法为今后的药物警戒相关研究提供了新方向。基于FAERS 数据库的药物警戒研究有助于识别药物上市后新的、罕见及潜伏时间长的不良反应,为补充药物安全信息提供客观证据。
综上所述,FAERS 数据库中CDK4/ 6 抑制剂相关的ONJ 信号不排除为假阳性可能,故在FAERS 数据库中进行药物相关不良事件数据挖掘时,需重视混杂因素(如并用药物)的影响,同时结合临床研究及医药相关知识综合分析,以减少药物假阳性信号的产生。

