UPLC-MS/MS 快速测定血液中布桂嗪
高章明,石景瑜,曾皓,张学军
1.上饶市公安局物证鉴定中心,江西 上饶 334000;2.上饶市广信区人民医院药剂科,江西 上饶 334100;3.江西省公安厅毒品检验鉴定中心,江西 南昌 330000
布桂嗪又名强痛定、AP-237,化学名称为1-正丁酰基-4-肉桂基哌嗪,英文名bucinnazine,属于国家管制的麻醉药品。1968 年,日本杏林制药员工ITO 等首次报道了布桂嗪的合成[1]。布桂嗪是一种速效、强效的镇痛药,属于阿片类镇痛药物,镇痛作用是吗啡的1/3、氨基比林的4~20 倍[2],主要对皮肤、黏膜、运动器官(包括关节、肌肉、肌腱等)的疼痛有明显的抑制作用,是目前我国治疗癌症以及相关慢性疼痛的首选镇痛药,在临床上适用于偏头痛、三叉神经痛、癌性疼痛等。布桂嗪连续超剂量使用可致耐受和成瘾,容易引起滥用,过量则可导致中毒死亡。目前,在欧美已出现布桂嗪作为新型毒品滥用的势头[3],在国内也有使用布桂嗪成瘾的案例报道[4-6],因此,建立高效、准确的布桂嗪检测方法对日常涉毒案件的侦破和临床治疗都具有十分重要的意义。
对血液中布桂嗪的检验,常见的前处理方式主要有液液萃取(liquid-liquid extraction)、固相萃取(solid phase extraction,SPE)、基质固相分散(matrix solid phase dispersion,MSPD)萃取等[7-8]。其中,液液萃取方法需要手动操作,过程繁琐,耗时长,目标物回收率偏低且需要消耗大量有机溶剂,容易对环境造成污染;SPE 和MSPD 萃取方法的检验成本较高,方法开发较为复杂。布桂嗪常见的分析方法有GC、GC-MS和高效液相色谱法(high performance liquid chromatography,HPLC)等[7-10]。GC 和HPLC 易受样品中复杂基质的干扰,导致定性不准确。GC-MS方法灵敏度较低,容易漏检。面对布桂嗪滥用案件的逐渐增加,亟须建立一种检验效率高、成本低、专属性强的方法。本研究拟通过优化的沉淀蛋白法,并结合超高效液相色谱-串联质谱法(ultra-high performance liquid chromatographytandem mass spectrometry,UPLC-MS/MS)特异性强、分析时间短、灵敏度高、重现性好等优点,建立血液中布桂嗪的UPLC-MS/MS 快速测定方法,并应用于实际案例,为司法案件提供准确快速的鉴定意见。
1 材料与方法
1.1 主要仪器与试剂
LCMS-8050 三重四极杆液相色谱质谱联用仪(日本岛津公司),配电喷雾离子源(electrospray ionization,ESI);Milli-Q 超纯水系统(美国Millipore 公司);RG-165AT 高速离心机(上海卢湘仪离心机仪器有限公司);DHG-9075A 电热鼓风干燥箱(上海一恒科学仪器有限公司)。
布桂嗪标准品(0.1 mg/mL,美国Cerilliant 公司),吗啡-d3(纯度≥98.0%,美国Sigma 公司),甲醇、乙腈(色谱纯,美国Honeywell 公司),甲酸、乙酸铵(色谱纯,上海安谱实验科技股份有限公司),0.22 µm 混合纤维素酯滤膜[岛津(上海)实验器材有限公司]。
1.2 标准工作溶液的配制
根据实验需要,用甲醇稀释布桂嗪标准品溶液得到质量浓度为1 µg/mL 的标准工作溶液。吗啡-d3用甲醇稀释成质量浓度为1 µg/mL 的内标工作液。将上述标准品溶液密封后置于冰箱中-20 ℃冷冻保存。
1.3 样品前处理
本研究使用沉淀蛋白法对血液样品进行前处理,分别考察乙腈溶液和甲醇溶液的沉淀效果,乙腈溶液的比例为100%乙腈、80%乙腈水溶液、50%乙腈水溶液,甲醇溶液的比例为100%甲醇、80%甲醇水溶液、50%甲醇水溶液。
取空白血液加入布桂嗪标准工作溶液,配制质量浓度为20、50、80 µg/L 的系列血液样品,取100 µL 上述3 种质量浓度的血液样品分别置于2 mL 具塞离心管中,加入1 µg/mL 吗啡-d3内标工作液5 µL,再加入900 µL 上述不同比例的甲醇和乙腈,涡旋混匀1 min后,14 800×g,高速离心5 min,取上清液,过0.22 µm混合纤维素酯滤膜,平行进样 3 次。
1.4 仪器条件
液相色谱条件:Shim-pack GIST C18色谱柱(2.1 mm×100 mm,2 µm;日本岛津公司),柱温40 ℃,流速0.4 mL/min。在流动相的选择方面,本研究考察0.1%甲酸水溶液-甲醇、0.1%甲酸水溶液-乙腈、5 mmol/L乙酸铵水溶液(含0.1%甲酸)-乙腈、5mmol/L乙酸铵水溶液(含0.1%甲酸)-甲醇4 种流动相,使用梯度洗脱。洗脱程序:初始流动相为10%B,0~3.0 min 10%B~28%B,3.0~5.0 min 28%B~100%B,5.0~7.0 min 100%B,7.0~7.01 min 100%B~10%B,7.01~8.0 min 10%B。总采样时间为8.0 min,进样量为5 µL。
质谱条件:在电喷雾正离子模式下进行多反应监测扫描;雾化器流速3 L/min,加热器流速10 L/min;接口温度300 ℃,加热块温度400 ℃;干燥气流速10 L/min。经优化后得到的布桂嗪质谱参数见表1。
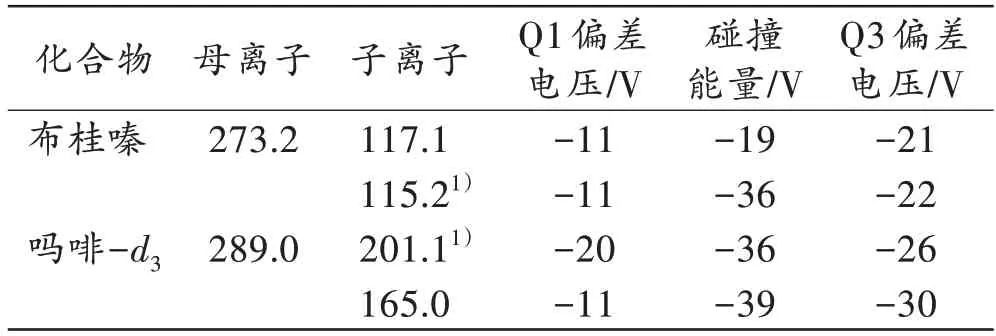
表1 布桂嗪和内标吗啡-d3的质谱参数Tab.1 Mass spectrum parameters of bucinnazine and morphine-d3
1.5 方法学验证
1.5.1 选择性
6 个不同来源的空白血液样品按1.3 节方法处理后进行UPLC-MS/MS 分析,观察血液中内源性物质对布桂嗪和吗啡-d3的检测是否存在干扰。
1.5.2 线性关系、检出限和定量限
取空白血液100 µL于2 mL具塞离心管中,加入布桂嗪标准工作溶液,配制质量浓度为0.1、0.5、1、2、5、10、20、50、100、200 µg/L 的系列血液样品,按1.3 节方法进行前处理后,按1.4 节条件进行分析,使用内标法定量,以质量浓度为横坐标,峰面积为纵坐标,绘制标准曲线。以信噪比(S/N)≥3 时的样品质量浓度为检出限,以信噪比(S/N)≥10 时的样品质量浓度为定量限。
1.5.3 基质效应
基质效应是指样品中除目标物以外的物质对分析结果的影响和干扰,通常表现为使目标物在仪器上的响应发生增强或抑制。用甲醇配制质量浓度为1、10和100 µg/L 的布桂嗪标准工作溶液进行UPLC-MS/MS分析,记录峰面积为S1。6 份不同来源的空白血液样品基质提取液添加相应的布桂嗪标准工作溶液进行UPLC-MS/MS 分析,记录峰面积为S2。以S2与S1的比值评价基质效应。
1.5.4 回收率
取空白血液100 µL 于2 mL 具塞离心管中,加入布桂嗪标准工作溶液,分别配制质量浓度为1、10 和100 µg/L 的布桂嗪血液样品,每个质量浓度6 份样品,按1.3 节方法进行前处理后,按1.4 节条件进行分析,记录峰面积为S3。以S3与S2的比值计算回收率,回收率需满足日常案件检验需要[11]。
1.5.5 准确度和精密度
依据《法医毒物分析方法验证通则》(SF/T 0063—2020)[12]计算准确度、日内精密度和日间精密度,准确度用偏倚(%)表示,日内和日间精密度均用相对标准偏差(relative standard deviation,RSD)表示。
取空白血液100 µL于2 mL具塞离心管中,加入布桂嗪标准工作溶液,分别配制低(1 µg/L)、中(10 µg/L)、高(100 µg/L)3 个质量浓度的血液样品,每个质量浓度6 份样品,按1.3 节方法进行前处理后,按1.4 节条件进行分析,连续测定3 d,计算测定结果的准确度。将上述3 种质量浓度的血液样品于1 d 内分析6 次,得日内精密度;连续测定3 d,得日间精密度。所得结果需满足体内样品分析要求[13]。
1.5.6 稳定性
针对血液样品在不同温度下的保存情况,设计血液中布桂嗪的长期稳定性实验。取空白血液100 µL于2 mL 具塞离心管中,加入布桂嗪标准工作溶液,分别配制低(1 µg/L)、高(100 µg/L)两个质量浓度的血液样品各24 份,分为4 组,每组包含低、高质量浓度血液样品各6 份,分别置于-25、0、25、50 ℃下保存10 d,于第5 天、第10 天各取样3 份,与新配制的低、高质量浓度血液样品同时按1.3 节方法处理后进行测定,所得准确度用偏倚(%)表示,偏倚在±15%以内,表明目标物在一定时间内可以稳定保存[12]。
2 结果与讨论
2.1 前处理条件的选择
实验结果表明,相同比例下,乙腈溶液提取的回收率比甲醇溶液高,在考察的3 种比例乙腈溶液中,80%乙腈水溶液回收率最高,提取效果最好。而使用100%乙腈提取时,涡旋混合后血液不能完全散开,容易凝成小球,影响回收率。最终选择80%乙腈水溶液作为提取溶剂。
2.2 色谱条件的优化
对4 种流动相进行考察,结果发现:选择乙腈为有机相时,布桂嗪的峰形和分离效果比甲醇好。在水相中加入少量乙酸铵,增强流动相极性,缓冲流动相pH 值,可进一步提高目标物的离子化效率。最终选择5 mmol/L 乙酸铵水溶液(含0.1%甲酸)-乙腈为流动相用于布桂嗪的分析,分析结果显示:布桂嗪峰形稳定,没有出现拖尾峰或前沿峰。布桂嗪和内标吗啡-d3的总离子流色谱图见图1。

图1 布桂嗪和吗啡-d3的总离子流色谱图Fig.1 Total ion chromatograms of bucinnazine and morphine-d3
2.3 方法学验证
2.3.1 选择性
实验结果表明,6 个不同来源血液样品中的内源性物质对布桂嗪和吗啡-d3无干扰,该方法选择性良好。
2.3.2 线性关系、检出限和定量限
布桂嗪在0.5~200 µg/L 范围内线性关系良好。血液样品加标后所得线性方程为y=0.023x+0.025,相关系数(r)为0.999 7,检出限为0.1 µg/L,定量限为0.5 µg/L。
2.3.3 基质效应
布桂嗪在血液中的基质效应为69.4%~73.8%(表2),血液中的基质对目标物有抑制作用,基质效应较为明显,所以本方法选择使用内标吗啡-d3来减少基质效应带来的影响。

表2 布桂嗪在血液中的基质效应、回收率、准确度和精密度Tab.2 Matrix effect,recovery,accuracy and precision of bucinnazine in blood (%)
2.3.4 回收率
血液中布桂嗪在3 个添加质量浓度(1、10、100 µg/L)的回收率见表2,回收率在78.3%~83.8%。
2.3.5 准确度和精密度
研究结果(表2)表明,本方法的准确度在3.1%~3.5%,日内精密度在1.9%~2.8%,日间精密度在2.8%~3.2%,日内和日间精密度均小于5%。
2.3.6 稳定性
研究结果(表3)表明,低质量浓度血液样品的稳定性低于高质量浓度血液样品。血液中布桂嗪在-25 ℃下保存时,低质量浓度血液样品的准确度(偏倚)在±4.5%范围内,高质量浓度血液样品的准确度(偏倚)在±3.0%范围内,稳定性均较好。在0 ℃下保存时,血液样品的准确度(偏倚)均在±8.6%范围内,较为稳定。在25 ℃和50 ℃下保存10 d 后,高质量浓度血液样品的准确度(偏倚)分别为±24.7%和±49.9%,均大于±15%。由此可见,在常温和高温下目标物不能长时间稳定保存,存储温度的升高会加速血液中布桂嗪的分解,所以对于血液样品的保存,建议短期冷藏、长期冷冻。

表3 布桂嗪在血液中的准确度(偏倚)Tab.3 Accuracy(bias)of bucinnazine in blood(n=3,%)
2.4 案例应用
某年12 月,一男子被发现死于家中,现场提取了死者的血液送检,由于受到设备的限制,仅在死者血液中检出芬太尼和利多卡因成分。4 年后,实验室将当年的血液再次解冻,使用本研究方法在血液中检出了芬太尼、利多卡因和布桂嗪成分(图2),其中布桂嗪质量浓度为22.8 µg/L、芬太尼质量浓度为40.2 µg/L、利多卡因质量浓度为88.9 µg/L。

图2 实际样品的多反应监测色谱图Fig.2 Multiple reaction monitoring chromatogram of practical sample
布桂嗪成人的用量为1次30~60 mg口服(每日3次)或者1 次50 mg 皮下或肌内注射(每日1~2 次),对于慢性中重度癌性疼痛患者,剂量可逐渐增加且第一次及总量可以不受常规剂量的限制[14],所以会造成布桂嗪在血液中的治疗浓度范围较大。YU 等[15]的研究结果显示,大鼠布桂嗪的亚致死量为1.0 g/kg;FOGARTY等[16]报道的4 例患者死后血液中布桂嗪的质量浓度范围为820~5 800 µg/L。本例死者血液中布桂嗪含量远未达到文献所报道的质量浓度,分析有以下两个原因:(1)死者生前存在多种药物滥用,有可能是多种药物间的协同作用导致死亡;(2)从药物稳定性方面分析,虽然检材长期在-25 ℃下保存,但存储时间过长,布桂嗪在血液中缓慢分解,导致测定的含量偏低。
3 结论
本研究通过优化前处理中的乙腈沉淀蛋白法与UPLC-MS/MS 条件,针对血液中的布桂嗪进行快速定性定量分析,具有取样量小、前处理过程简单高效、重现性好、仪器分析灵敏度高等优势,该方法的定量限可达0.5 µg/L,且检材在-25 ℃下冷冻保存可保证布桂嗪在血液中的稳定性。本方法在司法鉴定领域针对布桂嗪滥用的快速定性定量以及临床药物浓度监测方面有较高的应用价值。

