内镜下经椎板间入路腰椎减压融合术治疗腰椎滑脱症
李承蔚 李智斐 钟远鸣 黄保华 莫 怡 梁渊耀 蒙纪文 梁钦秋 杨 尹
内镜下经椎板间入路腰椎减压融合术治疗腰椎滑脱症
李承蔚1李智斐2钟远鸣2黄保华2莫 怡2梁渊耀1蒙纪文1梁钦秋1杨 尹1
(1.广西中医药大学,广西 南宁 530001;2.广西中医药大学第一附属医院,广西 南宁 530000)
目的:探讨内镜下经椎板间入路腰椎减压融合术治疗腰椎滑脱症的临床疗效。方法:采用全内镜下经椎板间入路腰椎减压融合术治疗25例单节段腰椎轻度滑脱的患者。记录手术操作过程、术后并发症等情况,术后1、3、6个月随访时记录腰痛及腿痛VAS评分、椎间隙高度以ODI指数,术后6个月记录椎体滑脱率、滑脱角、JOA评分,对比术前指标以评估疗效。结果:手术时间61~122 min,术中透视5~11次,术中出血量为52~110 mL,术后引流量64~116 mL,术后切口愈合良好,未出现明显感染,术后未出现严重并发症。术后1个月、3个月、末次随访(即术后6个月随访)时的腰痛、腿痛VAS评分均低于术前(<0.05)。末次随访时所测得的椎体滑脱率、滑脱角以及JOA评分均优于治疗前,各个时间点测得指标同术前指标差异均有统计学意义(<0.05)。结论:内镜下经椎板间入路腰椎融合术能在较安全的基础上实现充分的神经根减压、椎体间融合,显著改善患者腰椎滑脱所导致的腰腿痛症状及功能障碍,手术疗效较好。
腰椎滑脱症;内窥镜;经椎板间入路;腰椎减压融合术
引言
腰椎滑脱症(Lumbar spondylolisthesis,LS)是引起人们腰腿疼痛的主要腰部疾患之一,临床上多以轻度滑脱(Meyerding分级为Ⅰ度或Ⅱ度)为主。传统的开放式腰椎椎间融合手术被视为治疗各种退行性腰椎疾病的标准手术[1],而腰椎滑脱作为退行性腰椎疾病的主要组成部分,传统手术的治疗方式包括后路神经根减压、融合器植入、椎弓根螺钉内固定,由于腰椎滑脱常合并椎管狭窄、腰椎间盘突出等症,以上几种术式常结合使用,通过神经根减压、螺钉固定来恢复椎间盘和椎间孔高度,同时通过融合责任节段的椎间隙来重建腰椎节段的稳定性。但由于该术式为开放式手术,术中需要剥离较多腰部肌肉,存在着术中出血量较大、术后引流量多、住院时间长、感染风险偏大等诸多缺点,对老年患者及合并内科疾病的患者存在较大的创伤[2]。椎旁肌是支持脊柱伸展、维持腰椎前凸和实现脊柱动态稳定的关键[3],因此,不能忽视术中长时间的肌肉牵拉、剥离和肌腱附着剥离所造成的严重椎旁医源性损伤的风险[4]。近年来,全内镜下手术已被广泛应用于临床,从内镜系统、入路方向到融合器的选择都得到了长足的发展[5]。本研究纳入2018年6月至2021年6月在广西中医药大学第一附属医院脊柱骨伤科住院治疗,采用全内镜下经椎板间入路腰椎减压融合术治疗轻度腰椎滑脱患者25例,探讨该技术的短期临床应用及疗效。
1 资料与方法
1.1 一般资料
单中心回顾性分析2018年6月至2021年6月在广西中医药大学第一附属医院脊柱骨伤科行全内镜下经椎板间入路腰椎减压融合术治疗的轻度腰椎滑脱症患者的临床资料,共25例患者符合上述标准,纳入本研究中。详细资料:男性患者为15例,女性患者为10例,年龄45~61岁,所有病例均为腰椎前滑脱。术前完善腰椎DR正侧位、腰椎DR功能位(过伸过屈位)片以及腰椎CT及腰椎MRI提示滑脱节段:L4/5节段19例,L3/4节段6例。滑脱程度:18例为Ⅰ度滑脱,7例为Ⅱ度滑脱。伴随症状:所有患者均存在腰痛、单侧神经根性症状;23例患者有腰椎间盘突出症病史,其中16例患者存在间歇性跛行症状,影像学提示腰椎椎管狭窄。所有患者的腰椎滑脱病史在1.0~6.5年之间。
1.2 纳入标准与排除标准
纳入标准:(1)2018年6月至2021年6月在本院行全内镜下经椎板间入路腰椎减压融合术治疗的腰椎滑脱症患者;(2)有下腰部疼痛伴单侧根性症状;(3)Meyerding分级Ⅰ度或Ⅱ度腰椎滑脱患者。
排除标准:(1)合并重度骨质疏松症的患者;(2)严重的中央型椎管狭窄患者;(3)存在凝血障碍或严重内科疾病的患者;(4)合并脊柱感染、骨折、肿瘤的患者;(5)Meyerding分级Ⅲ度及以上的腰椎滑脱症;(6)依从性差的患者。
1.3 手术方法
(1)患者取俯卧位,手术采用全身麻醉,麻醉成功后,以L4/5节段为例,用脊柱专用定位板及C臂机透视定位并标记双侧L4、L5椎弓根及L4/5椎间隙。消毒铺巾,在C臂引导下将经皮螺钉穿刺植入于L4、L5双侧椎弓根,穿刺时注意在C臂透视下将L5双侧椎弓根螺钉方向平行L5椎体上终板或者稍微向头端倾斜,切忌向尾端倾斜;穿刺成功后植入导丝并留置。(2)将L5左侧椎弓根穿刺针孔向内扩大至一长约1.2 cm的横行切口,穿刺“铅笔头”沿切口传入至L4椎板下缘,逐级扩张,运用扩张器上下内外钝性剥离左侧L4椎板下1/2、L4/5椎板间隙及L5椎板上缘,植入通道。使用镜外环锯锯除左侧L4椎板下1/2及L4下关节突,用镜下椎板咬骨钳将L4/5左侧椎板间隙的黄韧带及L5椎板上缘、上关节突咬除,使硬膜及神经根暴露。(3)运用通道将神经根向内牵拉后,应用髓核咬钳咬出脱出髓核组织,运用镜下铰刀及刮勺刮除残余髓核及终板组织,放置通道下植骨漏斗进行椎间隙植骨。镜下放置自制神经剥离子,在剥离子外侧放置铅笔头后取出工作通道后,放置方形融合器植入通道,从该通道中植入椎间融合器;植入完成后退出融合器植入通道,再次放置工作通道观察左侧神经根,左侧神经根周围减压良好后再将工作通道向对侧倾斜,进行对侧减压。(4)双侧减压完成后使用原放置的椎弓根钉导丝植入万向长尾椎弓根螺钉,透视下观察椎体滑脱距离与L4、L5椎弓根螺钉后缘之间距离,保证此距离大致相同,放置纵行连接棒,先将L5椎弓根与纵棒扭紧后,双侧同时缓慢扭紧L4双侧螺母,从而促使L4椎体复位。C臂透视椎间融合器及钉棒位置良好。使用生理盐水冲洗伤口后,依次缝合伤口,无菌敷料覆盖。
1.4 术后处理及评估
术后24小时使用广谱抗生素预防感染。术后2天叮嘱患者佩戴腰围下地、床边缓慢行走,术后3~5天开始腰背肌功能锻炼,术后3个月内避免剧烈活动,包括弯腰、负重。
1.5 评价指标
(1)腰痛、腿痛视觉模拟评分(visual analogue scale,VAS);(2)Oswestry功能障碍指数(oswestry disability index,ODI);(3)滑脱率、滑脱角以及腰椎JOA评分(japanese orthopaedic association scores,JOA);(4)手术用时;(5)术中出血量;(6)术后引流量;(7)住院时间;(8)术后腰椎DR检查,测量所得椎间隙高度;(9)术后并发症情况。
1.6 统计学处理
采用SPSS 22.0统计分析软件处理。计量资料数据以均数±标准差(±)表示,多组间比较采用单因素方差分析;重复测量资料比较采用双因素重复测量方差分析;组间比较采用秩和检验以及检验。<0.05为差异有统计学意义。<0.001为差异有显著统计学意义。
2 结果
2.1 手术情况
手术顺利,术后患者未出现严重并发症,如椎间隙感染、急性硬膜外血肿、神经根离断、大血管损伤等。手术时间61~122 min,术中透视5~11次,术中出血量为52~110 mL,术后引流量64~116 mL,术后切口愈合良好,无感染。
2.2 术后功能恢复情况及影像学指标评价
患者均获得随访,术后1个月、3个月、末次随访(6个月)复查腰椎DR示椎间隙高度均高于术前(<0.05)。术后1个月、3个月、末次随访的腰、腿痛VAS评分及ODI指数均低于术前(见表1),术后末次随访发现滑脱率、滑脱角以及JOA评分均明显优于术前(见表2),差异具有统计学意义(<0.05)。
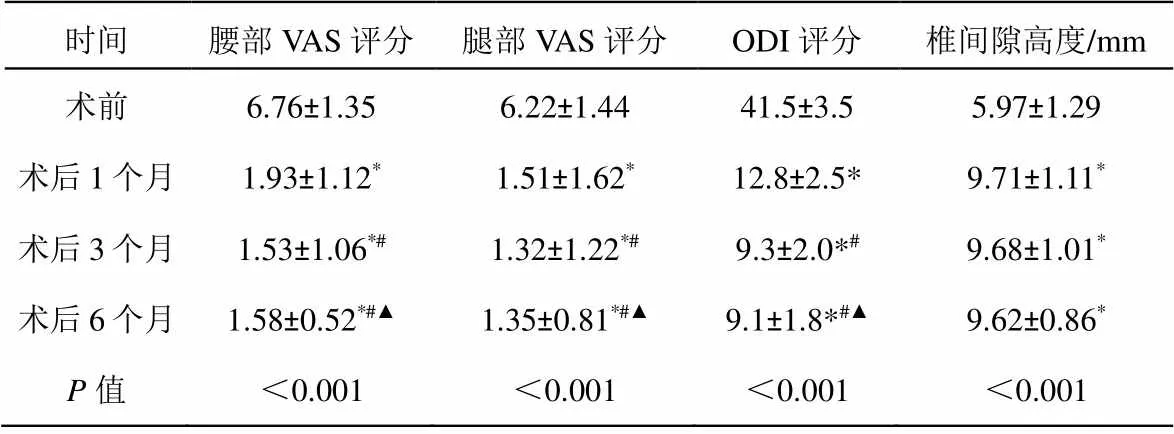
表1 本组手术前后各指标、影像及评分比较(n=25,`x±s)
注与术前比较:*<0.05;与术后1个月比较#>0.05;与术后3个月比较:▲>0.05。

表2 患者滑脱率、滑脱角、及JOA评分比较(n=25,`x±s)
采用配对样本检验来进行假设检验,结果显示,在指标“滑脱率”上,末次随访显著低于术前,差异有统计学意义;在指标“滑脱角”上,末次随访低于术前,且差异有统计学意义;在指标“JOA评分”上,末次随访高于术前,且差异有统计学意义。
2.3 典型病例
患者陈某,女,62岁,主要症状为腰痛,伴有双下肢根性疼痛,以右下肢为甚,行走时右足底麻木,间歇性跛行。术前影像见图1、图2;术中神经根、融合器及减压处理等情况见图3、图4、图5、图6;术后复查影像见图7、图8。
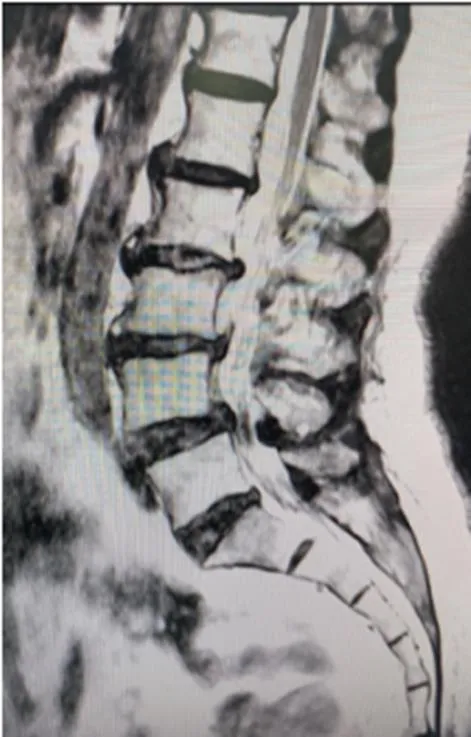
图1 术前MRI
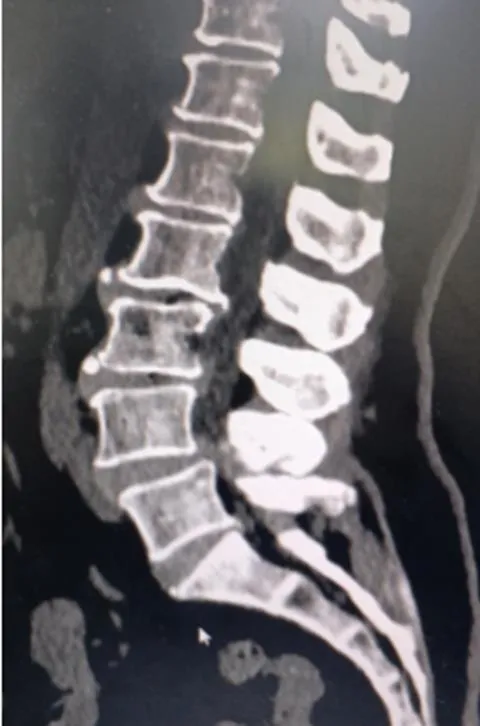
图2 术前CT
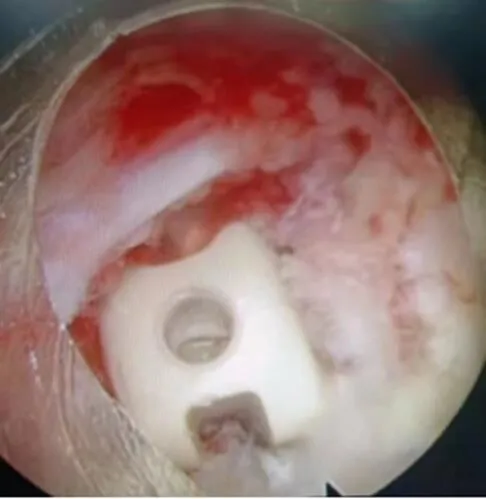
图3 术中神经根和融合器情况
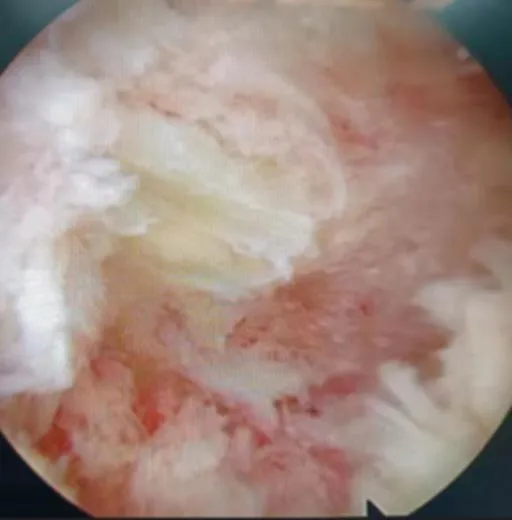
图4 术中终板处理后情况
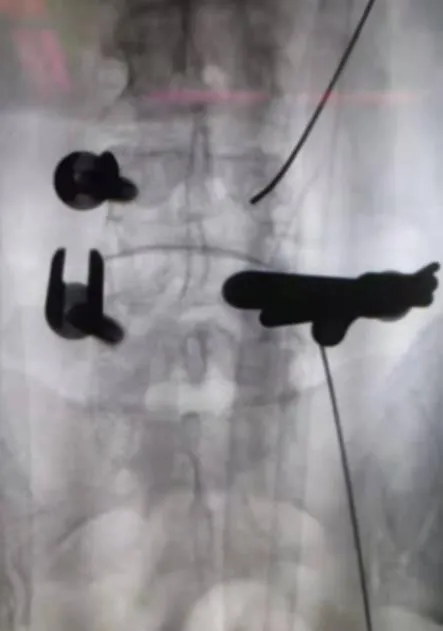
图5 术中工作套管置入
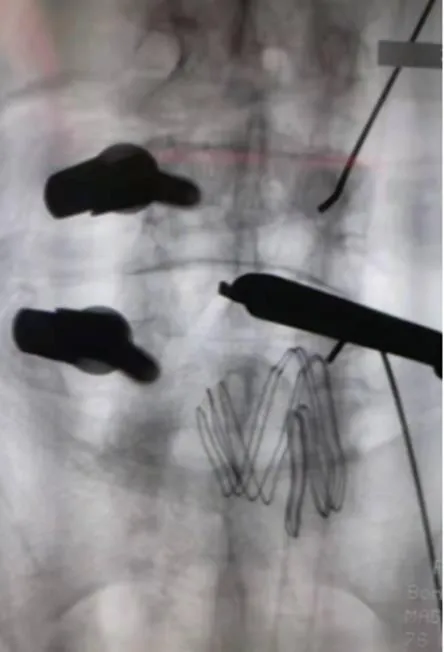
图6 术中对侧减压
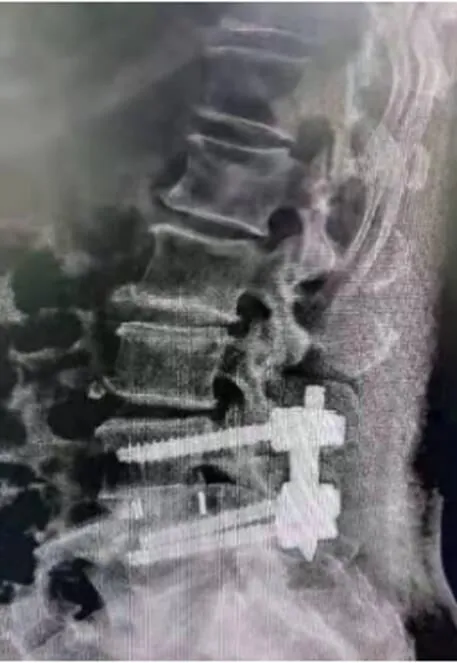
图7 术后DR椎弓根钉位置
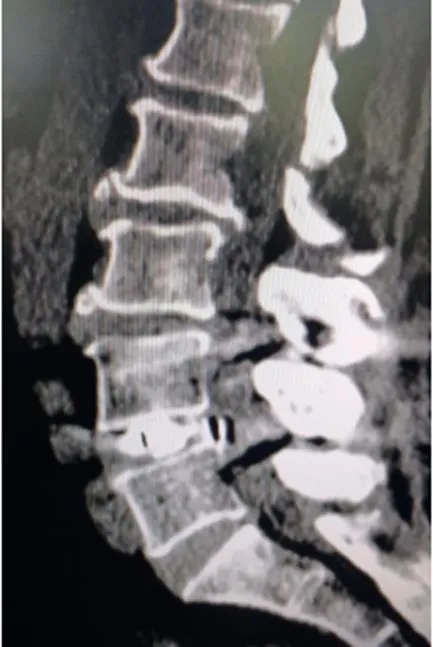
图8 术后CT示滑脱复位,融合器位置良好
3 讨论
3.1 内窥镜手术治疗腰椎退变
2012年,Osman[6]首先报道了使用内镜辅助下腰椎融合术治疗腰椎退行性疾病的疗效观察研究,他对60例保守治疗效果欠佳的退行性腰椎间盘疾病、椎管狭窄、腰椎滑脱患者行内镜下椎间隙减压植骨融合术,术后平均随访时间12个月,59.6%的患者术后达到坚固融合,36.2%的患者达到稳定融合,并发症发生率高达20%。该研究融合率相对较低的原因,可能与其手术团队没有对责任节段椎间隙植入自体骨与融合器有关,而本手术组的研究采用了自体骨与异体骨共同植入的方法,显著提高了融合率。Mengran Jin等[7]通过平均24个月的随访发现,接受经皮内镜下腰椎椎间融合术的39例患者的ODI、SF-36(MCS/PCS)和VAS评分明显优于术前,所有患者均实现了融合。
3.2 腰椎滑脱手术发展现状
关于腰椎滑脱手术复位的治疗,有学者[8,9]研究得出,复位完全与否并不是影响手术疗效的主要因素。术者可根据病人身体情况及术中具体所见尽力复位,但不需要强求解剖复位。苏江平等[10]对25例腰椎滑脱患者行滑脱复位手术治疗,根据术后滑脱复位情况,分为完全复位组和部分复位组,对两组进行6~40个月的随访,末次随访时,发现两组的复位程度虽然不同,但融合率无明显差异,且JOA评分较术前均明显降低,说明不同的复位程度对治疗效果无明显影响。本研究组的手术在内窥镜视野下充分减压完成后,使用原放置的椎弓根钉导丝植入万向长尾椎弓根螺钉,后放置纵行连接棒,促使椎体复位,术后末次随访发现滑脱率、滑脱角以及JOA评分均明显优于术前(见表2),虽然腰椎滑脱的复位程度不同,但患者仍能取得良好疗效,这可能是因为在手术治疗过程中,患者均得到良好的神经减压,使得患者临床症状改善。
近年来,治疗椎间盘突出和退行性腰椎滑脱症的微创手术发展较为迅猛,Kim等[11]通过多中心的回顾分析对比单侧双门脉内窥镜技术与开腹微创腰椎间盘摘除术的临床比较发现,相比于开放性手术,经椎间孔和经椎板间入路微创手术的住院时间更短,出血更少,手术时间更短,恢复工作的时间更早,同时背部和腿部疼痛的视觉模拟评分以及Oswestry残疾指数评分也保持相似。此外,目前主要在临床开展的术式还有经微创椎间孔入路腰椎椎间融合术(Minimally invasive transforaminal lumbar interbody fusion,MIS-TLIF),相比传统开放性腰椎融合术,MIS-TLIF的优点包括以下方面:对棘旁肌的损伤较开放性手术小,术中、术后出血量少,引流量低,术后恢复时间更短,以及感染风险小[12-14]。然而,必要的小关节和椎板切除可能对术后的症状缓解不利,也容易导致腰椎生物力学不稳定[15]。随着内镜技术发展,全内镜辅助下经椎板间入路腰椎减压融合术在继承了MIS-TLIF等微创手术的优点的基础上,还具有减压充分、术后并发症少、可视化强等新优势[16]。
3.3 内镜下经椎板间入路腰椎减压融合术的疗效优势
腰椎内窥镜手术发展最初是利用经椎间孔内窥镜进行腰椎间盘的摘除术,该类手术通过Kambin三角工作走廊取出突出的椎间盘组织。近几年,随着椎板间入路的引入,内窥镜手术设备和相应的内窥镜技术得到了快速发展。内窥镜治疗策略适用于各种情况,手术范围涵盖了从椎间盘突出到侧隐窝狭窄、椎管狭窄等腰椎退行性病变,同时也常合并减压或融合术式来治疗退行性腰椎滑脱等疾病[17]。退行性腰椎滑脱的过程始于小关节和椎间盘的退行性变破坏,这会导致一侧椎体的平移,使椎间水平不稳,退变过程也可能导致椎管移位或椎管狭窄。对于退行性腰椎滑脱症的手术治疗,目标是椎管狭窄的减压,和利用锥体融合及螺钉内固定技术稳定滑脱的节段,从而实现减压、融合以及复位。内镜下经椎板间入路的优势在于:利用持续镜下注水灌溉的优势和内窥镜高速钻头、咬牙钳、钳子和工作套管的应用,使镜下的视野、入路、操作更加方便,减压更加充分。
Ruetten等[18,19]在早期的一系列减压术中应用了经椎板间入路的技术,最初用于治疗腰椎间盘突出症,后来扩展到腰椎椎管狭窄症。在减压方面,经椎板间入路摘除责任节段的椎间盘突出近年来在临床上越来越受欢迎,它可以克服经椎间孔入路所面临的问题,即减少了腰椎间盘摘除所需的小关节切除,更好地维持腰椎稳定性。Park等[20]研究发现,为了保证完全减压,椎间盘突出通常必须在视觉控制下切除,即使在全内窥镜技术中也是如此。经椎板间隙入路术相对于经椎间孔入路减压更直接,因为该术的入路方向是跟传统开发性腰椎融合术一样,通过腰椎后侧入路,在椎板间隙选好穿刺点,突破黄韧带直达椎管,主要适用于中央椎管严重狭窄症的病例,实现神经背侧充分减压。同时,经椎板间入路的工作通道活动度更高,能够更方便地摘除高度移位或脱垂、游离较严重的髓核组织,实现更好的减压,从而为下一步的融合打好基础[21]。
本研究结果显示,25例患者术后1个月、3个月、末次随访(即术后6个月随访)时的腰痛、腿痛VAS评分均低于术前(<0.05)。末次随访时所测得的椎体滑脱率、滑脱角以及JOA评分均优于治疗前,各个时间点测得指标同术前指标差异均有统计学意义(<0.05),术中及术后未出现严重并发症。研究结果证明,全内镜辅助下经椎板间隙入路腰椎减压融合术具有以下优势:(1)该术式在可视化、较安全的前提下实现类似于传统开放手术的直接神经减压,减压效果较好。(2)该术式对结缔组织的损伤小,因为它采用了微创肌肉分离术,并无过多的肌肉切除,术后伤口愈合良好,切口感染发生率低。(3)降低了深静脉血栓形成或肺栓塞的风险。(4)可以保护椎间肌肉、小关节囊和韧带的附着,保持运动节段的稳定性,防止脊柱不稳定。
4 结论
综上所述,全内镜辅助下经椎板间隙入路腰椎减压融合术能在更安全的基础上实现更充分、直接的神经减压,改善患者腰椎滑脱所导致的症状,且手术并发症少,临床疗效较好。但本研究也存在一定局限性:单中心回顾,未与其他微创腰椎融合术进行对照研究等。因此,未来仍需进行多中心、多样本的对照研究,进一步论证全内镜下经椎板间入路腰椎减压融合术的治疗优势。
[1] HARMS J, ROLINGER H. Die operative behandlung der spondylolisthese durch dorsale aufrichtung und ventrale verblockung[J]. Thieme E-Journals, 1982, 120(3): 343-347.
[2] 朱本清,孙渊. 腰椎融合术的研究现状[J]. 实用骨科杂志,2013,19(7): 622-624.
[3] FAN S W, HU Z J, FANG X Q, et al. Comparison of paraspinal muscle injury in one-level lumbar posterior inter-body fusion: modified minimally invasive and traditional open approaches[J]. Orthopaedic Surgery, 2010, 2(3): 194-200.
[4] COLE C D, MCCALL T D, SCHMIDT M H, et al. Comparison of low back fusion techniques: Transforaminal lumbar interbody fusion (TLIF) or posterior lumbar interbody fusion (PLIF) approaches[J]. Current Reviews in Musculoskeletal Medicine, 2009, 2(2): 118-126.
[5] 韩振川,任博文,刘庆祖,等. 经皮脊柱内镜腰椎微创融合术的临床研究进展[J]. 解放军医学院学报,2021,42(9): 970-973,987.
[6] OSMAN S G. Endoscopic transforaminal decompression, interbody fusion, and percutaneous pedicle screw implantation of the lumbar spine: A case series report[J]. International Journal of Spine Surgery, 2012, 6(1): 157-166.
[7] JIN M, ZHANG J, SHAO H, et al. Percutaneous transforaminal endoscopic lumbar interbody fusion for degenerative lumbar diseases: A consecutive case series with mean 2-year follow-up[J]. Pain Physician. 2020, 23(2): 165-174.
[8] 侯平选. 不同复位程度对腰椎滑脱症患者临床疗效的影响[J]. 内蒙古医学杂志,2018,50(9): 1066-1067.
[9] 刘大凯,王罡,易东升. 腰椎滑脱不同复位程度对临床疗效的影响[J]. 当代医学,2017,23(27): 51-52.
[10] 苏江平,井万里. 腰椎滑脱部分与完全复位术后临床效果比较[J]. 中国药物与临床,2016,16(8): 1195-1196.
[11] KIM S K, KANG S S, HONG Y H, et al. Clinical comparison of unilateral biportal endoscopic technique versus open microdiscectomy for single-level lumbar discectomy: a multicenter, retrospective analysis[J]. Journal of Orthopaedic Surgery and Research, 2018, 13(1): 22.
[12] 王辉,喻亮,康照利. 微创经椎间孔入路椎间融合术治疗腰椎滑脱症[J]. 临床骨科杂志,2020,23(5): 622-625.
[13] PHAN K, RAO P J, KAM A C, et al. Minimally invasive versus open transforaminal lumbar interbody fusion for treatment of degenerative lumbar disease: Systematic review and Meta-analysis[J]. European Spine Journal. 2015, 24(5): 1017-1030.
[14] SCHIZAS C, TZINIERS N, TSIRIDIS E, et al. Minimally invasive versus open transforaminal lumbar interbody fusion: evaluating initial experience[J]. International Orthopaedics, 2009, 33(6): 1683-1688.
[15] LEE K H, YEO W, SOEHARNO H, et al. Learning curve of a complex surgical technique: minimally invasive transforaminal lumbar interbody fusion (MIS TLIF)[J]. Journal of Spinal Disordersand Techniques, 2014, 27(7): E234-E240.
[16] HEO D H, SON S K, EUM J H, et al. Fully endoscopic lumbar interbody fusion using a percutaneous unilateral biportal endoscopic technique: technical note and preliminary clinical results[J]. Neurosurgical Focus, 2017, 43(2): E8.
[17] WU P H, KIM H S, JANG I T. A narrative review of development of full-endoscopic lumbar spine surgery[J]. Neurospine. 2020, 17(Suppl 1): S20-S33.
[18] RUETTEN S, KOMP M, MERK H, et al. Surgical treatment for lumbar lateral recess stenosis with the full-endoscopic interlaminar approach versus conventional microsurgical technique: A prospective, randomized, controlled study[J]. Journal of Neurosurgery, 2009, 10(5): 476-485.
[19] RUETTEN S, KOMP M, MERK H, et al. Use of newly developed instruments and endoscopes: full-endoscopic resection of lumbar disc herniations via the interlaminar and lateral transforaminal approach[J]. Journal of Neurosurgery, 2007, 6(6): 521-530.
[20] PARK M K, PARK S A, SON S K, et al. Clinical and radiological outcomes of unilateral biportal endoscopic lumbar interbody fusion (ULIF) compared with conventional posterior lumbar interbody fusion (PLIF): 1-year follow-up[J]. Neurosurgical Review, 2019, 42(3): 753-761.
[21] 农明普,蒙法科. 对比不同入路行椎间孔镜下髓核摘除术在腰椎间盘突出症中的治疗效果[J]. 现代医学与健康研究,2022,6(8): 56-59.
Endoscopic Lumbar Interlaminar Decompression and Fusion for the Treatment of Lumbar Spondylolisthesis
Objective: To investigate the clinical effect of endoscopic lumbar interlaminar decompression and fusion in the treatment of lumbar spondylolisthesis. Methods: 25 patients with single segmental lumbar spondylolisthesis were treated by total endoscopic lumbar interlaminar decompression and fusion. The operation process and postoperative complications were recorded. VAS scores, intervertebral height and ODI index were recorded for lumbago and leg pain at 1, 3 and 6 months after the operation. Vertebral spondylolisthesis rate, spondylolisthesis Angle and JOA score were recorded at 6 months after the operation. The preoperative indexes were compared to evaluate the curative effect. Results: The operation time was 61 to 122 min, the intraoperative fluoroscopy was 5 to 11 times, the intraoperative blood loss was about 52 to 110mL, the postoperative drainage volume was 64 to 116mL, the postoperative incision healed well, there was no obvious infection, and no serious postoperative complications occurred. The VAS scores of low back pain and leg pain at 1 month, 3 months and the last follow-up (6 months after operation) were lower than those before operation (<0.05). The spondylolisthesis rate, spondylolisthesis angle and JOA score measured at the last follow-up were better than those before treatment, and the differences between the measured indicators at each time point and the preoperative indicators were statistically significant (<0.05). Conclusion: Endoscopic interlaminar lumbar fusion can achieve sufficient nerve root decompression and interbody fusion on the basis of safety, and significantly improve the symptoms of low back pain and dysfunction caused by lumbar spondylolisthesis in patients, and the surgical effect is good.
lumbar spondylolisthesis; endoscope; translaminar approach; lumbar decompression and fusion
R68
A
1008-1151(2023)09-0065-05
2022-08-24
广西重点研发计划“基于精准医疗模式下多节段腰椎管狭窄症诊治方案规范化及示范研究”(桂科AB20159018)。
李承蔚(1995-),男,广西中医药大学在读研究生,住院医师,研究方向为脊柱退行性疾病的中西医结合诊疗。
李智斐(1980-),男,广西中医药大学第一附属医院主任医师,硕士,研究方向为脊柱退行性疾病的中西医结合诊疗。

