伴BCR/ABL e13a3转录本阳性慢性粒细胞白血病患儿急变嗜碱性粒细胞白血病1例病例报告
郑方圆 王 淼 黄志卓 王 毓 刘玉鹏 张乐萍
1 病例资料
男,汉族,13岁,因“发热5 d”于2021年12月就诊于中国医科大学附属盛京医院。图1为患儿临床信息时间轴。

图1 患儿临床信息时间轴
患儿5 d前出现发热,体温38.9℃,伴流涕,口服头孢类抗生素发热无缓解。个人史、既往史和家族史均无异常。结合查体、辅助检查(图1)诊断为慢性粒细胞白血病慢性期(CML-CP)。予氟马替尼600 mg·d-1规律口服,偶有全身荨麻疹。治疗5个月达完全血液学反应,复查BCR/ABL e13a3IS融合基因定量明显降低。
患儿治疗11个月时无症状定期复查,外周血涂片、免疫分型检测异常,BCR/ABL e13a3IS融合基因定量升高(80.3%),ABL激酶区突变检测G250E突变阳性。诊断为CML急变期(CML-BP),予高三尖杉酯碱+达沙替尼诱导化疗。
考虑患儿在急变后化疗中出现颜面部及双下肢水肿等不耐受表现,暂停化疗,并转入北京大学人民医院儿科(我院)。入我院时查体肝肋下4 cm,脾肋下约10 cm,余未见异常。辅助检查:WBC 11.5×109·L-1,嗜碱性粒细胞2.53×109·L-1,Hb 95 g·L-1,PLT 19×109·L-1;外周血WBC分类示原始细胞4%,单核细胞10%,嗜酸性粒细胞3%,嗜碱性粒细胞22%,早幼粒细胞8%,中幼粒细胞8%,晚幼粒细胞2%。骨髓形态学示原始细胞20.5%,早幼粒细胞3.5%,中幼粒细胞6%,晚幼粒细胞3%,中幼嗜碱性粒细胞0.5%,晚幼嗜碱性粒细胞0.5%,杆状嗜碱性粒细胞细胞5%,分叶嗜碱性粒细胞14%(图2)。骨髓免疫分型示淋巴细胞占8.11%,主要为成熟T淋巴细胞;髓细胞占34.16%,为成熟粒细胞。R5占44.56%,表达CD33、CD56、CD13、CD11b、CD15dim、CD123、CD11c、CXCR4、CD9、CD203c,部分表达CD25、CD7,少数细胞表达CD117,为异常嗜碱性粒细胞;CD34+幼稚细胞占7.38%,表达CD34、CD56、CD33、CD9,部分细胞表达CD10、TdT,为异常幼稚髓细胞,考虑嗜碱性粒细胞白血病(BL)可能。
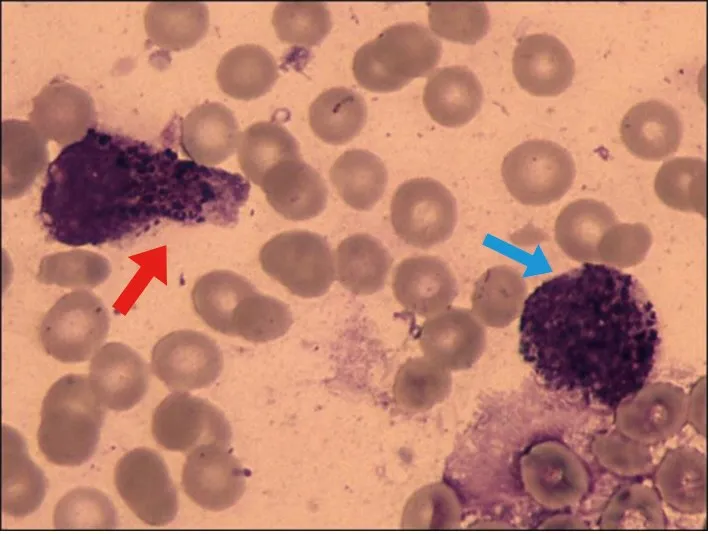
图2 患儿骨髓象(瑞氏染色,油镜,×100)
结合患儿病初诊断CML-CP,目前诊断为CML-BL。予奥雷巴替尼靶向治疗,并予VP[地塞米松10 mg·d-1(或等剂量换算成泼尼松)×14+长春地辛4.5 mg qw×2]再诱导化疗,期间未出现肿瘤溶解等,出现Ⅳ度骨髓抑制,对症处理后好转。化疗第15天外周血WBC分类示原始细胞5%,复查骨髓穿刺,骨髓形态学示骨髓增生Ⅰ级,原始细胞12.5%,早幼粒细胞11.5%,中幼粒细胞15%,晚幼粒细胞2.5%,分叶嗜碱性粒细胞4.5%。免疫残留和BCR/ABL e13a3IS融合基因定量提示未达完全缓解。继续予奥雷巴替尼靶向抗肿瘤,同时加用阿扎胞苷+维奈克拉,化疗过程顺利,期间出现胆红素代谢紊乱(总胆红素最高128.7 μmol·L-1,直接胆红素9.9 μmol·L-1),对症处理后好转。化疗结束后复查骨髓穿刺,形态学骨髓增生Ⅲ级,原始细胞1%,免疫残留可见0.26%异常表型原始细胞,BCR/ABL e13a3IS融合基因定量6.8%。
随访至2023年1月,患儿骨髓为完全缓解状态,目前继续口服奥雷巴替尼(30 mg,qod),拟行异基因造血干细胞移植治疗。
2 讨论
CML患者的BCR/ABL融合基因中,>95%的转录本类型是e13a2和e14a2[1]。e13a3为罕见转录本,成人CML中e13a3阳性率为0.1%~0.9%[2-5]。多项研究显示[2, 4, 6-9],在伴有e13a3的成人CML中,患者的酪氨酸激酶抑制剂(TKI)治疗反应、预后与典型转录本相似,甚至好于典型转录本。可能与e13a3转录本因缺失SH3结构域有关,可减少对STAT5信号通路的激活,从而弱化对白血病细胞的增殖刺激。e13a3转录本在儿童CML中比例及预后意义尚无相关报道。本文患儿初始治疗选择氟马替尼,在治疗后基因水平3个月达早期分子学反应。虽然治疗效果可,但在治疗过程中出现CML-BL急变,且出现G250E突变,e13a3转录本与发生突变及急变之间是否存在相关性尚不明确。
BL为罕见的血液系统恶性肿瘤[10],2016年WHO髓系肿瘤新分类中尚未明确继发性BL的诊断标准,目前国内外文献多为小样本数据或个案报道,且报道多继发于CML[11]。BL在形态学上表现为可辨认的嗜碱性粒细胞中含特异性胞质颗粒,瑞-吉染色时为暗紫色嗜碱颗粒,甲苯胺蓝染色时为红色颗粒。原始嗜碱性粒细胞形态学定义为含异染颗粒的原始细胞。流式细胞术检测的特点为:表达CD123、CD11b、CD203c、CD13和CD33,还可表达CD22、CD34和DR,但CD117常弱阳性或阴性[10,12]。本文患儿外周血嗜碱性粒细胞绝对值升高,同时骨髓流式结果显示有核细胞中异常嗜碱性粒细胞比例>40%,并且形态学可见嗜碱性粒细胞恶性克隆证据,故诊断为CML-BL。
CML-BL治疗方案尚不统一,在仅有的成人急性嗜碱性粒细胞白血病(ABL)以及CML-BL个案报道中,目前多按照AML的化疗方案,但研究认为CML-BL治疗效果不佳、病死率高[13-15]。维奈克拉是一种口服的Bcl-2选择性抑制剂,为Bcl-2蛋白家族成员的类似物,通过直接与Bcl-2蛋白结合,促进内在凋亡途径活化导致细胞死亡。体外实验表明,维奈克拉联合阿扎胞苷在AML细胞的增殖中表现出协同抑制作用。两者的联合应用为难治性AML提供了更多的治疗选择[16]。奥雷巴替尼是新一代BCR/ABL融合基因的TKI,可抑制BCR/ABL激酶和多种与肿瘤相关的激酶(包括KIT、FLT3、PDGFR和FGFR1等)发挥抗肿瘤功能。其对BCR/ABL野生型及耐药突变(如T315I、E255K/V、G250E、Y253H等)细胞都有较强活性[17]。本文患儿应用传统髓系方案、淋系方案联合靶向药治疗,均未缓解,后改为重靶向药轻化疗药的奥雷巴替尼联合维奈克拉、阿扎胞苷治疗,达到完全缓解,未出现明显不良反应,该治疗方案有望成为挽救性治疗的可行选择之一。

