抗菌药物管理项目对减少新生儿肺炎抗菌药物使用的质量改进研究
孟 瑶 丁翊君 王晓玲 齐宇洁
新生儿肺炎是新生儿死亡的主要原因,细菌是早发或晚发新生儿肺炎的主要病原。因氨基糖苷类相关的耳毒性,一线经验性抗菌治疗常选用第三代头孢菌素。对于非重症的社区获得性肺炎,应避免青霉素+酶抑制剂与第三代头孢菌素等抗菌药物联用。成人研究显示,抗菌药物联合用药并不能降低病死率或减少耐药细菌的产生[1]。抗菌药物管理方案(ASP)相关指南已在部分儿童医院发布并成功实施[2-6]。自2019年1月1日起,首都医科大学附属北京儿童医院(我院)开始实施NICU多学科团队(MDT)的ASP。本研究评估MDT-ASP实施前后NICU抗菌药物的使用情况,探讨实施MDT-ASP是否能减少新生儿肺炎的抗菌药物使用。
1 方法
1.1 研究设计 质量改进研究。以新生儿肺炎为研究对象,以2019年1月1日我院NICU开始实施MDT-ASP为时间点,回顾性纳入2018年1月1日至2018年6月30日的新生儿肺炎病例作为对照组,前瞻性纳入自2019年1月1日起收治的新生儿肺炎病例为干预组,样本量与对照组满足1∶1时截止纳入。观察两组新生儿肺炎抗菌药物(抗细菌药物和抗真菌药物)使用情况。
1.2 伦理和知情同意 本研究获得我院伦理审查委员会的批准(编号2018-k-37),并豁免知情同意。
1.3 研究对象纳入和排除标准 纳入确诊为新生儿肺炎[7]、胎龄≥35周的患儿。排除手术、先天性肺气道畸形和未使用抗菌药物的患儿。
1.4 干预方法
1.4.1 对照组(MDT-ASP实施前) 由主治医师基于抗菌谱经验性选择抗生素治疗。特殊病原或药物经感染科医师会诊。疑似败血症和脑膜炎的患儿分别行血培养和脑脊液培养。
1.4.2 干预组(MDT-ASP实施后) 自2019年1月1日起,我院开始实施NICU特色的MDT-ASP[8]。MDT-ASP团队包括新生儿科医师、临床药师、感染科医师、微生物室检验科医师和放射科医师等。MDT-ASP团队每周一对所有使用抗菌药物的患儿逐一进行抗菌药物管理查房。就抗菌药物使用的原因、抗菌药物的种类和成分、抗菌药物疗程的计划以及与使用抗菌药物有关的其他问题进行讨论。特殊患儿如多重耐药菌感染或危及生命的严重感染,需在感染科医师、微生物室检验科医师和放射科医师等会诊后决定。
1.5 结局指标 住院期间应用抗菌药物的使用情况。出院后序贯口服抗菌药物不进入本文分析。
1.5.1 主要结局指标 抗菌药物联合用药比例。联合用药指同时使用≥2种抗菌药物。
1.5.2 次要结局指标 ①抗菌药物使用种类;②抗菌药物治疗天数(DOT):每种抗生素暴露天数的总和,为抗生素总使用剂次除以24 h内给药次数;③住院时间(LOS);④抗菌药物使用变化:根据送检报告的阳性培养结果调整敏感的抗菌药物,或根据治疗效果经验性调整抗菌药物的使用;⑤NEC(改良Bell分期≥Ⅱ期)或在院死亡。
1.6 样本量计算 对照组抗菌药物联合用药比例为25%,MDT-ASP的目标为降低该比例的一半。为达到80%效能检测得出组间联合用药比例的差异,采用双侧Z检验,检验的显著性水平为0.05[9-13],样本量要求每组152例。
1.7 临床资料采集 ①母亲信息:分娩方式、妊娠期并发症(包括妊娠期高血压、糖尿病、甲状腺疾病和感染)、胎膜早破(PPROM)是否>18 h;②患儿信息:性别、胎龄、出生体重、单胎/双胎、出生日龄、5 min Apgar评分、新生儿急性生理评分-围生期扩展-Ⅱ评分(SNAPPE-Ⅱ)[14]、除肺炎或有创通气外的感染性诊断;③抗菌药物使用情况:抗菌药物名称、剂量、给药频次、开始用药时间、停药时间及原因。
1.8 统计学方法 采用SPSS 22.0软件进行统计分析。计数资料采用例数(%)表示,组间比较采用Pearsonχ2检验。符合正态分布的计量资料采用xˉ±s表示,组间比较采用t检验;非正态分布的计量资料采用中位数(范围)表示,组间比较采用Mann-WhitneyU检验。双侧P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 符合本文干预组和对照组纳入和排除标准的新生儿肺炎均为229例(干预组纳入时间截至2019年5月30日)。两组患儿在一般资料和母亲基本信息方面差异均无统计学意义(表1)。
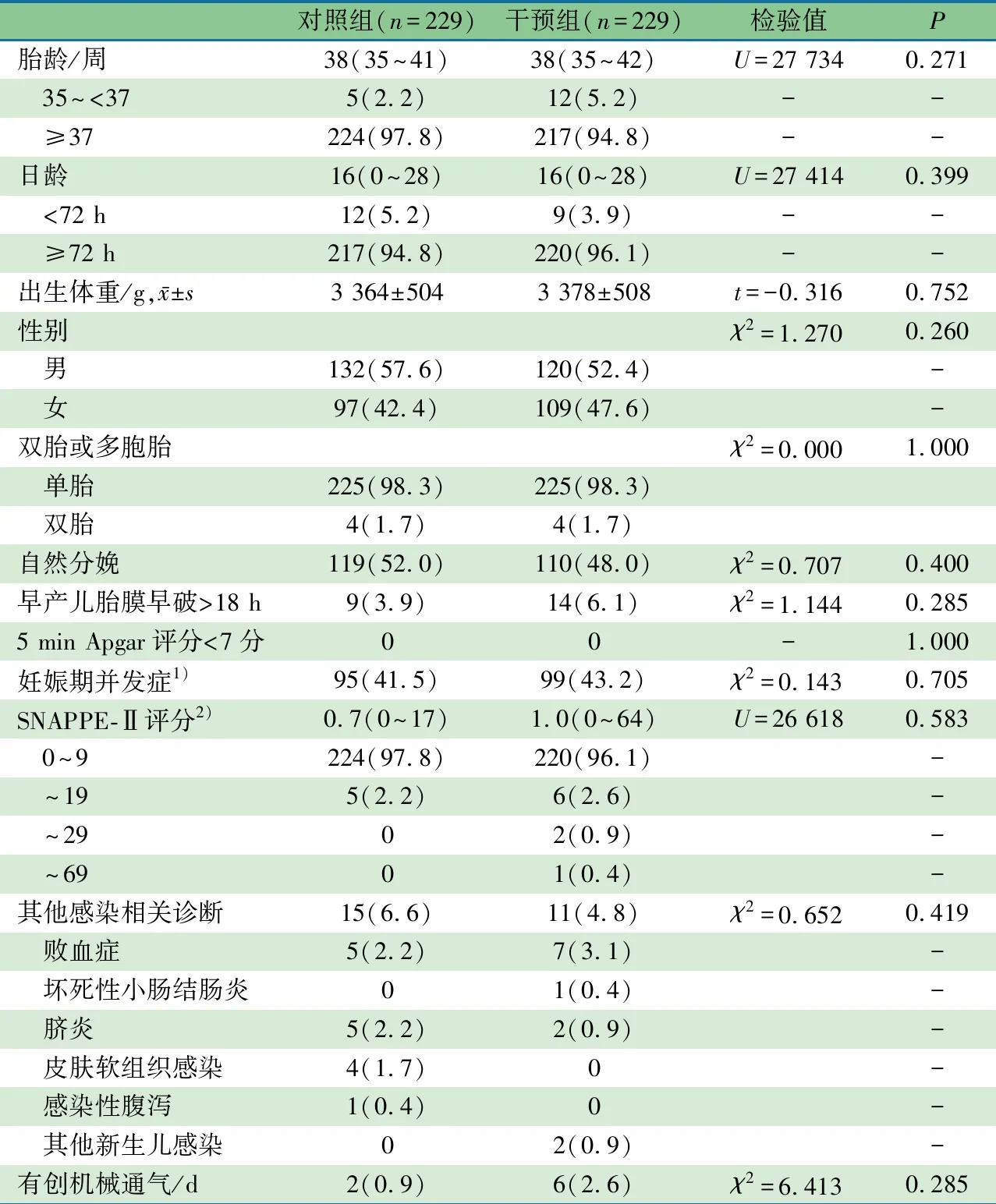
表1 干预组和对照组患儿及其母亲基本信息比较[n(%),M(范围)]
2.2 主要结局指标 无初始治疗仅应用口服抗菌药物的情况,联合用药均为住院期间抗菌药物静脉用药。对照组抗菌药物联合用药比例为24.5%(56/229),干预组抗菌药物联合用药比例为7.0%(16/229),两组比较差异有统计学意义(χ2=26.367,P<0.001)。
2.3 次要结局指标 表2显示,干预组与对照组相比,二代头孢菌素的使用明显增加,三代头孢菌素的使用明显减少,红霉素的使用略有减少,差异均有统计学意义。表3显示,对照组较干预组,DOT由12(3~60)d缩短至8(0~35)d(P<0.001),LOS由10(7~33)d缩短至9(5~46)d(P=0.005)。两组抗菌药物使用后出现NEC以及在院死亡的比例差异均无统计学意义。

表2 干预组和对照组抗菌药物使用[n(%)]
3 讨论
本研究MDT-ASP项目实施后成功地将抗菌药物联合用药比例从24.5%降低至7.0%,但在使用抗菌药物后的NEC和在院病死率等指标差异无统计学意义。MDT-ASP降低抗生素联合使用71.4%的原因是更有针对性的初始抗菌素选择,如MDT-ASP团队评估患儿单核李斯特菌或B族链球菌感染风险低,则不联用青霉素或加酶抑制剂的药物;对于非典型病原体感染,如不考虑混合细菌感染,则不联用头孢菌素。
对于早发性肺炎(即年龄<7 d),美国儿科学会建议最初使用氨苄西林和庆大霉素[15]进行经验覆盖。迟发性肺炎的经验性治疗建议选择万古霉素加氨基糖苷类作为初始治疗。碳青霉烯类(如美罗培南)是治疗产生广谱β-内酰胺酶的生物引起感染的首选药物[16]。在中国,由于氨基糖苷类药物可能引起听力损伤,儿科患者避免使用此类药物,头孢菌素被广泛应用于新生儿肺炎的经验性治疗。必要的抗菌药物联合使用,如需要覆盖单核李斯特菌或无乳链球菌时使用青霉素联合其他治疗药物,或重症患儿耐药菌的治疗需联合≥2种抗菌药物,在本研究MDT-ASP团队例会中均被判定为合理,不会减停此类联合用药。
革兰氏阴性杆菌可通过诱导或染色体介导的β-内酰胺酶活性迅速对头孢菌素产生耐药性[18,19]。美国一项大型观察性研究[20]发现,与接受庆大霉素的新生儿相比,接受头孢噻肟作为初始经验治疗的新生儿死于早发型败血症的风险增加。但在治疗可疑的革兰氏阴性感染时,因氨基糖苷类药物可能引起听力损伤,只能经验性使用第三代头孢菌素。因此呼吁有关部门再次评估氨基糖苷类药物对于新生儿人群使用的风险与获益,以期给予临床治疗更多的药物选择。
第三代头孢菌素对早期肺炎和社区获得性晚发型肺炎(日龄≥72 h)的常见病原体有活性,包括大肠埃希菌、克雷伯菌、敏感B组链球菌、金黄色葡萄球菌、化脓性链球菌和肺炎链球菌[17]。在大多数情况下,第三代头孢菌素和青霉素+酶抑制剂的联合使用是不必要的。本研究MDT-ASP实施后,显著减少了此类联合用药。
由于本研究纳入的新生儿肺炎中有相当比例是生后获得性晚发型肺炎,常见的病原体为肺炎链球菌等头孢菌素二代敏感的病原,因此干预组中更多的患儿选择了单用二代头孢菌素抗感染,而降低了三代头孢菌素的使用率,抗菌谱更窄,减少了广谱抗菌药物的使用。
无并发症肺炎的治疗疗程通常为10~14 d,包括口服和静脉用药。本研究重点是静脉内抗菌药物的使用,因此DOT小于推荐的治疗疗程,干预组较对照组,DOT下降约4 d,LOS下降约0.5 d。
本研究局限性:①单中心样本限制了本研究结果的外推性。②针对降低抗菌药物的使用级别、限定日剂量、严格控制抗菌药物使用指征等指标,本研究未获得定量结果。未来将进一步开展更多针对其他特殊疾病的ASP研究。
致谢:感谢首都医科大学附属北京儿童医院新生儿中心、国家儿童健康中心的全体工作人员对新生儿重症监护室ASP实施的支持。

