掺(氟)A-TiO2制备及其光催化反应动力学研究
张一兵,易志文
(上饶师范学院化学与环境科学学院,江西 上饶 334001)
随着我国工业的迅速发展,随之带来的水污染问题也日渐引起人们的关注,其中染料废水防治成为当务之急。甲基橙是化工生产的常用染料之一,有毒,分子结构较稳定,难以完全降解成CO2和H2O[1]。目前,处理染料废水的方法有生物处理法、化学氧化法、光催化法、吸附法、电解法等,这些方法可共同使用也可单独使用。光催化降解技术由于绿色环保、氧化能力强、设备简单、反应条件易控日受重视[2]。光催化材料主要为无机氧化物和无机硫化物,TiO2因具有稳定、高效、易得、对环境无污染等优点而成为光催化首选材料[2-18]。在TiO2的三种晶型(锐钛矿型A-TiO2、金红石型R-TiO2、板钛矿型B-TiO2)中,A-TiO2光催化降解有机物污染物的效率最佳[3]。不足之处是,较宽的TiO2禁带(Eg=3.2 eV)使其对太阳光的利用率不足5%[4],因此,人们探索诸多方法对TiO2进行改性,以期提高其光催化效率。掺杂是改性最常用的方法,目前多有Fe3+、Ag+、N、S掺杂改性的研究报道,但F掺杂报道较少且相关的动力学研究更少[5-8]。本研究以硫酸钛为原料,通过水热法制备了掺(氟)A-TiO2,采用X射线衍射(XRD,X-Ray Diffraction)、扫描电镜(SEM,Scanning Electron Microscopy)表征技术,分别考察制备试样的晶相和形貌;然后以甲基橙模拟降解对象,在可见光照下,探索甲基橙的初始浓度C0、掺(氟)A-TiO2用量m和掺氟量χ等因素对甲基橙溶液催化降解反应动力学的影响。
1 方法
1.1 主要仪器与药品
RD-100型高压釜(240℃,中国石油化工科学研究院)、Rigaku MiniFflex II型X射线衍射仪XRD(日本理学)、SU-8010型场发射扫描电镜SEM(日本日立)、2C50502085型722-可见分光光度计(上海欣茂仪器有限公司)、GZX-DH-40X45-4090689型电热恒温干燥箱(上海跃进医疗器械厂)。
化学纯硫酸钛(国药集团化学试剂有限公司)、分析纯甲基橙(国药集团化学试剂有限公司)、分析纯氟化钠(国药集团化学试剂有限公司)、分析纯尿素(广州化学试剂厂)、去离子水(自制)。
1.2 掺(氟)TiO2制备与表征
在21℃(实验环境温度)下将硫酸钛晶体用去离子水溶解,加氟化钠和尿素(摩尔分数:N/Ti4+=1/5)晶体,溶解形成0.15 mol/L的溶液。将溶液转移到内嵌聚四氟乙烯内胆的高压反应釜内,注意溶液体积最多占内胆容积的75%,密封釜盖后平移反应釜至烘箱内。通电控制烘箱温度,使其温度从室温升至170 ℃,在此温度下恒温加热4 h,断电,自然冷却至室温(注意:期间不能开烘箱门),将反应釜取出并过滤釜中混合物质,滤渣经去离子水--无水乙醇洗涤干净(用Ba2+检验SO42-的存在以确保滤渣洗净),继而转入烘箱干燥,自然冷却后取出封存待用[9]。本研究共制得掺氟量(摩尔分数)分别为0、2%、4%、5%、6%、8%的TiO2粉末,并对其进行XRD和SEM 表征。
1.3 光催化降解实验
配制所需浓度的甲基橙溶液(p H=6),测其起始吸光度A0,移取50 m L 溶液于200 m L 洁净干燥的烧杯中,加入适量的掺(氟)A-TiO2粉末,封杯口后放入暗箱内,在T=21℃下搅拌,用功率为60 W 白炽灯光照进行光催化降解反应。间隔适时取出适量溶液离心(除去A-TiO2粉末)后测吸光度At。
2 结果与讨论
2.1 X 射线衍射分析
图1是摩尔掺氟量分别为0和5%的制备试样的XRD 图谱。从图1可知,TiO2锐钛矿相的(101)(004)(200)(105)(211)和(204)晶面衍射峰无杂峰,说明产物为单一的锐钛矿型TiO2,即为纯相A-TiO2。2θ=25.3°的(101)的晶面衍射峰,峰形尖锐,强度较大,说明TiO2的结晶度优良;氟掺杂没有其他晶相,且无其他物质存在,可能是F-取代了O(F的半径0.133 nm 与O的半径0.132 nm 几乎相同)[5]。

图1 试样的XRD 图谱
2.2 扫描电镜分析
图2 为掺氟5%TiO2试样的不同放大倍数的SEM 图。图2(a)(b)显示TiO2粉末由诸多微米球组成,球径为1~4μm;图2(c)(d)为高倍镜下一个由众多纳米颗粒自组装的微米球,颗粒为八面体,粒径为30~50 nm;细小颗粒分散均匀,使得催化剂有大的比表面积,有利于它对污染物的吸附和光催化降解。

图2 掺氟5%试样的SEM 图
2.3 甲基橙初始浓度C0的影响
固定A-TiO2粉末的掺氟量χ=5%、用量m=0.3 g/L,变化甲基橙初始浓度C0分别为0.01、0.02、0.03、0.04、0.05 g/L,考察C0对光催化降解反应动力学的影响,结果如图3所示。图3(a)显示ln(C0/C)~t有较好的线性关系,说明此降解过程为化学动力学一级反应,其速率方程可表示为ln(C0/Ct)=kt+B。表1列出了由速率方程回归不同C0的一级反应动力学方程、表观速率常数k、相关系数R2和半衰期t1/2(t1/2=0.693/k)。
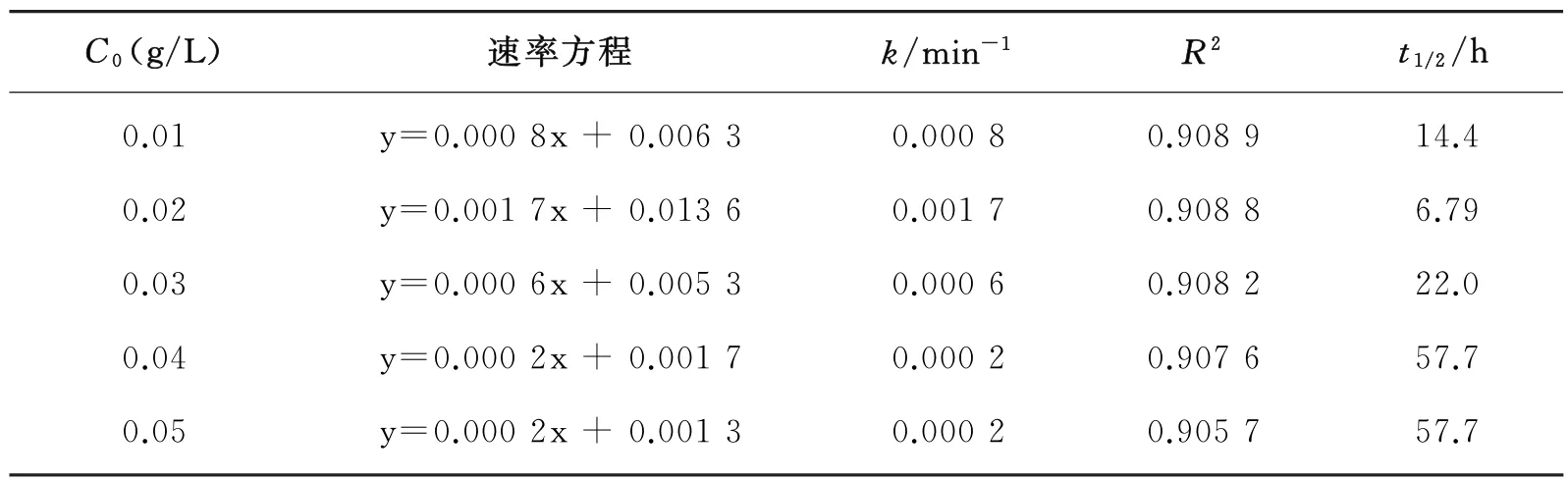
表1 不同初始浓度C 0下甲基橙的动力学方程及参数
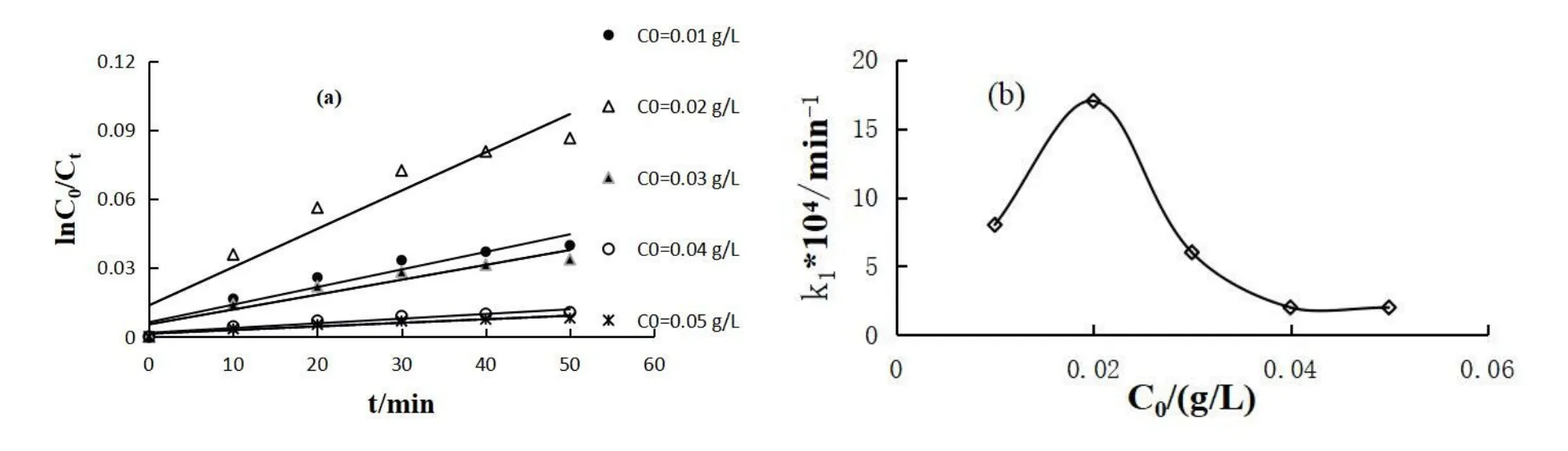
图3 C 0对甲基橙降解动力学的影响
图3(b)展示了C0对k的影响:随着C0的增大,k值经历了先增大后减小的过程,期间在C0=0.02 g/L时k达到最大值。当催化剂用量一定时,催化剂的表面积和活性位的总量也一定,随着底物初始浓度的升高,底物被催化剂吸附的量随之增大,光催化降解反应随之加快,速率常数不断增大,直到反应的k值达到最大。若继续加大初始浓度,由于催化剂的表面积和活性位的总量已经使用完毕,无力对多余的底物分子进行降解反应,即发生降解反应的底物分子数与加入底物分子的总量之比下降,且过多的底物会减弱催化剂对光的有效吸收及利用,所以初始浓度过大会使反应速率常数减小[12]。
2.4 催化剂用量m的影响
固定甲基橙初始浓度C0为0.02 g/L,A-TiO2粉末的掺氟量χ=5%,变化A-TiO2粉末的用量m分别为0.2、0.3、0.4、0.5 g/L,考察m对光催化降解反应动力学的影响,结果如图4所示。图4(a)显示ln(C0/C)~t有较好的线性关系,说明降解过程为化学动力学一级反应,其速率方程可表示为ln(C0/Ct)=kt+B。表2列出了由速率方程回归不同m的一级反应动力学方程、表观速率常数k、相关系数R2和半衰期t1/2。

表2 不同催化剂用量m 下甲基橙动力学方程及参数

图4 m 对甲基橙降解动力学的影响
图4(b)展示了m对k的影响:随着m的增大,k先增大后减小,期间在m=0.3 g/L时k达到最大值。当底物浓度一定时,催化剂的用量越多,经光照生成的活性组分如·OH、·O2、·OH2等就越多,故表观速率常数表现为不断增大,乃至最大。当催化剂用量过大时,虽然能增加反应活性位点数目,但过多的催化剂会发生团聚现象产生丁达尔效应,对光产生散射作用,导致到达催化剂表面的光子数量减少,结果反而降低反应速率[19]。
2.5 掺氟量χ的影响
固定甲基橙初始浓度C0为0.02 g/L,催化剂用量m=0.3 g/L,变化掺氟量χ分别为0、2%、4%、5%、6%、8%,考察χ对光催化降解反应动力学的影响,结果如图5所示。图5(a)显示ln(C0/C)~t有较好的线性关系,说明此降解反应为化学动力学一级反应,其速率方程可表示为ln(C0/Ct)=kt+B。表3列出了由速率方程回归不同m的一级反应动力学方程、表观速率常数k、相关系数R2和半衰期t1/2。

表3 不同氟掺杂量χ 下甲基橙动力学方程及参数

图5 氟掺杂量χ 对甲基橙降解动力学的影响
图5(b)展示了m对k的影响:χ增加k平缓地增大,当χ增至5%时,k达到最大值,而后随着χ增大,k变小。因为F、O 的原子半径很接近,F易掺杂到TiO2晶格中去,当F-替代晶格O2-时会造成电荷的失衡,导致催化剂表面酸性的提高(有利于对底物分子的吸收)、氧空位(重要的活性位,有利于自由基·O2、·OH等的生成[20-21])的产生和活性位的增加,从而减小光生载流子的复合速率[22];另外,F的氧化电位+3.6 eV远高于空穴h+的+2.7 eV,即F-难为h+氧化,故可提高F-TiO2的稳定性,同时增加TiO2对可见光的响应范围,从而提高反应速率[23]。当掺氟量过大(超过最佳值)时,因掺氟而形成的新能级成为电子空穴的复合中心(已被电化学阻抗谱所证明),反而降低催化效率[24]。
3 结论
3.1 采用水热法制备了掺(氟)TiO2粉末,XRD、SEM 表征表明产物为单一晶相的锐态矿型二氧化钛即ATiO2,粉末由诸多球径为1~4μm 的微米球组成;微米球由众多纳米颗粒自组装而成,颗粒为八面体,粒径30~50 nm。
3.2 在探索出的最佳条件(60 W 白炽灯照射、C0=0.02 g/L、p H=6、m=0.3 g/L,χ=5%、21℃、t=40 min)下,光催化降解甲基橙的过程表现为动力学一级反应。

