计数标准微球分散及浓度对酿酒酵母计数的比较
徐娟,陈翔宇,李蒙蒙,林丽军,陆利霞,刘元建,熊晓辉
(南京工业大学食品与轻工学院,江苏南京 211816)
微球(聚苯乙烯微球)广泛应用于生物医学、分析化学、标准计量以及吸附等领域[1]。荧光修饰的微球可作为计数标准微球对细胞进行计数[2,3]。Cunningham等[4]添加已知浓度计数微球对样品中的病毒进行荧光显微镜计数,结果表明在每毫升2.17×106~1.37×108个病毒的范围内该方法与膜过滤的计数结果无显著性差异(P=0.531)。Ou等[5]在对浓度为每毫升104~108个活死菌进行计数时,发现利用荧光微球的流式细胞术与琼脂平板计数之间线性关系一致。另外,用于流式细胞仪的标准微球类型不同,报道有浓度为每毫升1.0×108个的6.0 μm微球,浓度为每毫升106个的5.0~7.9 μm微球等[6,7]。但未有研究报道标准微球用于计数不同浓度细胞(病毒)时的适宜使用浓度。
国家标准GB/T 39730-2020《细胞计数通用要求流式细胞测定法》中对计数标准微球的使用浓度未说明,且对标准微球使用中的聚集问题缺少措施。ISO 20391-1:2018中对悬浮液中的细胞及微球需要保证均一性,才可实现所取样反映实际样品中的数量。已有研究表明体积分数低于1%的Tween 20和体积分数低于5%的Tween 80可有效降低微生物聚集且不会对细胞活性造成影响[8,9]。但缺少使用Tween 20和Tween 80促进标准微球的分散研究。本研究中发现,标准微球在液体中会发生聚集、结团现象,导致细胞计数的不准确,且产生显著影响。
依据计数标准微球法,对细胞和微球直接计数时统计的细胞和微球数量与计数结果相关。在显微镜直接计数过程中,当载玻片上统计的细胞或微球数量大于350个时,才能获得可靠的结果[10,11]。Braun等[12]在显微镜计数干燥土壤中的总细胞数实验中要求统计的细胞数量大于1 000个。而GB/T 39730-2020中仅说明需采集的微球及细胞的数量,但并未说明不同细胞浓度所对应的计数数量。
本文以计数标准微球和酿酒酵母ATCC9080为实验对象,研究了计数标准微球的分散条件及微球浓度对酿酒酵母细胞计数的影响,分析了标准微球及细胞统计数量对计数结果的影响,并将标准微球计数与平板计数结果进行了比较,为计数标准微球用于微生物的准确计数提供参考。
1 材料与方法
1.1 材料与试剂
计数标准微球(直径8 μm),知益微球科技有限公司;酿酒酵母ATCC9080(S.cerevisiae),本实验室保藏菌株;0.01 mol/L磷酸盐缓冲液(Phosphate Buffer Saline,PBS,pH值7.0),上海生工生物工程有限公司;Tween 20和Tween 80,国药集团化学试剂有限公司;酵母浸出粉葡萄糖培养基、马铃薯葡萄糖琼脂培养基,青岛海博生物技术有限公司。
1.2 仪器与设备
生物显微镜BM1000,南京江南永新光学有限公司;智能生化培养箱SHP-100,上海三发科学仪器有限公司。
1.3 实验方法
1.3.1 计数标准微球的悬液制备及分散
1.3.1.1 计数标准微球分散处理实验
(1)Tween 20对计数标准微球分散的影响
在无菌PBS缓冲液中加入不同体积的Tween 20,得到体积分数为0.02%、0.04%、0.06%、0.08%、0.10%、0.12%的Tween 20,采用0.22 μm滤膜过滤后得到不同体积分数的PBS吐温20溶液(PBS-Tween 20,PBST2)。称取0.0150 g微球粉末分别溶解于10 mL无菌PBS缓冲液和不同体积分数的PBST2中,经超声(50 Hz)分散至无肉眼可见结块后得到待测微球溶液。每个处理组重复三次。以无菌PBS缓冲液处理组为对照组,计算不同体积分数Tween 20处理的计数标准微球分散指数(I)。
(2)Tween 80对计数标准微球分散的影响
在无菌PBS缓冲液中加入不同体积的Tween 80,得到体积分数为0.02%、0.04%、0.06%、0.08%、0.10%、0.12%的Tween 80,采用0.22 μm滤膜过滤后得到不同体积分数的PBS吐温80溶液(PBS-Tween 80,PBST8)。其它同(1)处理,计算不同体积分数Tween 80处理的计数标准微球分散指数(I)。
1.3.1.2 计数标准微球分散指数测定
使用血球计数板计数标准微球溶液,观察分散处理前后微球分散情况,分散指数(I)计算见公式1[8]。
式中:
I——分散指数;
T1——分散后标准微球在血球计数板五个中格总数,个;
T0——对照组标准微球在血球计数板五个中格总数,个。
1.3.2 酿酒酵母菌悬液的制备
取用酵母浸出粉葡萄糖培养基在30 ℃,160 r/min培养18 h的酿酒酵母液体培养液,重悬后用无菌的PBS溶液进行十倍稀释得到一系列菌悬液。采用血球计数板对菌悬液进行三次重复计数,选取其中浓度为每毫升105~107个的菌液作为计数标准微球法和平板计数法的计数样品。
1.3.3 酿酒酵母浓度计数
1.3.3.1 标准微球计数酿酒酵母浓度
将0.0150 g微球粉末溶解于5 mL 0.08%的PBST2,用0.08% PBST2稀释后经血球计数板计数得到每毫升4.25×104、8.60×105、7.56×106、2.17×107个的微球溶液。移取100 μL制备的不同浓度微球溶液分别与100 μL待测酿酒酵母溶液混匀,制成微球、酿酒酵母的混合溶液后,用扁平玻璃毛细管吸取部分混合溶液在10×40倍镜下进行显微镜计数”,随机获取20~45个显微镜图像,使用ImageJ软件计数图像中酿酒酵母和微球[13]。每个样品进行三次重复并计算平均值及标准差,计算结果间的变异系数(Coefficient of Variation,CV)。
标准微球计数酿酒酵母浓度计算参考GB/T 39730-2020,见公式2。
式中:
C——酿酒酵母浓度,个/mL;
Ncell——单个图像中酿酒酵母的平均数量,个;
Nball——单个图像中标准微球的平均数量,个;
Qball——酿酒酵母中添加的计数标准微球总数量,个;
V——与标准微球混合的待测酿酒酵母溶液的原体积,mL;
D——酿酒酵母溶液的稀释倍数。
1.3.3.2 平板计数酿酒酵母浓度
将标准微球与酿酒酵母混合悬液采用平板计数酿酒酵母浓度,依据GB 4789.15-2016《食品安全国家标准食品微生物学检验霉菌和酵母计数》进行。
1.4 数据分析
Microsoft Office Excel 2010软件进行数据处理;Origin 2018进行图像绘制;IBM SPSS Statistics 26软件采用沃勒-邓肯法(Waller-Duncan)进行显著性分析,P<0.05为存在显著性差异。
2 结果与分析
2.1 计数标准微球分散处理结果
2.1.1 Tween 20对计数标准微球分散的影响
在使用流式细胞仪对荧光微球计数之前,先采用涡旋混合器对微球溶液进行混匀,但未说明标准微球是否分散及其效果[14]。图1是计数标准微球在不同体积分数Tween 20中的分布情况。

图1 不同体积分数的Tween 20对计数标准微球分散现象Fig.1 Dispersion of counting standard microspheres with different volume fractions of Tween 20
由图1a可知计数标准微球在未添加Tween 20的PBS溶液中存在大量聚集和分层现象(在显微镜图像中有的微球模糊),可见多个计数标准微球聚集体以及部分微球悬浮或沉淀情况。而计数标准微球的聚集会直接影响标准微球计数结果的准确性,因此在计数之前需要对标准微球进行混匀或者分散处理。
由图1b~1d可发现,不同体积分数的Tween 20促进标准微球分散,并随着Tween 20的体积分数增加,微球的聚集和分层现象逐渐改善;且体积分数在0.08%时微球聚集团变为单个分散的微球,不再分层。分散指数是指处理组与对照组在血球计数板五个中格总数的差值与对照组五个中格总数的比值。对于同一浓度微球悬液,处理后的分散指数越大,则说明与对照组相比,微球聚集减少,进入计数区的粒子数量越多,说明微球分层和聚集导致问题得到了改善。因此可通过分散指数判断分散效果。
由图2可知,不同体积分数的Tween 20处理组的分散指数较对照组均显著增加(P<0.05),表明该处理改善了微球的聚集情况,且随着Tween 20体积分数的增加,分散指数先增加后趋于稳定。其中当Tween 20体积分数为0.08%时,酿酒酵母分散指数为3.32,此后随着Tween 20体积分数增加,分散指数变化不显著(P>0.05),即体积分数为0.08%~0.12%的Tween 20对标准微球均有促分散效果。但增大Tween 20体积分数,在分散时会产生较多气泡。Brando等[15]发现涡旋或混匀时产生的微气泡会聚集微球并使得移取液中微球的数量发生变化。研究表明0.2%~1.0% Tween 20不会影响酿酒酵母细胞活性[8]。因此采用更低体积分数的0.08% Tween 20的微球溶液计数酿酒酵母也不会对其活性造成影响。另外如图3所示,实验中发现在含0.08% Tween 20的微球溶液中,除去因出芽繁殖形成的少数聚集外,酿酒酵母并未出现明显的聚集。Cilliers等[16]在奶酪匀浆中回收微生物群时,使用0.02%Tween 20和1 mmol/L EDTA来对微生物进行分散。然而在0.08% Tween 20中微球仍会存在极少数2~3个微球聚集(图1d),但这部分聚集仅占计数区域微球总数的1%,并不会对计数结果造成误差。

图2 不同体积分数的Tween 20对计数标准微球分散指数的影响Fig.2 Effect of different volume fractions of Tween 20 on the dispersion index of counting standard microspheres

图3 酿酒酵母在含有0.08% Tween 20的微球溶液中的分散状态Fig.3 Dispersion of S.cerevisiae in a microsphere solution containing 0.08% Tween 20
计数标准微球易发生团聚现象并且表面具有疏水性,疏水作用使微球在PBS溶液中无法形成稳定的溶液[17]。Tween 20是一种常用的非离子型表面活性剂,能在微球表面增加羧基、醚类等亲水性基团,可改善微球在水溶液中的分散,使得微球在溶液中能够均匀分散[18]。Jodar-Reyes[19]等也报道两亲性分子吸附在聚苯乙烯乳胶颗粒表面主要是依靠表面疏水区域之间的疏水吸引。因此通过Tween 20可改善标准微球聚集。
2.1.2 Tween 80对计数标准微球分散的影响
图4是计数标准微球在不同体积分数的Tween 80中的分布情况。由图4a可知,计数标准微球在未添加Tween 80的PBS溶液中存在计数标准微球聚集体以及部分微球悬浮或沉淀情况。与对照组相比,随着Tween 80体积分数增加,微球聚集的现象逐渐改善,微球聚集团减少并呈现单个分散的微球,表明Tween 80有助于计数标准微球的分散。
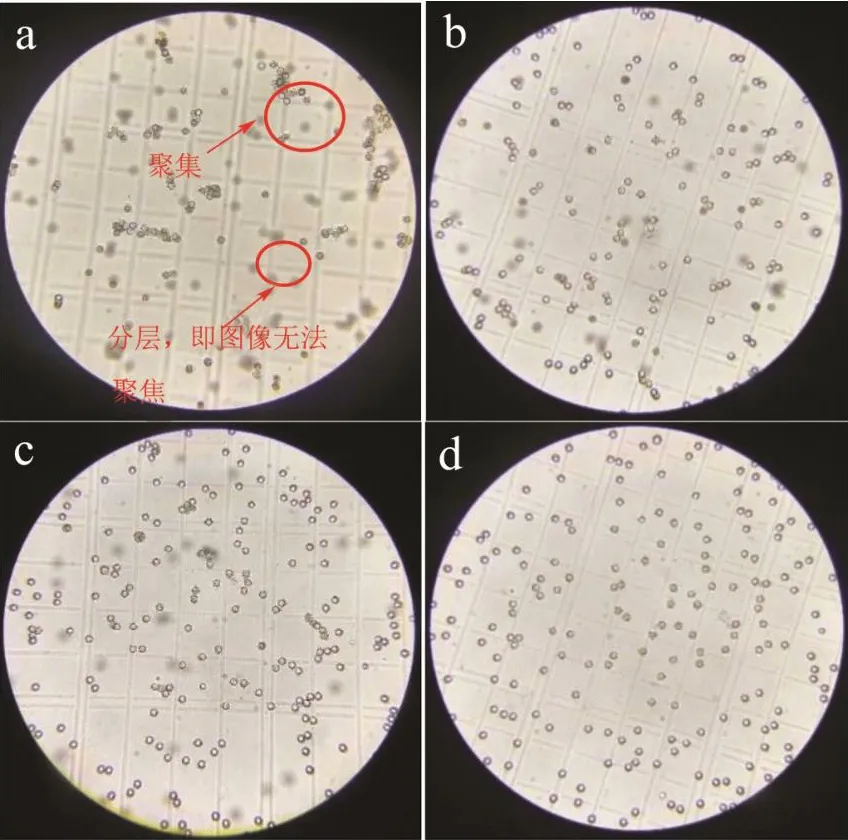
图4 不同体积分数Tween 80对计数标准微球分散现象Fig.4 Dispersion of counting standard microspheres with different volume fractions of Tween 80
根据图5可知,随着Tween 80体积分数的增加,分散指数先增加后趋于稳定。其中当Tween 80体积分数为0.06%时,酿酒酵母分散指数为3.37,此后随着Tween 80体积分数增加,分散指数变化不显著(P>0.05)。与对照组相比,Tween 80对计数标准微球的分散有显著效果(P<0.05),且当Tween 80体积分数达到0.06%~0.12%,分散结果达到最佳。与0.08%Tween 20相比,0.06% Tween 80也能使微球的最大分散指数达到3.30。

图5 不同体积分数的Tween 80对计数标准微球分散指数的影响Fig.5 Effect of different volume fractions of Tween 80 on the dispersion index of counting standard microspheres
与Tween 20类似,Tween 80是一种亲水性的表面活性剂,其分子结构中含有亲脂性的脂肪链和亲水性的氧乙烯链,对疏水性物质有助溶作用。因此加入Tween 80可能改变聚苯乙烯微球表面的疏水性,从而促进微球聚集体的分散。此外,对油脂类样品中微生物进行计数时,也常使用Tween 80形成均匀分散溶液,且5% Tween 80不会影响菌落总数的平板计数结果[9,20]。
2.2 计数标准微球浓度对不同浓度酿酒酵母细胞计数的影响
采用已知数量的微球对酿酒酵母进行计数是利用单个图像中酿酒酵母细胞与微球数量的比值等于原混合溶液中两者的比例,从而间接计算出待测酿酒酵母细胞的数量。当流式细胞仪无法精确控制或监测检测样本的体积,可通过加入已知数量的微球获得细胞的浓度[21]。为获得计数酿酒酵母细胞适宜的微球浓度,实验分别使用不同浓度的标准微球对酿酒酵母菌液进行计数。
实验发现,采用浓度小于每毫升105个的标准微球进行计数,大量图像中无微球存在,单个图像中微球平均数量小于1个。即微球浓度太低会导致其在单个图像中分布的数量较少,计数结果的稳定性差。Seo等[22]报道单个显微图像的细胞数小于45个会导致细胞计数结果之间的高度差异。当过滤器上细菌细胞数量小于105个时,显微镜计数会高估真实细菌浓度且高估范围为15.0%~99.3%[23]。另外,当标准微球的浓度大于每毫升107个时,导致整个图像中全部被微球充满,而影响对酿酒酵母细胞的识别统计。因此实验选取每毫升105、106、107个标准微球进行分析。
对不同浓度酿酒酵母分别添加不同浓度计数标准微球,采集显微图像后,计算获得酿酒酵母浓度结果见表1。表1表明,同一酿酒酵母样品添加每毫升105~107个微球,对酿酒酵母浓度结果无显著影响(P>0.05)。但通过比较添加不同浓度微球计数酿酒酵母的变异系数CV可知,对每毫升105~107个酿酒酵母进行计数使用每毫升106个的微球更优,且不同比例时组内变异系数分别为5.13%、1.56%、3.47%。
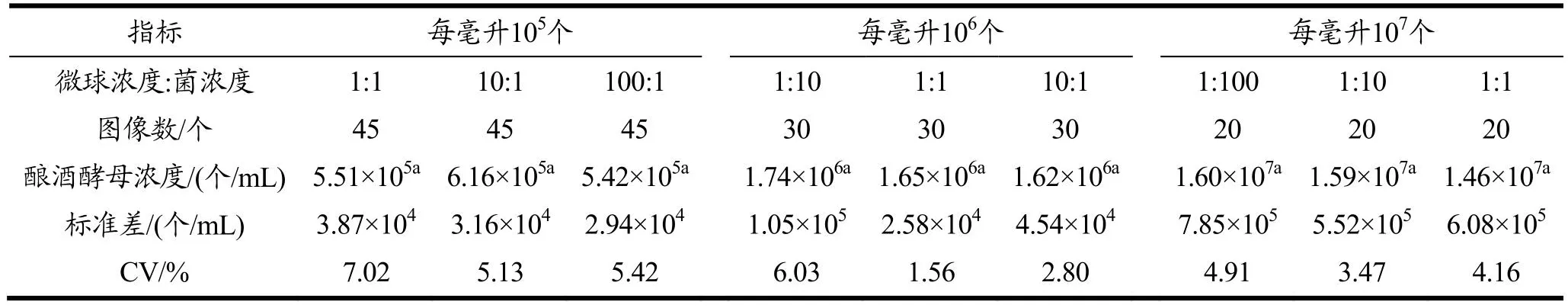
表1 不同浓度计数标准微球对酿酒酵母的计数结果Table 1 Results of counting S.cerevisiae by different concentrations of counting standard microspheres
图像计数结果的准确性与采集的图像数量有关。Muthukrishnan等[10]发现当载玻片上细菌不均匀分布时,至少需要计算20个随机图像或350个细菌细胞,才能可靠地估算载玻片上的细菌总数。Lander等[24]报道显微镜和原型激光扫描细胞仪对微球的计数结果存在波动,这是因为计数时随机选取的计数区域小,小于计数滤膜总面积的10%,该方法的随机性在对低浓度的粒子计数时会变得更加明显。从表1结果表明与每毫升106~107个的酿酒酵母相比,每毫升105个酿酒酵母在单个图像中的分布数量差异大,进而使计数结果的变异系数大。因此对于低浓度样品需要统计更多的图像才能使计数结果趋于稳定。在本研究中也发现对每毫升105~107个酿酒酵母计数,对应地采集图像数分别大于32、20、12个时计数结果趋于稳定。因此为保证计数结果准确,对每毫升105~107个酿酒酵母分别采集45、30和20个图像。
平板计数与标准微球计数酿酒酵母的结果如表2所示。统计学检验结果显示对于同一样品,两种定量检测结果间均无显著性差异(P>0.05)。另外,如图6所示,两种计数方法的拟合曲线为y=0.954 8x+0.395 5,相关系数R2=0.996 9,说明两者有较好的相关性,即使用标准微球计数的结果也是准确的。

图6 两种计数结果的相关性曲线Fig.6 Correlation curve between the counting results of the two methods
2.3 采集的计数标准微球数量对不同浓度酿酒酵母计数的影响
对于微生物计数,一般要求计数结果应保持在平均值±2SD范围内。另外,计数标准微球法中要求采集微球的总数目不应少于1 000个[25]。实验选取每毫升106个标准微球对每毫升105~107个酿酒酵母进行计数,每个样品进行3次重复,不同标准微球统计量对酿酒酵母计数结果的影响如图7所示。从图7表明,统计的微球总数量分别大于2 000个(采集细胞总数量大于200个)、1 500个(采集细胞总数量大于400个)、1 000个(采集细胞总数量大于2 600个)时,酿酒酵母计数浓度和单个图像中微球的平均数量趋于稳定,标准差逐渐减小。此时图7a~c中单个图像中微球的平均数量分别为68个、69个、72个,表明单个图像中微球的平均数量始终保持在平均值±2SD范围内(69.75±3.93个)。该结果补充了GB/T 39730中需要统计的微球及细胞数量,可更准确、方便获得细胞计数结果。


图7 统计的微球总数量对酿酒酵母浓度和单个图像中微球的平均数量的影响Fig.7 Effect of total statistical amounts of microsphere on the concentration of S.cerevisiae and the average number of microspheres in individual image
3 讨论
在采用标准微球对不同浓度微生物计数时,微球的分散、使用浓度以及对应的统计数量对计数结果有重要意义。已有研究表明微球聚集或取样以及溶液中存在微气泡均会导致计数结果出现偏差[15]。ISO 20391-1:2018中也提到聚集体或凝聚体会导致细胞计数不足,在计数前需制备分散良好的样品。为解决标准微球聚集问题,本研究表明0.08% Tween 20或0.06% Tween 80可有效分散计数标准微球,其较PBS对照组分散指数分别提高了3.32和3.37,微球浓度提高了4倍,表明微球分散均匀对结果的重要作用。这与Chae等[11]的研究成果一致,他认为微球在滤膜表面的分布不均会导致计数有偏差,因此在对微球进行计数时需要保证分布均匀,提高计数结果的准确性。
为确定标准微球用于计数不同浓度细胞时的适宜使用浓度,本研究表明,与每毫升105个微球对每毫升105~107个酿酒酵母计数相比,使用每毫升106个微球得到的计数结果数据稳定。这是因为当微球浓度过低时移取液中微球为泊松分布[26]。依据计数微球粒径,当标准微球的浓度高于每毫升107个时,微球会铺满整个图像进而影响对目标细胞的识别与统计。因此,选择适宜的计数微球浓度可利于结果的准确性,也为计数标准微球的应用提供参数。
此外,对微生物进行直接计数需明确统计数量,如显微镜计数样品至少需要统计400~1 000个细菌细胞[12,27]。通过本研究的统计分析,确立不同浓度细胞需要统计的微球数量,不同于GB/T 39730-2020中统计1 000个微球的要求,表明为准确获得细胞浓度需增加微球数量至2 000个。
本研究将计数标准微球与显微镜图像结合,为微生物快速计数提供了依据。传统的显微镜计数需已知测定的体积或者面积,当载玻片上形成菌膜的具体面积未知时,需要对载玻片上涂片的全部区域进行采集[28]。本实验基于微球计数无需已知计数室体积,利用微球与酿酒酵母的比例进行计数,可在普通的载玻片上或者在不能准确定量计数溶液的体积或过滤面积时进行计数。而传统荧光显微镜计数是基于膜面积进行细菌计数,检测成本高[29,30]。因此可进一步研究在载玻片上采用计数标准微球法代替膜过滤的方法对细菌进行计数。
4 结论
实验表明0.08% Tween 20溶液和0.06% Tween 80溶液对微球的分散效果最佳,分散均匀的标准微球可用于微生物的准确计数。以每毫升105~107个酿酒酵母为分析对象,每毫升106个标准微球对酿酒酵母计数结果的稳定性最好,统计的微球数量分别应不小于2 000、1 500、1 000个,细胞数量分别应不小于200、400、2 600个。在该计数条件下,其计数结果与平板计数结果一致。使用同一标准微球对不同浓度酿酒酵母组计数的单个图像中微球平均数量始终保持在平均值±2SD范围内,可准确获得酿酒酵母浓度,明确了GB/T 39730-2020标准微球使用条件。

