化学课堂中设计问题链培养科学推理能力的策略
张克龙
(瑞安市教育发展研究院, 浙江 瑞安 325200)
教育部颁布的《普通高中化学课程标准(2017年版2020年修订)》明确了化学学科核心素养主要包括“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”“科学态度与社会责任”五个方面[1]。“宏观辨识与微观探析”“证据推理与模型认知”“科学探究”“科学态度”等等素养的培养,均离不开科学推理能力。科学推理一般指:根据一个判断得出另一个判断的思维形式[2]。相关《普通高中物理课程标准(2017年版2020年修订)》的解读中,对“科学推理”做了进一步的分析:科学教育研究和实践中所提出的科学推理,不仅包括逻辑上的归纳推理、演绎推理和类比推理,而且包括分析与综合、抽象与概括、比较与分类等思维方式[3]。
因此,指向素养培育的高中化学教育,作为科学教育的重要分支,理应在课堂上培养学生的科学推理能力,让学习过程具有严密的结构化的逻辑关系,为发展学生学科核心素养提供更广阔的思维训练空间。一门科学真正打动学生的不是形式,而是内涵,真正吸引学生走上这条道路并持之以恒为之奋斗终生的,不是靠科学的好玩和有趣,而是靠科学逻辑的魅力[4]。
但在当下,课堂提问大多数只是关注事实性知识,具有挑战性和创造性的基本问题缺失,问题之间也没有逻辑关系,作为科学教育的科学推理、科学逻辑、科学思维培养无从谈起。比如,盐类水解的课堂教学,教师设计的大多数问题是CH3COONa溶液、NH4Cl溶液pH等于7吗?CH3COONa溶液中c(H+)与c(OH-)相等吗?c(Na+)与c(CH3COO-)相等吗?什么是盐类水解?盐类水解方程式书写要注意哪些事项?预测盐溶液酸碱性方法是什么?Na2CO3水溶液呈碱性还是酸性?水解平衡常数的表达要注意什么?盐类水解的影响因素有哪些?盐类水解在生活生产中有哪些应用?
回答完以上这些问题,虽然也能让学生达成课程标准提出“认识盐类水解的原理和影响盐类水解的主要因素”的学习目标,但问题都是引导学生进行机械记忆,形成的知识是识记型的碎片化知识,导致错过科学推理、科学思维等方面能力培养,诊断与发展学科核心素养的课程目标没有落地。教师应该要安排知识从哪儿来,将到哪儿去的本原性问题,围绕是什么,为什么,怎么样,以什么方法等基本问题,引发学生思考,应用分析、推理、归纳、演绎等高阶思维,能动地开展探究。比如教师可以设计盐类水解的基本问题,形成问题链:什么是弱酸、什么是弱碱,以氨水与醋酸溶液为例说说溶液中存在的微粒,以及这些微粒之间的动态变化(是什么的问题;盐类水解概念哪儿来的问题)。醋酸钠、氯化铵溶液中存在哪些微粒,这些微粒之间会有怎样动态变化(是什么的问题;盐类水解概念哪儿去的问题)。CH3COONa溶液为什么呈碱性,NH4Cl溶液为什么呈酸性,其他弱酸盐、弱碱盐为什么也会有类似水溶液性质(为什么的问题)。CH3COONa溶液、NH4Cl溶液中弱酸根、弱碱阳离子完全与水反应了吗?怎样的化学变化叫盐类水解,怎样表达盐类水解反应方程式(怎么样的问题)。还记得怎样描述可逆反应进行的限度吗?醋酸根水解、铵根离子水解的水解平衡常数如何表达,与对应的弱酸、弱碱的电离平衡常数有怎样关系(怎么样的问题)。用什么方法证明盐类发生了水解,设计实验探究盐类水解影响因素,如何表达盐类水解中各种微粒浓度之间的存在关系,想一想生活用什么试剂除去油污,可以采用哪些措施增进试剂的去油污能力,设计一套简易的泡沫灭火器(什么方法的问题)。通过这样的问题链,引发学生运用分析、推理等高阶思维,不仅发展学生的科学推理能力,更能有效建构盐类水解认知模型,有效达成盐类水解的学习目标,诊断并发展学生微观探析、证据推理、科学探究等学科核心素养水平。
那么,在具体课堂实践中如何设计问题链,培育发展学生的科学推理能力?
一、根据科学推理逻辑环节设计问题链,培育学生的科学推理能力
科学推理是一种过程性素养,也是一种能力思维形式。在培养科学推理能力的教学过程中,需要培养学生归纳、演绎和类比等高阶思维,还要训练学生分析与综合、抽象与概括、比较与分类等思维方式。这些高阶思维的培养与思维方式训练是蕴含在科学推理的逻辑环节中。培养学生科学推理能力课堂问题设计,需要通过对宏观现象或真实情境梳理,转化成需要学生思考,开展探究的问题链,得出宏观现象背后的分子、原子、离子、电子等微观粒子组成、结构、性质、转化等规律,形成概念与规律。
比如,如图1所示将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿棕色铁锈环(b)。对于这个实验现象,大多数的老师会以铁发生吸氧腐蚀搪塞图1中出现的现象。其实,教师可以按照科学推理逻辑环节设计问题链,增进学生对电化学腐蚀的学科理解:此现象发生的金属腐蚀是电化学腐蚀吗?是哪一类腐蚀呢?是简单的吸氧腐蚀吗?能设计实验证实你的猜想吗?铁的生锈部位和腐蚀发生的部位为什么不同呢?沿着此四问为背景,设计能解决问题的问题链(如图2所示),建构金属的电化学腐蚀的结构化认识,发展学生证据推理与模型认知、宏观辨识与微观探析等学科核心素养,培养学生的科学推理能力。比如,帮助学生形成“氧浓差电池腐蚀的原理”认识思路,开展学生科学推理思维可视化的实验探究活动设计如下:

图1 滴有NaCl水溶液的铁板
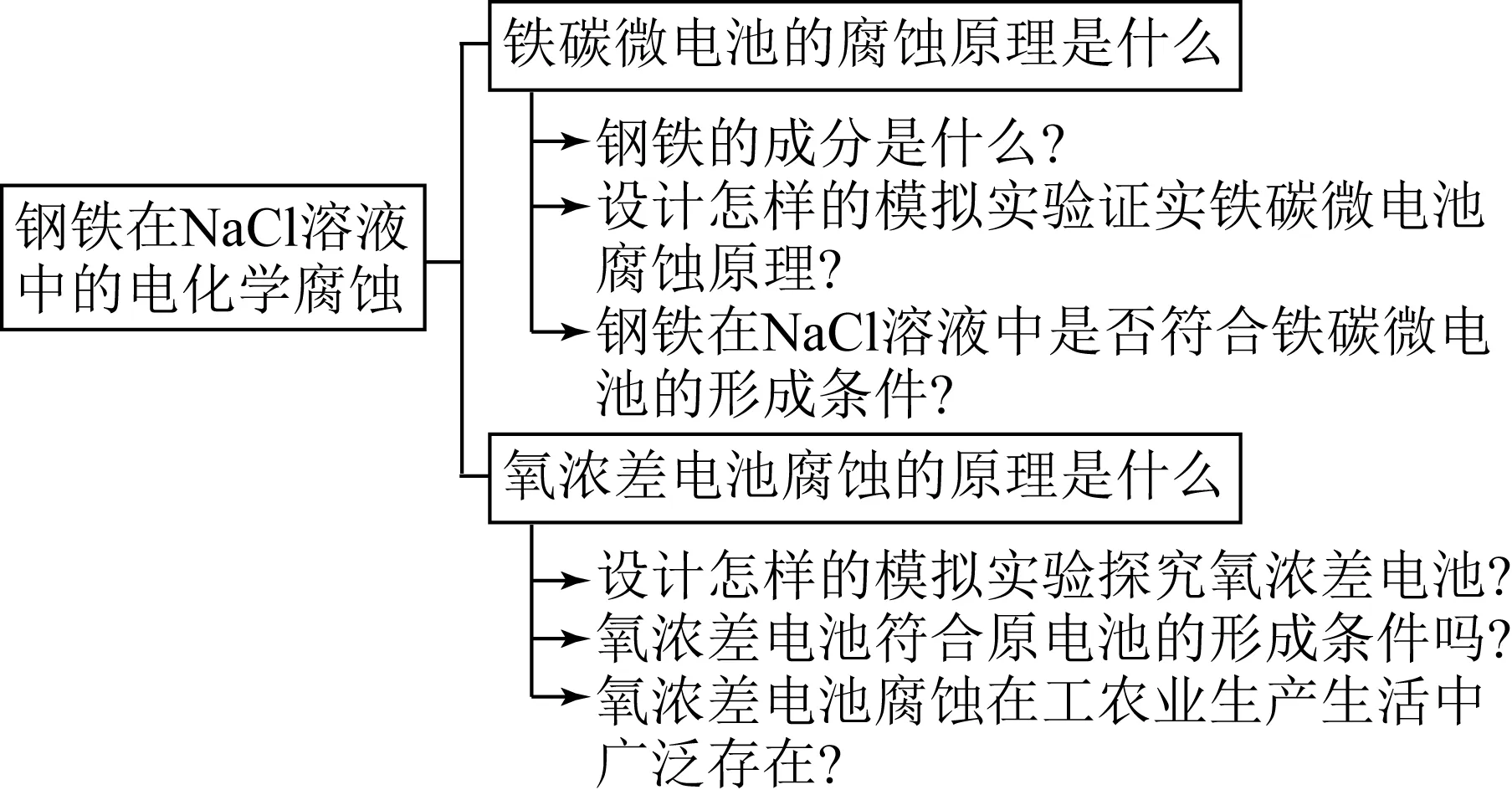
图2 探究钢铁在NaCl溶液中发生电化学腐蚀问题链
【问题1】设计怎样的模拟实验探究氧浓差电池?
【类比:氢氧燃料电池】学生采用类比推理的思维,模仿氢氧燃料双液电池,设计如图3所示的以铁分别作正负电极的双液电池,发现电流指针发生偏转。
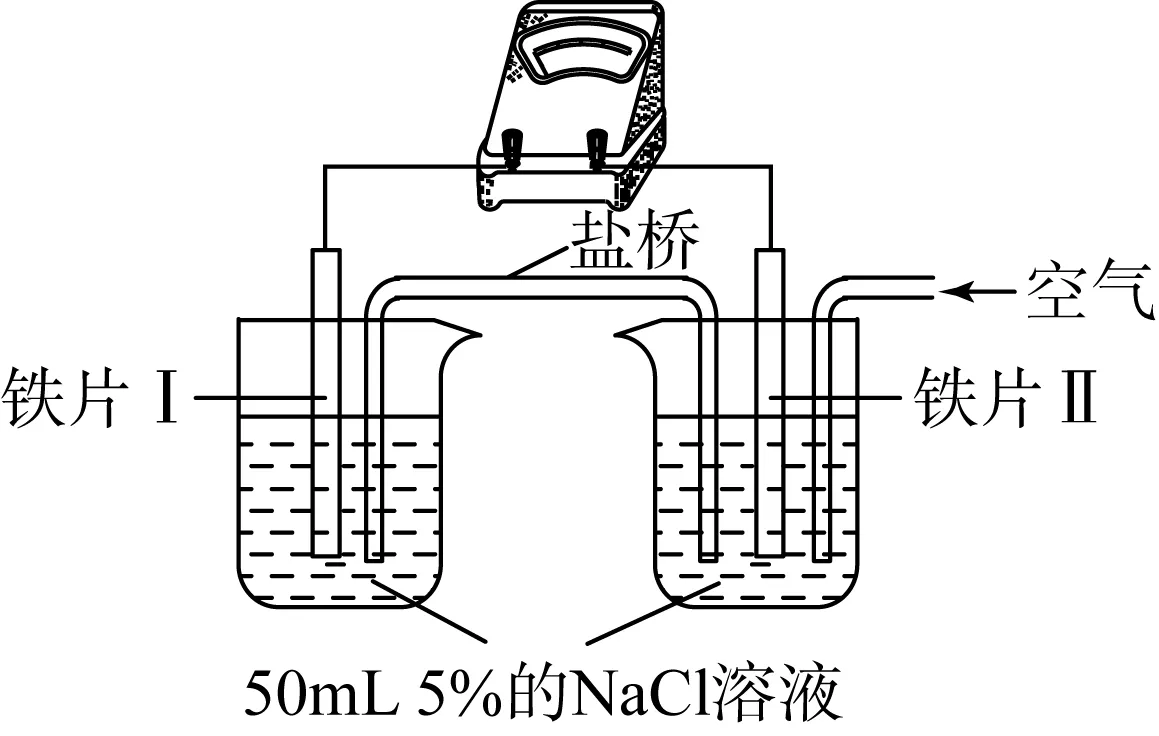
图3 铁片在NaCl溶液中发生氧浓差电池腐蚀
【问题2】图3的氧浓差电池装置符合原电池的形成条件吗?
【分析与综合的思维方式】往图3所示的左边烧杯中加入K3Fe(CN)6溶液检验有FE2+生成,往右边烧杯中加入酚酞检验有OH-生成,电流计指针发生偏转,形成左边铁作负极,右边铁作正极的氧浓差电池认知模型。
【问题3】图1所示的铁是发生了氧浓差电化学腐蚀吗?
【比较与分类的思维方式】学生通过比较图1中(a)与(b)处O2浓度不同,类比图3的氧浓差电池的实验现象,肯定了图1发生的是氧浓差电化学腐蚀。
【问题4】氧浓差电池的腐蚀在工农业生产生活中广泛存在吗?
【演绎、归纳思维,抽象与概括的思维方式】学生通过对图1与图3的归纳分析,抽象与概括出氧浓差电池的4个特征:有O2参加;不同区域的O2浓度不同;活泼金属做电极;腐蚀与生锈分布在2个区域。进一步通过演绎,发现生活中的金属裂缝处的锈蚀,钉在木板中锈蚀了的铁钉,浸入水中的锈蚀铁闸等。
二、设计引发学生探究为什么的问题链,培育学生的科学推理能力
培育学生科学推理能力的课堂与指向学科素养发展的教学是一样的,都是关注化学知识的生长过程,都是基于观察到的现象(或情境),通过模型建构、证据推理、微观探析、科学探究等学科素养训练,形成化学概念、规律,如图4所示。但传统教学中比较关注化学知识是什么,然后应用学到的知识去解决问题,在解决问题的过程中进一步去理解知识的内涵与外延,导致知识的获得是识记型,而不是生长型,学生的科学推理能力培养缺失了场域。因此,教师需要在课堂上设计引发学生探究为什么的问题链,在学生形成化学概念、规律的过程中诊断并发展学生的学科核心素养,培养学生的科学推理能力。如表1所示,引发学生探究“为什么”的问题和传统教学知识识记型问题对比分析。
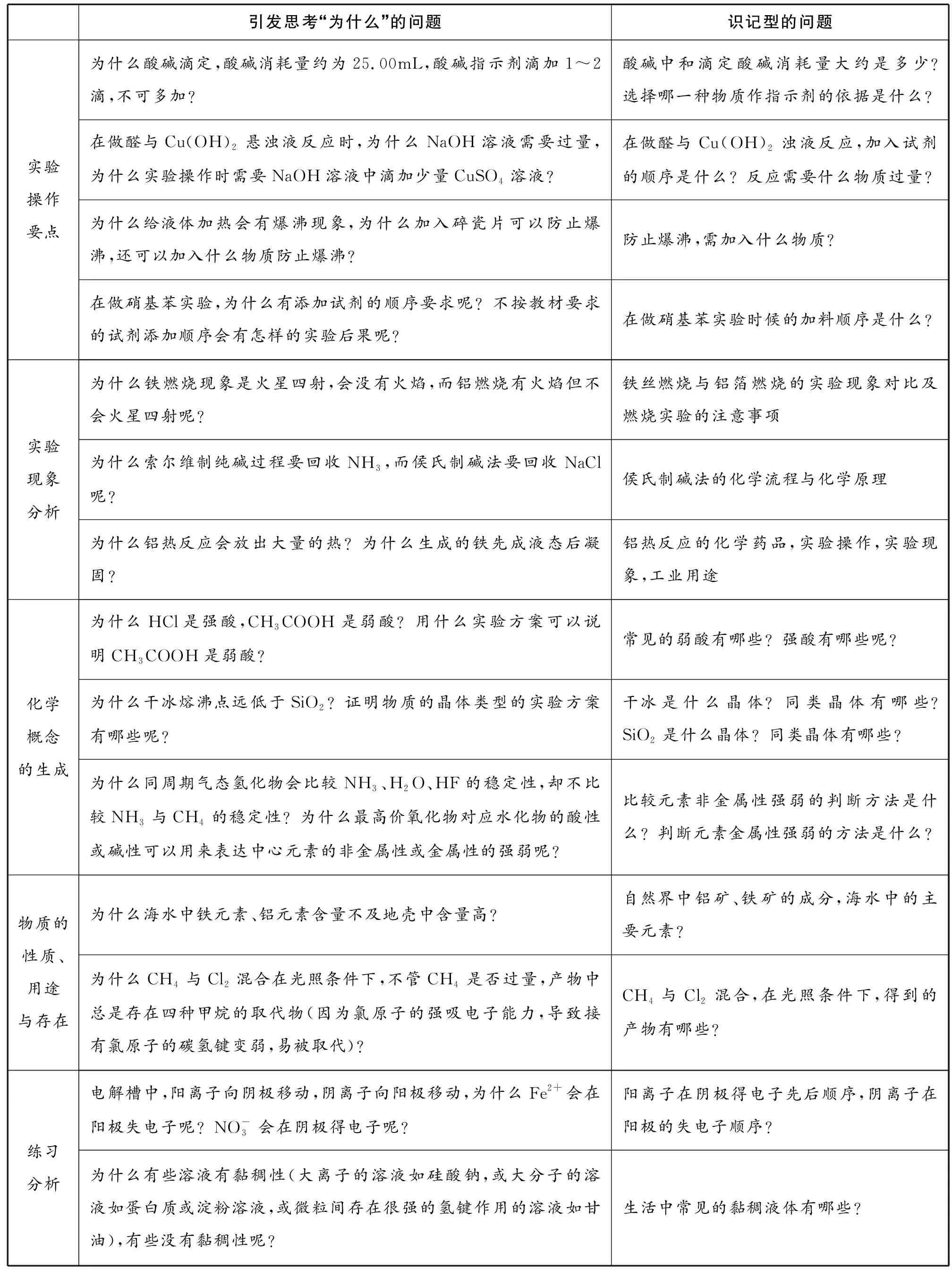
表1 引发学生探究“为什么”的问题和传统教学知识识记型问题对比分析
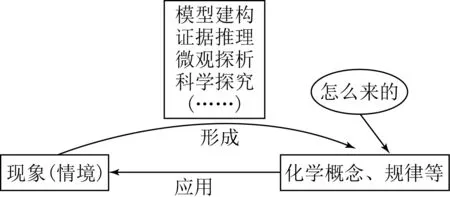
图4 指向科学推理能力培育的课堂结构
为什么的问题不仅能培养学生的理解能力、阐述能力,更是因为会引发学生开展归纳、演绎和类比等高阶思维活动,训练学生分析与综合、抽象与概括、比较与分类等思维方式,诊断并发展学生模型建构、证据推理、微观探析、科学探究等学科核心素养水平,进而培养了学生的科学推理能力。
三、基于真实情境预设适切的问题链,培育学生的科学推理能力
科学推理需要严密的逻辑,因此问题链的设计也必须要逻辑清晰、结构严密。为此,教师需要增进学习内容的学科理解,对课程标准中提出的教学目标要有清晰完整的认知,对学生在学习过程中可能产生的问题站在促进学生科学推理能力培养的角度有较充分的预设。在此基础上,创设真实合适的情境,根据科学推理的逻辑环节设计问题链,让学生通过归纳、演绎和类比等高阶思维,采用分析与综合、抽象与概括、比较与分类等思维方式解决问题,在解决问题的过程中继续生成挑战性问题,增进对所学内容的理解,培养科学推理能力(如图5所示)。
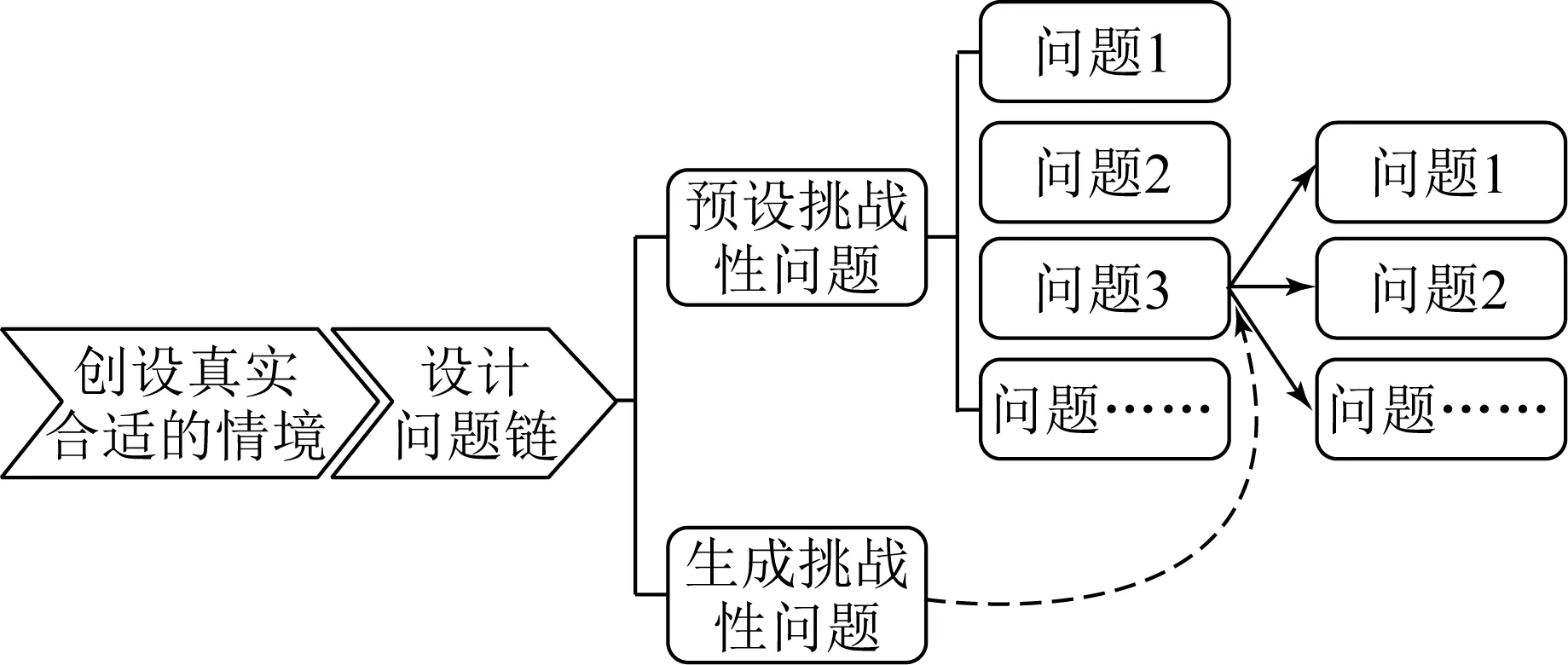
图5 课堂问题链设计的关系图
以人教版《高中化学》必修第二册第六章第二节“化学反应速率”教学为例。传统的教学中,教师会通过迁移物理学科中速率,得出化学反应快慢如何表达,形成化学反应速率概念。接着应用反应速率概念解决练习,通过练习得出同一个反应,不同反应物与生成物之间的速率大小与化学反应的配平系数成正比。
如图5所示,培育学生科学推理能力教学设计,教师应该从生活生产中选择几件涉及化学反应快慢的事件,如爆炸,溶液中离子反应,大多数的有机反应,牛奶变质,铁桥生锈,溶洞形成等,从真实情境,预设挑战性问题链:①化学科学为什么要提出反应速率概念?(why)②怎么样对化学反应速率进行表达?(how)③我们可以从哪些视角表达化学反应速率的快慢?紧接着,教师提出“如何表达相同质量块状与粉末状的CaCO3和等体积等浓度稀盐酸反应的快慢”。学生生成挑战性问题:①观察产生气泡的快慢,可行吗?②观察剩余固体CaCO3的多少,可行吗?③用手触摸反应容器,感受外壁温度的高低,可行吗?④将两种反应分别置于借助托盘天平两边,反应慢的这一边会下沉,可行吗?⑤借助温度计,或密度计,或pH计,或者指示剂等,可行吗?根据学生提出的挑战性问题,开展实验探究,发现①④可行,②③不可行。教师进一步提出挑战性问题:①是哪一种物质在单位时间里什么量的变化来明确反应速率快慢的呢?④中各种情况,又是针对反应体系中哪种物质表达的什么物理量在单位时间里变化来表达反应速率快慢的呢?你认为同一个反应用不同的物质表达反应速率,其速率之间有关系吗?通过这样的科学推理的思维显性教学,让学生在真实情境中体会化学学科开展化学反应速率研究的价值与意义,理解反应速率表达方法的内涵与外延,经历化学反应速率用反应物或生成物浓度在单位时间的变化来表达的概念生成过程,明确同一个反应,不同反应物与生成物之间的速率大小与化学反应的配平系数成正比等,不仅建构了结构化的化学反应速率概念认识,而且诊断并发展了证据推理与模型认知,宏观辨识与微观探析等学科核心素养的发展。
打个比方,非科学推理的教学,就像跟团旅游,学生是从中间某个点(化学反应速率概念的模型)上车的。而采用培养科学推理能力培养的教学,学生几乎是从起点(生活与生产中纷繁复杂的化学反应)上车的,这样做的优点是:①能让学生体验到“化学源于生活”,②学生亲身经历了概念的科学推理过程,而这往往是我们从化学视角认识“众多生活与生产中的化学现象”的第一步。
四、根据课堂学生反馈生成问题链,培育学生的科学推理能力
当下的大多数课堂,学生是沿着教师预设的学习过程开展学习,教师不能了解学生的想法,导致学生缺乏持续学习的动力,被动接受知识,课堂不仅难以达到最佳思维碰撞的教与学状态,而且因为缺失学生对学习内容的质疑,缺失学生自己提出有挑战性的问题,导致科学推理能力培养缺失学生自我生长的场域,因此,笔者结合图5的课堂设计问题链的设计思路,提出如图6所示的根据课堂学生反馈生成问题链,培养学生科学推理能力设计思路。
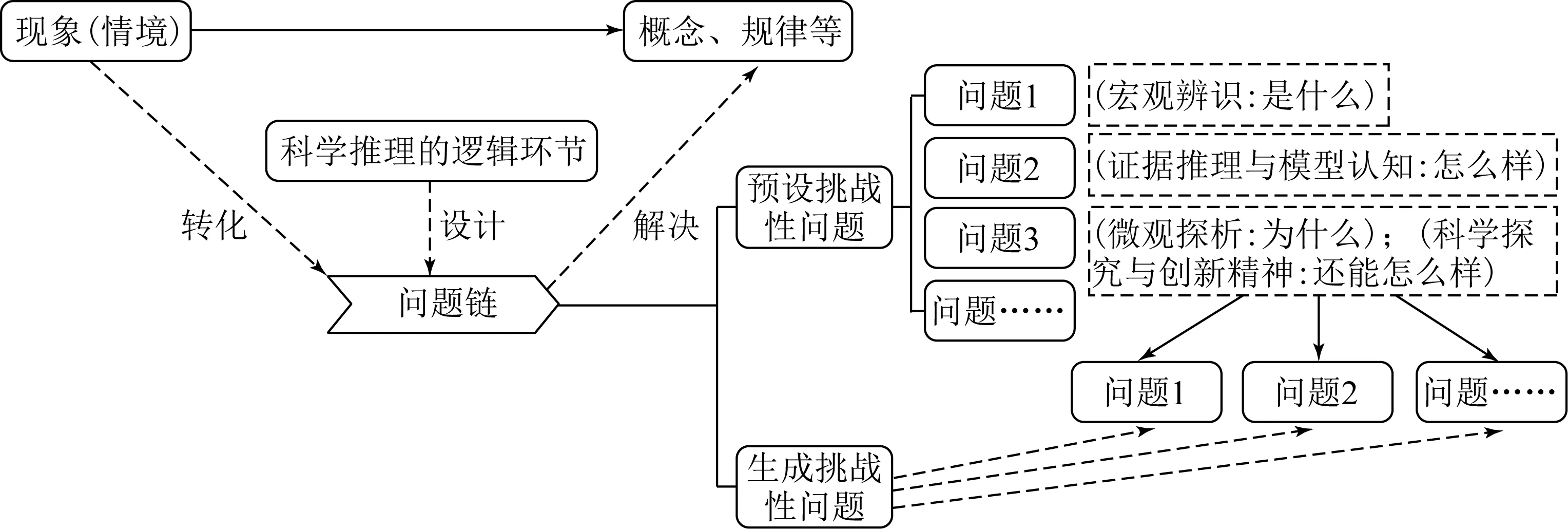
图6 根据课堂学生反馈生成问题链的设计思路
以人教版选择性必修1《化学反应原理》第三章第一节“强电解质和弱电解质”教学为例,教材P56实验3-1的目的是探究“CH3COOH是弱电解质”,安排了3个比较实验,分别是浓度都是0.1moL/L HCl与CH3COOH,比较它们的pH的大小,导电能力强弱,与镁条反应的快慢,得出等同浓度盐酸与醋酸溶液中H+是不同的,CH3COOH只有部分发生电离,形成结论说醋酸是弱电解质,但这样的学习过程,对于学生而言,还完全不能够建立弱电解质电离是动态的可逆过程,即未电离的醋酸分子还能继续电离,已电离出的醋酸根离子与溶液中氢离子会重新结合成醋酸分子。因此,教师要根据教学中重难点,结合学生的课堂反馈,动态生成挑战性问题链,组织学生进行科学推理。具体按照图6所示的教学设计思路:
【现象(情境)】盐酸与醋酸是生活与生产中常见的酸,请同学们举一些生活与生产中的例子,说说这两种酸腐蚀性,参加反应速率的快慢,酸性强弱。
【按照科学推理的逻辑环节设计问题链】
问题1:盐酸与醋酸从分类的角度讲,属于哪一类物质(属于酸)?理由是什么(电离出的阳离子都是H+)?根据生活与生产中的实例,盐酸与醋酸的酸性有区别吗(宏观辨识:是什么的问题)?
问题2:设计实验方案,证明醋酸在水溶液不能完全电离(证据推理与模型认知:怎么样的问题)。
学生:开展教材中3-1实验,测等浓度盐酸与醋酸的pH,导电能力,与镁条反应等。得出结论醋酸在水溶液中没有完全电离。
【生成挑战性问题】
问题3:为什么醋酸没有完全电离呢?还没有电离的醋酸分子会电离吗?能用实验方法证明已电离出的醋酸根与氢离子会结合醋酸分子吗?能用实验证实未电离的醋酸分子还能继续电离吗?还能有其他方法证明醋酸分子在水溶液建立动态的可逆电离过程吗?(属于学生课堂质疑,开展微观探析,产生为什么的科学推理过程,也是激发学生产生还能怎么样的科学推理、科学探究与科学创新的过程。)
从以上教学设计可知,教师通过设计问题链引导学生逐步分析、推理建构起弱电解质动态可逆电离的结构化认识过程中,体验了用科学推理是分析揭示物质变化的重要方法和思维方式,感受了严谨认真、敢于质疑的科学态度。
科学推理能力是从科学视角解决真实问题的关键能力,从长远的学生发展角度来讲,培养学生的科学推理能力比掌握一些化学知识更具有普遍的价值。开展基于问题链培养学生科学推理能力的课堂教学,对教师的专业素养提出很高的要求,教师需要进一步增进化学学科理解,从学科溯源的角度,设计本原性、结构化认识的一整串问题链,同时需要从单元的视角、某一素养进阶发展要求等不同的角度,进行大问题链的设计,整体规划对学生科学推理能力的培养。

