2型糖尿病患者肥胖相关指标与糖尿病肾病的关系探讨
蔡艳云,徐静
(1.陕西省黄陵县人民医院,陕西 延安 727300;2.西安交通大学第二附属医院,陕西 西安 710000)
糖尿病(Diabetes Mellitus,DM)是一组多病因性代谢性疾病,其发病原因为胰岛素分泌不足和(或)作用缺陷,临床上以慢性血糖升高为主要特征。近30多年来,我国糖尿病的发病率显著增高,根据流调显示,我国糖尿病患者人数已经位居全球第一,其患病率高达11.6%,约1.14亿例[1],其中2型糖尿病(type 2 diabetes mellitus,T2DM)占90%以上,而糖尿病的并发症已逐渐成为患者致残、致死及医疗成本加重的主要原因,其中糖尿病肾病(diabetic kidney disease,DKD)为常见的重要微血管病变之一,在我国糖尿病肾病的患病率约为20%-40%[2]。
糖尿病肾病(diabetic kidney disease,DKD)是糖尿病微血管并发症的一种,是在长期高血糖基础上出现的慢性肾脏病(chronic kidney disease,CKD),临床上以白蛋白尿和(或)肾小球滤过率(estimated glomerular filtration rate,eGFR)下降持续超过3个月为主要特征[3]。既往研究中提出,糖尿病肾病的发生、发展是多种危险因素共同作用的结果,其危险因素包括不良生活习惯、年龄、病程、血糖、血压、肥胖(尤其是腹型肥胖)、血脂、环境污染物等。
肥胖是一种慢性代谢性疾病。近年来肥胖人数急剧增长,肥胖已成为全球问题。肥胖不仅给个人带来了严重的健康问题,同时也给家庭和社会增加了更大的经济负担。肥胖现已成为主要的医学社会问题,而在我国,随着人民生活水平的迅速提高,肥胖的患病率也呈快速升高趋势[4]。有关流行病学调查发现,我国居民已有近1/4合并超重或肥胖,且这一趋势在大城市远高于小城市及农村。
1 资料与方法
1.1 临床资料 选取2017年6月-2018年6月在我院内分泌科住院的、资料完整的糖尿病患者870例为研究对象,所有受试者均确诊为2型糖尿病。现根据研究对象的尿白蛋白与肌酐比值(UACR)水平分为糖尿病肾病组(UACR≥30mg/g,共264例)和非糖尿病肾病组(UACR<30mg/g,共606例)。本研究经医院伦理委员会审批通过。
1.2 诊断标准
1.2.1 糖尿病肾病的诊断标准 根据《中国2型糖尿病防治指南(2020年版)》,糖尿病肾病常常是根据持续存在的尿白蛋白与肌酐比值(UACR)增高和(或)肾小球滤过率(eGFR)下降、同时排除其他慢性肾脏病(chronic kidney disease,CKD)而作出的临床诊断。
1.2.2 肥胖的诊断标准 ①根据《肥胖症基层诊疗指南(实践版2019)》[4]对BMI、WC诊断标准总结见表1、表2。②根据中国肥胖工作组制定的标准[5],以WHR男性≥0.90、女性≥0.85为中心型肥胖(见表3)。③国际上大多采用WHtR>0.5作为中心型肥胖的评判标准,我国中年人群中心型肥胖评价标准也采用以上标准。根据腹型肥胖的新指标及其临床意义,以0.5作为WHtR的正常值切点值,WHtR≥0.5为中心型肥胖。④内脏脂肪指数VFI=内脏脂肪面积(cm2)/10cm2,分30个等级,四个等级段,分别是:1-9正常;10-14偏高;15-29高;30很高。将VFI指数>15定义为肥胖。⑤体脂肪率TBF又称体脂百分比,是体内脂肪质量占总体质量的比值,可直接反映人体脂肪含量与比例。WHO提出判定中心型肥胖的TBF切点为:男性≥25.0%,女性≥30.0%(见表4)。

表1 BMI值诊断肥胖的标准

表2 WC诊断中心型肥胖的标准

表3 WHR诊断中心型肥胖的标准

表4 TBF诊断中心型肥胖的标准
1.3 排除标准 其他3种类型的糖尿病,包括1型糖尿病(type 1 diabetes mellitus,T1DM)、妊娠期糖尿病(gestational diabetes mellitus,GDM)及其他特殊类型糖尿病;合并糖尿病急性代谢紊乱,包括糖尿病酮症酸中毒(diabetic ketoacidosis,DKA)、高渗性高血糖状态(hyperglycemic hyperosmolar status,HHS);或合并其他系统急性感染者;已经确诊合并原发性肾脏疾病者;合并其他原因所致的蛋白尿,如运动、心力衰竭、泌尿系感染等;资料收集不完整者。
1.4 方法
1.4.1 一般指标 收集两组受试者的一般项目(年龄、糖尿病病程、高血压病程);相关的实验室检查,研究对象连续禁食8-10h后,第二天早晨采集静脉血,以收集统计患者的相关实验室指标,用于检测空腹血糖、血脂,以上检测均采用全自动生化仪测定;糖化血红蛋白(glycated hemoglobin A1c,HbA1c)采用高效液相色谱法测定;研究对象的尿白蛋白/肌酐比值(UACR)采用散射比浊法实施检测。
1.4.2 肥胖指标 所有患者均脱鞋,测量身高、体重、腰围(WC)、臀围,计算BMI、WHR及WHtR。VFI及TBF测量:采用BCA-2A人体成分分析仪,使用直接节段多频率生物电阻抗(DSM-BIA)测量法,对患者相关指标实施检测,要求患者空腹,测量前排空大小便,运动后休息至少30分钟、维持站立姿势约15分钟左右,测量之前将身上手机、钥匙、项链、戒指、手链、钢笔等金属制品全部取下,脱去鞋袜,站立于人体成分分析仪测量体重,输入身高、年龄、性别,握住手柄电极按要求位置站立测量,测量VFI、TBF。
1.5 统计学分析 数据采用SPSS23.0软件分析,其中计量资料采用(±s)表示,组间比较使用独立样本t检验;计数资料采用频数(n)表示,组间比较使用卡方检验。之后通过单因素Logistic回归分析寻找与糖尿病肾病相关的危险因素,然后以多因素Logistic回归分析与糖尿病肾病相关的危险因素,构建回归模型,绘制ROC曲线。
2 结果
2.1 糖尿病肾病组和非糖尿病肾病组一般指标的比较 两组患者中糖尿病肾病组的年龄、糖尿病病程、高血压病程、HbA1c、总胆固醇(Total cholesterol,TC)、低密度脂蛋白胆固醇(low density lipoprotein,LDL)高于非糖尿病肾病组,具有统计学差异(P<0.05);糖尿病肾病组和非糖尿病肾病组在空腹血糖(Fasting plasma glucose,FPG)、甘油三酯(triglyceride,TG)、高密度脂蛋白胆固醇(high density lipoprotein,HDL)水平方面无统计学差异(P>0.05)。详见表5。
表5 糖尿病肾病组和非糖尿病肾病组一般指标比较(±s)
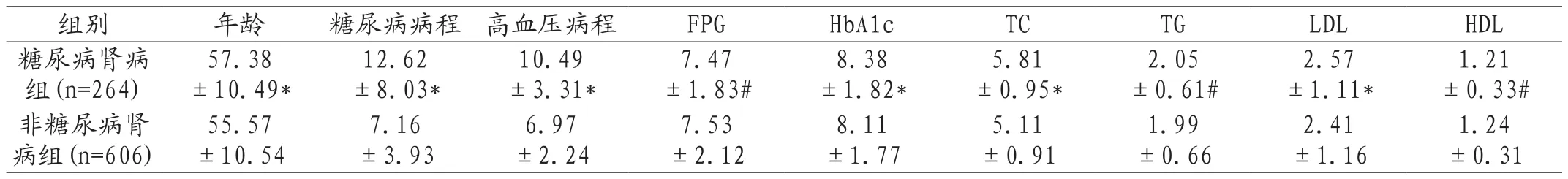
表5 糖尿病肾病组和非糖尿病肾病组一般指标比较(±s)
注:和非糖尿病肾病组相比,*P<0.05;#P>0.05。
组别年龄糖尿病病程高血压病程FPGHbA1cTCTGLDLHDL糖尿病肾病组(n=264)1.21±0.33#非糖尿病肾病组(n=606)57.38±10.49*12.62±8.03*10.49±3.31*7.47±1.83#8.38±1.82*5.81±0.95*2.05±0.61#2.57±1.11*55.57±10.54 7.16±3.93 6.97±2.24 7.53±2.12 8.11±1.77 5.11±0.91 1.99±0.66 2.41±1.16 1.24±0.31
2.2 肥胖指标与糖尿病肾病的关联分析
2.2.1 糖尿病肾病组和非糖尿病肾病组肥胖指标的比较 和非糖尿病肾病组比较,糖尿病肾病组的BMI、WC、WHtR、WHR、VFI、TBF均高于非糖尿病肾病组,具有统计学差异(P<0.05)。详见表6。
表6 糖尿病肾病组和非糖尿病肾病组肥胖指标的比较(±s)

表6 糖尿病肾病组和非糖尿病肾病组肥胖指标的比较(±s)
注:和非糖尿病肾病组相比,*P<0.05。
组别BMIWCWHtRWHRVFITBF糖尿病肾病组(n=264)26.50±3.60*94.84±10.46*0.58±0.06*0.94±0.05*16.94±2.65*31.41±6.41*非糖尿病肾病组(n=606)24.15±2.8388.92±8.850.53±0.050.91±0.0514.07±1.9523.73±5.06
2.2.2 肥胖指标水平对糖尿病肾病影响的单因素分析 以BMI≥28(kg/m2)、WC(男性≥90cm,女性≥85cm)、WHtR≥0.5、WHR(男性≥0.90,女性≥0.85)、VFI≥15、TBF(男性≥25%,女性≥30%)水平定义肥胖,分析肥胖相关指标与糖尿病肾病的关系。
以是否并发糖尿病肾病为因变量,以各肥胖指标为自变量,采用单因素Logistic回归分析与糖尿病肾病发生相关的肥胖指标。单因素分析结果显示,以上相关肥胖指标均为糖尿病肾病发生的危险因素。详见表7。
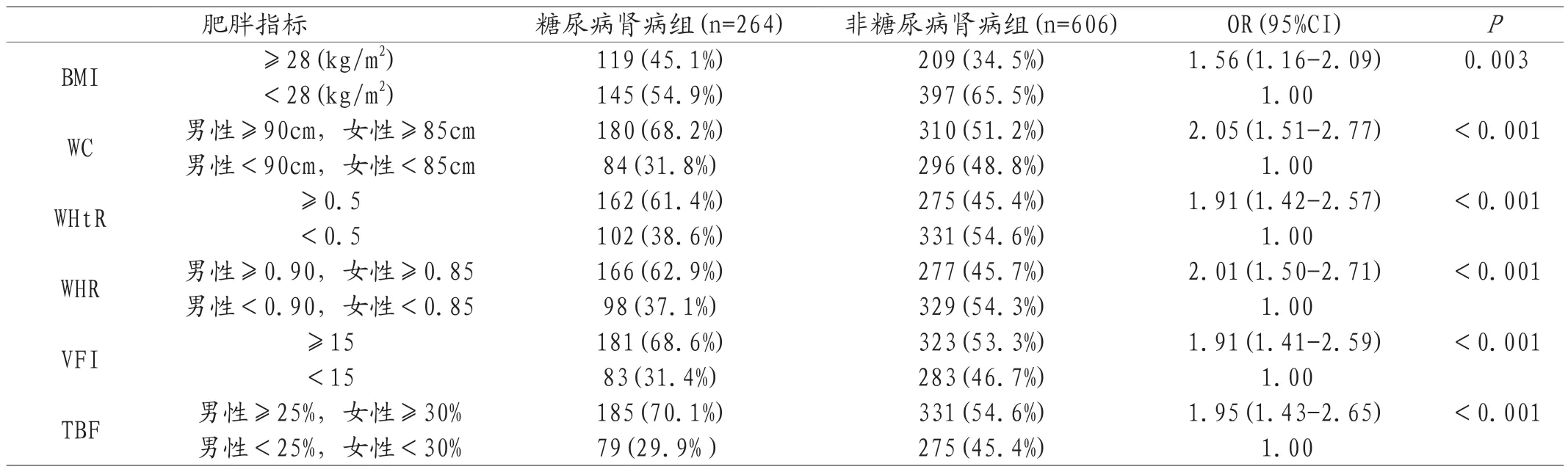
表7 肥胖指标水平对糖尿病肾病影响的单因素分析
2.2.3 肥胖指标与糖尿病肾病关联的多因素分析 通过多因素回归分析,将是否合并糖尿病肾病视为因变量。以各肥胖指标为自变量,校正协变量后,进行多因素Logistic回归模型显示,在校正了协变量的影响后,WC、WHtR、WHR、VFI、TBF为糖尿病肾病发生的独立危险因素。详见表8。

表8 肥胖指标与糖尿病肾病关联的多因素分析
2.3 Logistic回归模型的ROC分析 ROC曲线显示运用糖尿病病程、WC、WHtR、WHR、VFI、TBF共6个变量建立的完全预测模型,曲线下面积(Area under curve,AUC)为0.899,95%可信区间为0.873-0.925,灵敏度为72.25%,特异度为90.40%。详见图1。

图1 Logistic回归模型的ROC分析
3 讨论
在我国,肥胖现已成为严重的健康问题,随着社会发展、经济进步及人们饮食结构的改变,导致我国肥胖患病率逐年升高,其中成人超重患者占27.8%,成人肥胖患者占5.5%。我国部分中心城市的肥胖患病率增长更加迅速,甚至已经高于美国等发达国家。而肥胖与糖尿病、高血压及心脑血管疾病的发生均具有一定的相关性,多项临床研究及流行病学调查发现,糖尿病及糖尿病肾病发生的一个重要的危险因素即为肥胖[6]。现有的研究中,以BMI、WC、WHtR、WHR作为衡量肥胖的指标,分析其与糖尿病及糖尿病肾病的相关性研究较多,且已发现以上肥胖指标与2型糖尿病患者糖尿病肾病的发生存在密切关系。
此次研究中,BMI、WC、WHtR、WHR、VFI及TBF均属于肥胖的评价指标,研究中针对870例糖尿病患者展开分析,分析以上各肥胖指标与糖尿病肾病的关系,发现糖尿病肾病组各肥胖指标均偏高,两组对比具有统计学差异(P<0.05),但在多因素Logistic回归中校正了年龄、糖尿病病程、血糖、血脂等协变量后,发现BMI在两组之间无统计学差异(P>0.05),而WC、WHtR、WHR、VFI及TBF是糖尿病肾病的独立危险因素,经过本次研究能够发现,糖尿病肾病中腹型肥胖是一个主要影响因素。考虑BMI为体重与身高计算的结果,因受人群种族及性别、年龄等不同的影响,相互之间比较,存在一定的偏差,且因其未涉及脂肪分布部位的情况,故不能很好地反映肥胖的特点,对于脂肪分布情况也无法有明确认识,体内的脂肪组织分布情况会导致肥胖本身具有差异,所以脂肪储积部位不同对糖尿病肾病发生的影响也存在差异。由此可见,和全身肥胖相比,腹型肥胖对糖尿病肾病的影响更大。
而在腹型肥胖相关指标中,传统的人工测量方法[7]主要有WC、WHtR、WHR等,因实施检测者的不同均存在一定的测量误差,精确度差。而其中WC只考虑了腰围的大小,其他影响因素不能很好地同时反映;WHtR及WHR无法区分脂肪为皮下脂肪或是内脏脂肪;而VFI是衡量中心型肥胖的重要指标之一,VFI=VFA(cm2)/10cm2,与内脏脂肪组织的面积有关;TBF是指人体脂肪与体重的百分比,不仅可以评估人体的肥胖程度,还可以发现一些隐性肥胖的患者。
目前对VFI及TBF的测定有MRI、CT、DEXA、超声、生物电阻抗法等,MRI和CT虽然精确度高,但考虑其辐射大、花费高,故难以用于临床筛查;DEXA测试设备的要求较高、体积大,不便携带;超声可以可靠地估计腹部脂肪厚度,但在测量脂肪组织面积方面的有效性和可靠性尚需进一步研究;而在此次研究中,通过人体成分分析生物电阻抗法测定VFI及TBF可以更好地反映内脏脂肪情况,是一种通过电学方法测定人体成分的技术,其工作原理是通过借助置于体表的电极系统向人体送入微弱的交流电信号,利用人体各组织的导电性不同来推测人体各成分在体内的含量,可用于量化内脏脂肪,且具有经济、简便、无辐射、可动态监测的优势,同时受身高影响小,无性别差异,弥补了上述不足,能更好地反映腹部脂肪分布的情况,对临床工作提供了更加方便及适用的方法,能更好地用于临床工作[7-8]。
综合以上分析后,本研究将有意义的指标纳入回归模型,构建回归方程,Logistic回归分析模型对糖尿病肾病发生风险进行预测的ROC曲线下面积为0.899,95%可信区间为0.873-0.925,灵敏度为72.25%,特异度为90.40%。但还需要进一步的临床实验来证实其在临床中的应用价值。
综上所述,肥胖和糖尿病肾病的发生存在密切关系,尤其是腹型肥胖相关指标。在肥胖诊断中,单纯实施BMI检测存在一定不足,因此可以和WC等腹型肥胖指标检测相结合,以实现对肥胖2型糖尿病患者糖尿病肾病发生风险的预测,有助于早期预防和干预,以期降低患者糖尿病肾病的发病率,也可以对糖尿病肾病患者生活质量起到改善作用。在临床治疗过程中也可以结合患者的体脂分布特点以及临床特征实施针对性治疗。对于腹型肥胖2型糖尿病患者,则需要注重改变自身饮食结构,提高饮食合理性,增加体育运动,以实现对糖代谢紊乱及腹型肥胖的有效控制,从而可以实现对糖尿病肾病的预防以及缓解,降低患者的残疾率和死亡率[9-10]。

