基于RhoA/ROCK通路探讨电针心包经穴对急性脑缺血大鼠神经轴突生长抑制因子的影响
唐雅妮,肖豆 ,马文娟 ,谢峥嵘 ,潘江 ,娄必丹 ,章薇 ,陈成
1.长沙民政职业技术学院,湖南 长沙 410004;2.湖南中医药大学第一附属医院,湖南 长沙 410007;3.同济大学附属杨浦医院,上海 200090;4.长沙市中医医院,湖南 长沙 410100
急性脑缺血是由不同原因导致大脑供血动脉狭窄或闭塞而出现脑部供血障碍,继而引起神经功能障碍或脑组织缺血性坏死,是脑卒中最常见的类型,约75%的患者会发生与神经相关的功能障碍[1-2]。脑缺血后功能的恢复与神经修复和再生有关[3],缺血损伤后神经生长抑制因子表达升高是导致神经再生障碍的关键原因[4]。研究发现,Ras同源基因家族成员A(RhoA)及其下游效应因子Rho相关卷曲螺旋形成蛋白激酶(ROCK)Ⅱ参与神经轴突出芽、生长等生理过程,RhoA/ROCK通路可以调控神经轴突损伤后的再生[5]。针灸作为补充和替代疗法,能有效治疗缺血性脑卒中[6-8],改善神经功能缺损及相关功能障碍[9],通过调节中枢神经系统,特别是神经再生、修复和改善神经元突触功能,对脑缺血损伤产生有益影响[10-12]。本研究在前期研究[13-16]基础上,从RhoA、ROCKⅡ角度探讨电针心包经穴对急性脑缺血大鼠的神经修复作用及机制,为临床从心治脑提供实验依据与相关理论基础。
1 材料与方法
1.1 动物
SPF级成年雄性SD大鼠90只,体质量(235±15)g,购自湖南斯莱克景达实验动物有限公司,动物许可证号SCXK(湘)2016-0002。饲养于温度(22±2)℃、相对湿度55%~70%环境,自然光照,适应性饲养1周后开始实验,造模前禁食24 h。
1.2 主要试剂与仪器
大鼠RhoA ELISA试剂盒(上海酶联,货号ml038156),ROCKⅡ ELISA试剂盒(武汉华美,货号CSB-EL020059RA),二步法试剂盒(北京中杉金桥,货号PV-9003),DBA试剂盒(北京中杉金桥,货号ZLI-9018),β-actin抗体(美国Proteintech,货号66009-1-Ig),RhoA抗体(美国Proteintech,货号10749-1-AP),ROCKⅡ抗体(美国Proteintech,货号21645-1-AP),HRP标记羊抗鼠二抗(美国Proteintech,货号SA00001-1),HRP标记羊抗兔二抗(美国Proteintech,货号SA00001-2),反转录试剂盒(中国北京康为世纪,货号CW2569),Trizol(美国Thermo,货号15596026)。0.30 mm×15 mm一次性华佗牌毫针、SDZ-Ⅱ型华佗电针治疗仪(苏州医疗用品厂有限公司);H1650R型台式高速冷冻离心机(湖南湘仪);PW-812型全自动酶标洗板机(深圳汇松);MB-530型多功能酶标分析仪(深圳汇松);PIKO REAL 96型荧光定量RCP仪(美国Thermo);SPL0960型荧光PCR板(美国Thermo);DYY-6C型电泳仪(北京六一);DYCZ-40D型转膜仪(北京六一)。
1.3 分组与造模
采用随机数字表法将90只大鼠随机分为空白组18只、假手术组18只、造模组54只。造模成功后,将造模组随机分为模型组、心包经组和肺经组,每组18只。各组再随机分配至干预7、14、21d 3个时间点,每个时间点6只。
根据Zea Longa方法[17],并结合前期研究[13-16],采用颈外动脉插入线栓法建立大脑中动脉栓塞(MCAO)模型。空白组仅捆绑处理,假手术组只分离血管不插入栓线。造模完成后24 h采用Zea Longa 5级4分制评分法对大鼠进行神经功能缺损评分,选取评分为1~3分大鼠纳入实验。
1.4 干预
根据手三阴经“从胸走手”循行方向,选取大鼠瘫痪侧肢体不同神经节段的常用腧穴代表心包经和肺经。以“天泉”“曲泽”“内关”“大陵”代表心包经、“天府”“尺泽”“列缺”“太渊”代表肺经,腧穴定位参照《实验针灸学》[18]。造模成功后次日开始针刺,毫针刺入大鼠上肢瘫痪侧穴位,针刺深度3~4 mm,接电针治疗仪。心包经组以“天泉”“曲泽”为一组,“内关”“大陵”为一组;肺经组以“天府”“尺泽”为一组,“列缺”“太渊”为一组。正极接近心端腧穴,负极接远心端腧穴,选用连续波,频率20 Hz,输出电压2~4 V,电流强度4~6 mA,以大鼠上肢轻颤为度,刺激时间30 min/次,连续干预6 d,间隔1 d,共21 d。
1.5 指标检测
1.5.1 HE染色
干预结束后,大鼠用10%水合氯醛(0.3 mL/100 g)腹腔注射麻醉,断头,取梗死区脑组织,用乙醇和二甲苯脱水,石蜡包埋并切片,烤片脱蜡,水化后用苏木精-伊红染色,树胶封片,显微镜下观察。
1.5.2 ELISA检测
大鼠麻醉处死后,取腹主动脉血4~5 mL,4 ℃、3000 r/min离心15 min,分离血清,按照ELISA试剂盒说明书操作,根据标准品的吸光度制作标准曲线,计算血清RhoA、ROCKⅡ含量。
1.5.3 免疫组化染色
按照免疫组化试剂盒说明操作,标本采集后常规制作石蜡切片,抗原热修复后滴加RhoA、ROCKⅡ一抗(1∶200),4 ℃孵育过夜,滴加二抗(1∶200),37 ℃孵育30 min,DAB显色,苏木素复染,各级乙醇脱水,中性树胶封片,显微镜下观察梗死区脑组织阳性表达(黄色、棕黄色或褐色染色),每张切片随机观察5个不重叠视野,采集图像后用Image-Pro Plus 6.0软件测定阳性表达的平均光密度。
1.5.4 RT-PCR检测
取梗死区脑组织,提取组织总RNA,紫外分光光度计测定浓度,将RNA反转录合成cDNA,进行RTPCR扩增,运用primer5软件设计引物(见表1)。以β-actin为内参,2-ΔΔCt法计算mRNA相对表达量。

表1 各基因PCR引物序列
1.5.5 Western blot检测
取梗死区脑组织,每100 mg组织加入RIPA裂解液1 mL,吸取上清液,用BCA法测定蛋白浓度。加入上样缓冲液加热、变性后,进行电泳,转移至NC膜,5%脱脂奶粉室温密封60 min,加入RhoA一抗(1∶1000)、ROCKⅡ一抗(1∶3000)、β-actin一抗(1∶5000),4 ℃孵育过夜。洗膜,与HRP标记二抗室温孵育90 min。用ECL化学发光液曝光后显影。采用Quantity One软件分析条带灰度值,以目标蛋白与内参蛋白的灰度值比值计算目标蛋白相对表达量。
1.6 统计学方法
采用SPSS22.0统计软件进行分析。计量资料以±s表示,数据符合正态分布用方差分析,方差齐用LSD法,方差不齐用Tambane's T2 或Games-Howell法;不符合正态分布用多个独立样本比较的秩和检验。P<0.05表示差异有统计学意义。
2 结果
2.1 电针对模型大鼠梗死区脑组织病理形态的影响
空白组、假手术组大鼠脑组织神经元结构完整,细胞胞浆丰富,核仁清晰;模型组大鼠脑组织神经细胞数量减少,细胞核固缩,间质染色稀疏;与模型组比较,心包经组和肺经组大鼠脑组织神经细胞形态有所改善,核固缩程度减轻,神经元数量增加,心包经组改善更为明显。见图1。
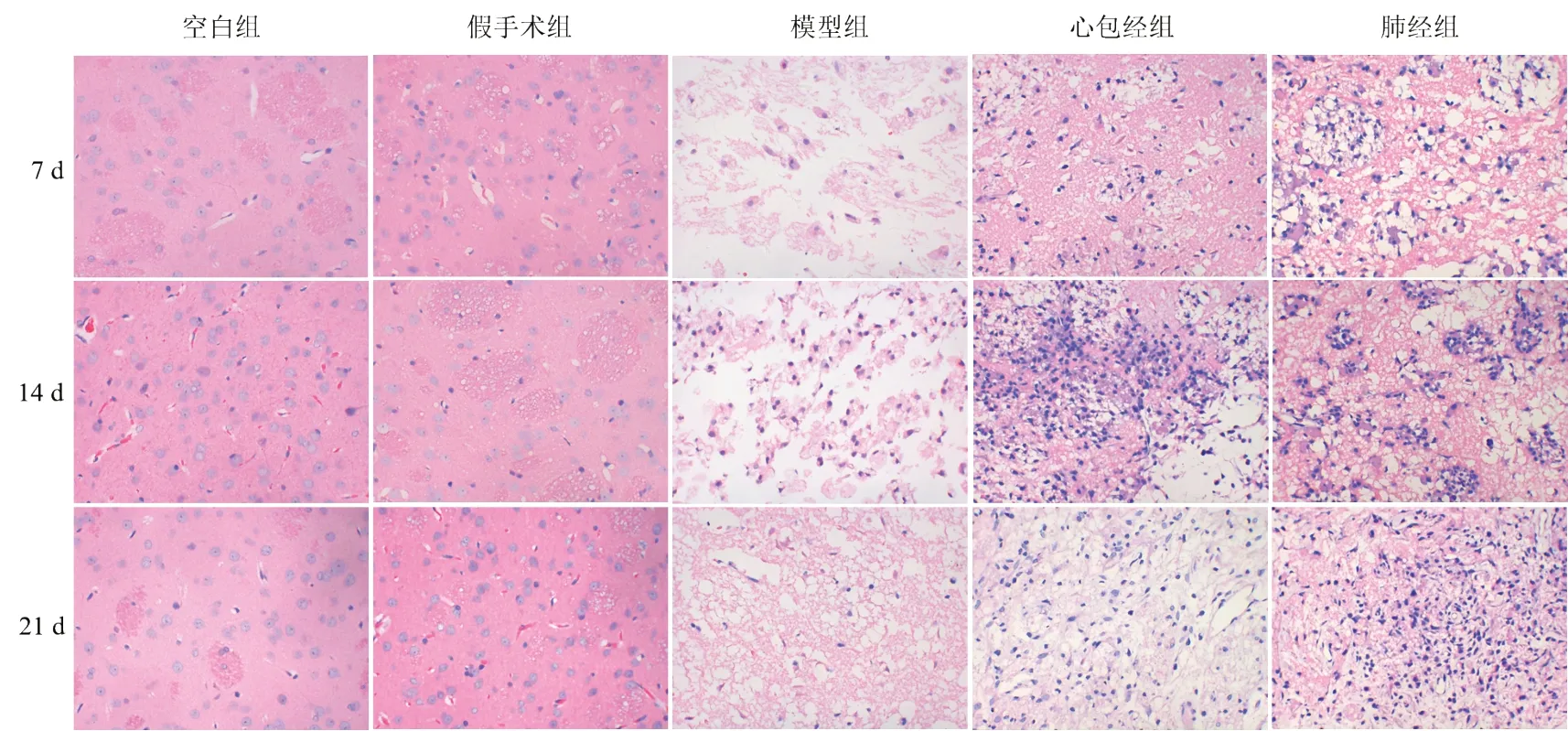
图1 各组大鼠梗死区脑组织形态(HE染色,×400)
2.2 电针对模型大鼠血清RhoA、ROCKⅡ含量的影响
与空白组、假手术组同一时点比较,模型组大鼠各时点血清RhoA、ROCKⅡ含量明显增加(P<0.01);与模型组同一时点比较,心包经组大鼠各时点血清RhoA含量明显减少(P<0.05),14、21 d血清ROCKⅡ含量明显减少(P<0.01);与肺经组同一时点比较,心包经组大鼠7、14 d血清RhoA含量明显减少(P<0.01),14、21 d血清ROCKⅡ含量明显减少(P<0.01,P<0.05)。见图2。

图2 各组大鼠血清RhoA、ROCKⅡ含量比较(±s,每组6只)
2.3 电针对模型大鼠梗死区脑组织RhoA和ROCKⅡ表达的影响
与空白组、假手术组同一时点比较,模型组大鼠各时点梗死区脑组织RhoA、ROCKⅡ表达明显升高(P<0.01);与模型组同一时点比较,心包经组大鼠各时点梗死区脑组织RhoA、ROCKⅡ表达明显降低(P<0.01),肺经组大鼠14、21 d梗死区脑组织RhoA、ROCKⅡ表达明显降低(P<0.05,P<0.01);与肺经组同一时点比较,心包经组大鼠14、21 d梗死区脑组织RhoA表达明显降低(P<0.05),各时点ROCKⅡ表达明显降低(P<0.01)。见图3~图5。

图3 各组大鼠梗死区脑组织RhoA阳性表达(免疫组化染色,×400)
图4 各组大鼠梗死区脑组织ROCKⅡ阳性表达(免疫组化染色,×400)

图5 各组大鼠梗死区脑组织RhoA、ROCKⅡ表达比较(±s,每组6只)
2.4 电针对模型大鼠梗死区脑组织RhoA、ROCKⅡmRNA表达的影响
与空白组、假手术组同一时点比较,模型组大鼠各时点梗死区脑组织RhoA、ROCKⅡ mRNA表达升高,差异有统计学意义(P<0.01);与模型组同一时点比较,心包经组大鼠各时点梗死区脑组织RhoA、ROCKⅡ mRNA表达降低,差异有统计学意义(P<0.01,P<0.05);与肺经组同一时点比较,心包经组大鼠21 d梗死区脑组织RhoA、ROCKⅡ mRNA表达降低,差异有统计学意义(P<0.01)。见图6。

图6 各组大鼠梗死区脑组织RhoA、ROCKⅡ mRNA表达比较(±s,每组6只)
2.5 电针对模型大鼠梗死区脑组织RhoA、ROCKⅡ蛋白表达的影响
与空白组、假手术组同一时点比较,模型组大鼠各时点脑组织梗死区RhoA、ROCKⅡ蛋白表达明显升高(P<0.01);与模型组同一时点比较,心包经组大鼠各时点脑组织梗死区RhoA、ROCKⅡ蛋白的表达均降低(P<0.05,P<0.01),肺经组7、14 d RhoA蛋白表达明显降低(P<0.05),21 d ROCKⅡ蛋白表达明显降低(P<0.01);与肺经组同一时点比较,心包经组大鼠各时点梗死区脑组织RhoA、ROCKⅡ蛋白表达明显降低(P<0.01)。见图7、图8。

图7 各组大鼠梗死区脑组织RhoA、ROCKⅡ蛋白免疫印迹

图8 各组大鼠脑组织梗死区RhoA、ROCKⅡ蛋白表达比较(±s,每组6只)
3 讨论
脑缺血的继发性损害因素有多种,大脑一旦发生梗死,由于中枢神经系统的修复与再生能力有限,神经损伤后很难完全恢复。中枢神经系统损伤的修复受神经因子促进因素与神经轴突生长抑制因素的双重调节,因此有效抑制神经轴突生长抑制因子的表达是促进神经功能恢复的重要途径,对脑卒中神经轴突重建和恢复具有重要意义[19]。研究表明,电针“神庭”“百会”能降低海马组织RhoA蛋白表达,改善MCAO大鼠学习记忆能力[20]。作为治疗缺血性脑卒中的靶点,ROCK抑制剂已被证实通过改变炎症、血小板、内皮功能、平滑肌收缩和神经元再生,在神经保护、脑卒中预防和恢复方面发挥有益作用[21]。ROCKⅠ主要在非神经元组织中表达,ROCKⅡ主要在脑和脊髓中表达。故本实验以RhoA、ROCKⅡ为切入点,研究电针心包经穴对急性脑缺血大鼠神经轴突生长抑制因子的影响。
RhoA/ROCK信号通路激活会抑制神经轴突生长,因此,下调NogoA/RhoA/ROCK通路可消除抑制急性脑缺血后神经再生的障碍[22]。Nogo-A与其受体蛋白NgR结合后,启动下游RhoA/ROCK信号通路,从而抑制轴突生长,阻碍神经修复和再生[23]。RhoA是小G蛋白超家族中Rho家族亚族的成员,ROCK是Rho GTP酶的下游效应分子。RhoA通过激活肌动蛋白抑制轴突生长,因此,神经元中RhoA缺失时会刺激神经轴突再生反应[24]。神经树突、轴突的生长和轴突的导向都离不开RhoA磷酸化,磷酸化后的RhoA被激活,脑缺血可使失活的RhoA蛋白被激活,进而刺激下游效应分子ROCK,变为活化状态的ROCK与GTP结合体,活化状态的ROCK将激活ROCK底物[25]。Yamashita等[26]发现,在急性脑缺血大鼠中神经元轴突ROCKⅡ表达和活性均增加,说明ROCKⅡ在缺血性神经元损伤中起关键作用。
本研究结果显示,模型组大鼠各时点梗死区脑组织神经细胞数量减少、结构紊乱,且血清RhoA、ROCKⅡ含量及梗死区脑组织mRNA和蛋白表达均高于空白组和假手术组,提示急性脑缺血后导致大鼠神经轴突生长抑制因子增加,可能与RhoA/ROCK通路激活有关。心包经组大鼠梗死区脑组织神经细胞形态改善,且血清RhoA、ROCKⅡ含量及梗死区脑组织mRNA和蛋白表达均低于模型组,提示电针心包经穴能改善细胞形态,下调神经轴突生长抑制因子表达,其机制可能与抑制RhoA/ROCK通路激活有关。且电针心包经穴下调神经轴突生长抑制因子表达效果优于电针肺经穴,可能与经脉具有特异性有关。谢峥嵘等[27-28]研究电针手厥阴心包经穴对MCAO大鼠不同时点脑组织SYP、PSD-95及神经生长抑制因子表达的影响也证实了脑缺血后电针心包经穴优于肺经穴。
综合本实验结果,电针心包经穴能下调急性脑缺血大鼠血清RhoA、ROCKⅡ含量及梗死区脑组织RhoA、ROCKⅡ表达,其机制可能与抑制RhoA/ROCK通路激活相关。

