苏云金芽孢杆菌BT 蛋白动物安全性试验
刘鼎阔,董惠峰,宁未萌,刘阔,刘芳,李源,胡鹏程*
(1.鼎正新兴生物技术(天津)有限公司,天津 300383;2.天津农学院,天津 300393;3.天津市生物饲料添加剂企业重点实验室,天津 300383;4.天津市饲用小分子蛋白工程中心,天津 300383)
苏云金芽胞杆菌(Bacillus thuringiensis,Bt)在营养生长阶段会产生外泌型的VIP 蛋白,进入出芽生殖期后在芽孢内会伴生一种特殊的伴孢晶体CRY 蛋白,这些蛋白均具有杀虫效果,统称BT 蛋白[1]。BT 蛋白的杀虫机制已经得到广泛研究,基本途径为虫体的中肠上皮细胞存在特异位点,可以在与BT 蛋白结合后引起膜穿孔,最终导致虫体死亡[2-4]。该机制主要作用于鳞翅目昆虫,因哺乳动物的肠细胞表层不含BT 蛋白受体,所以人和家畜动物对这种蛋白不敏感,因此BT 蛋白作为一种无害杀虫剂在杀虫领域得到广泛应用[5-6]。但是BT 蛋白的毒理作用是否会因为其在体内积累而引起哺乳动物的病变目前尚无确定结论,所以本文旨在通过加大苏云金芽孢杆菌浓度,选择健康小鼠为靶动物,了解BT 蛋白纯化液对动物的临床表现、生理生化指标的影响,为该产品在临床上的应用提供理论依据。
1 材料与方法
1.1 材料与仪器
雌性健康小鼠40 只(实验动物许可证:SYXK(京)2020-0053),体重18 ~22 g;苏云金发酵BT 蛋白纯化液,鼎正新兴生物技术(天津)有限公司;蛋白胨、酵母粉,天津市北联精细化学品开发有限公司。
SHY-2A 恒温水浴摇床,上海比郎仪器制造有限公司;H1850R 低温离心机,湖南湘仪实验室仪器开发有限公司;Countess 3 血球计数仪,赛默飞世尔科技公司;FDC NX500iVC 血生化仪,富士胶片医疗系统有限公司;HS-3315 组织切片机,北京莱博瑞杰科技有限公司;ECLIPSE SI 显微镜,尼康精机(上海)有限公司。
1.2 方法
1.2.1 试验动物分组
将试验小鼠随机分为4 组,每组10 只,分组情况见表1。
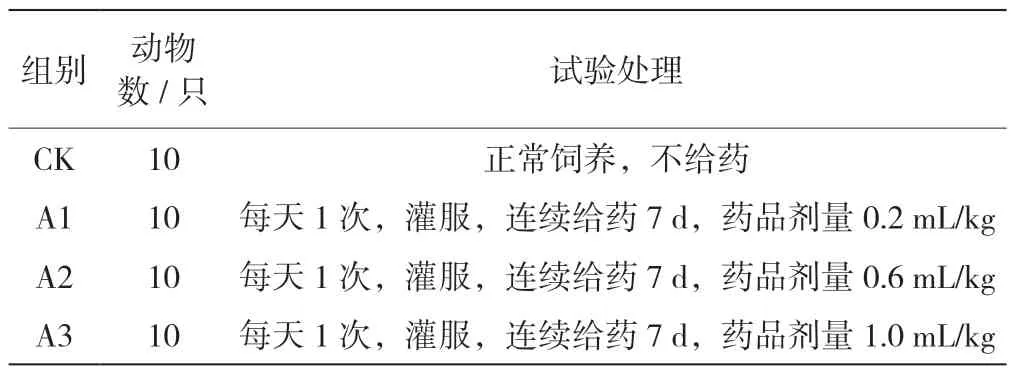
表1 试验动物分组与处置
1.2.2观察指标
一般动物安全性实验观察周期在7 ~28 d,本实验考虑发酵制品储存周期不宜过久,且储存期越长,污染风险越高;另考虑BT 蛋白在胃肠环境极易吸收,7 d足以产生足够的积累,所以确定第7 d 观察相关指标。
1.2.2.1临床观察
试验期间每日观察受试动物是否出现与药物相关的不良反应,如呼吸与行为异常、精神抑制及排粪异常等情况。
1.2.2.2体重
对试验前及试验结束后受试小鼠称量体重,做好记录。
1.2.2.3血样分析
(1)采血及处理方法。所有动物分别在给药前和给药结束后采血,分两管放置;其中1 管为带抗凝剂的离心管,用于血常规分析;另一管不带抗凝剂,血液样品于室温下静置2 h,2 500 r/min 离心5 min,取上层血清,-20 ℃保存,用于血液生化指标分析。
(2)血常规分析。取加抗凝剂管全血进行白细胞计数(WBC)、白细胞分类[嗜中性粒细胞(NE)、淋巴细胞(LY)、单核细胞(MO)、嗜酸性粒细胞(EO)、嗜碱性粒细胞(BA)]、红细胞计数(RBC)、血红蛋白(HGB)、红细胞压积(HCT)、血小板计数(PLT)等指标分析。
(3)血液生化指标分析。取血清进行丙氨酸氨基转换酶(ALT)、天门冬氨酸转换酶(AST)、尿素氮(BUN)、肌酐(Cr)、白蛋白(ALB)、总蛋白(TP)、总胆固醇(CHO)、甘油三酯(TG)等指标分析。
1.2.2.4解剖学检查
对靶动物进行大体解剖学检查,对心、肝、脾、肺、肾等脏器有选择地做病理学剖检和病变组织观察,了解该制剂临床应用的安全性。
1.3 统计分析
数据以均值±标准差格式展示,采用SPSS 13.0中卡方检验分析组间差异,P<0.05 和P<0.01 分别表示差异显著和极显著。
2 结果与分析
2.1 给药后临床观察
各组动物给药后的呼吸、行为、精神、排粪、食欲等均正常,未出现不良反应。
2.2 给药前后体重变化
给药前和给药后动物体重结果见表2。结果表明,给药前后各组小鼠的体重差异不显著(P>0.05)。
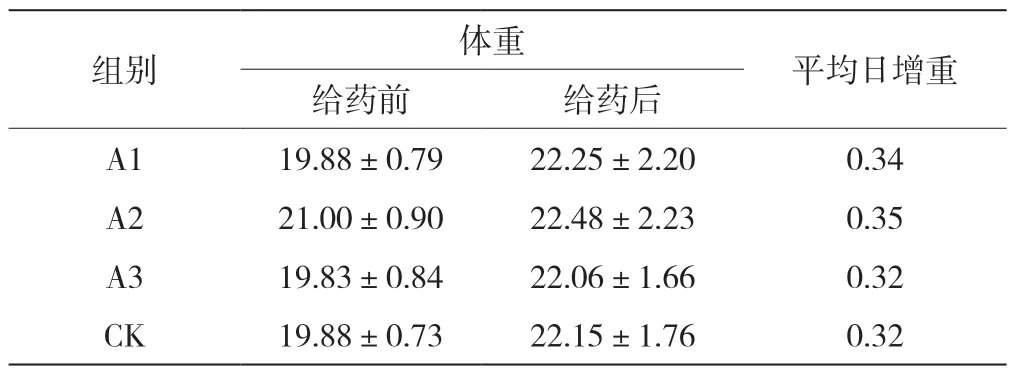
表2 给药前和给药后小鼠体重变化(单位:g)
2.3 血常规分析结果
各组小鼠的血常规指标检测结果见表3。从表3中可以看出,各剂量组给药前后的血常规指标与正常组比较差异不显著(P>0.05),说明Bt 发酵纯化上清液在0.2 mL/kg、0.6 mL/kg、1.0 mL/kg 剂量范围对血液常规指标没有明显的影响。

表3 不同剂量Bt 发酵纯化上清液对小鼠血常规指标的影响
2.4 血液生化分析结果
小鼠的血液生化指标检测结果见表4。从表4 中可以看出,各剂量组给药前后的血液生化指标与正常组比较差异不显著(P>0.05),说明Bt 发酵纯化上清液在0.2 mL/kg、0.6 mL/kg、1.0 mL/kg 剂量范围对血液生化指标没有明显的影响。
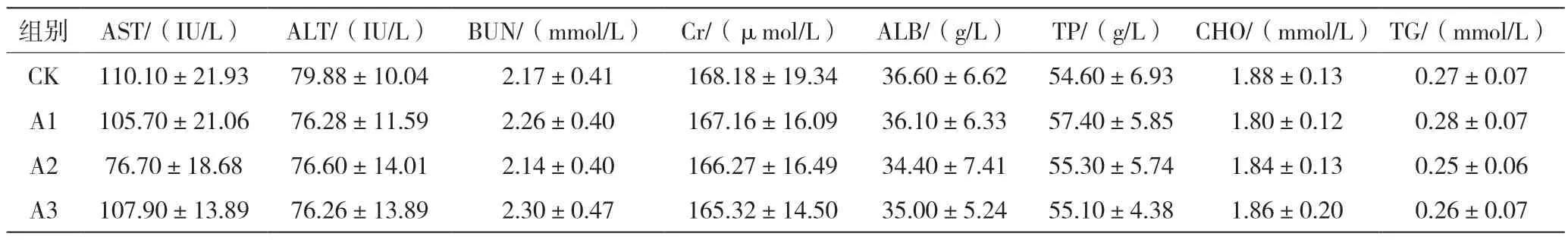
表4 不同剂量Bt 发酵纯化上清液对小鼠血液生化指标的影响
2.5 尸体解剖及组织观察结果
1.0 mL/kg 剂量组和对照组的心、肝、脾、肺、肾的组织切片见图1。大体剖检结果和组织学检查均无明显的肉眼可见病理变化。

图1 组织切片
3 结论
综上所述,Bt 发酵纯化上清液按0.2 mL/kg、0.6 mL/kg、1.0 mL/kg 剂量给药,小鼠体态特征与对照组相比未见异常;血常规、血液生化分析等检测结果显示两组差异不显著;给药结束后解剖小鼠,制作组织切片,通过10 倍和40 倍显微镜观测仍未见病理变化。由此说明,Bt 发酵纯化上清液的生物安全性极高。

