哌拉西林他唑巴坦钠诱导血液病患者免疫性溶血反应观察
董晓锋,郝宝岚,祁 欣,兰帅奇,任 磊,周 健,李 珍
1)郑州大学附属肿瘤医院(河南省肿瘤医院)输血科 郑州 450008 2)郑州大学附属肿瘤医院(河南省肿瘤医院)血液科 郑州 450008
青霉素类抗菌药哌拉西林他唑巴坦钠在血液病患者抗感染治疗过程中发生药品不良反应(adverse drug reaction,ADR)的报道越来越多[1-3],部分患者出现药物诱导的免疫性溶血反应,严重的甚至发生危及患者生命的药物诱导的免疫性溶血性贫血(drug-induced immune hemolytic anemia,DIIHA)。既往ADR诊断都是依据临床医师的经验判断,实验室诊断滞后,无法第一时间提供实验室检查依据。本研究收集了153例血液病患者在不同用药时间的血液样本,采用微柱凝胶技术检测哌拉西林他唑巴坦钠药物抗体,旨在为临床ADR的诊断提供实验依据。
1 对象与方法
1.1 研究对象选择2020年7月至2021年6月在河南省肿瘤医院住院期间静脉使用标准剂量哌拉西林他唑巴坦钠的血液病患者。纳入标准:①2周内无哌拉西林他唑巴坦钠治疗史。②哌拉西林他唑巴坦钠使用前不规则抗体筛查和直接抗球蛋白试验(direct antiglobulin test,DAT)均为阴性。③哌拉西林他唑巴坦钠使用前药物抗体阴性。排除资料有缺失的患者,共纳入153例研究对象。
1.2 主要试剂与仪器哌拉西林他唑巴坦钠注射液(4.5 g/支,珠海联邦制药股份有限公司)。微柱凝胶抗球蛋白检测卡(瑞士达亚美公司,江苏力博医药生物技术股份有限公司),抗球蛋白试剂(上海血液生物医药有限责任公司),哌拉西林他唑巴坦钠诱导型溶血检测试剂盒(江苏中济万泰生物医药有限公司),巴比妥钠(福建闽东力捷迅药业)。KA-2200型离心机(日本久保田公司),TD-3A型血型血清学多用离心机、孵育器(长春博研科学仪器有限责任公司)。
1.3 检测方法
1.3.1哌拉西林他唑巴坦钠药物致敏细胞的制作制作方法参照美国血库协会技术手册[4]。取2只烧杯,分别标记为药物致敏细胞和对照细胞。标记为药物致敏细胞的烧杯中,加入600 mg哌拉西林他唑巴坦钠和15 mL巴比妥钠缓冲液,而后加入1 mL洗涤的O型压积红细胞;标记对照细胞的烧杯中不加药物,所加红细胞与缓冲液的种类、量与药物致敏细胞烧杯相同; 将上述细胞悬液充分混匀后室温中孵育1 h(期间混匀数次),孵育后的红细胞用巴比妥钠缓冲液洗涤3次,并配成体积分数5%红细胞悬液备用,用于哌拉西林他唑巴坦钠药物抗体检测。
1.3.2DAT操作 采用微柱凝胶法。采集首次用药后第3、5、7和10天患者的血液标本,用生理盐水洗涤3次后配制成体积分数0.5%~1.0%的红细胞悬液,抽取50 μL红细胞悬液加入包被有抗IgG+抗C3的微柱凝胶抗球蛋白检测卡中,置于专用离心机离心5 min后观察结果并记录。红细胞下沉到微柱凝胶管底部形成细胞扣为阴性反应,表明红细胞表面没有抗体未被致敏;红细胞滞留在微柱凝胶表面或分散在凝胶中并未下沉底部为阳性反应,表明红细胞表面存在抗体而被致敏。
1.3.3哌拉西林他唑巴坦钠药物抗体检测 采用微柱凝胶法,按照哌拉西林他唑巴坦钠诱导型溶血检测试剂盒说明操作,检测首次用药后第3、5、7和10天患者的血液标本。红细胞下沉到微柱凝胶管底部形成细胞扣为阴性,红细胞滞留在微柱凝胶表面或分散在凝胶中并未下沉底部为阳性。
1.4 统计学处理采用SPSS 20.0进行统计分析。用药不同时间DAT阳性率、药物抗体阳性率的比较及不同组间性别的比较采用广义估计方程、χ2检验或Fisher精确概率法;不同组间年龄的比较采用两独立样本t检验。检验水准α=0.05。
2 结果
2.1 研究对象的基本情况153例中,男87例,女66例;年龄4~80岁;急性淋巴细胞白血病14例,急性髓系白血病38例,慢性淋巴细胞白血病4例,慢性粒细胞白血病12例,骨髓增生异常综合征24例,再生障碍性贫血7例,多发骨髓瘤34例,淋巴瘤17例,其他血液病3例。
2.2 用药不同时间哌拉西林他唑巴坦钠药物抗体与DAT阳性率比较见表1、2。DAT阳性率随用药时间的延长而增加;DAT阳性组中药物抗体阳性率与用药时间无关。
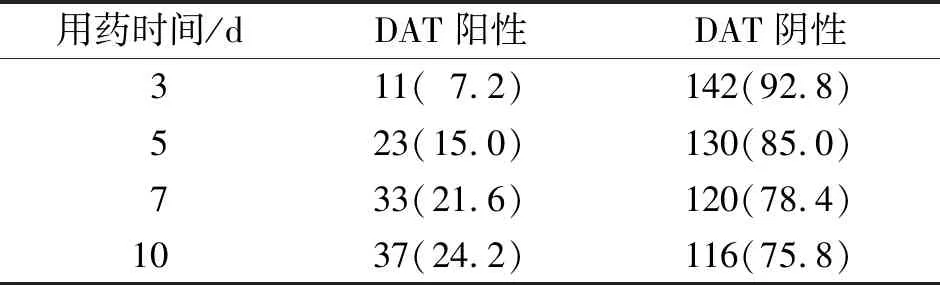
表1 哌拉西林他唑巴坦钠用药后不同时间DAT结果 例(%)

表2 哌拉西林他唑巴坦钠用药后DAT阳性组中药物抗体结果 例(%)
2.3 各组研究对象基本情况比较根据用药后第10天的检测结果将纳入的153例患者分为DAT阴性组(116例)和DAT阳性组(37例),将DAT阳性患者分为药物抗体阴性组(28例)和药物抗体阳性组(9例)。两组性别、年龄比较,差异均无统计学意义。见表3、4。

表3 DAT阴性和阳性患者基本情况比较

表4 DAT阳性的药物抗体阴性和阳性患者基本情况比较
3 讨论
近年来,随着对药物抗体的深入研究,已了解到使用抗菌、心血管、化疗等药物治疗后都可以产生药物抗体[5]。哌拉西林他唑巴坦钠作为一类半合成青霉素药物,与其他青霉素类药物一样,具有强大的抗菌作用,广泛应用于血液病患者的抗感染治疗中,同时大量临床实践发现,哌拉西林他唑巴坦钠是引起ADR的主要药物之一[6]。部分使用哌拉西林他唑巴坦钠的患者DAT可出现阳性结果,有的甚至出现DIIHA症状[7-8]。本研究在9例药物抗体阳性患者中发现1例多发骨髓瘤患者在没有出血的情况下输注悬浮红细胞后血红蛋白不升反降,血红蛋白一直维持在50 g/L左右,生化检验显示间接胆红素升高,提示有溶血性贫血,停用哌拉西林他唑巴坦钠后再次输注悬浮红细胞,血红蛋白明显升高。
药物抗体、新生儿溶血病、自身免疫性贫血、血型不合的输血等都可以引起DAT阳性[9-11]。患者DAT阳性证明其体内红细胞膜上存在不完全抗体,预示存在一定的溶血风险,但不能明确原因。有学者[12]发现部分DAT阳性患者体内可以检测到药物抗体。然而,药物抗体引起溶血的临床症状常常不典型,难以与血液病自身的症状相鉴别,有的仅仅是DAT阳性[13]。
本研究显示153例血液病患者DAT阳性率随用药时间延长而增加。大部分DAT阳性患者并没有出现溶血症状,也没有其他溶血的实验室证据。进一步分析用药10 d的患者,DAT阴性组(116例)和DAT阳性组(37例)性别、年龄分布比较,差异无统计学意义。分析原因:虽然不完全抗体致敏红细胞,尤其是半抗原药物哌拉西林他唑巴坦钠与红细胞膜表面蛋白共价结合形成半抗原/蛋白复合物[14],破坏红细胞,但是红细胞破坏的速度低于骨髓代偿能力,即使患者存在溶血,但贫血症状不明显。作者认为用药期间在没有其他溶血实验室证据时,在没有出血的情况下,患者输血后血红蛋白不升反降,或者一直维持在一个很低的水平,不能排除DIIHA的可能。
进一步分析发现,DAT阳性组中药物抗体阳性率与用药时间无关,用药5 d后药物抗体的阳性率趋于稳定。分析用药10 d的DAT阳性患者药物抗体检测情况,药物抗体阳性组(9例)和药物抗体阴性组(28例)性别、年龄无差异。分析原因:在用药期间观察到DAT阳性,为避免DIIHA的发生,临床医生在尚未检测到哌拉西林他唑巴坦钠药物抗体情况下选择停药或者换药。再者,初次免疫应答产生的药物抗体量少,以现有的检测技术不足以检出哌拉西林他唑巴坦钠抗体。
综上,临床血液病患者在使用哌拉西林他唑巴坦钠治疗过程中,需要动态监测药物抗体,确保临床用药安全有效,避免DIIHA的发生。