通关藤化学成分及其细胞毒活性
贾祎萍,吴子薇,李晓波,王嘉祺,时晓颖,王梦月*,韩永龙
(1.上海交通大学药学院,上海 200240;2.上海交通大学医学院附属第六人民医院药剂科,上海 200233)
通关藤又名通关散、通光藤、乌骨藤、奶浆藤、通天散、龙爪草、下奶藤,为萝藦科植物通关藤Marsdeniatenacissima(Roxb.) Wight et Arn.的干燥藤茎,始载于《滇南本草》,历史悠久,其性微寒味苦,入肺经,具有止咳平喘、祛痰、通乳、清热解毒等功效,可治疗喘咳痰多、产后乳汁不通、风湿肿痛、疮痈等,应用广泛[1]。现代研究发现,通关藤具有抗炎、止咳、平喘、抗肿瘤等作用,可用于治疗气管炎、扁桃体炎、咽炎、膀胱炎、肺炎、哮喘、肿瘤,效果显著[2-3]。近年来,课题组发现,通关藤水煎液制剂——通关藤注射液具有增强紫杉醇抗乳腺癌作用[4],通关藤C21甾体化合物能够逆转肿瘤细胞对紫杉醇的耐药性[5]。为系统阐明通关藤的抗肿瘤作用物质基础,本研究对通关藤水煎液化学成分进行研究,从中分离得到12 个化合物,其中,新化合物1 个,新天然产物1 个,部分化合物具有细胞毒活性。
1 材料
Bruker Avance 600 MHz 核磁共振仪 (德国Bruker 公司,配有13C/1H/15N TCI 超低温探头,TMS 为内标);Agilent 1290 UPLC-Q-TOF 质谱联用仪、Agilent 1260 Infinity Ⅱ制备型高效液相色谱仪(美国Agilent 公司);P-2000 型全自动数字旋光仪(日本分光株式会社);YMC 色谱柱 (10 mm×250 mm,5 μm,日本YMC 公司);EYELA N-101型旋转蒸发仪(日本东京理化器械株式会社);DZF-6050 型真空干燥箱(上海一恒科学仪器有限公司);SK6200H 超声清洗器(上海科导超声仪器有限公司);WFH-203B 三用紫外分析仪(上海耀壮检测仪器设备有限公司);Varioskan Flash 多功能酶标仪(美国Thermo 公司)。
D101 大孔吸附树脂(天津德力特环保科技有限公司);柱层析用硅胶(200~300 目,青岛海洋化工有限公司);HSGF254硅胶G 高效薄层色谱板(烟台江友硅胶开发有限公司);ODS 反相硅胶(40~63 μm,德国Merck 公司)。乙腈(色谱纯,上海百灵威化学技术有限公司);乙醇、甲醇、二氯甲烷(分析纯,上海泰坦科技股份有限公司)。
人肺癌细胞A549、人肝癌细胞Bel-7402 (中国科学院上海细胞库)。MTT、5-氟尿嘧啶(国药集团化学试剂公司);RPMI 1640 培养基 (美国Thermo 公司)。
通关藤由南京圣和药业有限公司提供,经上海交通大学药学院王梦月副教授鉴定为萝藦科植物通关藤Marsdeniatenacissima(Roxb.) Wight et Arn.的干燥茎藤。凭证标本(MT202101) 保存于上海交通大学药学院。
2 提取与分离
取通关藤5 kg,加10 倍量水,煎煮3 次,每次1 h,过滤,滤液浓缩至2 L;加16 L 85%乙醇,搅匀,4 ℃放置24 h,过滤,滤液回收乙醇,浓缩至1.5 L;再加12 L 乙醇,4 ℃放置48 h,过滤,滤液回收乙醇,浓缩得浸膏1 L。
浸膏经大孔树脂柱,依次用水,30%、60%、90%乙醇梯度洗脱,90% 乙醇洗液减压回收溶剂,得醇提物(4.60 g)。醇提物经硅胶柱分离,以甲醇-二氯甲烷(0 ∶1~1 ∶4) 梯度洗脱,得Fr.A~Fr.B。Fr.A (0.3 g) 经制备HPLC 纯化,以甲醇-水(1 ∶1~1 ∶19) 梯度洗脱(检测波长210 nm),得Fr.A1~Fr.A3。Fr.A1 (32 mg) 经制备HPLC纯化,以乙腈-水(77 ∶23) 梯度洗脱(体积流量5 mL/min,检测波长254 nm),得化合物3 (tR=11.98 min,2.37 mg)、4 (tR=3.85 min,0.76 mg)。Fr.A2 (48 mg) 经制备HPLC 纯化,以乙腈-水 (7 ∶ 13~4 ∶ 1) 梯度洗脱 (体积流量4 mL/min,检测波长210 nm),得化合物1 (tR=41.61 min,3.56 mg)、2 (tR=30.78 min,5.63 mg)。Fr.A3 (52 mg) 经制备HPLC 纯化,以乙腈-水(2 ∶3) 洗脱(体积流量5 mL/min,检测波长254 nm),得化合物5 (tR=6.65 min,8.4 mg)、6 (tR=8.49 min,1.1 mg)。Fr.B (3.4 g) 经硅胶柱分离,以甲醇-二氯甲烷(1 ∶99~1 ∶4) 梯度洗脱,得Fr.B1~Fr.B4。Fr.B1 (231 mg) 经硅胶柱纯化,以甲醇-二氯甲烷(1 ∶19~3 ∶17) 梯度洗脱,得化合物7 (6.1 mg)。Fr.B2 (845 mg) 经硅胶柱纯化,以甲醇-二氯甲烷(1 ∶19~3 ∶17) 梯度洗脱,得化合物8 (11.4 mg)、9 (3.1 mg)、10(6.6 mg)。Fr.B3 (459 mg) 经ODS 柱纯化,以甲醇-水(2 ∶3~4 ∶1) 梯度洗脱,得化合物11(1.7 mg)、12 (4.0 mg)。
3 结构鉴定

图1 化合物1 结构式及主要相关信息Fig.1 Chemical structure and key correlations of compound 1
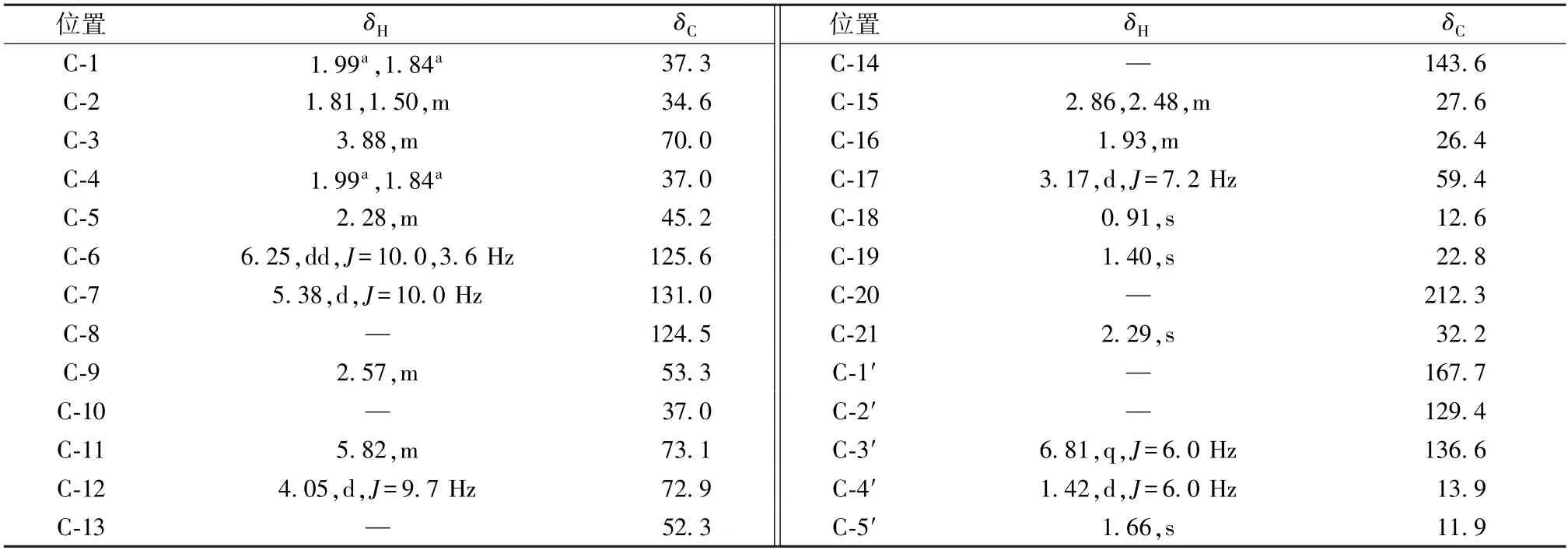
表1 化合物1 的1H-NMR、13C-NMR波谱数据Tab.1 1H-NMR and 13C-NMR spectroscopic data on compound 1
化合物2:白色粉末。1H-NMR (C5D5N,600 MHz)δ:1.31 (3H,d,J=4.4 Hz,H-4'),1.39(3H,s,H-19),1.68 (3H,s,H-18),1.50(3H,s,H-21),3.84 (1H,m,H-3),4.85(1H,m,H-12α),4.86 (1H,m,H-11β),6.40(1H,d,J=4.4 Hz,H-3');13C-NMR (C5D5N,150 MHz)δ:38.2 (C-1),31.5 (C-2),68.7(C-3),38.2 (C-4),44.8 (C-5),28.3 (C-6),35.7 (C-7),78.5 (C-8),58.3 (C-9),39.3(C-10),70.4 (C-11),73.4 (C-12),46.4 (C-13),80.6 (C-14),35.7 (C-15),34.4 (C-16),55.5 (C-17),17.2 (C-18),16.7 (C-19),99.9(C-20),24.5 (C-21),167.9 (C-1'),128.9(C-2'),138.4 (C-3'),12.1 (C-4'),14.1 (C-5')。以上数据与文献[9] 报道基本一致,故鉴定为12-O-惕各酰基-通关藤苷元A。
化合物3:棕色粉末。1H-NMR (C5D5N,600 MHz)δ:6.93 (1H,d,J=2.0 Hz,H-2),6.81(1H,d,J=8.0 Hz,H-5),6.80 (1H,dd,J=8.0,2.0 Hz,H-6),3.81 (1H,d,J=9.6 Hz,H-7),2.41 (1H,m,H-8),3.63 (1H,dd,J=8.9,6.4 Hz,H-9a),4.19 (1H,t,J=6.4 Hz,H-9b),3.77 (3H,s,3-OCH3),6.90 (1H,s,H-2'),7.15 (1H,s,H-5'),2.70 (1H,dd,J=13.1,4.1 Hz,H-7'a),2.92 (1H,dd,J=13.1,4.1 Hz,H-7'b),2.24 (1H,m,H-8'),3.53 (1H,dd,J=8.9,6.4 Hz,H-9'a),3.99(1H,t,J=6.4 Hz,H-9'b),3.56 (3H,s,4'-OCH3);13C-NMR (C5D5N,150 MHz)δ:135.8(C-1),112.2 (C-2),147.9 (C-3),145.9 (C-4),115.5 (C-5),121.8 (C-6),49.0 (C-7),49.9 (C-8),72.3 (C-9),126.2 (C-1'),111.6(C-2'),147.2 (C-3'),146.4 (C-4'),116.4(C-5'),132.8 (C-6'),31.6 (C-7'),42.0 (C-8'),71.5 (C-9'),54.8 (3-OCH3),55.0 (3'-OCH3)。以上数据与文献 [10] 报道基本一致,故鉴定为isoshonanin。
化合物4:白色粉末。1H-NMR (C5D5N,600 MHz)δ:6.84 (2H,s,H-2,6),5.03 (1H,d,J=6.3 Hz,H-7),3.41 (1H,m,H-8),4.60(1H,d,J=8.6 Hz,H-9a),3.94 (1H,overlapped,H-9b),3.47 (1H,m,H-8'),4.10(1H,dd,J=9.6,8.3 Hz,H-9'a),3.90 (1H,dd,overlapped,H-9' b),3.75 (6H,s,3,5-OCH3);13C-NMR (C5D5N,150 MHz)δ:127.4(C-1),104.0 (C-2),149.1 (C-3),132.4 (C-4),149.1 (C-5),104.0 (C-6),84.5 (C-7),46.3 (C-8),71.0 (C-9),179.2 (C-7'),43.7(C-8'),68.4 (C-9')。以上数据与文献[11] 报道基本一致,故鉴定为caruilignan D。
化合物5:白色粉末。1H-NMR (C5D5N,600 MHz)δ:8.08 (1H,s,H-2),7.31 (1H,d,J=8.2 Hz,H-5),8.17 (1H,d,J=8.2 Hz,H-6),3.76 (3H,s,3-OCH3);13C-NMR (C5D5N,150 MHz)δ:124.7 (C-1),113.6 (C-2),148.1(C-3),152.5 (C-4),116.0 (C-5),124.7 (C-6),168.9 (C-7),55.5 (3-OCH3)。以上数据与文献[12] 报道基本一致,故鉴定为香草酸。
化合物6:白色粉末。1H-NMR (C5D5N,600 MHz)δ:7.90 (2H,s,H-2,6),3.82 (6H,s,3,5-OCH3);13C-NMR (C5D5N,150 MHz)δ:121.8 (C-1),108.2 (C-2),148.5 (C-3),142.1 (C-4),148.5 (C-5),108.1 (C-6),169.0 (C-7),56.0 (3,5-OCH3)。以上数据与文献[12] 报道基本一致,故鉴定为丁香酸。
化合物7:白色粉末。1H-NMR (C5D5N,600 MHz)δ:1.38 (3H,s,H-19),1.64 (3H,s,H-18),1.48 (3H,s,H-21),2.71 (1H,s,H-9),3.88 (1H,m,H-3),4.35 (1H,m,H-12α),4.60 (1H,m,H-11β);13C-NMR(C5D5N,150 MHz)δ:38.7 (C-1),31.5 (C-2),72.1 (C-3),38.3 (C-4),46.6 (C-5),28.2(C-6),33.8 (C-7),78.8 (C-8),59.0 (C-9),36.0 (C-10),71.2 (C-11),72.1 (C-12),45.3(C-13),81.4 (C-14),34.9 (C-15),23.6 (C-16),54.4 (C-17),17.9 (C-18),16.0 (C-19),99.6 (C-20),24.7 (C-21)。以上数据与文献[13] 报道基本一致,故鉴定为通关藤苷元A。
化合物8:白色粉末。1H-NMR (C5D5N,600 MHz)δ:4.91 (1H,brs,H-29a),4.74 (1H,brs,H-29b),3.53 (1H,m,H-3),1.82 (3H,s,H-30),1.22 (3H,s,H-27),1.04 (3H,s,H-26),1.03 (3H,s,H-25),1.02 (3H,s,H-24),0.79 (3H,s,H-23);13C-NMR (C5D5N,150 MHz)δ:179.0 (C-28),151.2 (C-20),109.7 (C-29),77.9 (C-3),56.5 (C-17),55.7(C-5),50.7 (C-9),49.5 (C-19),47.5 (C-18),42.6 (C-14),40.9 (C-8),39.3 (C-1,4),38.3 (C-13),37.4 (C-10),37.3 (C-22),34.6 (C-7),34.3 (C-21),32.7 (C-16),31.0(C-15),30.1 (C-23),28.1 (C-2),25.9 (C-12),22.0 (C-11),19.2 (C-30),18.5 (C-6),16.4 (C-24),16.2 (C-25),16.1 (C-26),14.7(C-27)。以上数据与文献[14] 报道基本一致,故鉴定为白桦脂酸。
化合物9:白色粉末。1H-NMR (C5D5N,600 MHz)δ:1.01 (3H,t,J=2.8 Hz,H-4'),1.05(3H,d,J=2.8 Hz,H-3'),1.21 (3H,s,H-19),1.26 (3H,s,H-18),1.53 (3H,d,J=6.0 Hz,H-6‴),2.03 (3H,s,H-6″),2.24(3H,s,H-21),2.88 (1H,brd,J=6.5 Hz,H-17β),3.60 (3H,s,3″-OCH3),3.82 (3H,s,3‴-OCH3),4.15 (1H,brs,H-3‴),4.80 (1H,d,J=9.5 Hz,H-1″),4.81 (1H,d,J=8.0 Hz,H-1‴),4.82 (1H,d,J=10.0 Hz,H-12α),5.67 (1H,t,J=10.0 Hz,H-11β);13C-NMR(C5D5N,150 MHz)δ:35.6 (C-1),30.5 (C-2),71.4 (C-3),38.1 (C-4),44.5 (C-5),27.3 (C-6),32.5 (C-7),67.1 (C-8),52.1(C-9),39.7 (C-10),69.2 (C-11),80.0 (C-12),46.5 (C-13),72.4 (C-14),27.1 (C-15),25.2 (C-16),62.3 (C-17),9.5 (C-18),13.1(C-19),209.8 (C-20),30.2 (C-21),170.4(12-COOH),20.8 (12-COOH),175.71 (C-1'),34.5 (C-2'),18.3 (C-3'),18.8 (C-4'),97.2(C-1″),38.2 (C-2″),83.8 (C-3″),83.0 (C-4″),73.1 (C-5″),18.4 (C-6″),57.5 (3″-OCH3),101.8 (C-1‴),73.1 (C-2‴),84.5 (C-3‴),74.8 (C-4‴),71.8 (C-5‴),18.9 (C-6‴),61.8 (3‴-OCH3)。以上数据与文献[15] 报道基本一致,故鉴定为11-O-异丁酰基-12-O-乙酰基通关藤苷元B-3-O-茯苓二糖苷。
化合物10:白色粉末。1H-NMR (C5D5N,600 MHz)δ:1.02 (3H,t,J=7.5 Hz,H-4'),1.17(3H,d,J=7.0 Hz,H-5'),1.21 (3H,s,H-19),1.28 (3H,s,H-18),1.54 (3H,d,J=6.0 Hz,H-6‴),2.01 (3H,s,H-6″),2.24(3H,s,H-21),2.90 (1H,brd,J=6.5 Hz,H-17β),3.55 (3H,s,3″-OCH3),3.85 (3H,s,3‴-OCH3),4.15 (1H,brs,H-3‴),4.82 (1H,d,J=9.5Hz,H-1″),4.92 (1H,d,J=8.0 Hz,H-1‴),4.99 (1H,d,J=10.0 Hz,H-12α),5.67 (1H,t,J=10.0 Hz,H-11β);13C-NMR(C5D5N,150 MHz)δ:35.6 (C-1),30.5 (C-2),71.4 (C-3),38.1 (C-4),44.5 (C-5),27.3 (C-6),32.5 (C-7),67.1 (C-8),52.1(C-9),39.7 (C-10),68.5 (C-11),80.0 (C-12),46.5 (C-13),72.4 (C-14),27.1 (C-15),25.2 (C-16),62.3 (C-17),9.5 (C-18),13.1(C-19),210.5 (C-20),30.2 (C-21),171.0(12-COOH),20.8 (12-COOH),174.0 (C-1'),44.3 (C-2'),26.6 (C-3'),11.6 (C-4'),15.6(C-5'),97.9 (C-1″),38.2 (C-2″),86.5 (C-3″),83.6 (C-4″),73.2 (C-5″),18.6 (C-6″),57.5 (3″-OCH3),102.4 (C-1‴),73.7 (C-2‴),84.5 (C-3‴),75.0 (C-4‴),72.1 (C-5‴),19.2(C-6‴),62.5 (3‴-OCH3)。以上数据与文献[16] 报道基本一致,故鉴定为通关藤苷H。
化合物11:白色粉末。1H-NMR (C5D5N,600 MHz)δ:1.21 (3H,s,H-19),1.25 (3H,s,H-18),1.52 (3H,d,J=6.5 Hz,H-6‴),1.56(3H,d,J=6.0 Hz,H-6″),1.65 (3H,d,J=5.5 Hz,H-4'),1.77 (3H,s,H-5'),2.12(1H,brd,J=6.5 Hz,H-17β),2.42 (1H,brd,J=9.5 Hz,H-4‴),2.91 (3H,s,3″-OCH3),3.50 (3H,s,3‴-OCH3),3.81 (1H,brs,H-3‴),4.14 (1H,d,J=8.0 Hz,H-1″),4.77(1H,d,J=8.0 Hz,H-1‴),5.30 (1H,d,J=8.0 Hz,H-12α),5.42 (1H,d,J=10.0 Hz,H-11β),6.86 (1H,q,J=5.5 Hz,H-3');13CNMR (C5D5N,150 MHz)δ:37.5 (C-1),29.5(C-2),75.8 (C-3),34.9 (C-4),43.7 (C-5),27.0 (C-6),25.0 (C-7),66.5 (C-8),51.6(C-9),39.1 (C-10),68.8 (C-11),74.9 (C-12),45.9 (C-13),71.5 (C-14),31.9 (C-15),26.9 (C-16),59.4 (C-17),13.9 (C-18),16.7(C-19),210.0 (C-20),30.0 (C-21),170.4(12-COOH),20.2 (12-COOH),167.0 (C-1'),128.8 (C-2'),138.0 (C-3'),11.9 (C-4'),14.1 (C-5'),97.3 (C-1″),37.5 (C-2″),79.4(C-3″),83.0 (C-4″),71.7 (C-5″),18.4 (C-6″),56.9 (3″-OCH3),101.8 (C-1‴),73.0 (C-2‴),83.8 (C-3‴),74.4 (C-4‴),70.7 (C-5‴),18.9 (C-6‴),61.8 (3‴-OCH3)。以上数据与文献[16] 报道基本一致,故鉴定为通关藤苷G。
化合物12:白色粉末。1H-NMR (C5D5N,600 MHz)δ:1.39 (3H,s,H-19),1.48 (3H,s,H-18),1.54 (3H,d,J=6.5 Hz,H-6‴),1.70(3H,d,J=4.5 Hz,H-6″),1.81 (1H,m,H-5″),1.90 (1H,s,H-17β),2.55 (2H,dd,J=14.0,11.0 Hz,H-2″),2.69 (1H,s,H-9),3.21 (1H,d,J=8.5 Hz,H-4‴),3.82 (1H,t,J=2.5 Hz,H-3‴),4.19 (1H,dd,J=6.5,4.0 Hz,H-12α),4.35 (1H,t,J=5.5 Hz,H-11β),4.88 (1H,d,J=9.5 Hz,H-1‴);13C-NMR(C5D5N,150 MHz)δ:38.1 (C-1),29.8 (C-2),77.4 (C-3),35.5 (C-4),46.9 (C-5),28.9 (C-6),25.6 (C-7),67.1 (C-8),52.1(C-9),39.7 (C-10),70.3 (C-11),75.5 (C-12),46.0 (C-13),71.3 (C-14),34.7 (C-15),27.5 (C-16),60.0 (C-17),13.4 (C-18),16.6(C-19),210.5 (C-20),30.5 (C-21),171.0(12-COOH),20.6 (12-COOH),166.5 (C-1'),131.9 (C-2'),130.2 (C-3'),129.4 (C-4'),134.9 (C-5'),129.4 (C-6'),130.2 (C-7'),97.8 (C-1″),36.5 (C-2″),79.9 (C-3″),83.5(C-4″),72.3 (C-5″),19.0 (C-6″),57.4 (3″-OCH3),102.4 (C-1‴),73.6 (C-2‴),84.4 (C-3‴),74.9 (C-4‴),72.1 (C-5‴),19.4 (C-6‴),62.4 (3‴-OCH3)。以上数据与文献[16] 报道基本一致,故鉴定为通关藤苷I。
4 细胞毒活性研究
采用MTT 法进行细胞毒活性评价[17]。将处于对数生长期的A549、Bel-7402 细胞用0.25% 胰酶消化成细胞悬液,调整细胞密度为5×104/mL,接种于96 孔板中,每孔100 μL,培养24 h 后,吸弃原培养液,分为对照组、阳性组(5-氟尿嘧啶)、实验组。除对照组外,其余各组加入含相应的培养基,质量浓度为12.5、25、50、75、100 μg/mL,每孔100 μL,设置3 个复孔,对照组加入等体积无血清培养基。给药48 h 后,每孔加入20 μL 5 μg/mL MTT 溶液,混匀后孵育4 h,吸弃上清液,加入150 μL DMSO,振荡混匀15 min,待其各孔中紫色结晶完全溶解后,在490 nm 波长处测定光密度(OD) 值,重复3 次,计算细胞存活率,公式为细胞存活率=(OD实验组/OD对照组) ×100%。通过SPSS 软件计算IC50值,数据以(±s) 表示。
结果显示,化合物1~2、7、10、12 能抑制A549、Bel-7402 细胞的生长,IC50值均小于25 μmol/L,具有细胞毒活性,其中化合物1~2 活性最强,与阳性药物5-氟尿嘧啶作用相当。其余化合物未显示出明显细胞毒活性,IC50值大于100 μmol/L。结果见表2。
表2 各化合物对A549、Bel-7402 细胞的IC50值(μmol/L,±s,n=3)Tab.2 IC50 values of various compounds on A549 and Bel-7402 cells(μmol/L,±s,n=3)

表2 各化合物对A549、Bel-7402 细胞的IC50值(μmol/L,±s,n=3)Tab.2 IC50 values of various compounds on A549 and Bel-7402 cells(μmol/L,±s,n=3)
化合物A549Bel-7402 1 8.3±1.37.5±0.4 7.7±0.89.2±0.7 7 14.6±1.820.4±1.2 9>10024.7±2.6 1014.6±1.322.4±1.8 1119.4±2.1>100 1220.9±1.117.0±2.0 5-氟尿嘧啶7.2±0.58.4±0.9 2
5 讨论
通关藤除传统应用外,亦开发成抗肿瘤药物——通关藤注射液(消癌平注射液),用于恶性肿瘤,尤其是原发性肝癌、食管癌、胃癌,还具有改善免疫功能、减毒增效作用,常与细胞毒性化疗药物联合应用于肿瘤的治疗[18],但其抗肿瘤作用物质基础尚不明确[19]。本研究首次对通关藤水提取物中的化学成分进行研究,从中分离得到12 个化合物,其中新化合物1 个,新的天然产物1 个,首次从通关藤中分得的化合物4 个;此外,还分得通关藤苷H、I、G 等。研究发现,通关藤苷元A、通关藤苷H 等具有保护肝癌小鼠肝功能、抑制鼻咽癌细胞增殖及转移等作用[20-21]。本研究结果亦发现,通关藤醇A、12-O-惕各酰基-通关藤苷元A、通关藤苷元A、通关藤苷H、通关藤苷I 等C21甾体类化合物均具有细胞毒活性,本研究结果丰富了通关藤的抗肿瘤作用物质基础,为其进一步开发利用提供了科学参考。

