热带西太平洋沉积物浮游有孔虫壳体发育过程的三维重建与壳体形态对生态和古海洋的指示意义
段佰川,李铁刚
自然资源部第一海洋研究所,青岛 266061
生物体的形态受功能和结构约束的影响,这意味着生物体的形态特征与其所处的环境和生态系统有关。然而,某些无运动能力的浮游生物,如浮游有孔虫、放射虫和硅藻等,这类生物的矿化骨骼具有多样的形态特征,但目前这些特征并不能提供明确的功能信息。有人提出,无运动能力的浮游生物的骨骼在调节水柱中的受力平衡方面起到一定作用[1-2],但其产生作用的机制尚不清楚。
浮游有孔虫是一类重要的具有生物矿化壳体的浮游单细胞原生生物,广泛分布于全球海洋中。其壳体形态进化模式已经得到广泛研究[3]。这一类群在生物演化史中的成功和其丰富的多样性一部分归因于它们能够利用生活水体中的垂直栖息地分区[4]。浮游有孔虫不仅具有因属种而异的平均栖息深度,而且在其个体生长过程中也会发生栖息深度的变化,然而,控制它们垂直分布的因素仍然不明确[5],前人提出了钙质壳体在调节这一类群的浮力和水体中垂向位置的作用[1]。此外,浮游有孔虫的形态分层与它们在上层水体中所生活的不同深度相对应[4]。因此,浮游有孔虫的功能形态、生活深度和垂直迁移之间可能存在密切关系。研究者提出了多种浮游有孔虫维持悬浮状态的机制,包括利用海洋表层的湍流再悬浮[6],浮游有孔虫细胞质中原生质组成(如原纤维体)的生理调节[4,7-8],以及骨架本身也有拖曳的特征和结构[9]。另外,浮游有孔虫的垂向迁移除了自身的因素,也与水团的性质密切相关,如温度、盐度、营养状况等的影响[4]。
为了更好地理解浮游有孔虫壳体的形态功能,研究不仅需要关注总体形态,而且还需要关注壳体的生长过程。浮游有孔虫在生长过程中遵循特定规律,即在其现有的壳体外生长新的房室,壳体的总体形态主要由这些房室的生长过程决定[4,10-12]。尽管理解形态功能对于研究浮游有孔虫的生物学、生态学和演化过程具有重要意义,但目前对此的认识仍然有限[13-14]。Lipps[15]的研究表明,壳体形态可能与有孔虫的密度、浮力以及抵抗下沉和湍流的能力有关。Caromel[13]则查明了大小、形状和钙化对沉降速度的影响,表明这些因素的内在限制可能比流体动力学功能更重要,决定了浮游有孔虫的深度分布和壳体形态。然而,个体发生过程作为总体形态的主要制约因素,却很少进行相关的研究。
对于有孔虫而言,钙质壳体内部记录了个体发育的过程,并可以使用各种方法进行分析[16-20]。在这些方法中,高分辨率X 射线扫描和三维重建因其准确性、全面性和非破坏性而脱颖而出[21]。这种方法已成功应用于底栖有孔虫,提供了可视化、基本测量[22-24],并揭示了细胞生长(通过腔室体积表示)与自然节律相关的恒定且显著的振荡[25]。在浮游有孔虫的研究中,这种方法已被用于研究进化与发育之间的联系,揭示壳体的生长和结构的基本模式[26],并证明在个体发育过程中表面积与体积比的变化可以影响有机体对环境变化的脆弱性[12,27]。尽管取得了这些进展,与底栖有孔虫相比,浮游有孔虫中观察到的多样的壳形态的生态学意义仍然不明确。
为了解浮游有孔虫如何通过钙质壳体的增长调节其受力,并理解壳体形态的生态学意义,本文重点研究了温跃层无刺浮游有孔虫属种个体。这些属种受到表面湍流的影响较小,且不具有像棘刺或外延的原生质网等复杂结构,这些结构会产生额外的下沉阻力。在这些相对简单的形态中,低密度的原生质可能是抵消钙质壳体重力的主要因素,使得浮力调节过程相对于有刺类群更为简单。本研究的目标是利用高分辨率X 射线扫描和三维重建技术,结合一定的假设,揭示钙质壳体的发育如何影响这些生物的迁移行为。
1 材料和方法
1.1 样品选择
本研究选择了5 个无刺浮游有孔虫的标本进行研究:Globorotalia menardii、G. tumida、G. truncatulinoides、 Pulleniatina obliquiloculata和Candeina nitida。此外,还选择了一种混合层种Globigerinoides ruber用于比较研究。这些标本来自于热带西太平洋海底沉积物柱状样顶部样品,海水深度约2 000 m。选择这个深度是为了确保标本的完全发育,并展示我们的方法在沉积物样品中的适用性。
标本的保存状态是一个重要考虑因素。无论是壁内还是壁外的矿物沉淀都可以与生物矿化骨架区分开,并可以在图像处理过程中去除。溶解是一个更大的挑战,因为它很容易影响到壳体的内部房室,导致早期生长阶段的数据丢失。然而,本研究使用的所有标本都保存了从第一个房室到最后一个房室的完整生长序列,表明保存状态良好。本研究在选择扫描个体时,在大量个体中进行筛选,选择了形状、大小具有代表性特征,保存完整且无不规则发育房室的个体,具有一定的普遍意义。
1.2 断层扫描
无论是Micro-CT 还是SRXTM(同步辐射X 射线断层显微术)[21]都可以提供适合我们研究的高分辨率图像,而SRXTM 技术更加方便。上述标本在上海同步辐射装置的BL13W 站进行扫描,像素长度为0.65 μm。扫描标本时旋转了180°,拍摄了501 个投影。X 射线束的能量设定为14.5 keV,以优化最大对比度。然后,使用Lanczos 滤波器对数据集进行重采样,并将像素大小增加一倍,以获得更好的信噪比和更快的计算速度。
1.3 三维重建
该研究使用Amira 5.3.2 软件(Mercury Computer Systems Ltd, www.tgs.com)进行了重建和分析。每个腔室的壳体和腔室需要手动分割重建。基于其不同的形态和灰度,将钙质壳体中的次生成分(例如包括的沉积物和自生矿物)手动去除。壳体和腔室的体积直接从软件中提取。
1.4 个体发育过程中的平均密度
如上所述,我们假设对于温跃层种无刺浮游有孔虫,平均密度是调节浮力的主要因素,因此可以通过重建个体发育过程中的平均密度变化分析浮力调节。在这里,我们模拟发育过程中个体的密度变化,假设钙质壳体完全被原生质填充,并拥有一定量的壳外原生质。这可以表示为方程:
其中,ρn.mean为具有n个腔室的生物体的平均密度;ρcyt为有孔虫原生质的湿密度,ρcal为2.71g/cm3;Vi.shell和Vi.cav分别为从初房开始数第i个腔室的壳和腔室的体积;Vextra为外部原生质的体积。目前关于ρcyt在个体发育或物种间的变异还不清楚。在这里,我们使用Korsun[28]计算的1 g/cm3作为一个近似估计值。
估算Vextra的过程遵循了无刺浮游有孔虫腔室形成的报道过程[4]。我们设想了两个腔室形成过程的快照,其中第一个是在腔室的芽胚(bulge)形成和钙化过程开始之前。此时,外壳原生质被收回到壳内,然后一个具有薄透明膜覆盖和光密内部的细胞质凸起从孔口产生,同时新腔室的轮廓由原始腔室形成,但没有钙质添加到壳内[4]。此时,将新形成的腔室的体积分配给Vextra。因此,我们可以计算每个腔室形成过程中的这些特定时间片段的平均密度,用方程(2)表示为densitymin。
我们考虑的第二个个体发育阶段是当所有原生质完全缩回到壳内并填满壳腔时,假设这个阶段代表了一个健康个体所需要的最少原生质量,对应于每个个体发育阶段的最大密度。使用方程(3)来计算ρn.max,表示为densitymax,即个体的平均密度的上限。
每个发育阶段中通过计算得到的平均密度只能近似于实际密度,主要误差来自于每个浮游有孔虫物种原生质密度数据的缺失,以及由于壳体分层所导致的难以准确分离各个阶段的壳体,目前尚无法弥补这些缺陷方法,需要进一步的研究。尽管存在这些限制,我们认为模型捕捉到了细胞体积、室壁形状和厚度变化对生命周期中个体密度影响的重要方面,并可能控制浮力和垂直迁移。
本研究中还包括了一种混合层栖息的有刺浮游有孔虫G. ruber,采用方程(2)和(3)进行比较。尽管无刺属种和有刺属种具有相似的室内增加模式,混合层湍流可能为G. ruber和其他混合层属种提供额外的浮力[6],而刺和原生质的结合可能显著影响其流体动力学特性,并使浮力调节过程复杂化,本研究不做深入探讨。
2 结果
研究重建了6 个浮游有孔虫标本的个体发育序列,所有标本都显示出了较为保守一致的发育过程,如表1 所示。对于生长过程中房室大小的变化,第二个房室较初房变小,之后的房室体积迅速增大,总体积呈指数级增长,直至终房增长速度可能出现放缓(G. menardii、G. tumida)或减小(C.nitida)。对于生长过程中形态的变化,所有属种在初期阶段都是平旋,之后变成各个属种独特的形态。
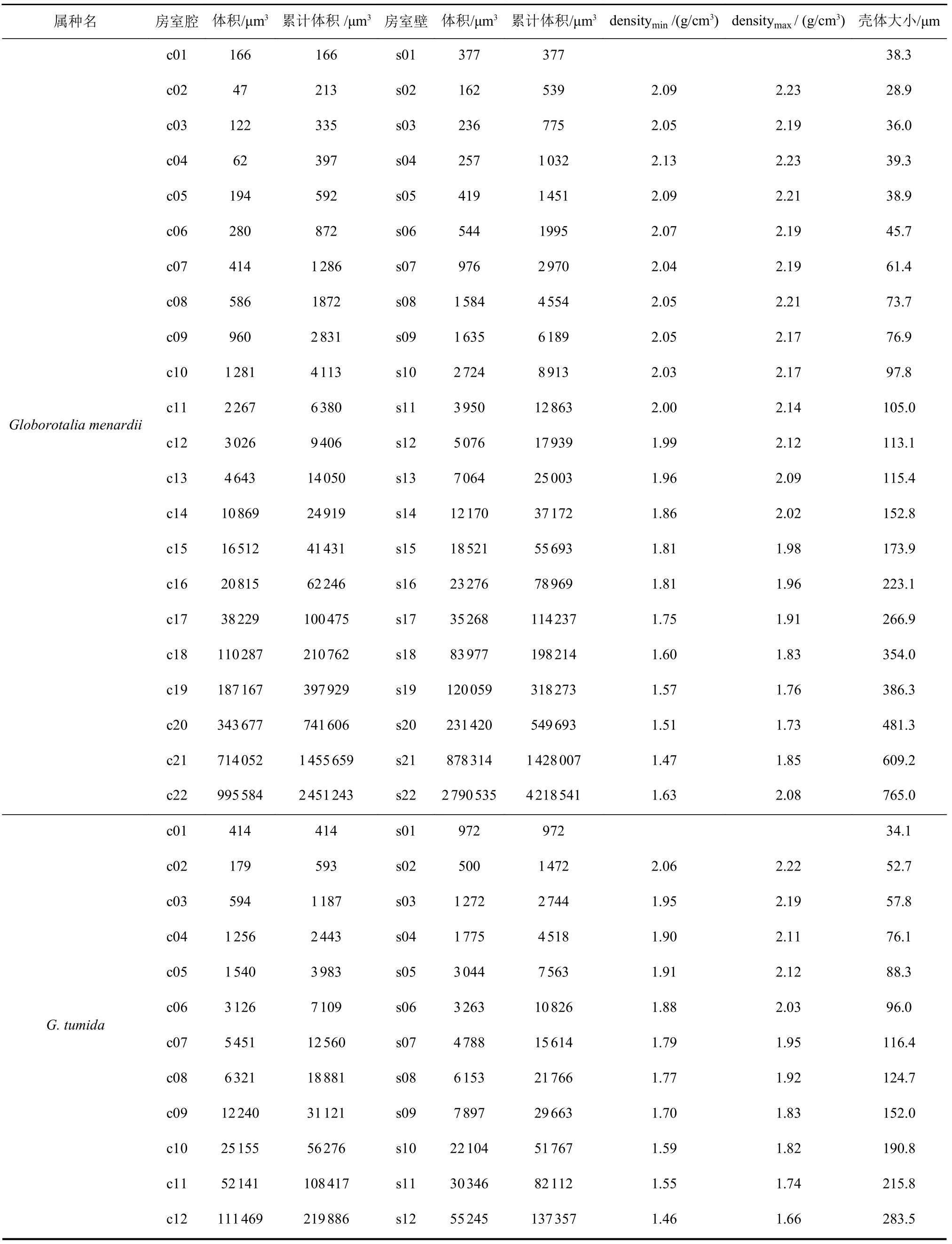
表1 6 个研究标本的壳体数据统计Table 1 The test data of six research specimens of Globorotalia menardii, G. tumida, G. truncatulinoides, Pulleniatina obliquiloculata,Candeina nitida, and Globigerinoides ruber. The data includes the volume (μm3) of each chamber and shell, the calculated mean density value (g/cm3), and the test dimensions (μm)
使用软件识别了每个生长阶段的房室腔和房室壁,并计算了它们的体积。使用方程(2)和(3),计算了上述两个转变阶段中生物体(壳体加原生质)的平均密度。每个标本的平均密度数据见表1。这里,使用densitymin和densitymax来代表ρmin和ρmax,其中densitymax表示每个生长阶段健康的浮游有孔虫可能达到的最大密度。如下所示,平均密度为1.20~2.23 g/cm3,这在野外实际观察或估算[29-31]的合理范围内。
G. menardii标本由22 个房室组成,个体发育导致了平均密度的总体降低(图1A,图2)。densitymin从3 个房室阶段的2.13 g/cm3降至20 个房室阶段的1.47 g/cm3。由于厚碳酸钙外壳的生长,densitymin在21 个房室阶段开始增加,并达到1.63 g/cm3。densitymax显示了类似的趋势,最终阶段的值为2.08 g/cm3,接近个体发育初始阶段的densitymin2.09 g/cm3,其主要原因是形成了厚碳酸钙外壳。

图1 6 个研究标本的个体发育平均密度变化和壳体生长模式Fig.1 The mean density and size growth patterns of six study specimens (Globorotalia menardii, G. tumida, G. truncatulinoides,Pulleniatina obliquiloculata, Candeina nitida, and Globigerinoides ruber)

图2 Globorotalia menardii 个体发育过程的三维渲染图字母序号代表每个生长阶段。比例尺分别表示以下长度数值,A: 20 μm,B: 14 μm,C: 16 μm,D: 16 μm,E: 16 μm,F: 17 μm,G: 23 μm,H: 33 μm,I:30 μm,J: 37 μm,K: 35 μm,L: 37 μm,M: 37 μm,N: 53 μm,O: 56 μm,P: 76 μm,Q: 85 μm,R: 113 μm,S: 118 μm,T: 145 μm,U: 178 μm,V, W, X: 211 μm。Fig.2 Three-dimensional rendering of the ontogeny of Globorotalia menardii
G. tumida标本由19 个房室组成,形状与G. menardii相似,个体发育的平均密度变化趋势显示出不同的模式(图1B,图3)。densitymin从1 个房室阶段的2.06 g/cm3降至12 个房室阶段的1.40 g/cm3,然后在18 个房室阶段增加至1.58 g/cm3。densitymax显示类似的模式,只有在个体的最终阶段,由于厚碳酸钙外壳的增加,进一步将密度增加至1.90 g/cm3,接近初始密度2.06 g/cm3。
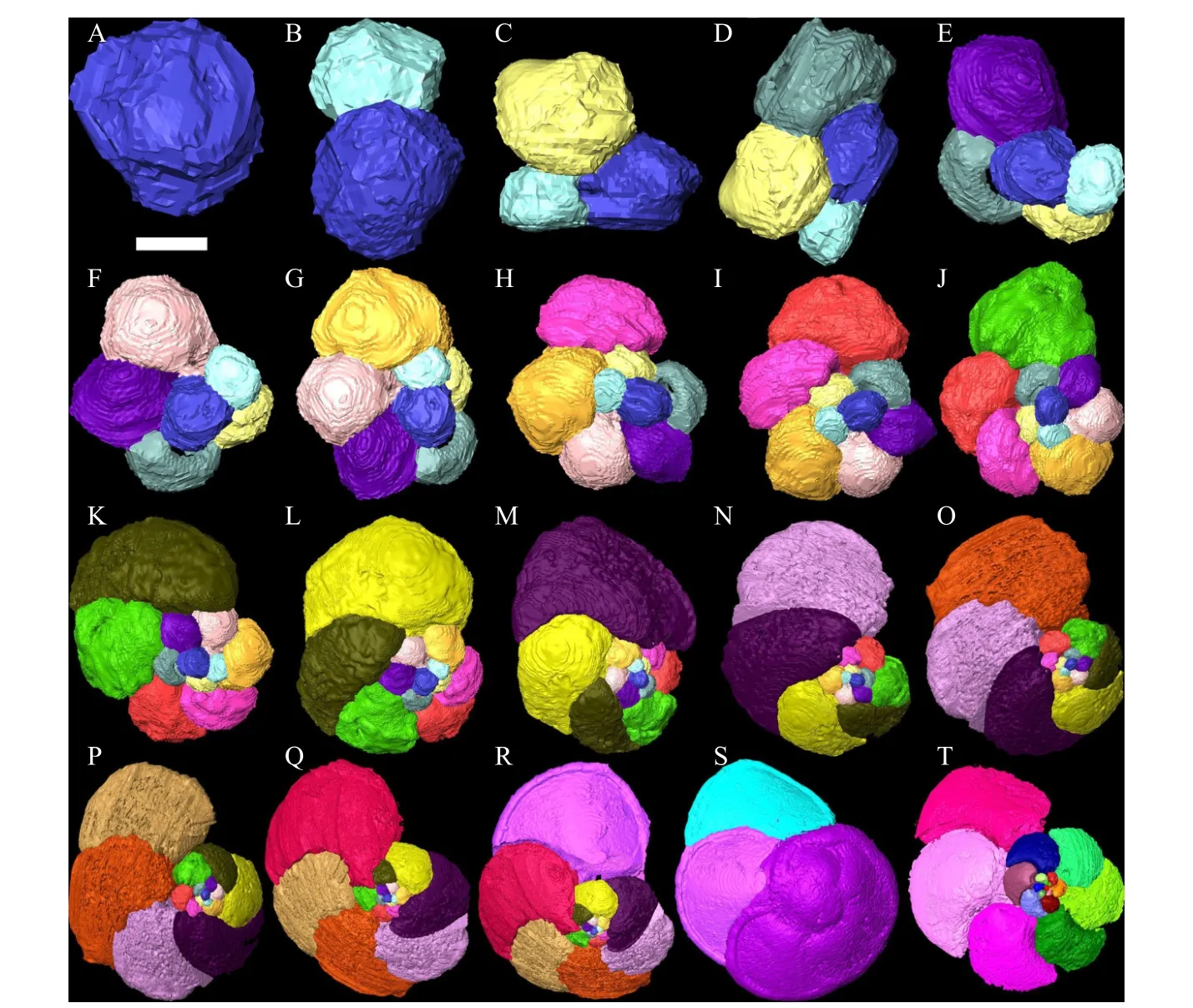
图3 Globorotalia tumida 个体发育过程的三维渲染图字母序号代表每个生长阶段。比例尺分别表示以下长度数值,A: 12 μm,B: 15 μm,C: 18 μm,D: 22 μm,E: 27 μm,F: 31 μm,G: 35 μm,H: 41 μm,I:47 μm,J: 57 μm,K: 67 μm,L: 83 μm,M: 112 μm,N: 151 μm,O: 163 μm,P: 192 μm,Q: 224 μm,R: 274 μm,S, T: 304 μm。Fig.3 Three-dimensional rendering of the ontogeny of Globorotalia tumida
G. truncatulinoides标本含有17 个房室,密度变化模式较为复杂(图1C,图4)。密度最小值从初房阶段的1.96 g/cm³增加到5 个房室阶段的2.00 g/cm³,然后在16 个房室阶段下降到1.49 g/cm³,在12 个房室阶段,这种下降趋势发生变化。然而,密度最大值显示,从4 个房室阶段到6 个房室阶段,以及从9 个房室阶段到12 个房室阶段,增长趋势更为明显。最终阶段显示密度最大值为1.87 g/cm³,接近初始密度最小值1.96 g/cm³。
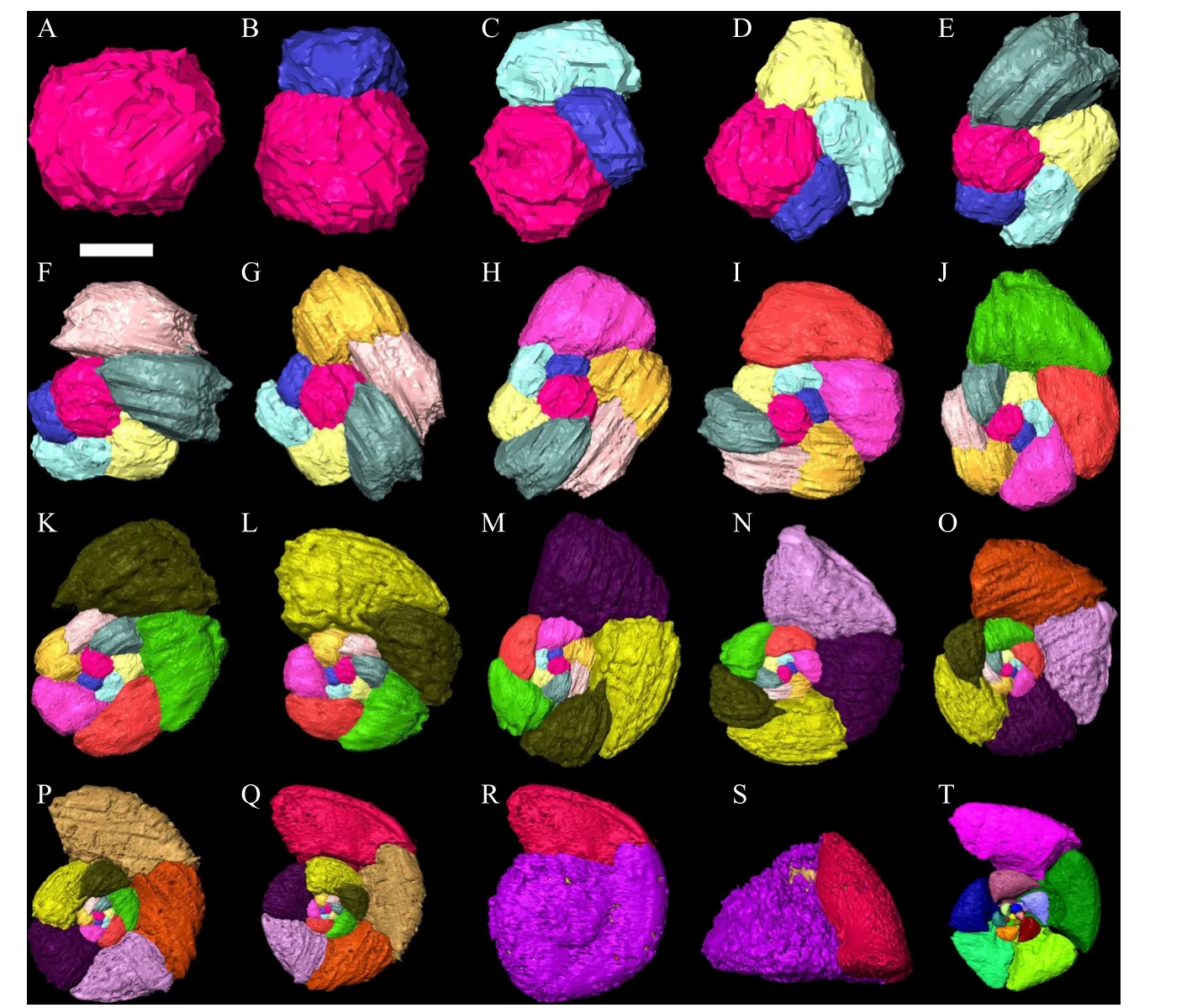
图4 Globorotalia truncatulinoides 个体发育过程的三维渲染图字母序号代表每个生长阶段。比例尺分别表示以下长度数值,A: 9 μm,B: 13 μm,C: 15 μm,D: 18 μm,E: 23 μm,F: 28 μm,G: 30 μm,H: 34 μm,I:40 μm,J: 50 μm,K: 58 μm,L: 76 μm,M: 89 μm,N: 112 μm,O: 134 μm,P: 160 μm,Q, R, S, T: 200 μm。Fig.4 Three-dimensional rendering of the ontogeny of Globorotalia truncatulinoides
P. obliquiloculata标本由13 个房室组成,个体生长导致了密度最小值从初房阶段的1.73 g/cm3迅速减小到7 个房室阶段的1.29 g/cm3(图1D,图5)。从8 个房室阶段到12 个房室阶段,密度最小值逐渐从1.28 g/cm3降低到1.22 g/cm3。密度最大值显示类似的趋势,厚碳酸钙外壳的形成大大增加了密度最大值,达到了1.63 g/cm3的最终阶段,接近初始密度最小值1.73 g/cm3。总体而言,密度较Globorotalia属的个体低,这主要是由于其房室形状更接近球形,且细胞质与壳体碳酸盐的比例较高有关。
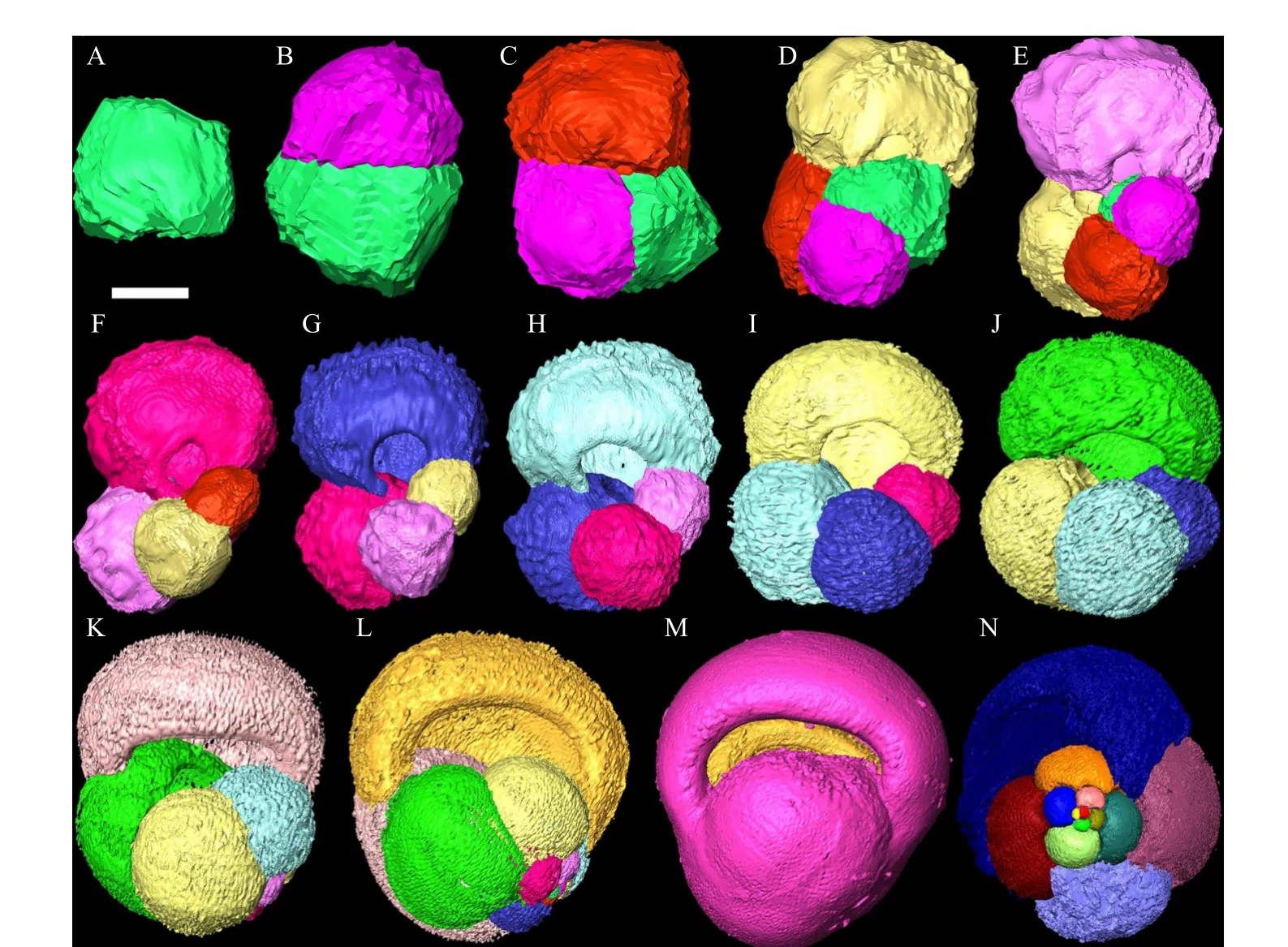
图5 Pulleniatina obliquiloculata 个体发育过程的三维渲染图字母序号代表每个生长阶段。比例尺分别表示以下长度数值,A: 16 μm,B: 15 μm,C: 17 μm,D: 23 μm,E: 30 μm,F: 41 μm,G: 55 μm,H: 68 μm,I:85 μm,J: 103 μm,K: 115 μm,L: 130 μm,M, N: 170 μm。Fig.5 Three-dimensional rendering of the ontogeny of Pulleniatina obliquiloculata
C. nitida标本含有14 个房室(图1E,图6)。个体生长过程中的密度最小值较低,并呈现出总体下降的趋势,范围从2 个房室阶段的1.75 g/cm3减小到12 个房室阶段的1.24 g/cm3。可以识别出两个生长阶段:密度最小值先从1 个房室阶段的1.50 g/cm3迅速下降到6 个房室阶段的1.25 g/cm3,然后在1.57 g/cm3到1.70 g/cm3之间振荡,直到最后阶段。1 个房室阶段的密度下限为1.50 g/cm3,数值异常低,可能与它在现代浮游有孔虫中拥有最大的初房有关;最后一个阶段的密度上限相对较低,没有额外的方解石沉淀。
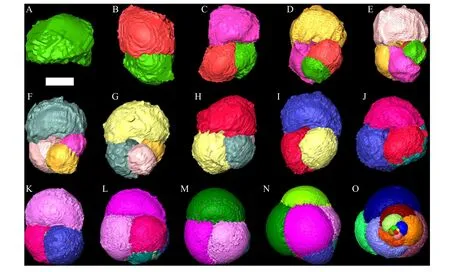
图6 Candeina nitida 个体发育过程的三维渲染图字母序号代表每个生长阶段。比例尺分别表示以下长度数值,A: 13 μm,B: 17 μm,C: 23 μm,D: 29 μm,E: 37 μm,F: 49 μm,G: 63 μm,H: 77 μm,I: 92 μm,J: 110 μm,K: 138 μm,L: 154 μm,M: 166 μm,N, O: 171 μm。Fig.6 Three-dimensional rendering of the ontogeny of Candeina nitida
G.ruber标本中包含17 个房室,最后一个阶段出现钙化(图1F,图7)。密度下限从2 房室阶段的2.13 g/cm3降至12 房室阶段的1.43 g/cm3,然后在1.57 g/cm3至1.70 g/cm3之间振荡,直到最后阶段。密度上限呈类似趋势。值得注意的是,在11 房室阶段和15 房室阶段之间,密度上限和密度下限之间的差异特别大。
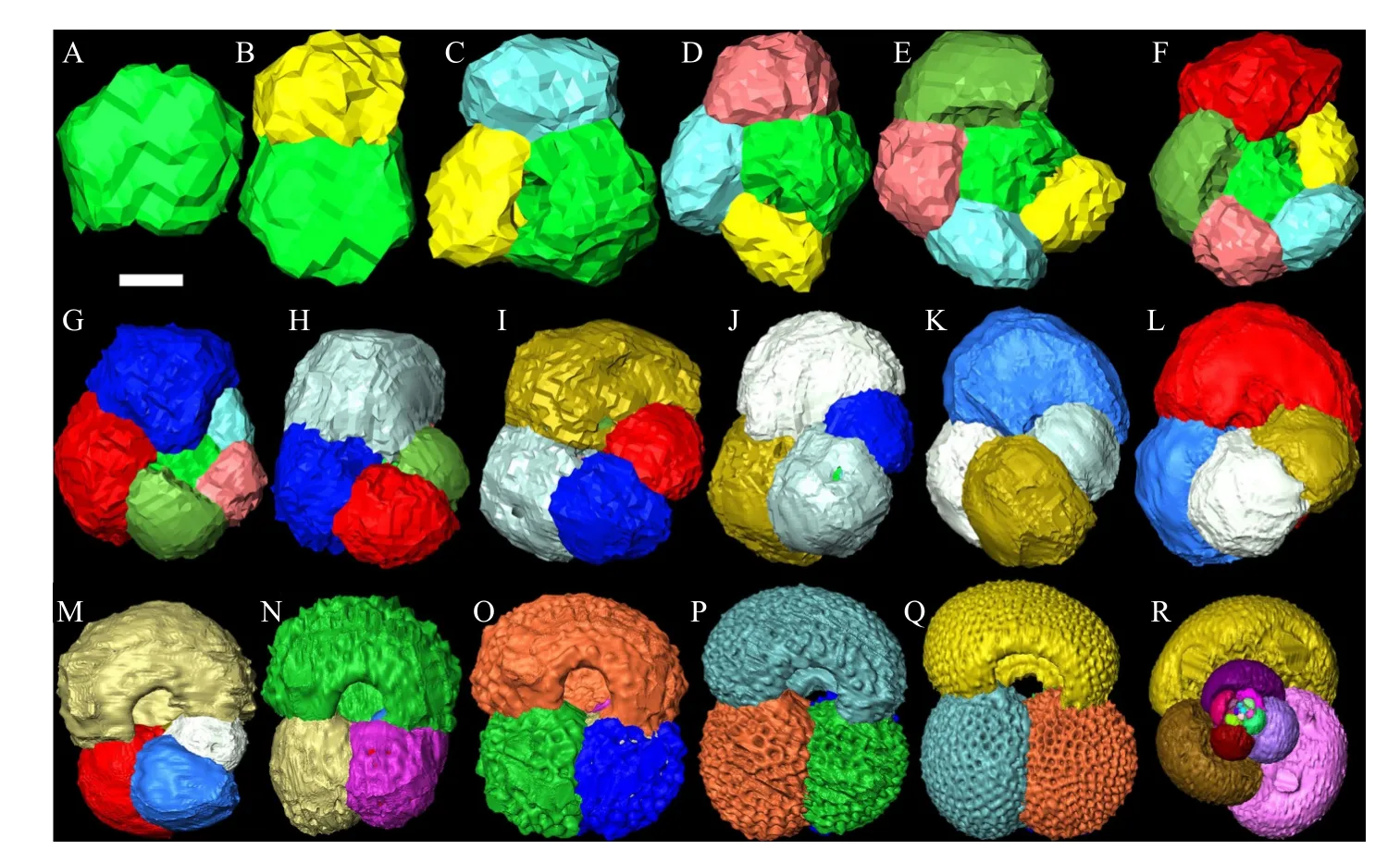
图7 Globigerinoides ruber 个体发育过程的三维渲染图字母序号代表每个生长阶段。比例尺分别表示以下长度数值,A: 6 μm,B: 6 μm,C: 6 μm,D: 9 μm,E: 9 μm,F: 11 μm,G: 13 μm,H: 16 μm,I: 17 μm,J: 19 μm,K: 23 μm,L: 28 μm,M: 39 μm,N: 58 μm,O: 69 μm,P: 83 μm,Q, R: 96 μm。Fig.7 Three-dimensional rendering of the ontogeny of Globigerinoides ruber
3 讨论
个体发育的平均密度变化可能与浮游有孔虫的垂直迁移行为中特定物种对壳体功能的调节密切相关[4,32-34]。通过流体动力学的方法,模拟得到了壳体大小和形状对沉降的影响[13],结果表明当物体密度保持恒定时,沉降速度与大小近似呈线性关系,而与形状无关。在这里,我们增加了对壳体和细胞质质量,即平均密度,在个体发育过程中的相对贡献的考虑,这在研究的标本中表现出显著的种间差异。尽管前人研究了包括大小、总体形状、横截面形状、盘卷方向和个体发育过程等在内的许多壳体的形态指标,以确定形态与生活环境的关系[27,29,35-39],但本工作针对个体生长过程中平均密度变化模式的特定生态意义的研究为进一步讨论潜在机制提供了可能。
我们提出,受densitymin和densitymax的约束,平均密度变化模式界定了壳体调节浮力以维持生理功能的范围。其中,densitymin表示个体在特定发育阶段结束时可以达到的最小平均密度,而densitymax表示后续阶段中该个体在健康状态下的最大平均密度(假设细胞质在最后阶段不收缩)。 在此范围内的所有平均密度值对该个体来说都是可用的,由钙质壳体和细胞质质量的比率决定。因此,对于温跃层无刺浮游有孔虫属种,个体发育过程中的个体平均密度变化可能由水团的性质、食物、光线等因素共同作用,决定了浮游有孔虫的垂向迁移行为。
3.1 浮游有孔虫个体生长过程中平均密度变化的生态意义
温跃层无刺浮游有孔虫属种的平均密度变化可能是调节它们浮力状况的因素之一,并可能控制幼年阶段上升和末期阶段下沉。在幼年阶段,所有研究的标本都显示出慢速增长、扁平的低螺旋的形状,并且雷诺数低于0.5[13],这可能导致较慢的沉降速度或悬浮。在个体生长的末期阶段,钙质加厚会显著增加平均密度,而对壳体大小影响不大,从而导致下沉行为。对于中间阶段,平均密度变化可能不是流体力学性质的主要控制因素,而壳体形状的多样性、壳体尺寸的比较快速增大以及雷诺数的变化使调节过程复杂化。我们认为,在这些阶段,平均密度和壳体形状变化共同影响流体力学行为,可能是影响多样化的垂直分布的因素之一。
对于本研究中的温跃层无刺浮游有孔虫属种个体,个体发育过程的平均密度变化模式显示在约100 μm 之前,densitymin和densitymax都呈缓慢下降趋势,之后有所下降,而densitymin和densitymax主要在最后两个腔室中明显增大。尽管在不同的属种之间存在差异,在前期发育阶段中,densitymin和densitymax之间的差异表现出相对稳定的值,表明这些发育阶段的壳体具有类似的调节能力范围。从成年阶段开始,densitymin和densitymax之间的差异逐渐增加,扩大了调节能力范围,并对应着更大的迁移范围。在最后阶段中密度最大值的显著增加极大地提高了生物体下降的能力,这与繁殖有关。
本研究分析了混合层有刺浮游有孔虫G.ruber以进行比较。结果表明,其密度变化模式可能与浮力没有直接关系,因为该物种具有刺和大量外部细胞质。从1 个腔室至10 个腔室阶段的个体发生发育密度显示出迅速下降的趋势,而壳体的尺寸缓慢增加;这些阶段存在刺[18],这可以极大地提高其下沉的阻力(图7F)。这些特征可能表明了一个快速的上升过程。在11 个腔室阶段之前,densitymin和densitymax之间的差异表现出微小的振荡,表明相对稳定的浮力调节能力。然而,从12 个腔室到最终阶段,平均密度变化显著,densitymin和densitymax之间的差异显著增加,表明其增强的负浮力调节能力,可能受到混合层湍流、壳体刺状构造和外壳原生质网的影响。
3.2 对浮游有孔虫的形态演化和古海洋学意义的启示
作为无自主运动能力的浮游生物,浮游有孔虫如何调节其在水体中的垂直位置仍然是个悬而未决的问题。先前的研究表明,这个过程可能与壳体形态的多样性有关,但机制尚不清楚。我们认为,浮游有孔虫壳体中记录的平均密度变化的信息可能对解决此类问题至关重要,并且通过分析可以更好地理解浮游有孔虫壳体形态的多样性。有孔虫成年个体的壳体形态是通过增加不同形状、位置和壁厚的新房室来构建的[10-12],这导致了不同发育阶段平均密度的差异。这种差异可以改变浮力状态和浮力调节范围,从而成为影响占据水体中不同的垂直生态位的因素之一。为了适应变化的水体分层结构,浮游有孔虫可以通过个体生长过程中的形态变化实现浮力的调节,最终表现为壳体形态的演化。
另一个重要的领域是利用沉积物中的浮游有孔虫的壳体来恢复古海洋学和古气候学的信息。虽然形态学是生物生活环境的重要指标,但是对浮游有孔虫壳体形态而言,这方面的研究并不广泛。主要原因是壳体的形态功能并不清晰,也没有有效的指标来将形态学与古海洋变量联系起来。壳体形态的演化受到个体发育进程的影响,反映了生物体适应水体结构或营养层变化而调节浮力的能力的过程。因此,定量化的壳体形态的变化指标可能成为古代海洋水体分层结构变化的一个潜在指标。
4 结论
作为调节浮游有孔虫流体动力学行为的重要因素,平均密度在个体发育过程中显示出相当大的变化,并且其变化模式在不同形态的种类中也有所不同。平均密度的变化可能是调节浮游有孔虫在初始和最终阶段垂直迁移的影响因素之一。温跃层无刺浮游有孔虫个体发育过程中的平均密度变化显示,形态变化通过个体发育导致不同浮力调节能力,限制了个体发育过程中的垂直迁移行为。有刺浮游有孔虫G. ruber的结果显示,其个体发育后期的平均密度变化显著,表明壳刺对浮力调节的较大影响。这种认识对浮游有孔虫的形态演化和古海洋应用具有重要意义。个体发育中的平均密度变化可能是浮游有孔虫在个体发育过程中实现垂向迁移的方式之一。浮游有孔虫壳体形态差异反映的个体发育过程中平均密度的变化可能与水团的性质、食物、光线等因素共同作用,决定了浮游有孔虫的垂向迁移行为。本文提出了在古海洋学应用中引入浮游有孔虫壳体形态指标,尤其是恢复古海洋水体结构方面的可能性。
致谢:感谢上海同步辐射光源BL13W 站的何友、谢红兰和付亚楠对扫描工作的帮助,同时感谢“科学”号科考船和船员对沉积物样品采集的帮助。

