生长分化因子15变化轨迹对老年非ST段抬高型急性冠状动脉综合征患者预后的预测价值
叶芳 阮筱珠 朱夏玲
323020 丽水市中心医院心血管内科 温州医科大学附属第五医院
生长分化因子15(growth differentiation factor 15,GDF-15)是一种反映细胞应激和炎症而分泌的细胞因子,其水平与多种主要不良心血管事件(major adverse cardiac events,MACE)相关[1-2]。据报道,GDF-15对于急性冠状动脉综合征(acute coronary syndrome,ACS)随访发生心力衰竭相关入院(hospitalization for heart failure,HHF)或死亡风险有较高的临床预后预测价值[3-4]。近期发布的《生长分化因子-15在急性冠状动脉综合征中急诊临床应用的专家共识》建议ACS患者早期检测GDF-15用于患者危险分层、评估预后[5]。然而,既往研究较少纳入老年非ST段抬高型ACS(non-ST-segment elevated ACS,NSTE-ACS)患者,且GDF-15的动态变化轨迹是否能增加预后预测价值尚不清楚[6]。此外,使用GDF-15能否预测恶性室性心律失常的研究也很少。因此,我们通过回顾性分析丽水市中心医院心内科临床试验数据库,比较不同GDF-15变化轨迹对老年NSTE-ACS患者随访3年发生MACE风险的预测价值,并分析影响MACE的相关因素。
1 对象和方法
1.1 研究对象
回顾性队列研究。分析浙江丽水市中心医院的临床试验数据库,共纳入2015年1月至2020年1月入住心内科的1 522例老年NSTE-ACS患者,每例患者每年至少测量一次GDF-15水平。利用潜在混合模型识别暴露期间 (2016—2023年) 的GDF-15水平确定了五种不同变化轨迹:低水平-稳定(Q1组,620~1 324 ng/L,248例)、中低水平-稳定(Q2组,1 325~1 576 ng/L,366例)、中高水平-稳定(Q3组,1 577~1 783 ng/L,559例)、高水平-稳定(Q4组,1 784~1 991 ng/L,274例)和高水平-升高(Q5组,>1 991 ng/L,75例)。
纳入标准:(1)年龄60~85岁,男女不限;(2)NSTE-ACS的诊断符合《 非ST段抬高型急性冠状动脉综合征基层诊疗指南(2019年)》[7],包括急性胸痛、胸闷等临床症状以及心电图和心肌酶等实验室检查结果;(3)入院前6个月无ACS发生;(4)GDF-15等临床资料完整,无缺失;(5)同意并完成随访3年的计划。排除标准:(1)年龄≥86岁或年龄<60岁;(2) 合并肺栓塞、主动脉夹层等;(3)入院前6个月发生ACS、急性心力衰竭、急性呼吸衰竭、急性肝肾功能衰竭;(4) 入院前6个月进行大手术;(5)合并肿瘤等严重疾病,预期寿命少于1年;(6)精神异常或认知障碍,难以配合完成研究;(7)基线和随访结局数据缺失。
本研究纳入的所有患者或亲属知情同意,符合医学伦理的要求,我院伦理委员会已经审核并批准[伦理号:科研伦审(2023)第(132)号]。
1.2 方法
根据研究计划书,从我院电子病历系统整理收集患者的基线临床资料,包括:(1)人口学资料,例如年龄、性别、吸烟、饮酒和体质指数;(2)病史资料,例如糖尿病、高脂血症、陈旧心肌梗死、冠状动脉血运重建、既往卒中、心房颤动、慢性肾脏病;(3)NSTE-ACS类型,包括不稳定性心绞痛、非ST段抬高型心肌梗死;(4)实验室检查资料,例如血常规、空腹血糖(fasting blood glucose,FBG)、肌钙蛋白I(troponin I,TNI)、N末端B型利钠肽原(N-terminal pro-B-type natriuretic peptide,NT-proBNP)、GDF-15、尿酸、血肌酐、总胆固醇(total cholesterol,TC) 、三酰甘油(triglyceride,TG) 、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C) 、高密度脂蛋白胆固醇 (high-density lipoprotein cholesterol,HDL-C) ;(5)冠状动脉情况:SYNTAX评分、左主干/三支病变比例;(6)超声心动图资料,例如左心室射血分数、左室收缩末期内径、左室舒张末期内径、左心室质量指数;(7)药物治疗资料,例如抗血小板、抗凝、钙通道阻滞剂、血管紧张素转换酶抑制剂(angiotensin-converting enzyme inhibitors,ACEI)、血管紧张素Ⅱ受体阻滞剂(angiotensin Ⅱ receptor blockers,ARB)、盐度质激素受体拮抗剂(mineralocorticoid receptor antagonist,MRA)、β受体阻滞剂、利尿剂和他汀;(8)再灌注治疗资料,例如溶栓、经皮冠状动脉介入治疗、冠状动脉旁路移植。
1.3 随访计划
由我科两名受过临床试验培训、专门负责本研究的医师进行随访计划,主要通过随访门诊或电话进行。记录随访3年的MACE风险发生情况,包括死亡、HHF或室性心律失常(需植入心脏转复除颤器治疗的室性心动过速/心室颤动)的复合事件。
1.4 统计学方法

2 结果
2.1 各组患者的基线资料比较
如表1所示,1 522例老年NSTE-ACS患者中,男性805例(52.9%),年龄60~87岁,平均为(72.2±7.5)岁。五组的年龄、饮酒史、吸烟史、体质指数、糖尿病、心房颤动、非ST段抬高型心肌梗死的患病率以及血红蛋白、FBG、TNI、NT-proBNP、GDF-15、血尿酸、左室射血分数、左室收缩末期容积、SYNTAX评分和左主干/三支病变比例等的差异具有统计学意义(均为P<0.05)。

表1 五组患者的基线资料比较
2.2 各组患者的治疗比较
如表2所示,五组的治疗相似,但利尿剂应用率和急诊经皮冠状动脉介入治疗比例等的差异具有统计学意义(均为P<0.05)。

表2 五组患者的治疗资料比较
2.3 各组患者的预后比较
由表3所示,中位随访35个月期间,失访73例(4.5%)。随访期间共发生了206例(13.5%)MACE,包括37例(2.4%)死亡,104例(6.8%)HHF和65例(4.3%)室性心律失常(需ICD治疗的室性心动过速/心室颤动)。根据混杂变量校正后,GDF-15变化轨迹与HHF风险之间存在显著关联(HR=1.594,95%CI:1.035~2.743),与死亡风险之间也存在显著关联(HR=1.152,95%CI:1.007~1.441),但未发现GDF-15变化轨迹与室性心律失常(需ICD治疗的室性心动过速/心室颤动)风险之间存在显著关联(HR=1.137,95%CI:0.950~1.813)。
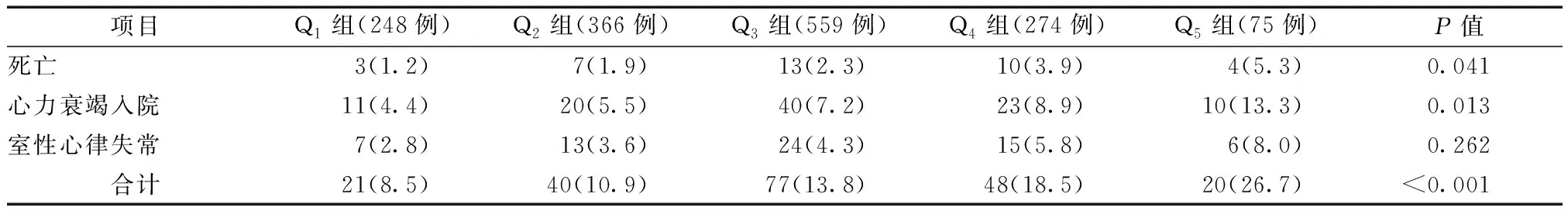
表3 五组患者随访预后情况比较[例(%)]
Kaplan-Meier生存分析和Log-Rank检验结果发现,与低水平-稳定组相比,高水平-升高组、高水平-稳定组、中高水平-稳定组和中低水平-稳定组的心力衰竭入院的HR分别是2.214(95%CI:1.493~3.285)、1.431(95%CI:1.137~1.834)、1.356(95%CI:1.108~1.647)和1.263(95%CI:1.026~1.529)。
2.4 患者发生MACE的危险因素分析
多因素Cox回归分析结果提示,GDF-15变化轨迹(HR=1.484)、年龄(HR=1.136)、吸烟史(HR=1.285)、陈旧心肌梗死(HR=1.247)、NT-proBNP(HR=1.425)、TNI(HR=1.293)、左室质量指数(HR=1.173)和ACEI/ARB治疗(HR=0.874)是发生MACE的相关因素。校正其他因素后,仍发现GDF-15变化轨迹与发生MACE显著相关(HR=1.264)。
2.5 GDF-15及其变化轨迹预测MACE的价值比较
ROC曲线结果显示(图1),GDF-15变化轨迹对MACE的预测价值较高(AUC=0.786),高于NT-proBNP(AUC=0.771)、GDF-15(AUC=0.755)和TNI(AUC=0.739)。

TNI:肌钙蛋白Ⅰ:CDF-15:生长分化因子15;NT-proBNP:N末端B型利钠肽原图1 各指标对心血管事件发生风险的预测价值比较
3 讨论
本研究纳入1 522例老年NSTE-ACS患者中,中位随访35个月。发现根据混杂变量校正后,GDF-15变化轨迹与HHF风险之间存在显著关联,与死亡风险之间也存在显著关联,但未发现GDF-15变化轨迹与室性心律失常(需要ICD治疗的室性心动过速/心室颤动)风险之间存在显著关联。ROC曲线显示GDF-15变化轨迹对MACE的预测价值较高。因此,GDF-15变化轨迹与老年NSTE-ACS患者随访发生MACE风险明显相关,提示连续测量GDF-15可优化老年NSTE-ACS患者的风险分层,具有重要的临床应用价值。
GDF-15变化轨迹可能能够提供识别老年ACS人群的MACE的发生风险。近期EurHeartJ上发表了一篇研究文章,研究人员使用来自8个试验(包括53 486例患者)的汇总数据进行个体患者荟萃分析。基线GDF-15水平作为一个连续变量进行分析,并使用已建立的临界点(<1 200 ng/L、1 200~1 800 ng/L和>1 800 ng/L)来评估其对HHF、心血管死亡/住院的预后性能,并使用经临床变量调整的Cox模型评估预测价值。结果发现,较高的GDF-15水平与心血管死亡率、HHF和MACE的增加显著且独立相关(均为P<0.001)。然而,GDF-15水平与发生心肌梗死和卒中的显著相关性仅在近期ACS后稳定患者中存在[8]。另一项研究也证实,GDF-15提高了预测死亡风险的价值。在一项全国性前瞻性研究-日本晨间测量-家庭血压(J-HOP)研究中,研究人员测量了3 562例有心血管危险因素的门诊患者血浆中GDF-15的水平[9]。参与者根据GDF-15的三分位数进行分层,并对全因死亡和心血管疾病进行随访。在平均6.6年的随访期间,155例出现全因死亡,81例出现卒中事件(包括脑梗死和颅内出血),141例出现心脏事件(包括冠状动脉疾病和心力衰竭)。在调整传统危险因素和其他预后生物标志物后,与最低的三分位数相比,最高GDF-15水平组的全因死亡和卒中事件均显著增加[9]。同既往研究类似[10],通过回顾性分析1 522例老年ACS患者的GDF-15变化轨迹,我们发现GDF-15变化轨迹与HHF风险之间存在显著关联,与死亡风险之间也存在显著关联。因此,GDF-15变化轨迹在优化老年NSTE-ACS患者风险分层方面具有更好的潜在价值。
与传统生物标志物(如NT-proBNP、TNI等)比较,GDF-15对于ACS的危险分层也有较好的临床价值。对于ACS患者,GDF-15是预测预后的新型标志物,GDF-15水平增高是发生MACE的高风险因素。Stahrenberg等[11]研究发现,循环GDF-15水平与超声心动图检测的左室射血分数、6 min步行距离以及SF-36评分等均明显相关。研究者进一步还证实,对于射血分数正常心力衰竭患者,GDF-15的预测价值优于NT-proBNP[11]。对于严重肥胖的个体,与NT-proBNP相比,GDF-15预测左室舒张功能不全的价值也更高[12]。对于慢性心力衰竭患者,Kempf等[13]发现循环GDF-15水平与全因病死风险存在明显的等级相关关系,多因素Cox回归分析进一步证实循环GDF-15水平是预测慢性心力衰竭患者死亡的最强因素。在J-HOP研究中,发现将GDF-15纳入全因死亡预测模型可显著改善对预后的区分和重分类能力。对于卒中事件,GDF-15具有与NT-proBNP和高敏肌钙蛋白T相似的诊断准确性。在伴有心血管危险因素的日本门诊患者中,与NT-proBNP和高敏肌钙蛋白T相比,GDF-15显著改善了全因死亡的风险分层。超出了传统危险因素等预后预测标志,GDF-15与卒中事件风险增加相关。然而,其对卒中事件的预测能力与NT-proBNP和高敏肌钙蛋白T相当[9]。我们的研究显示,对老年NSTE-ACS患者,GDF-15变化轨迹对MACE的预测价值较高,高于入院时NT-proBNP、GDF-15和TNI水平。因此,多种生物标志物联合检测能够从多方位、多角度评估疾病进展,能进一步提高预后预测的准确性。一些研究发现,联合检测循环GDF-15和NT-proBNP水平,能明显提高对AMI患者预测预后的准确性[14-16]。目前,循环GDF-15不能替代传统心血管生物标志物,建议将GDF-15与传统标志物联合检测,以助临床医生指导ACS患者的预后评估[5]。
GDF-15可能通过影响心肌纤维化介导MACE的发生。GDF-15是转化生长因子β细胞因子超家族的成员,在大多数人体组织中低水平表达。心肌细胞中GDF-15的表达是由缺血、机械应变、促炎细胞因子、氧化应激和神经激素激活等损伤触发的,尽管其作用尚不清楚。GDF-15在心力衰竭中升高,并与不良结局相关,但其与心肌纤维化和其他特征的关系尚不清楚。近期的一项研究中,在吡非尼酮治疗心力衰竭(PIROUETTE)试验纳入的患者随机接受吡非尼酮或安慰剂治疗[17]。研究人员在基线和预先设定的时间点测量了受试者GDF-15水平,并评估了GDF-15对吡非尼酮的反应以及与基线患者特征的相关性。在多变量分析中,男性、糖尿病、较高的NF-proBNP水平、较低的肾功能以及较短的基线6 min步行距离与基线LogGDF-15相关[17]。基线整体纵向应变受损是52周内GDF-15增加的最强预测因子。由此可见,在心力衰竭患者中,循环中GDF-15水平似乎不受心肌纤维化的影响,可能是整体生理紊乱的标志。因此,GDF-15与患者整体心脏生理功能紊乱相关,定期监测GDF-15,特别是联合NT-proBNP和心肌酶等其他指标,可能有助于及时识别发生MACE的高风险个体[18-20]。
综上所述,GDF-15水平与老年NSTE-ACS患者发生MACE的风险独立相关。因此,GDF-15变化轨迹或可作为MACE风险的早期预警的临床指标,对临床具有重要的借鉴意义。建议将GDF-15与传统标志物联合检测,以助临床医生指导ACS患者的预后评估。但是,本研究为单中心分析,各组的基线资料不匹配,样本量有限,没有检测累积GDF-15水平,故还需要更多研究证实。
利益冲突:无