生长激素在卵巢储备功能减退病人体外受精-胚胎移植拮抗剂方案中的临床应用
王葳,汤美玲,周晓燕,武依娜,王召朋,张琦
近年来,行体外受精/卵胞质内单精子注射-胚胎移植(in vitro fertilization/intracytoplasmic sperm injection and embryo transfer,IVF/ICSI-ET)助孕的病人中,卵巢储备功能减退(DOR)人群的占比显著上升,主要表现为卵母细胞数目、质量的降低以及卵巢低反应等,进而显著影响了临床妊娠率。研究发现,DOR病人可出现抗米勒管激素(anti-Müllerian hormone,AMH)水平下降、窦卵泡计数(antral follicle count,AFC)下降、卵泡刺激素(follicle stimulating hormone,FSH)水平增加,并导致生育功能障碍[1-2]。DOR主要和年龄及遗传有关,近年来受到环境、社会等多方面因素的影响,DOR病人的发病率逐年上升。研究发现,相较于正常女性,DOR病人诱发排卵难度增加,卵泡发育不良,胚胎质量差,子宫内膜容受性不佳,因此受孕能力下降,临床妊娠率低并且流产率升高[3-4]。
研究表明,生长激素能够刺激全身器官的生长发育,增加蛋白质的合成,减缓脂肪代谢速率,学者们在卵巢、卵母细胞、子宫内膜细胞上也发现了生长激素受体,说明生长激素可以结合受体作用于女性生殖系统[5]。一项研究发现,在DOR病人体外受精-胚胎移植(IVF-ET)助孕周期中添加生长激素,可以帮助病人提高胚胎种植率和临床妊娠率、改善妊娠结局[6]。目前DOR的病人有多种超促排卵方案,如拮抗剂方案、高孕激素状态下促排卵(progestin primed ovarian stimulation,PPOS)方案、双刺激方案、微刺激方案以及自然周期等[7],在考虑助孕时间成本和尽量实现鲜胚移植的情况下,拮抗剂方案不失为首选方案。本研究探讨DOR病人IVF/ICSI-ET拮抗剂方案助孕周期中添加生长激素后对胚胎质量及子宫内膜容受性的影响。
1 资料与方法
1.1 一般资料 回顾性分析选择2019年10月至2021年9月于皖北煤电集团总医院生殖医学科行IVF/ICSI治疗的89例病人(共97个周期)纳入本次研究。研究对象为采用拮抗剂方案的DOR病人,年龄(36.01±4.34)岁。其中在超促排卵过程中添加生长激素的病人为生长激素组(53个周期),未添加生长激素的病人为对照组(44个周期),比较两组病人的临床助孕效果差异。纳入标准:(1)月经第2~3天双侧卵巢AFC≤5~7枚,FSH>10 U/L或FSH/黄体生成素(LH)≥2.0~3.6,血清AMH≤1.1 μg/L,以上三项符合一项[8];(2)控制性超促排卵采用拮抗剂方案;(3)新鲜周期移植。排除标准:(1)子宫畸形或宫腔粘连等宫腔异常;(2)输卵管积水;(3)免疫性疾病及其他不适合妊娠的全身性疾病;(4)男方严重少弱畸精症。本研究符合《世界医学协会赫尔辛基宣言》相关要求,病人或其授权委托近亲属对研究方案签署知情同意书。
1.2 方法
1.2.1 控制性促排卵方案 月经第2~3天根据病人年龄、基础性激素水平、AFC等予以重组FSH(果纳芬,每支450 U、每支75 U,雪兰诺瑞士)或尿源性FSH/尿促性素(丽申宝/HMG,每支75 U,珠海丽珠公司),生长激素组在前一周期黄体期或者本周期促性腺激素(Gn)启动时添加重组人生长激素(批次20190726,20200312,20210128等,批号S19990021,安苏萌,每支4 U,安科生物),对照组未添加生长激素。当出现以下情况1条或以上开始加用拮抗剂(GnRH antagonist,GnRH-A):(1)优势卵泡直径达到14 mm时;(2)优势卵泡达12 mm,血清雌二醇值超过1 098 pmol/L;(3)血清LH值超过10 IU/L、优势卵泡大小为12 mm左右,同时血清雌二醇值超过549 pmol/L。皮下注射醋酸西曲瑞克(批次P00434A,P00490B,P00505B等,进口药品注册证号H20140476,思则凯,每支0.25 mg,雪兰诺瑞士),0.125~0.25 mg/d,并持续应用至人绒毛膜促性腺激素(hCG)日。
1.2.2 扳机、取卵、体外受精 若双侧卵巢中存在1~2枚卵泡大小超过16~18 mm,则给予绒促性素5 000~10 000 U(hCG,每支5 000 U,珠海丽珠制药),35~36 h后利用17G单/双腔穿刺针(库克,美国)进行取卵(个别病人预防卵泡早排提前取卵)。根据第五版精液标准[9]评估精液质量进行IVF。若观察4~6 h受精率未超过30%,则行早补救ICSI受精。
1.2.3 胚胎移植及黄体支持 培养3~5 d后在B超引导下进行卵裂胚或囊胚移植,取卵后应用黄体酮注射液60 mg/d(每支20 mg,浙江仙琚制药) 和地屈孕酮20~30 mg/d(达芙通,每片10 mg,雅培荷兰)给予黄体支持,两周后检查血清β-hCG水平,若出现阳性则表明妊娠,移植后28~30 d B超观察到孕囊则判断为临床妊娠。
1.3 观察指标 病人年龄、不孕年限、不孕类型、身体质量指数(BMI)、AFC、基础FSH、LH、雌二醇值、AMH值、Gn天数及用量、hCG日雌二醇、LH值,hCG日子宫内膜厚度及分型、平均获卵数、成熟卵数,正常受精率(双原核受精数/IVF获卵数或ICSI成熟卵数×100%)、卵裂率(双原核卵裂数/双原核受精数×100%)、优质胚胎率(D3优质胚胎数/双原核受精数×100%)、平均移植胚胎数、移植胚胎类型、胚胎种植率(孕囊数/移植胚胎数×100%)、临床妊娠率(临床妊娠周期数/鲜胚移植周期数×100%)及早期流产率(早期流产周期数/临床妊娠周期数×100%)。
1.4 统计学方法 所得数据用SPSS 23.0软件进行分析。计数资料用周期数表示,符合正态分布定量资料用表示,两组间比较采用两独立样本t检验,定性资料比较采用χ2检验或Fisher确切概率法,logistic回归分析临床妊娠与生长激素的相关性。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况比较 生长激素组与对照组比较,病人的年龄、不孕年限、不孕类型、BMI、AFC、基础FSH、LH、雌二醇值、AMH值差异无统计学意义(P>0.05),见表1。

表1 两组卵巢储备功能减退病人一般情况比较
2.2 促排卵周期指标 生长激素组与对照组比较,病人的Gn用药天数及用量、hCG 日雌二醇、LH值、hCG日子宫内膜厚度及A-B/B/B-C/C型子宫内膜差异无统计学意义(P>0.05),生长激素组A型子宫内膜明显高于对照组,且差异有统计学意义(P<0.05),见表2。

表2 两组卵巢储备功能减退病人促排卵周期指标比较
2.3 实验室关键指标 生长激素组与对照组比较,平均获卵数、成熟卵数、正常受精率、卵裂率无统计学意义(P>0.05),生长激素组优质胚胎率高于对照组,且差异有统计学意义(P<0.05),见表3。
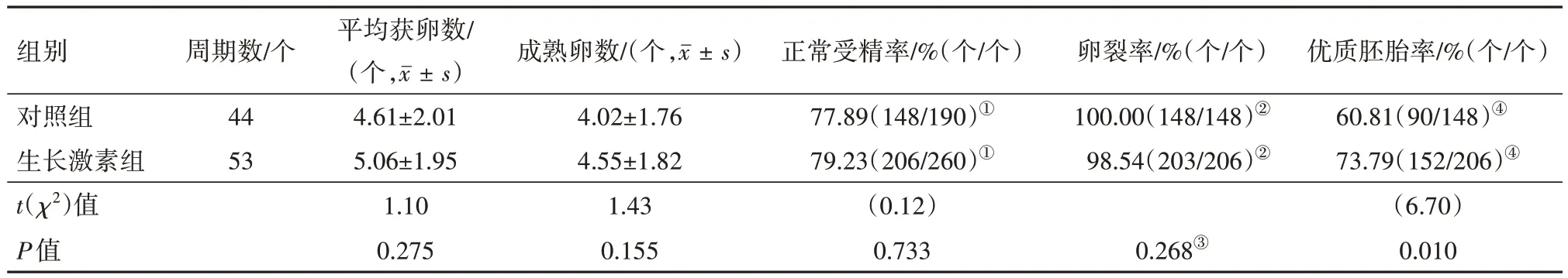
表3 两组卵巢储备功能减退病人实验室关键指标比较
2.4 新鲜周期移植临床结局 生长激素组与对照组比较,平均移植胚胎数、移植胚胎类型、临床妊娠率及早期流产率无统计学意义(P>0.05),生长激素组胚胎种植率高于对照组(P<0.05),见表4。
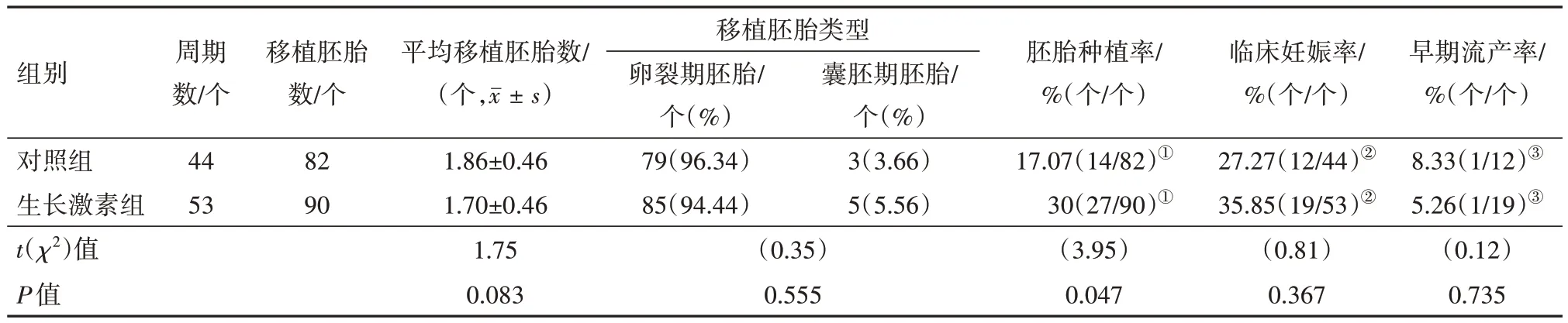
表4 两组卵巢储备功能减退病人新鲜周期移植临床结局比较
2.5 logistic回归分析 单因素logistic回归分析显示,使用生长激素与临床妊娠相关性差异无统计学意义(β=0.40,P=0.368)。多因素logistic回归分析发现移植胚胎数与临床妊娠的相关性检验差异有统计学意义(β=1.33,P=0.029),未发现使用生长激素、年龄、不孕年限、不孕类型、基础FSH等与临床妊娠有关(P>0.05),见表5。
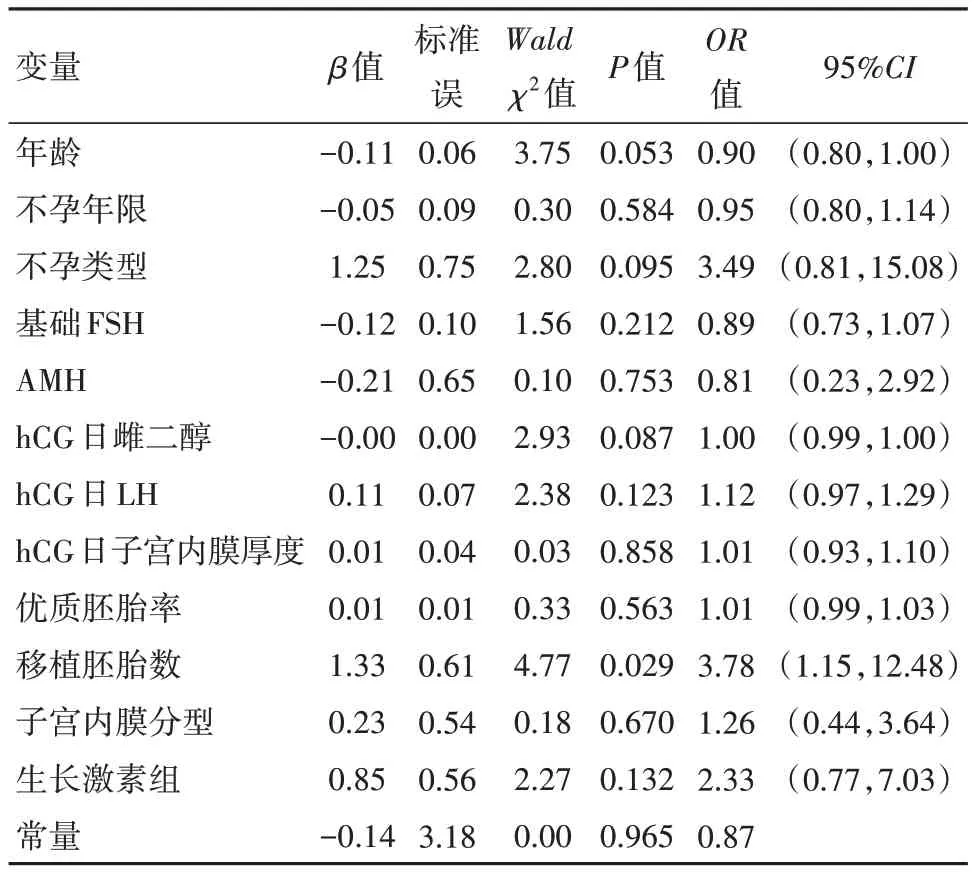
表5 卵巢储备功能减退89例临床妊娠影响因素的logistic回归分析
3 讨论
DOR带来的助孕难点是卵母细胞数目和质量的降低,出现FSH负反馈升高,或者低水平AMH[10]。年龄是DOR的主要影响因素[11],遗传、环境、手术、放化疗及免疫等因素也可能造成DOR的发生。年龄越大,获得妊娠的机会越少[12],在IVF治疗中常常因卵巢低反应、高周期取消率而影响妊娠结局,且DOR病人因卵子数量和质量低下,即使给予大剂量促性腺激素,其获卵数、优质胚胎率及临床妊娠率也很难有明显的提升。不仅大大增加了治疗难度,同时也带来病人的经济负担和心理压力。为了改变DOR病人的现状,提高临床妊娠率,我们将生长激素运用于IVF-ET治疗过程中来加强促排卵的效果,探讨是否能帮助病人获得良好的妊娠结局。对于DOR病人有各种促排方案[13-14],PPOS方案和拮抗剂方案的探讨仍然比较热门,一项研究发现,拮抗剂方案和PPOS方案在抑制LH峰的作用上并没有明显差别,拮抗剂方案可以获得较多优质胚胎[15]。此外,考虑PPOS方案需要冻胚移植,增加了时间成本和胚胎冻融损伤风险,我们仍然将拮抗剂方案作为DOR病人的首选方案。
生长激素主要由垂体分泌,由下丘脑生长激素释放激素以及生长抑素共同调节。研究显示,生长激素可以增加高龄病人卵巢颗粒细胞中生长激素受体(GHR)、卵泡刺激素受体(FSHR)、黄体生成素受体(LHR)的密度并逆转其失调的受体表达,使卵母细胞功能线粒体数量显著增加,调节卵泡的募集[5]。生长激素参与调控血管活性因子,如VEGF的表达,提高卵巢血液灌注和改善卵巢微环境[16]。生长激素还可以促进卵巢及子宫内膜中IGF-1的合成,IGF-1可以增加甾体激素的合成,促进卵泡发育和成熟,使子宫内膜细胞增殖与血管化,有助于胚胎的植入与着床[17-18]。研究发现,对高龄DOR病人应用生长激素到IVF-ET治疗过程中,可明显减少Gn用量及促排天数,优质胚胎数和临床妊娠率得到明显提高[19-20]。本研究发现,在病人超促排卵过程中,其中添加生长激素组Gn天数和用量没有明显的降低,hCG日雌二醇值、LH值与对照组差异无统计学意义。生长激素组的A型内膜较多(P<0.05)。临床上通过B超观察子宫内膜的厚度和形态来预测子宫内膜的容受性,大体分为A、B、C三种类型,研究表明,在促排卵过程中测量卵泡接近成熟时的内膜形态,与未妊娠病人相比较,A型及B型子宫内膜在妊娠病人当中的比例较高[21]。由此推测生长激素可能有助于子宫内膜形态的改善进而提高容受性。但本研究行logistic回归分析未发现子宫内膜形态与临床妊娠的相关性(P>0.05)。本研究中因病人的AFC有限,虽然平均获卵数、成熟卵数、正常受精率、卵裂率没有显著增加,但优质胚胎率显著增加(P<0.05)。新鲜周期移植的胚胎数目和类型也是临床结局的关键因素[22],本研究中DOR病人获得囊胚的数量不多,两组之间移植胚胎数量和类型差异无统计学意义,生长激素组胚胎种植率明显高于对照组(P<0.05)。生长激素组临床妊娠率、早期流产率与对照组差异无统计学意义,logistic回归分析也未发现生长激素与临床妊娠的相关性,分析其原因可能与样本量小,或者有其他因素影响有关。通过logistic回归分析发现移植胚胎数与临床妊娠的相关性(β=1.33,P=0.029)。后期将增加样本量,进一步分析生长激素对临床结局的影响。究竟何时添加生长激素最为合适,目前还没有统一的说法。有研究显示,提前4周或以上使用生长激素对卵巢低反应的病人进行预处理,减少Gn总量同时获优质胚胎数、种植率和临床妊娠率等均显著提高,若病人经济状况良好,可在进周期前1~4周甚至更早使用生长激素预处理[23-24]。后期随着样本量的增加将对添加生长激素不同方案的病人其临床结局及相关机制进行深入研究,以发现更适宜病人的用药方案。
综上所述,DOR降低育龄女性生育功能,影响IVF-ET治疗效果,在IVF-ET助孕周期内,通过加用生长激素提高胚胎质量,改善子宫内膜形态,增加胚胎移植率,但未发现其在提高临床妊娠率方面的明显作用。

