苦丁茶结合酚的提取优化及其对α-葡萄糖苷酶的抑制作用
厉莉,史硕硕,王鑫,耿可赞,张飞俊,胡婷
(武汉工程大学 环境生态与生物工程学院,湖北 武汉 430205)
苦丁茶主要由冬青属植物的叶子制成,已有2 000多年的历史[1]。苦丁茶含有丰富的多酚、黄酮、精油、三萜等活性物质[2],具有明显的降血糖、抗氧化、抗炎、抗肿瘤、抗肥胖、保肝等活性[3-4]。结合酚是通过化学共价键、氢键和疏水相互作用与细胞壁组分(如膳食纤维)结合,经溶剂萃取后,再经碱性/酸性/酶解从剩余固体残渣中提取而得[5-7]。研究表明,碱性水解释放出来的结合酚物质的总量要远高于酸水解[8-9]。
调查表明,我国的糖尿病患者已达1.3 亿人,其中2 型糖尿病是糖尿病患者中患病最多的类型之一,也是世界范围内导致死亡和残疾的主要原因之一[10-11]。食用碳水化合物是维持血糖的主要途径之一,胃肠道中存在的α-葡萄糖苷酶,能够催化人们所食用的碳水化合物中的α-1,4 糖苷键裂解,从而形成葡萄糖[12-13]。阿卡波糖是临床上以α-葡萄糖苷酶为靶点的有效降糖药,但它对胃肠道有副作用[14-15],长期使用该药物会导致腹痛腹泻、肠胃功能紊乱等症状[16]。因此,开发具有维持血糖稳定作用的天然有效物质具有很大的前景[17-19]。已有研究表明,从植物中提取出的结合酚对α-葡萄糖苷酶的抑制活性显著[5,20-21]。
目前鲜有苦丁茶结合酚的提取和降血糖的活性研究,本文主要以苦丁茶为原料,优化其结合酚的提取工艺并研究其对α-葡萄糖苷酶的抑制作用,旨在为苦丁茶结合酚作为健康食品辅料的开发提供参考。
1 材料与方法
1.1 材料与试剂
苦丁茶:市售;大孔树脂(AB-8、NKA-9、HPD-100、D101、X-5、ADS-7 和S-8 型)、α-葡萄糖苷酶(50 U/mg)、对硝基苯基-α-D-吡喃葡萄糖苷(p-nitrophenyl α-Dglucopyranoside,pNPG):上海源叶生物科技有限公司;十二水合磷酸氢二钠、十二水合磷酸二氢钠、碳酸钠、无水乙醇、浓盐酸、福林酚、氢氧化钠、没食子酸(均为分析纯):国药集团化学试剂有限公司。
1.2 仪器与设备
旋转蒸发器(RE-2000A):上海亚荣生化仪器厂;烘箱(PHG-9246A):上海龙跃仪器设备有限公司;可见分光光度计(V-5100):上海元析仪器有限公司;电子分析天平(ME104E/O2)、pH 计(EF-20):梅特勒-托利仪器有限公司;多功能酶标仪(Multiskan FC):赛默飞世尔科技有限公司;真空冷冻干燥机(LGJ-60A):上海豫明仪器有限公司;超声清洗仪(SB25-12DT):宁波新芝生物科技股份有限公司。
1.3 试验方法
1.3.1 原料预处理
首先将苦丁茶研磨并过40 目筛,随后置于常温下储存。取100 g 苦丁茶粉末,并使用50%乙醇溶液进行浸提,乙醇溶液与样品液料比20∶1(mL/g),将混合物装入烧杯中,随后在50 ℃超声波(600 W)中浸提1.6 h,浸提结束后,抽滤分离滤液和滤渣。将滤渣再次浸提,尽可能除去游离态结合酚,收集苦丁茶滤渣并将其完全干燥,于阴凉干燥处室温保存。
1.3.2 苦丁茶结合酚的提取单因素试验
取0.5 g 苦丁茶渣,分别以氢氧化钠浓度、液料比(即氢氧化钠溶液与苦丁茶渣之比)及提取时间为因素,以结合酚含量为指标,进行单因素试验设计。
1.3.2.1 氢氧化钠浓度的选择
在液料比20∶1(mL/g)、提取时间3 h、提取温度50 ℃条件下,采用超声辅助提取法,探究不同氢氧化钠浓度(5、6、7、8、9 mol/L)对苦丁茶结合酚含量的影响。
1.3.2.2 液料比的选择
在氢氧化钠浓度8 mol/L、提取时间3 h、提取温度50 ℃条件下,采用超声辅助提取法,探究不同液料比[10∶1、20∶1、30∶1、40∶1、50∶1(mL/g)]对苦丁茶结合酚含量的影响。
1.3.2.3 提取时间的选择
在氢氧化钠浓度8 mol/L、液料比40∶1(mL/g)、提取温度50 ℃条件下,采用超声辅助提取法,探究不同提取时间(1、2、3、4、5 h)对苦丁茶结合酚含量的影响。
1.3.3 响应面设计及分析
在单因素试验的基础上,以氢氧化钠浓度、液料比、提取时间作为自变量,以苦丁茶结合酚含量作为响应值,采用三因素三水平的方法进行响应面优化,如表1 所示,使用软件Design Expert.V8.0.6.1 进行分析。

表1 响应面因素水平设计Table 1 Optimized independent variables and their coded and actual values

表2 底物和α-葡萄糖苷酶溶液浓度Table 2 Substrate and α-glucosidase solution concentrations
1.3.4 结合酚含量测定
采用福林酚法测结合酚含量。首先称取没食子酸0.10 g,配制溶液为1.0 mg/mL。分别取0.1、0.2、0.3、0.4、0.6、0.8、1.0 mL 配制完成的没食子酸溶液于反应管中,补加纯水至10 mL;分别取1 mL 没食子酸(空白为1 mL 纯水)于试管中,加入福林酚0.5 mL,摇匀,反应5 min;加1.5 mL 20% Na2CO3,并添加7 mL 纯水,摇匀,室温下放置1 h(黑暗中),使用分光光度计于765 nm下测定吸光值。
1.3.5 结合酚的纯化
参考朱洁等[22]的方法并稍加修改。选取AB-8、NKA-9、HPD-100、D101、X-5、ADS-7 和S-8 型7 种常用的大孔树脂,分别称1 g,并置于相同规格大小的锥形瓶中。将冻干的苦丁茶结合酚粉末用纯水复溶,并测定其结合酚含量,将该溶液的结合酚浓度记为C0(mg/mL)。取20 mL(记为V1)溶液倒入锥形瓶中,将锥形瓶放置在摇床中,180 r/min、30 ℃下振摇24 h,测定滤液的结合酚含量,将滤液的结合酚浓度记为C1(mg/mL)。按照公式(1)计算大孔树脂对苦丁茶结合酚吸附率(A,%)。
将滤干的树脂用纯水洗净并滤干,将树脂重新放入洗净烘干的锥形瓶中,加入20 mL 配制好的60%乙醇溶液,180 r/min、30 ℃下振摇24 h,60%乙醇洗脱液体积记为V2(mL),测定溶液的结合酚浓度,记为C2(mg/mL)。大孔树脂解吸率(D,%)按公式(2)计算。
1.3.6 苦丁茶结合酚对α-葡萄糖苷酶的抑制作用
1.3.6.1 酶活力的测定
参考Tian 等[23]和张海龙[24]的方法并稍加修改。采用96 孔板,将20 μL 2.5 mmol/L 的对硝基苯基-α-D-吡喃葡萄糖苷和20 μL 0.6 U/mL 的α-葡萄糖苷酶添加到120 μL 的磷酸缓冲液(pH6.8,0.1 mol/L)中,于37 ℃下孵育20 min。加入80 μL 浓度为0.2 mol/L Na2CO3终止反应。使用酶标仪在405 nm 处测定吸光值。以20 μL 的磷酸缓冲液代替酶作为空白对照。
1.3.6.2 最适酶浓度的选择
参考张永军等[25]的方法并稍加修改。加入适量的α-葡萄糖苷酶,测定酶反应初速率为△A/min,使其速率介于0.03~0.25 之间。加入底物pNPG 后开始计时,在反应进行1 min 后,加入Na2CO3以停止反应,随后使用酶标仪测出反应溶液的吸光值,吸光值表示酶与底物反应后,生成对硝基苯基(p-nitrophenyl,pNP)在405 nm 下的吸光值。
1.3.6.3 不同浓度的结合酚对α-葡萄糖苷酶半抑制浓度的确定
将苦丁茶结合酚配制为0.5、0.8、1.0、1.2、1.5、2.0、3.0、4.0、5.0、6.0 mg/mL,取20 μL 的苦丁茶结合酚与20 μL 的α-葡萄糖苷酶反应10 min,加入20 μL 的pNPG 于37 ℃下继续孵育20 min,反应结束后立即加入80 μL 的Na2CO3终止反应。记测试组的吸光值为AA;以20 μL 的磷酸缓冲液代替酶作为测试空白组,记Aa;以20 μL 的磷酸缓冲液代替样品作为对照组,记AB;以20 μL 的磷酸缓冲液代替样品,并以20 μL 的磷酸缓冲液代替酶作为空白组,记Ab。使用酶标仪于405 nm 波长处测定吸光值,并且根据下列公式计算抑制率(X,%)[26]。
1.3.6.4 苦丁茶结合酚对α-葡萄糖苷酶抑制类型的研究
参考Xiong 等[27]的方法并稍作修改。选取浓度为2 mg/mL 苦丁茶结合酚,并测定酶浓度分别为0.2、0.6、1.0、1.6 U/mL 和2.4 U/mL 的酶反应初速率。抑制组添加结合酚溶液,无抑制组则用纯水代替样品溶液,利用分光光度计进行吸光值的测定。以酶浓度(U/mL)为横坐标,酶解速率V 为纵坐标作图。依照动力学图的特征,分析结合酚对α-葡萄糖苷酶的抑制类型。
1.3.6.5 可逆性抑制类型的研究
在反应体系中,首先加入2.5 mg/mL 和5.0 mg/mL的pNPG,接着加入1.2 U/mL 的α-葡萄糖苷酶,最后加入浓度分别为0.5、1.0、1.5、2.5 mg/mL 的结合酚溶液,使用酶标仪测出反应的吸光值,并由此求出反应速率。按Dixon 的双倒数作图法作图,横坐标为结合酚浓度(mg/mL),纵坐标为酶反应速率的倒数1/V,根据图确定α-葡萄糖苷酶的可逆性抑制的类型。
1.4 数据处理
图像采用Origin 和Design-Expert.V8.0.6.1 绘制,利用SPSS 软件处理试验数据并分析数据显著性,当P<0.05 表示显著性差异。
2 结果与分析
2.1 苦丁茶结合酚单因素试验结果
各因素对苦丁茶结合酚含量的影响见图1。
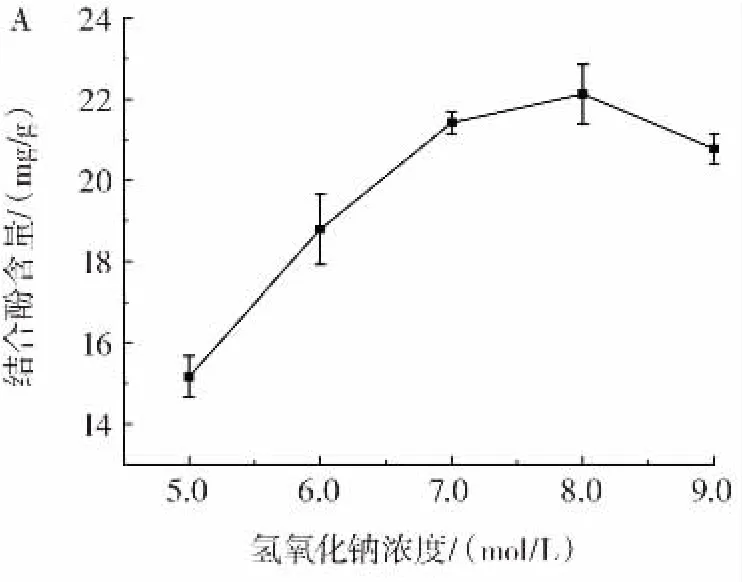
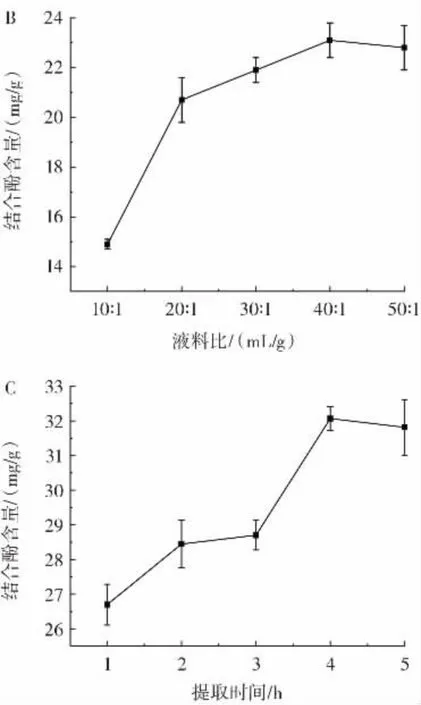
图1 苦丁茶结合酚提取单因素结果Fig.1 Single factor results of the extraction of Kuding tea binding polyphenols
由图1A 可知,氢氧化钠浓度在5.0~8.0 mol/L 时,结合酚含量随着氢氧化钠浓度的增加而增加,当浓度为8.0~9.0 mol/L 时,结合酚含量随着氢氧化钠浓度的增加而减少。可能是由于碱浓度过高,导致酚基发生氧化反应,从而破坏结合酚的结构,使其无法被提取。因此,选取7、8、9 mol/L 这3 个浓度进行响应面试验优化。由图1B 可知,液料比为10∶1~40∶1(mL/g)时,结合酚含量随着溶剂量的增加而增加,而在液料比为40∶1~50∶1(mL/g)时,结合酚含量随着溶剂量的增加而减少。可能是由于溶解度的限制,提取液对结合酚的溶解能力有限,当达到饱和状态时,溶液中无法再溶解更多的结合酚,导致提取量降低。因此,选取30∶1、40∶1、50∶1(mL/g)3 个水平进行响应面试验设计。图1C中,提取时间在1~4 h 时,结合酚含量随着提取时间的延长而增加,而在4~5 h 时,结合酚含量随着时间的延长而减少。可能是由于结合酚的降解,在提取过程中,随着反应时间的延长,结合酚可能发生降解或转化,生成其他化合物,从而导致提取量降低。因此,选取3、4、5 h 3 个水平进行响应面试验设计。
2.2 苦丁茶结合酚提取工艺的响应面优化试验
2.2.1 试验结果及方差分析
响应面试验结果见表3。
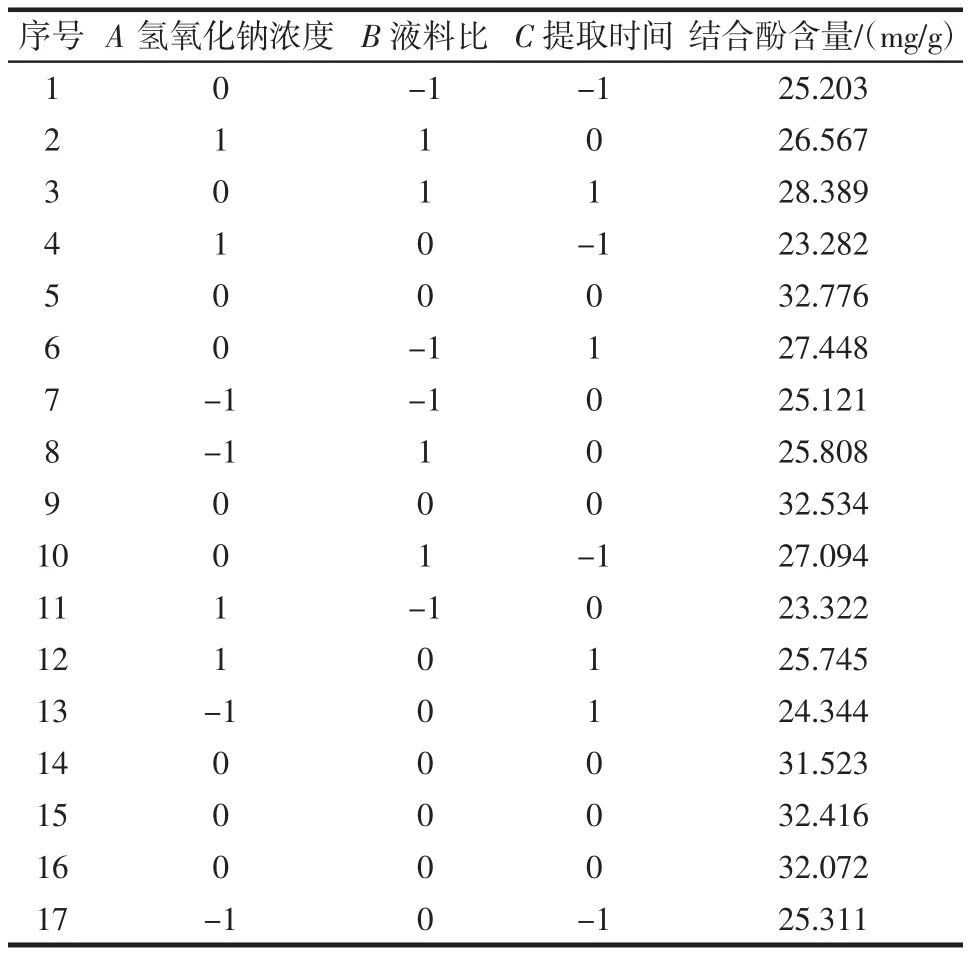
表3 响应面试验结果Table 3 Results of response surface tests
由表3 可知,苦丁茶结合酚含量二次多项回归方程为Y=32.06-0.21A+0.85B+0.63C+0.64AB+0.86AC-0.24BC-4.61A2-2.25B2-2.78C2。
对试验结果进行方差分析,结果见表4。
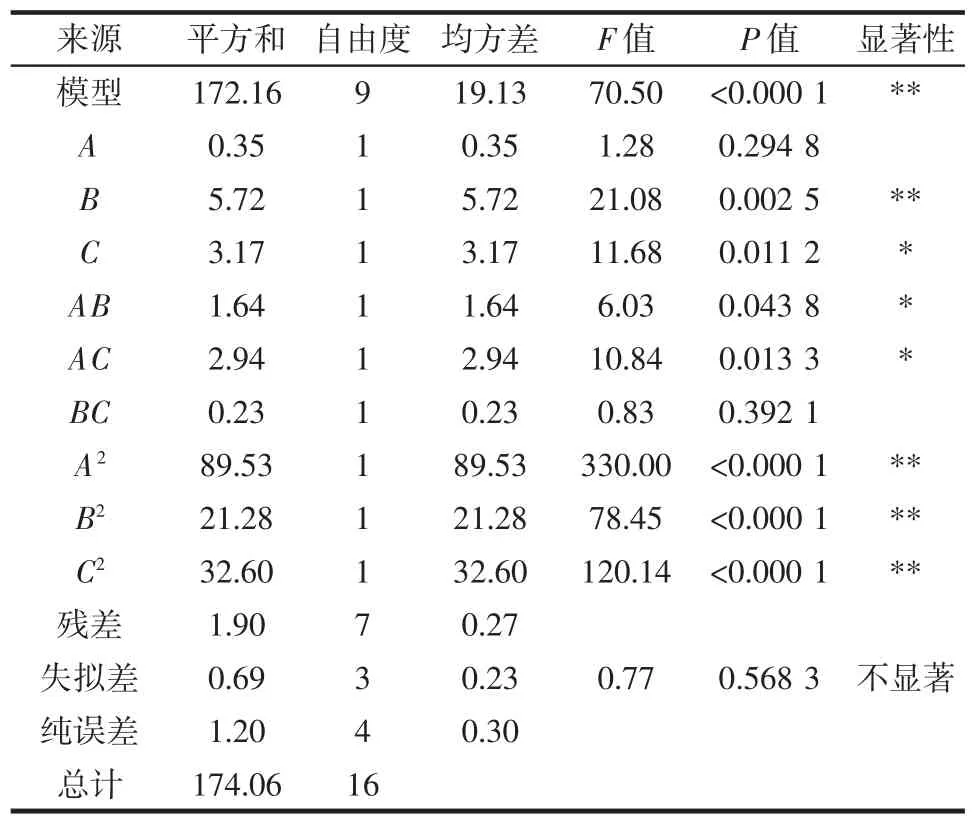
表4 回归方程各项方差分析Table 4 Variance analysis of regression equations
由表4 可知,该模型P<0.000 1,属于极显著差异,失拟差为0.568 3,P>0.05,即失拟差不显著,且R2=0.989 1,能够证明模型的可靠性和准确性。一次项A影响不显著,B 影响极显著,C 影响显著;交互项AB、AC 对响应值影响显著,BC 不显著;二次项A2、B2、C2均对响应值影响极显著。由此得知响应值会受到多个因素的相互影响。根据F 值,各因素对苦丁茶结合酚含量的影响顺序为液料比>提取时间>氢氧化钠浓度。
2.2.2 苦丁茶结合酚提取工艺的响应面图分析
变量的等高线图和三维图及其交互作用见图2。
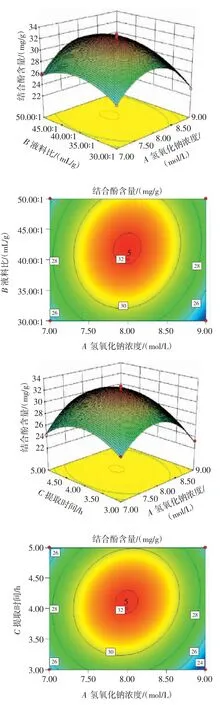
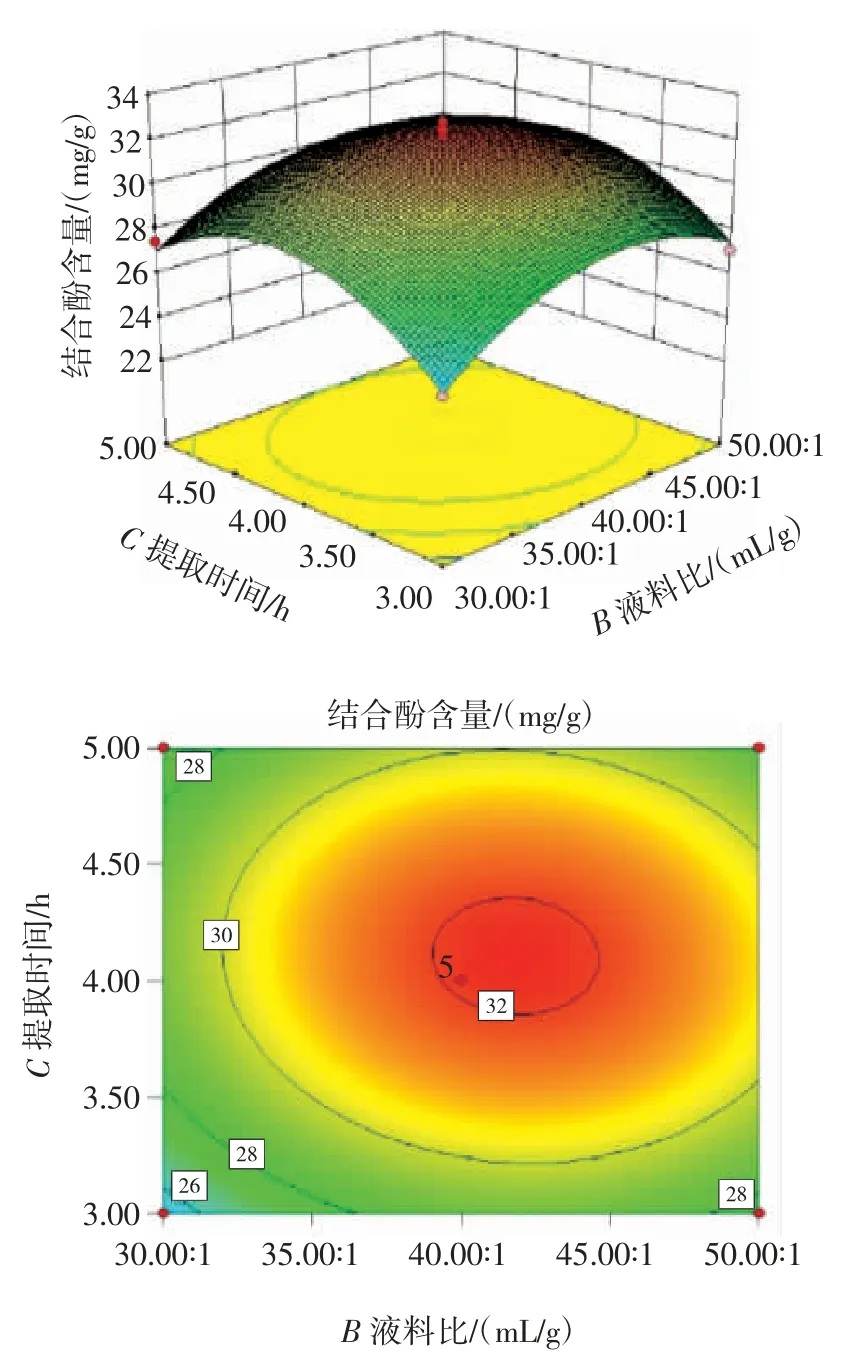
图2 变量的等高线图和三维图及其交互作用Fig.2 Contour and 3D plots of variables and their interactions
由图2 可知,氢氧化钠浓度与液料比之间立体图陡峭,交互作用显著;氢氧化钠浓度与提取时间之间立体图陡峭,交互作用显著;液料比与提取时间之间立体图较平缓,与统计分析数据一致,交互作用不显著。
根据响应面回归方程,预测出苦丁茶结合酚的最佳提取工艺条件为氢氧化钠浓度8.54 mol/L、液料比42.56∶1(mL/g)、提取时间4.19 h。在此条件下,苦丁茶结合酚的含量为30.84 mg/g。结合实际优化提取工艺条件为氢氧化钠浓度8.5 mol/L、液料比43∶1(mL/g)、提取时间4.2 h。重复3 次试验,最终得到苦丁茶结合酚的含量为(29.8±2.0)mg/g。实际测得的结合酚含量与预测值极为接近,进一步验证了模型的准确性。
2.3 大孔树脂筛选结果
不同类型大孔树脂的吸附率和解吸率见图3。
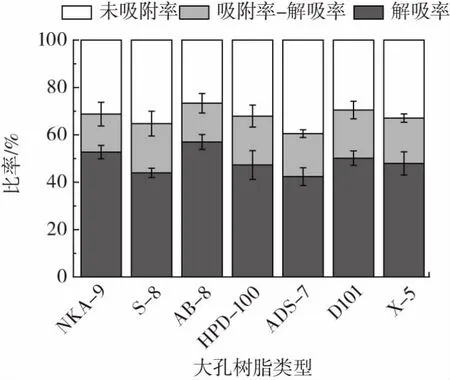
图3 不同类型大孔树脂的吸附率和解吸率Fig.3 Adsorption and resolution rates of different types ofmacroporous resins
由图3 可知,不同类型的大孔树脂对苦丁茶渣结合酚吸附率及解吸率的影响均不同。从吸附率来看,AB-8 大孔树脂的吸附率最高,NKA-9、HPD-100、D101、X-5 大孔树脂吸附相近,而ADS-7 大孔树脂吸附率最低。从解吸率来看,AB-8 大孔树脂的解吸率最高,NKA-9、D101 大孔树脂解吸率次之,其他大孔树脂的解吸率较低。综上,选择AB-8 大孔树脂纯化苦丁茶结合酚。
2.4 α-葡萄糖苷酶最适酶浓度的测定
酶浓度过高或者过低都不利于建立科学的反应动力学方程,因此要使测定的反应速率(以△A/min 表示)在0.03~0.25[25,28]。测定α-葡萄糖苷酶在7 min 内的反应动力进程曲线,结果如图4 所示。
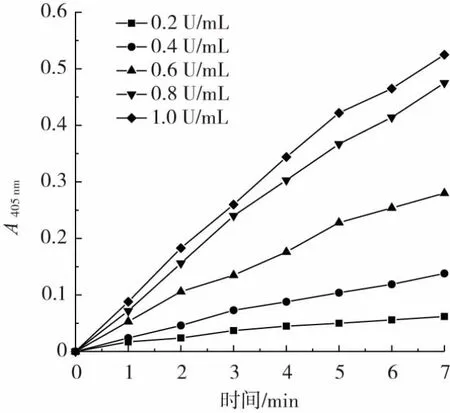
图4 α-葡萄糖苷酶不同浓度下的反应进程曲线Fig.4 Reaction progression curves of α-glucosidase at different concentrations
由图4 看出,酶浓度增大时,酶反应的初始速率随之升高,计算3 min 内的酶反应速率,即用纵坐标值/时间,当酶浓度在0.6 U/mL 及其以上时,反应的初始速率为0.03~0.25,选取酶浓度0.6 U/mL 进行后续试验。
2.5 结合酚对α-葡萄糖苷酶的半抑制浓度
不同浓度的结合酚对α-葡萄糖苷酶的抑制率见图5。
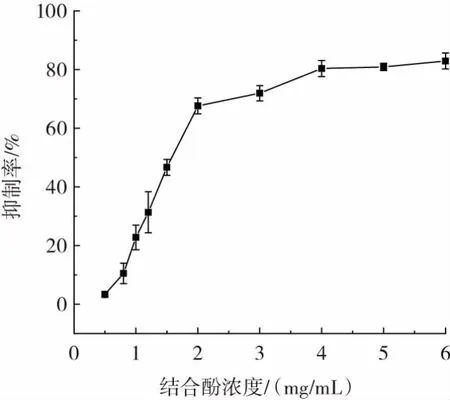
图5 不同浓度的结合酚对α-葡萄糖苷酶的抑制率Fig.5 Inhibition rates of α-glucosidase by different concentrations of binding polyphenols
由图5 可以看出,随着苦丁茶结合酚的浓度增大,其抑制率也增大,这表明结合酚活性成分含量会影响α-葡萄糖苷酶抑制效果。根据试验结果可以计算出苦丁茶结合酚对α-葡萄糖苷酶的半抑制浓度IC50为1.90 mg/mL。
2.6 结合酚对α-葡萄糖苷酶抑制类型
抑制剂对酶的抑制类型分为可逆抑制和不可逆抑制,当在测定酶活力时,所加入的体系中不存在抑制剂,其速率直线通过原点;当存在可逆抑制剂时,其速率直线通过原点且斜率略低;当存在不可逆抑制剂时,其速率直线不通过原点。结合酚对α-葡萄糖苷酶的抑制动力学曲线如图6 所示。
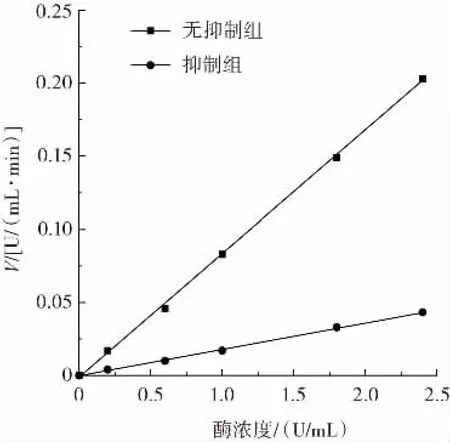
图6 结合酚对α-葡萄糖苷酶的抑制动力学曲线Fig.6 Inhibition kinetics of α-glucosidase by binding polyphenols
2.7 可逆性抑制类型的研究
可逆性抑制类型有3 种,分为竞争性、非竞争性、混合性抑制类型。已经确定抑制机理时,选取两个底物浓度,采用Dixon 作图法作图,探究苦丁茶结合酚浓度、底物浓度与酶解速率之间的关系,确定抑制类型和抑制常数。以结合酚浓度为横坐标轴,以1/V(V 为酶解速率)为纵坐标轴,两底物浓度得到的两条直线相交于横坐标轴则为非竞争性抑制,相交但不交于横坐标属于竞争性抑制,平行则为反竞争性抑制。交点对应的横坐标绝对值为非竞争性抑制常数Ki。结合酚对α-葡萄糖苷酶的可逆性抑制双倒数图见图7。
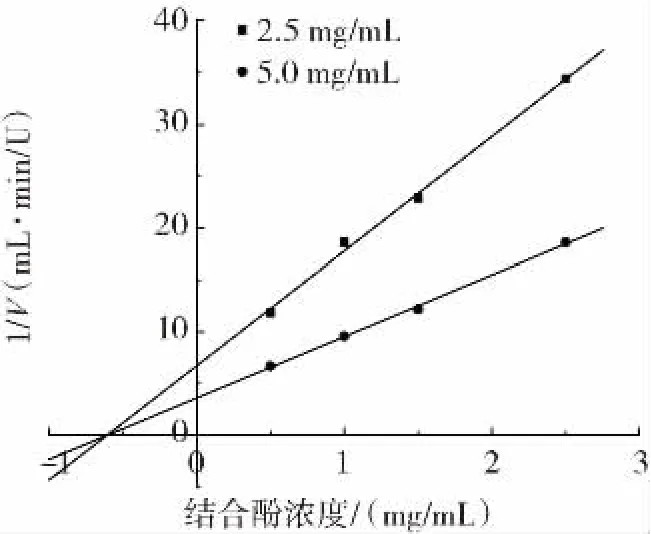
图7 结合酚对α-葡萄糖苷酶的可逆性抑制双倒数图Fig.7 Reversible inhibition of α-glucosidase by binding polyphenols
由图7 可知,抑制类型为非竞争性抑制,通过计算得出Ki为0.60 mg/mL。
3 结论
本文分析了氢氧化钠浓度、液料比和提取时间3个因素对苦丁茶结合酚含量的影响,并且探究了不同类型的大孔树脂对苦丁茶结合酚的吸附效果,此外,研究了苦丁茶结合酚对α-葡萄糖苷酶的抑制作用。结果表明,苦丁茶结合酚最佳工艺参数为氢氧化钠浓度8.5 mol/L、液料比43∶1(mL/g)、提取时间4.2 h,此工艺条件下,测得结合酚含量为(29.8±2.0)mg/g;7 种不同类型的大孔树脂中,AB-8 大孔树脂对苦丁茶结合酚的吸附率和解吸率最高;苦丁茶结合酚对α-葡萄糖苷酶的抑制作用明显,其半抑制浓度为1.90 mg/mL。分析苦丁茶结合酚对α-葡萄糖苷酶的反应动力曲线图,得知其抑制类型为可逆性非竞争性抑制,抑制常数Ki 为0.60 mg/mL。苦丁茶结合酚易于提取且成本较低,可作为天然α-葡萄糖苷酶抑制剂,具有应用前景。本研究对苦丁茶结合酚进行研究,优化了苦丁茶结合酚的提取条件,揭示了其对α-葡萄糖苷酶的明显抑制作用,证明苦丁茶中不可萃取结合酚的可利用价值。

