氮肥增效剂的应用与展望*
胡佳玉, 张 晶, 孔 波, 王庆彬, 胡承孝
(1.新型肥料湖北省工程实验室/华中农业大学微量元素研究中心 湖北武汉 430070; 2.华中农业大学理学院 湖北武汉 430070; 3.山东蓬勃生物科技有限公司 山东泰安 271099)
我国是世界氮肥生产和施用的第一大国,尤其在蔬菜、果树、花卉等经济效益较高的作物生产中,氮肥用量是普通大田作物的数倍甚至数十倍[1],氮肥超量施用现象十分普遍,但我国氮肥表观利用率仅为30%~35%,远低于世界平均水平[2]。 氮肥增效剂一直被认为是提高氮肥利用率的重要手段之一,主要包括硝化抑制剂、脲酶抑制剂、氨稳定剂及其他新型增效剂[3]。 本文通过文献分析,比较不同氮肥增效剂在提高作物氮肥利用率、生物量和产量及改善农产品品质、减少温室气体排放等方面的效果,为高效、合理利用氮肥增效剂提供参考。
1 氮肥增效剂的作用
1.1 硝化抑制剂
硝化抑制剂是能够抑制土壤中硝化细菌、亚硝化细菌等微生物活性的物质的总称,适宜配合铵态氮肥或尿素施用[4]。 现已发现有数百种化合物具有硝化抑制效应,主要有氰胺类、含氮杂环化合物、含硫化合物、烃类及其衍生物等四大类[5],其中双氰胺(DCD)、3,4-甲基吡唑磷酸盐(DMPP)、1-甲基吡唑-1-羧酰胺(CMP)、2-氯-6-三氯甲基吡啶(CP)、乙炔(C2H2)等已在农业生产上得到应用[6]。 但DCD 需达到氮肥用量的10%才有显著的硝化抑制效果,且作为水溶性制剂易淋溶流失,存在环境污染风险[7-8]。
硝化抑制剂通过抑制土壤中发生的硝化、亚硝化及反硝化过程,延缓土壤中铵态氮向硝态氮转化,延长作物吸收、利用矿化态氮的时间。 土壤中参与亚硝化反应的细菌主要有亚硝化单胞菌属、亚硝化螺菌属、亚硝化球菌属和亚硝化叶菌属;参与硝化反应的细菌主要有硝化杆菌属、硝化刺菌属和硝化球菌属[9]。 反硝化作用一般发生在嫌气或低氧的环境,在硝酸还原酶、亚硝酸还原酶、一氧化氮还原酶、氧化亚氮还原酶的催化作用下依次还原为、NO、N2O、N2,参与反应的细菌主要有假单胞菌属、产碱杆菌属[10]。
DCD 的氨基(—NH2)和亚氨基(=NH)与NH3结构相似,以底物竞争形式干扰氨氧化细菌(AOB)对底物的利用[11];Nuti 等[12]认为,DCD 能抑制AOB 呼吸作用的电子转移并干扰细胞色素氧化酶的功能。 DMPP 仅抑制氨氧化过程中向NH2OH 的转化[13];Kong 等[14]发现DMPP 抑制了氨氧化古菌(AOA)和AOB 的细胞特异性活性。 CP 是氨单加氧酶(AMO)的一种催化底物,但对AMO 的亲和能力弱,通过氧化产物6-氯吡啶甲酸螯合AMO 活性位点上的Cu2+产生抑制作用[15]。 乙炔作为AMO 的底物,参与催化氧化生成高活性不饱和环氧化物,并与催化氧化反应的蛋白质发生共价结合使其失活而抑制硝化作用[16]。
1.2 脲酶抑制剂
脲酶抑制剂是一类能抑制土壤中脲酶活性的物质的总称,在减缓尿素氮转化、抑制氨挥发、延长氮供应时间等方面有突出作用。 国际上已开发了70 多种脲酶抑制剂,主要包括重金属离子类(如阴离子、过渡金属离子)、羟肟酸类(如乙酰氧肟酸)、磷酰胺类[如正丁基硫代磷酰三胺(NBPT)、环乙基磷酸三酰胺(CNPT)、硫代磷酰三胺(TPT)、磷酰三胺(PT)、正丙基硫代磷酰三胺(NPPT)等]、磷酸盐类、杂环类化合物、金属配合物等,其中应用较为广泛的主要有NBPT/n-(正丁基)硫代磷酰三胺(nBTPT)、对苯二酚(HQ)和苯基磷酰二胺/苯基磷酸二酰胺(PPD/PPDA)等3 种[17]。
有机小分子类脲酶抑制剂控制尿素水解的作用机制主要有:①非竞争性抑制,即醌类和酚类脲酶抑制剂与脲酶的巯基(—SH)发生作用,形成硫桥(—S—S—)抑制脲酶活性;②竞争性抑制,即酰胺类脲酶抑制剂含有的N、O 原子与脲酶的Ni原子对接形成配位体(Ni—O、Ni—N),降低尿素与脲酶活性中心结合的概率;③部分脲酶抑制剂通过微生物活性抑制或延缓脲酶的形成,间接抑制尿素的水解作用;④重金属离子(如Ag+、Hg2+)与脲酶结合改变了脲酶活性中心和结构,导致丧失分解尿素的能力。
NBPT 结构基团中的硫基(—S)和正丁胺基[—NH(CH2)3CH3]增加了NBPT 与脲酶结合的概率,—NH2易与脲酶活性部位—SH 结合[18]。 HQ通过氧化还原作用使4 ~8 个—SH 变成—S—S—而降低脲酶活性[19]。 PPD 与尿素分子结构非常相似且亲和力极高,其本身及其水解产物磷酰二胺(DAP)能占据酶活性中心或引起酶蛋白三级结构改变产生位阻效应,阻碍酶活性中心与尿素底物结合,抑制尿素分解[20]。
1.3 氨稳定剂
氨稳定剂是一类可以减少氨挥发损失的物质的总称,主要包括无机酸、有机酸、无机盐类及具有吸附性能的天然物质等,其中农业生产上应用较多的有沸石、腐殖酸和麦饭石。 氨稳定剂较少单独使用,通常与抑制剂类增效剂混合或与肥料混合,用于开发基质复合与胶黏型缓/控释肥料[9]。
1.3.1 沸石
天然沸石是一种铝硅酸盐矿物,因Al3+替代Si4+使铝氧四面体出现负电荷点且需阳离子来补偿;沸石内部具有较多的孔隙和通道,比表面积大,易与土壤中的阳离子发生交换和吸附作用[21-22]。 因此,沸石可以增强土壤对的吸附能力从而提高有效性[23-24]。
1.3.2 腐殖酸
腐殖酸调节植物-土壤体系氮素利用的机制:①促进植物根系硝酸盐吸收同化相关基因的表达,如腐殖酸使玉米根系硝酸盐吸收相关的基因(ZmNRT2.1 和MHA2) 及硝酸盐同化基因(NR1)均显著上调表达[25-26];②驱动植物根系内硝酸盐转运,2 种高亲和力硝酸盐转运系统,即组成型高亲和力转运系统(cHATS)和诱导型高亲和力转运系统(iHATS),均因腐殖酸刺激H+-ATP 酶活性产生质子驱动硝酸盐的转运[27];③抑制AOA、AOB 等微生物群落组成和数量变化,延缓、的生成[28];④腐殖酸的官能团与脲酶的—SH 作用形成较大粒径的络合物从而抑制脲酶的活性[29],尤其是腐殖酸能长时间稳定脲酶活性,使尿素缓慢分解并提高氮肥利用率[30]。 因此,腐殖酸既能够促进氮素吸收、同化、转运,又能够抑制脲酶转化。
2 氮肥增效剂的应用
2.1 硝化抑制剂
2.1.1 提高氮肥利用率
不同硝化抑制剂可提高氮肥利用率(NUE)4.19% ~69.9%,平均增幅为17.1%,其中CaC2、DMPP、 DCD 的NUE 提高幅度均高于30%,见表1[31-39]。

表1 不同硝化抑制剂提高作物NUE 的效果
2.1.2 提高作物产量
不同硝化抑制剂可提高作物产量-0.5%~134.4%,平均增产16.4%,其中DCD 的增产效果大多在10% 以上, 优于其他硝化抑制剂,见表2[38,40-53]。
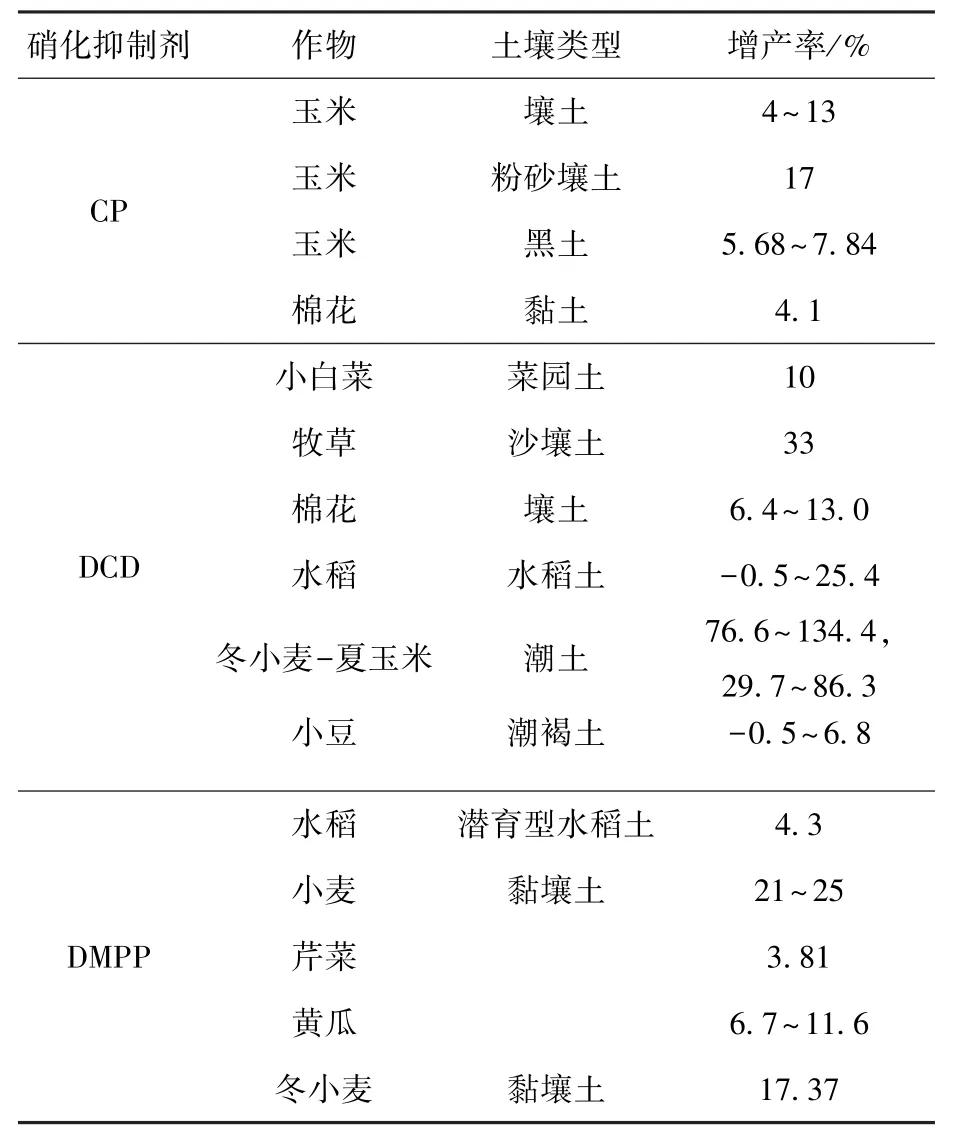
表2 不同硝化抑制剂提高作物产量的效果
2.1.3 改善农产品品质
各种硝化抑制剂均可降低作物产品器官中硝态氮含量,并提高可溶性糖、可溶性蛋白、抗氧化物(如维生素C)的含量,显著改善农产品品质(见表3)[51,54-57]。
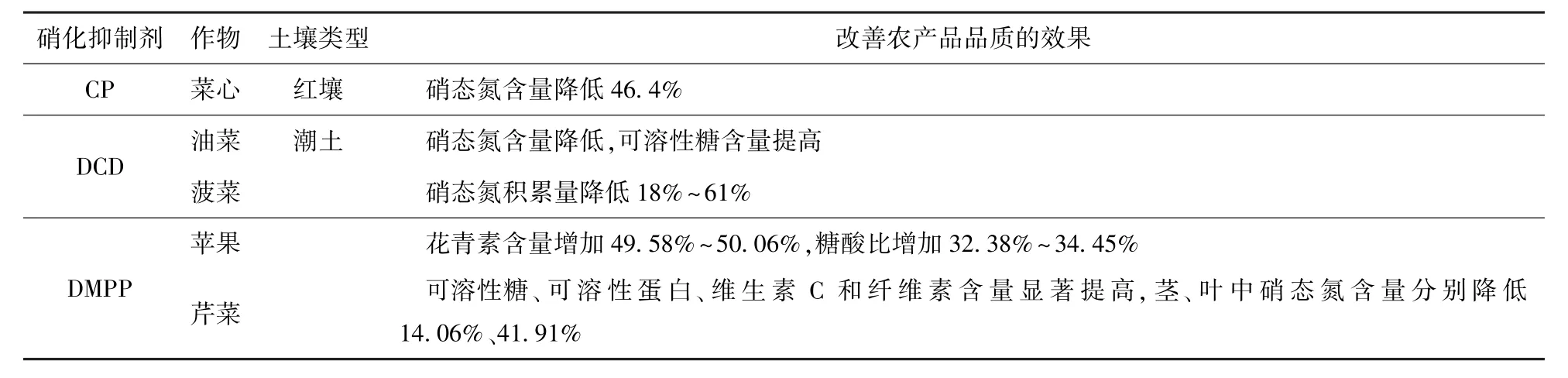
表3 不同硝化抑制剂改善农产品品质的效果
2.1.4 减少土壤温室气体排放
N2O 是一种能破坏大气臭氧层的温室气体,土壤中发生的硝化和反硝化过程是N2O 产生的主要途径,菜地因施用氮肥产生的N2O 排放量占中国农田总排放量的20%左右[58-59]。 硝化抑制剂可使施入土壤的氮素更多的以铵态氮的形式存在,进而减少N2O 的排放。 硝化抑制剂在不同氮肥水平下均能减少N2O 的排放,减排效果随施氮量的增加而增大[60]。 硝化抑制剂一般可减少N2O 排放量10.0%~98.0%,平均为28.1%;可减少CO2排放量26.9%~56.4%,平均为42.5%;可减少NO 累积排放量25.0% ~77.0%,平均为51.0%[47,50,52,58-69]。 硝化抑制剂减少土壤温室气体排放的效果见表4。

表4 硝化抑制剂减少土壤温室气体排放的效果
2.2 脲酶抑制剂
2.2.1 提高NUE
脲酶抑制剂可以提高NUE 7.1%~54.9%,平均为10.1%,见表5[70-74]。

表5 脲酶抑制剂提高NUE 的效果
2.2.2 提高作物产量
脲酶抑制剂能够延长氮肥供应时间,提高作物根系活力和固氮酶活性,促进作物生长[20];增产效果显著,可提高作物产量1.83%~50.4%,平均为9.5%,见表6[49,70,75-79]。
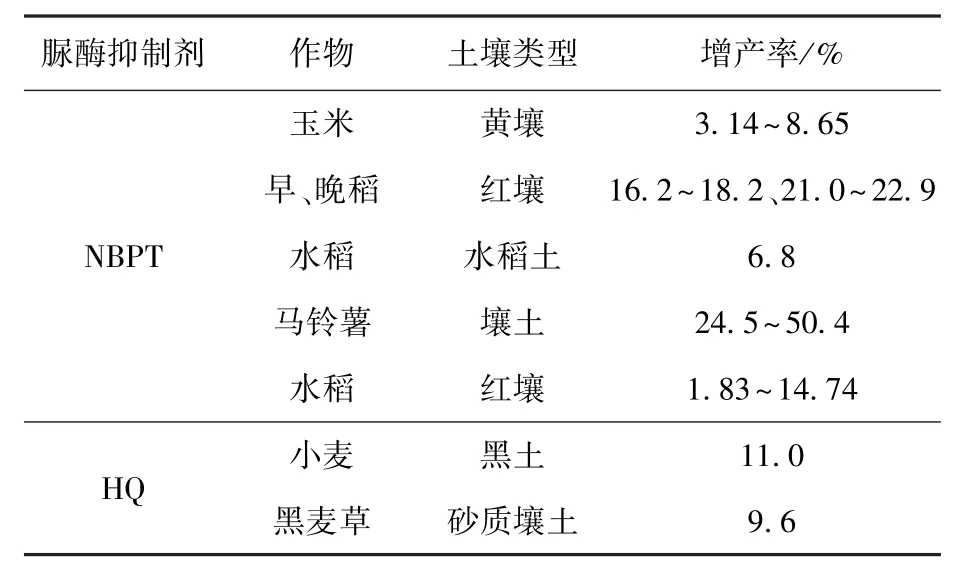
表6 脲酶抑制剂提高作物产量的效果
2.2.3 减少温室气体排放
脲酶抑制剂可以减少氨挥发11.8% ~78.0%,平均为37.0%;此外,还可以分别减少CH4、N2O 排放7.8%~58.2%、11.7%~62.3%,平均分别为25.8%、35.9%。 脲酶抑制剂减少温室气体排放的效果见表7[79-86]。
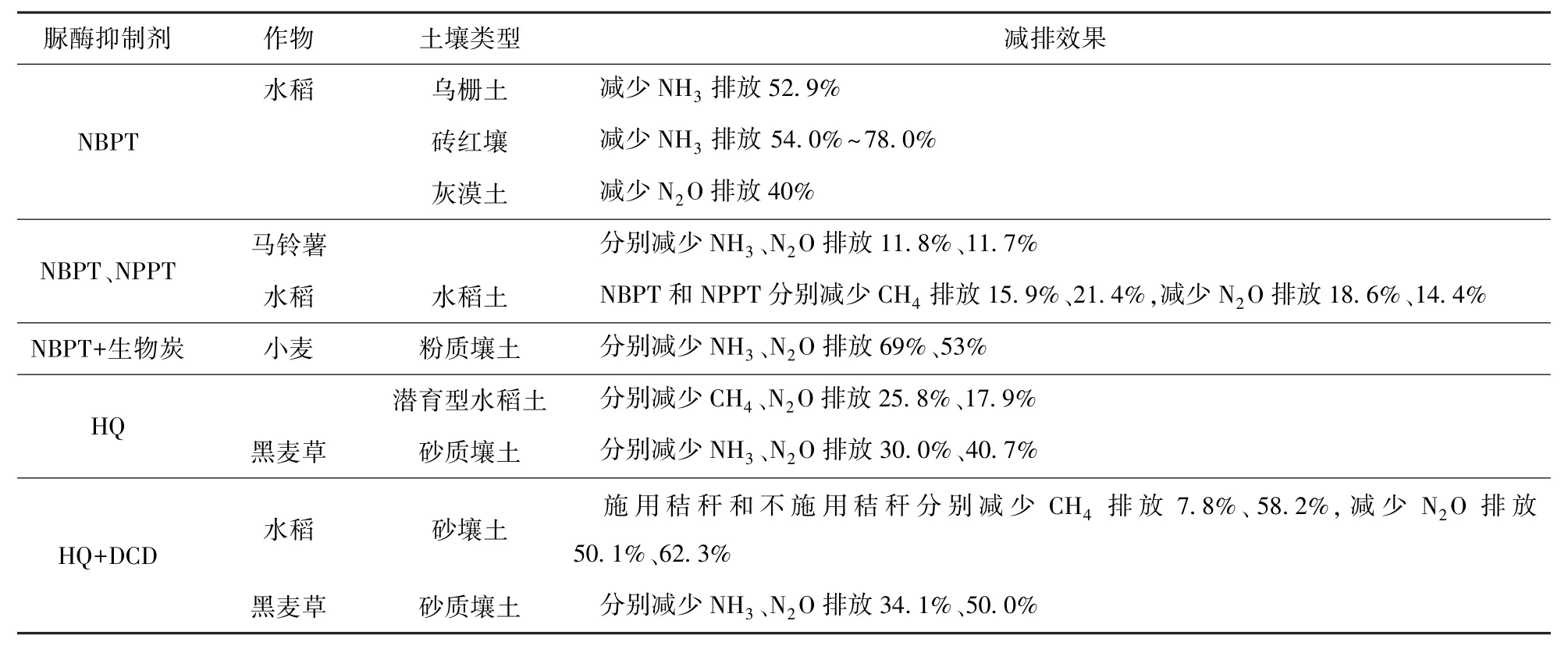
表7 脲酶抑制剂减少温室气体排放的效果
2.3 氨稳定剂
2.3.1 提高NUE 和产量
氨稳定剂沸石、生物炭、腐殖酸依次提高NUE 0.63% ~85.2%、8.0% ~35.9%、1.87% ~93%,平均分别为17.4%、4.7%、24.0%;依次平均提高作物产量42.3%、12.6%、13.2%。 氨稳定剂提高NUE 和作物产量的效果见表8[22,84,87-99]。

表8 氨稳定剂提高NUE 和作物产量的效果
2.3.2 改善农产品品质
氨稳定剂可降低农产品的硝酸盐含量,提高维生素C、可溶性糖、蛋白质含量,进而显著改善农产品品质。 氨稳定剂改善农产品品质的效果见表9[95-98,100-101]。

表9 氨稳定剂改善农产品品质的效果
2.3.3 减少氮损失
表10 结果[84,102-110]表明:氨稳定剂沸石既降低了氨挥发累积速率,减少氨挥发损失6% ~48.7%(平均为30.7%),又减少 了氮淋失-7.7%~36.7%(平均为22.7%);生物炭具有吸附或NH3的能力,可减少NH3、N2O 挥发损失20%左右;腐殖酸进入土壤后能抑制施肥区尿素的水解,减少氨挥发损失13.39% ~40.9% (平均为26.1%)、氮淋失52.1%,但也有报道腐殖酸会提高土壤脲酶活性,促进NH3挥发[111-112]。
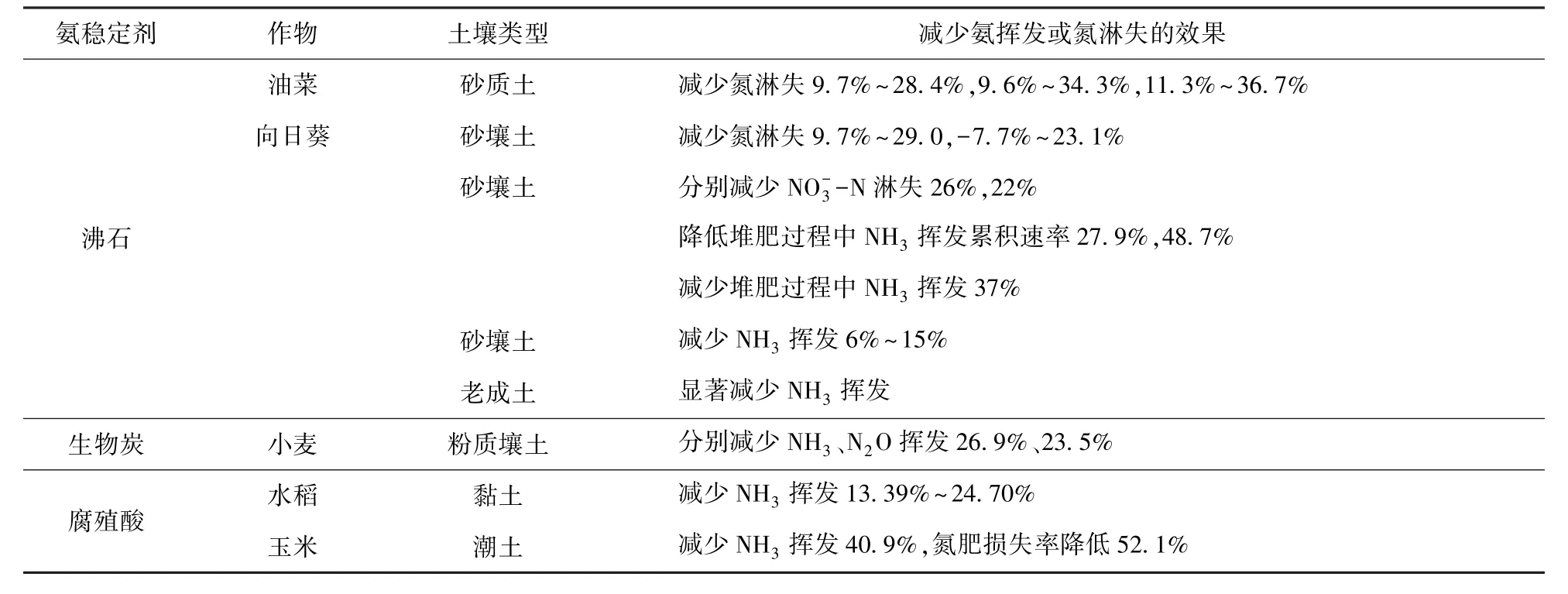
表10 氨稳定剂减少氨挥发或氮淋失的效果
3 新型肥料增效剂
3.1 内生菌提取物ZNC
内生菌提取物ZNC 的商品名为“智能聪”,来源于沙棘内生菌宛氏拟青霉。 ZNC 的田间施用量很少,效果却非常明显,一方面可提高NUE 或氮含量,增加作物产量或生物量-22.1%~64.2%(平均18.1%);另一方面可提高植株超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、过氧化物酶(POD)的活性,促进新生器官(如根、芽)发育,降低病害发生率0.70%~74.4%(平均为20.5%)。ZNC 是通过激发植物自身代谢活力,促进养分吸收利用和植株生长发育,增强抗性,提高产量(见表11)[113-122]。
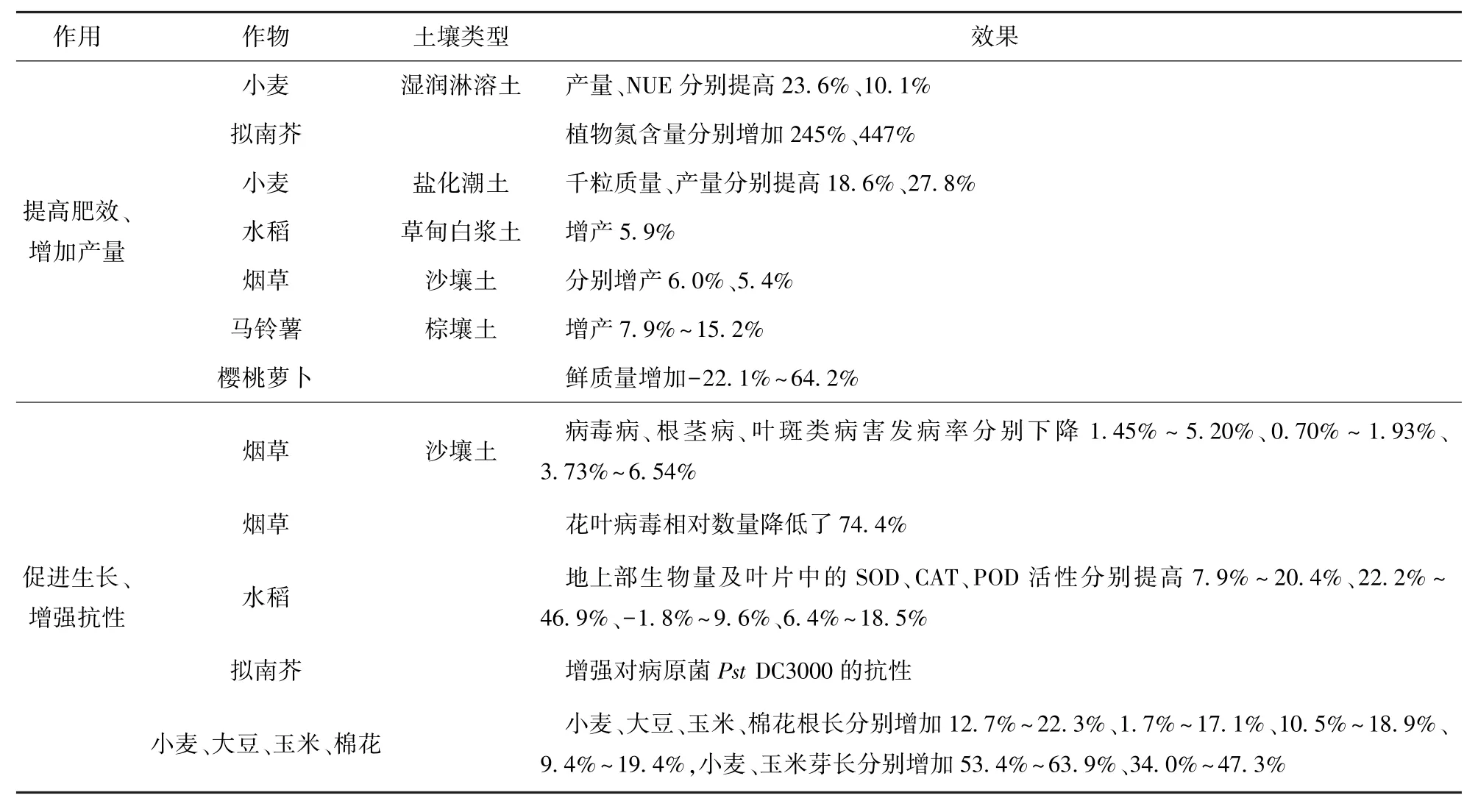
表11 内生菌提取物ZNC 的作用及效果
ZNC 的田间高效施用技术和作用机制都亟需进一步的研究。
3.2 植物源硝化抑制剂
植物源硝化抑制剂(BNIs)是一种环境友好型抑制剂,是由植物根系产生和分泌,现已发现湿生臂形草[123]、高粱[124]、水稻[125]、苦楝树[126]、杨梅[127]等能够释放生物硝化抑制剂。 BNIs 主要通过抑制氨单加氧酶和羟胺氧化还原酶来抑制硝化作用, 不同来源BNIs 的抑制方式不同, 见表12[124-131]。

表12 植物源硝化抑制剂的来源和作用机制
BNIs 通过抑制土壤硝化细菌和反硝化细菌的活性,减少因硝化和反硝化作用引起的氮素损失及温室气体排放。 已有研究发现,BNIs 可提高NUE 2.6%~6.7%(平均4.5%),增加产量5.6%~39.4%(平均10.3%),减少N2O 排放18.1% ~96%(平均40.0%),表明植物源硝化抑制剂在减少N2O 排放方面的潜力巨大。 植物源硝化抑制剂的作用和效果见表13[128,132-137]。
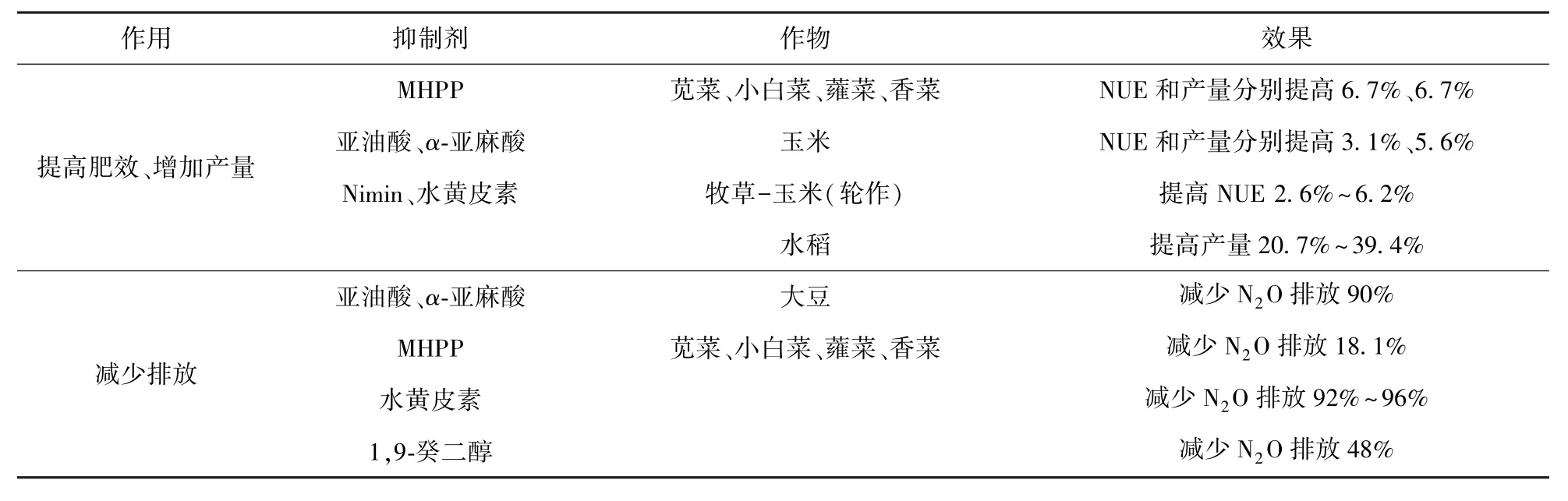
表13 植物源硝化抑制剂的作用及效果
4 讨论与展望
基于文献数据,对NUE 的提高,硝化抑制剂平均为17.1%,脲酶抑制剂平均为10.1%,氨稳定剂沸石、生物炭、腐殖酸依次为17.4%、4.7%、24.0%,ZNC 和BNIs 平均在7.0%左右,表明硝化抑制剂的效果较为突出和显著。 硝化抑制剂平均减少N2O、CO2、NO 排放分别为28.1%、42.5%、51.0%;脲酶抑制剂平均减少氨挥发37.0%,平均减少CH4、N2O 排放分别为25.8%、35.9%;沸石和腐殖酸平均减少氨挥发分别为30.7%、26.1%,BNIs 平均减少N2O 排放40.0%;即在减少温室气体排放方面,硝化抑制剂的效果较好,脲酶抑制剂的效果较广,BNIs 的潜力巨大。在作物增产方面,硝化抑制剂、脲酶抑制剂平均增产分别为16.4%、9.5%,氨稳定剂沸石、生物炭、腐殖酸平均增产依次为42.3%、12.6%、13.2%,ZNC 和BNIs 平均增产分别为18.1%、10.3%,各增效剂大多增产15%左右。 在改善作物品质方面,硝化抑制剂尤其是DCD 可以显著降低农产品中硝酸盐的积累量,并提高可溶性糖、可溶性蛋白、维生素C 的含量,氨稳定剂尤其是腐殖酸能够显著提高维生素C、可溶性糖的含量及糖酸比,ZNC 能增强植物抗性、降低病害发生率。 总体而言,硝化抑制剂、脲酶抑制剂、氨稳定剂在提高NUE、产量、产品品质和减少温室气体排放、氮损失等方面都有显著的作用和效果;ZNC 和BNIs 分别在氮肥增效、温室气体减排等方面具有特殊作用。
硝化抑制剂、脲酶抑制剂大多为化学合成,既存在用量大、价格贵的问题,又存在环境污染和生态安全风险,如醌类化合物易伤害土壤微生物、作物,CP 施用量为8.0 ~14.0 mg/kg 时可使大豆地上部和地下部生物量减少50%[138]。 氨稳定剂主要通过吸附等物理过程以及促进作物利用来提高NUE,环境污染、生态安全风险不大,但也存在用量过大及资源不足的问题。 为此,相关研究人员通过实施新的策略以达到提高NUE 和减少氮环境污染的目的:①氮肥减量与增效配合,如氮肥减量20% 配合增效剂使玉米增产10.24% ~17.05%,实现减氮不减产[139];②配合增效,即2 种或2 种以上的氮肥增效剂配合使用,如HQ 配合DCD 可减少CH4排放量58%[140],DMPP 配合生物炭显著降低了中性水稻土的AOB 丰度并分别提高水稻籽粒产量、NUE 为8.5%、10.6%[102];③开发新型多功能产品,如湖南泰谷生态工程有限公司开发了一种由多种植物粉末、黄腐酸、植物生长调节剂等配制而成的氮肥有机增效剂[141]。
《“十四五”全国农业绿色发展规划》中提出:以化肥减量增效为重点,集成推广科学施肥技术;开发农业生态价值,落实2030 年前力争实现碳达峰的要求,研发种养业生产过程温室气体减排技术。 这意味着氮肥增效剂在化肥减量增效、温室气体减排中的作用将得到进一步的重视和充分发挥。 基于氮肥增效剂已有的研究和应用,以推动农业绿色发展为主导,围绕投入品绿色、减量,建议按照减量增效、内生增效、整合增效深入推进氮肥增效剂的研究和应用:①减量增效,即基于作物养分科学定量以减少肥料尤其氮肥用量的条件下,研究和评价增效剂的作用和效果,避免增效剂屏蔽过量施肥的低效;②内生增效,即基于作物自身代谢活力、能力,在促进养分吸收利用和生长发育的前提下,研究和揭示增效剂的作用和机制,避免增效剂遮挡化学过程的负效;③整合增效,即基于作物生长环境因子、过程,在保障植株健康和生态安全的基础上,整合和发挥增效剂的作用和功能。 因此,应全链条研究和设计肥料增效剂,即以生物源(如ZNC 和BNIs)增效剂的“促生”作用为主导,以物理性(如腐殖酸)增效剂的“载体”作用为支撑,以化学性(如HQ、DCD 等)增效剂的“靶向”作用为辅助,积极推进增效剂向绿色、少量、高效转变。

