急性脑卒中机械取栓术后病人症状性脑出血预测模型构建分析
李 亮,张继伟,孙文浩,王 广,田 甜,于 淼
机械取栓术因其可以快速改善血管闭塞状态,有效改善传统静脉溶栓治疗的效果,提高血管再通率,降低病人死亡率和致残率[1],目前已成为急性缺血性脑卒中的主要外科治疗手段。虽然机械取栓再通率高,安全性佳,但仍可能存在如脑高灌注损伤、血管再闭塞等相关并发症,且随着时间延长,颅内出血的发生风险也有所增加[2],因此有必要构建一个关于急性脑卒中机械取栓术后病人症状性脑出血的预测模型,为脑出血的预防和治疗提供必要的理论支持。
1 资料与方法
1.1 一般资料 本研究共纳入2017-2020年于我院就诊的急性脑卒中行机械取栓术的病人156例,根据术后22~36 h内是否发生症状性脑出血分为出血组(n=17)和未出血组(n=139),并收集所有病人性别、年龄、基础疾病等临床资料。
1.2 纳入及排除标准 纳入标准:(1)临床诊断符合急性缺血性脑卒中[3],且为大动脉闭塞,30岁<年龄<90岁;(2)不符合静脉溶栓指征直接取栓的病人;(3)发病到治疗时间为:前循环≤6 h;(4)静脉溶栓治疗效果不明显者;(5)病人及其家属知晓本研究并签署知情同意书。排除标准:(1)合并严重基础疾病,如心肾功能不全、免疫系统疾病、脏器功能衰竭等;(2)入组前2个月内存在手术史;(3)CT示颅内出血或大面积新发脑梗死者;(4)活动性出血或明显出血倾向者;(5)对造影剂过敏者。
1.3 观察指标 (1)临床一般资料:根据病例系统,收集病人的临床一般资料,包括病人性别、年龄、既往史、栓塞部位、入院NIHSS评分、机械取栓的次数等。(2)随访资料:根据资料收集表收集病人术后22~36 h内随访情况,观察病人是否出现症状性脑出血。症状性脑出血判定标准:术后22~36 h行头颅CT检查,观察是否发生症状性脑出血,参照ECASS Ⅲ[4]标准将症状性脑出血定义为CT检查示脑出血,NIHSS评分≥4分。
1.4 统计学方法 采用t检验、χ2检验和多因素logistic回归分析,通过MedCalcV18.06.12软件构建受试者工作特征曲线(ROC)并计算曲线下面积(AUC)进行模型分析。
2 结果
2.1 2组病人临床一般资料的比较 2组间年龄、空腹血糖、糖化血红蛋白、心房颤动(房颤)、术前NIHSS评分、取栓次数比较差异均有统计学意义(P<0.05~P<0.01),性别、高血压、糖尿病、高脂血症、血管闭塞部位、术前静脉溶栓治疗、术后ASPECT评分比较差异均无统计学意义(P>0.05)(见表1)。
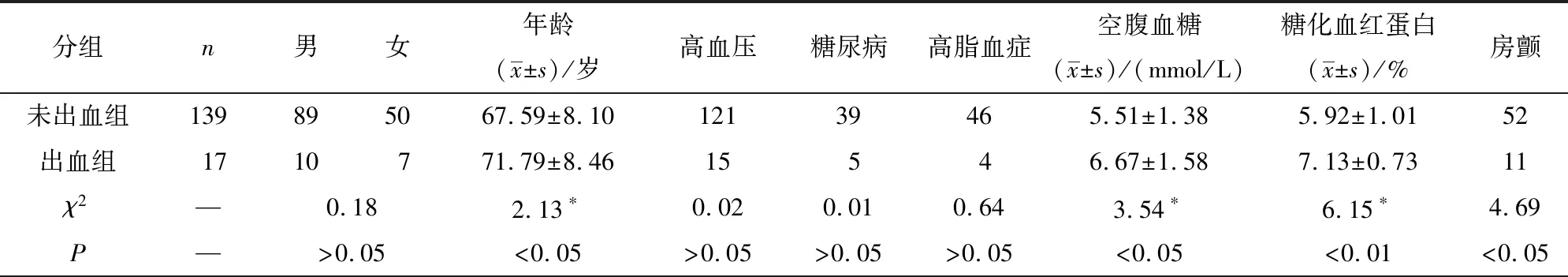
表1 2组病人临床一般资料的比较
2.2 预测模型构建 将未出血组和出血组间存在统计学差异的6个变量纳入logistic回归分析,结果显示:空腹血糖、糖化血红蛋白、房颤、NIHSS评分、取栓次数为急性脑卒中病人行机械取术后22~36 h内发生症状性脑出血的独立危险因素(P<0.01)(见表2)。
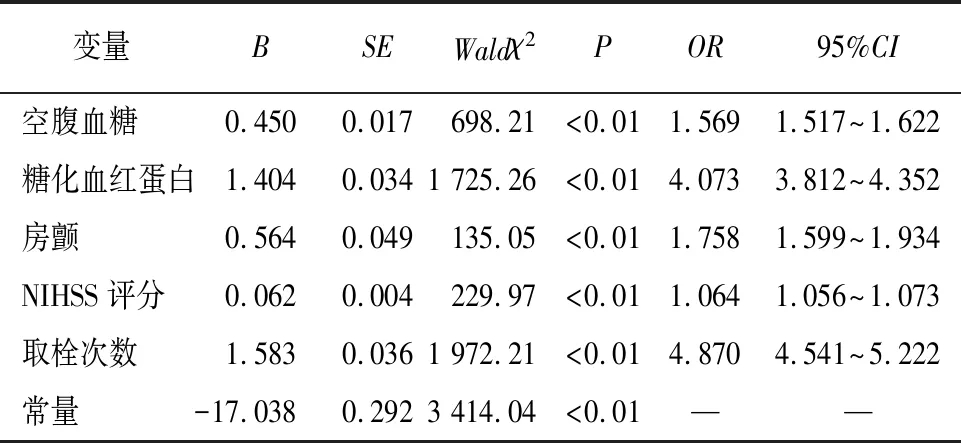
表2 逐步多因素二元logistic回归
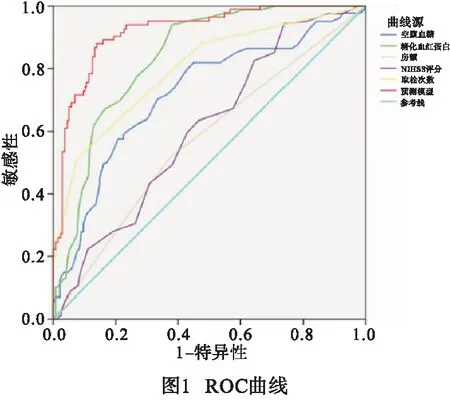
2.3 预测模型分析 根据二元logistic回归分析,将5个独立危险因素构建ROC曲线,结果显示,空腹血糖≥5.55 mmol/L,糖化血红蛋白≥6.15%,存在房颤,NIHSS评分≥11.50分,取栓次数≥2.5次时,急性脑卒中机械取栓后病人22~36 h内出现症状性脑出血风险增加。此时NIHSS评分的敏感度(94.40%)、取栓次数的特异度(92.50%)最高(P<0.01)(见图1、表3)。
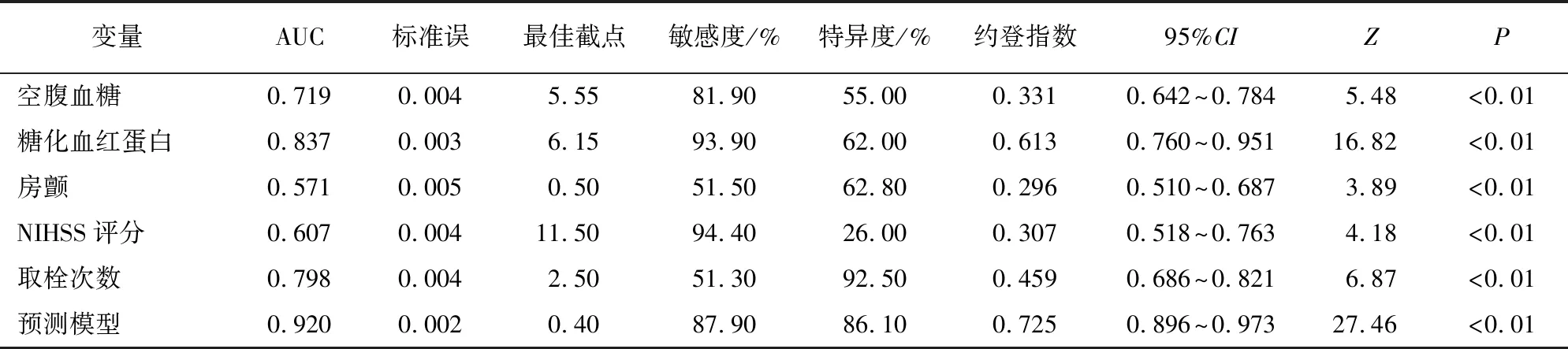
表3 急性脑卒中机械取栓后症状性脑出血预测模型
3 讨论
急性缺血性脑卒中因其发病率高、致残致死率高,已成为我国成人死亡的最主要原因之一。临床上的主要治疗手段是发病4.5 h内给予静脉溶栓,尽可能短时间内使已闭塞的血管再通,挽救缺血半暗带组织[5]。但静脉溶栓存在时间窗较窄,血管再通率低,治疗效果不佳,病人获益率较低等不足[6]。而机械取栓可以通过影像直接剥离栓子,实现血管再通,进一步扩大了病人入院救治的时间窗,为更多病人提供治疗机会,并显著提升血管再通率,改善病人临床预后,目前已逐步得到了广泛应用[7-8]。但相关研究[9-10]表明,机械取栓术有可能会增加急性脑卒中病人出血性转归不良的风险,因此有必要构建一个关于急性脑卒中机械取栓术后病人症状性脑出血的预测模型,为脑出血的预防和治疗提供必要的理论支持。
本研究共纳入年龄、性别、高血压病史、糖尿病病史等13个因素作为可能的预测因素。根据病例系统及随访资料,收集病人的临床资料,以机械取栓术后22~36 h内出现症状性脑出血为结局。将单因素分析中具有统计学意义的6个变量纳入logistic回归分析,结果显示:空腹血糖、糖化血红蛋白、房颤、NIHSS评分、取栓次数为急性脑卒中病人行机械取术后22~36 h内发生症状性脑出血的独立危险因素。通过MedCale软件构建ROC曲线并计算AUC进行模型分析,结果显示:空腹血糖≥5.55 mmol/L,糖化血红蛋白≥6.15%,存在房颤,NIHSS评分≥11.5分,取栓次数≥2.5次时,急性脑卒中机械取栓后病人22~36 h内出现症状性脑出血风险显著增加。其构建的模型下面积明显大于其他5个单独变量(P<0.01),说明构建的预测模型具有较好的预测效果。
本研究通过对156例急性脑卒中性机械取栓术后进行跟踪随访发现:术后22~36 h内出现症状性脑出血者共17例(10.9%),这与王瑞等[11-12]的研究结果相似。logistic回归分析结果显示:空腹血糖、糖化血红蛋白、房颤、NIHSS评分、取栓次数均为急性脑卒中病人行机械取术后22~36 h内发生症状性脑出血的危险因素。即病人空腹血糖越高、糖化血红蛋白越高、出现房颤、NIHSS评分越高、取栓次数越多,急性脑卒中病人机械取栓术后22~36 h内出现症状性脑出血的概率就越大。
空腹血糖和糖化血红蛋白均反映病人的血糖情况,当大动脉血管闭塞发生急性脑卒中发生时,机体高血糖状态促进机体糖原进行无氧酵解,乳酸等酸性物质堆积,使机体酸性增加,抑制机体各种酶的活性,并促进线粒体形态功能改变及其凋亡[13],并通过增加氧自由基加重病灶损伤,导致脑出血风险增加[14]。同时,当机体缺氧时,由于血管内膜完整性被破坏,血管通透性增加,红细胞外渗也会导致病人空腹血糖、糖化血红蛋白增加。
附在心房的栓子随着房颤脱落后可随体循环进入脑血管导致脑栓塞,造成心源性脑栓塞。血管被栓塞后,血管壁缺氧缺血坏死导致功能障碍,远端血供中断,当机械取栓治疗、血供恢复后,可能会在坏死管壁处出现渗血或出血[15]。同时,随着取栓后一些微小栓子可随血液发生移位,可能导致更大面积的脑梗死,缺氧缺血状态进一步加重血管内膜的损伤,加剧红细胞外渗,从而导致脑出血的风险增加[16]。
NIHSS评分表示卒中后神经功能缺损,分数越高表示神经缺损越严重。入院时NIHSS评分越高,表明急性缺血性卒中大血管闭塞的风险越高,即缺血缺氧症状明显,此时进行机械取栓后,极易引起大脑再灌注损伤,导致氧化应激反应及炎症反应出现,破坏血脑屏障,导致颅内出血[17]。
取栓次数增加有可能进一步破坏血管内膜,使血管损伤加重,引起继发性血栓形成,造成血管出血或再闭塞。当取栓恢复血供后,侧支循环不良的病人可能出现局部灌注过度,血管压力增加,导致红细胞外渗,引发出血[18]。
综上所述,空腹血糖、糖化血红蛋白、房颤、NIHSS评分、取栓次数均可作为急性脑卒中病人行机械取术后症状性脑出血的预测指标。可以帮助医护人员尽早预防并识别潜在的颅内出血,提高病人生命质量。本研究的局限性:本研究作为单中心研究,可能存在一定的结果偏倚,后期可进行多中心研究,增加样本量,增加结果的准确度。

