QuEChERS-UPLC-MS/MS法测定豆芽中15种喹诺酮类药物残留
张汝凡,闫瑛楠,郑婕
河南省食品和盐业检验技术研究院(郑州 450003)
豆芽是我国的一种传统食材,因其营养丰富且价格低廉深受消费者喜爱[1-2]。然而豆芽在培育的过程中极易受到各种微生物的侵蚀,其中以克雷伯菌属和埃希菌属的数量最多[3]。为防止豆芽腐败,部分生产者会在生产运输中添加喹诺酮类抗生素。喹诺酮是一种广谱抗菌药,其效用明显且价格相对较低,能够有效抑制细菌内的脱氧核糖核酸旋转酶的活性,使其无法做到正常分裂,从而达到杀菌作用[4-5]。有研究表明,长期食用含有喹诺酮类药物残留的食品会导致相关药物在人体内蓄积,可能会造成食用者消化系统、中枢神经系统及消化系统(消化系统改为肝肾心脏)等产生不良反应[6-7],同时也会导致人体的耐药性变强,进而影响相关疾病的治疗效果[8-11]。因此,为保障消费者的健康和安全,开展豆芽中喹诺酮类药物检测非常有必要。
针对豆芽中的喹诺酮类药物的检验方法以高效液相色谱-串联质谱法为主[12-15],前处理方法有液液萃取法[16]、固相萃取法[17]和QuEChERS法[18]等,但是这些方法都存在不同程度的问题。QuEChERS法作为一种广泛用于农产品检测的新型快速前处理技术,对样品中的蛋白质及脂类去除效果明显[19-23]。试验旨在建立一种快速便捷的QuEChERS检测方法,为豆芽中喹诺酮药物残留的风险监测提供更加高效精准的技术支持。
1 材料与方法
1.1 材料与试剂
豆芽,从郑州市各大市场、超市随机抽取。标准物质:恩诺沙星(enrofloxacin,CAS号:93106-60-6)、环丙沙星(ciprofloxacin,CAS号85721-33-1)、诺氟沙星(norfloxacin,CAS号70458-96-7)、达氟沙星(danofloxacin,CAS号112398-08-0)、培氟沙星(pefloxacin,CAS号70458-92-3)、沙拉沙星(sarafloxacin,CAS号98105-99-8)、氧氟沙星(ofloxacin,CAS号82419-36-1)、奥比沙星(orbifloxacin,CAS号113617-63-3)、双氟沙星(difloxacin,CAS号98106-17-3)、氟罗沙星(fleroxacin,CAS号79660-72-3)、依诺沙星(enoxacin,CAS号74011-58-8)、司帕沙星(sparfloxacin,CAS号111542-93-9)、氟甲喹(flumequine,CAS号42835-25-6)、噁喹酸(oxolinic acid,CAS号26893-27-6)、洛美沙星(lomefloxacin,CAS号98079-51-7),质量浓度均为100 μg/mL,纯度均为100%,天津阿尔塔科技有限公司。甲酸、乙腈(质谱纯,德国默克公司);试验用水为Milli-Q超纯水;氯化钠(天津科密欧化学试剂有限公司);乙二胺-N-丙基硅烷(PSA,Biosun有限公司);无水硫酸镁(MgSO4,天津大茂化学试剂厂);十八烷基硅烷(C18,上海安谱公司)。
1.2 仪器与设备
高效液相色谱-质谱/质谱仪(Agilent 1290-6470,安捷伦科技有限公司);电子分析天平(ME204,梅特勒托利多科技有限公司);高速冷冻离心机(SIGMA 4-16KS,德国SIGMA公司);振荡器(MV-3000,北京莱谱科技有限公司);涡旋混合器(WH966,上海康华生化仪器制造有限公司);超声波清洗器(KQ-500TDB,昆山超声仪器有限公司);全自动氮吹仪(ORGN-EVAP24,美国Organomation公司)。
1.3 试验方法
1.3.1 样品前处理
称取5 g(精确至0.001 g)豆芽样品置于50 mL塑料离心管中,加入混合标准溶液,加入10 mL 1%甲酸乙腈溶液,加入5 g氯化钠,涡旋混合1 min,超声提取15 min后,以10 000 r/min离心5 min,上清液转移至50 mL离心管中,残渣用10 mL 1%甲酸乙腈溶液同法重复提取1次,合并2次上清液,充分混匀,待净化。吸取5 mL上清液于QuEChERS提取净化管中(含100 mg MgSO4+100 mg C18),剧烈振荡2 min,以10 000 r/min离心5 min,精密吸取2 mL上清液于10 mL离心管中,在40 ℃水浴中氮气吹至近干,残渣中加入1 mL 20%乙腈水溶液,涡旋溶解,过0.22 μm有机滤膜后,供高效液相色谱-质谱/质谱仪测定。
1.3.2 基质标准溶液配制
分别准确吸取15种喹诺酮类标准物质各100 μL于同一10 mL容量瓶中,用乙腈稀释并定容至刻度,振荡摇匀后,作为混合标准储备液,于-20 ℃避光保存。选择豆芽空白样品进行提取、净化等前处理,得到空白基质溶液。准确吸取一定量的混合标准储备液,用豆芽空白基质溶液将混合标准储备液稀释成质量浓度为1,2,5,10,20和50 ng/mL的系列基质匹配标准工作溶液。
1.3.3 色谱条件
色谱柱Agilent Eclipse XDB-C18(2.1 mm×100 mm,1.8 μm);流速0.3 mL/min;柱温30 ℃;进样量2 μL;流动相A为0.1%甲酸水溶液,B为乙腈,流动相梯度;洗脱条件见表1。

表1 流动相梯度洗脱条件
1.3.4 质谱条件
离子源采用电喷雾离子源(ESI),正离子扫描;气帘气压力(CUR)5 psi;电喷雾电压(IS)4 000 V(正离子模式);离子源温度(TEM)340 ℃;质谱扫描方式采用多反应监测模式(MRM);15种喹诺酮类药物的质谱参数见表2。
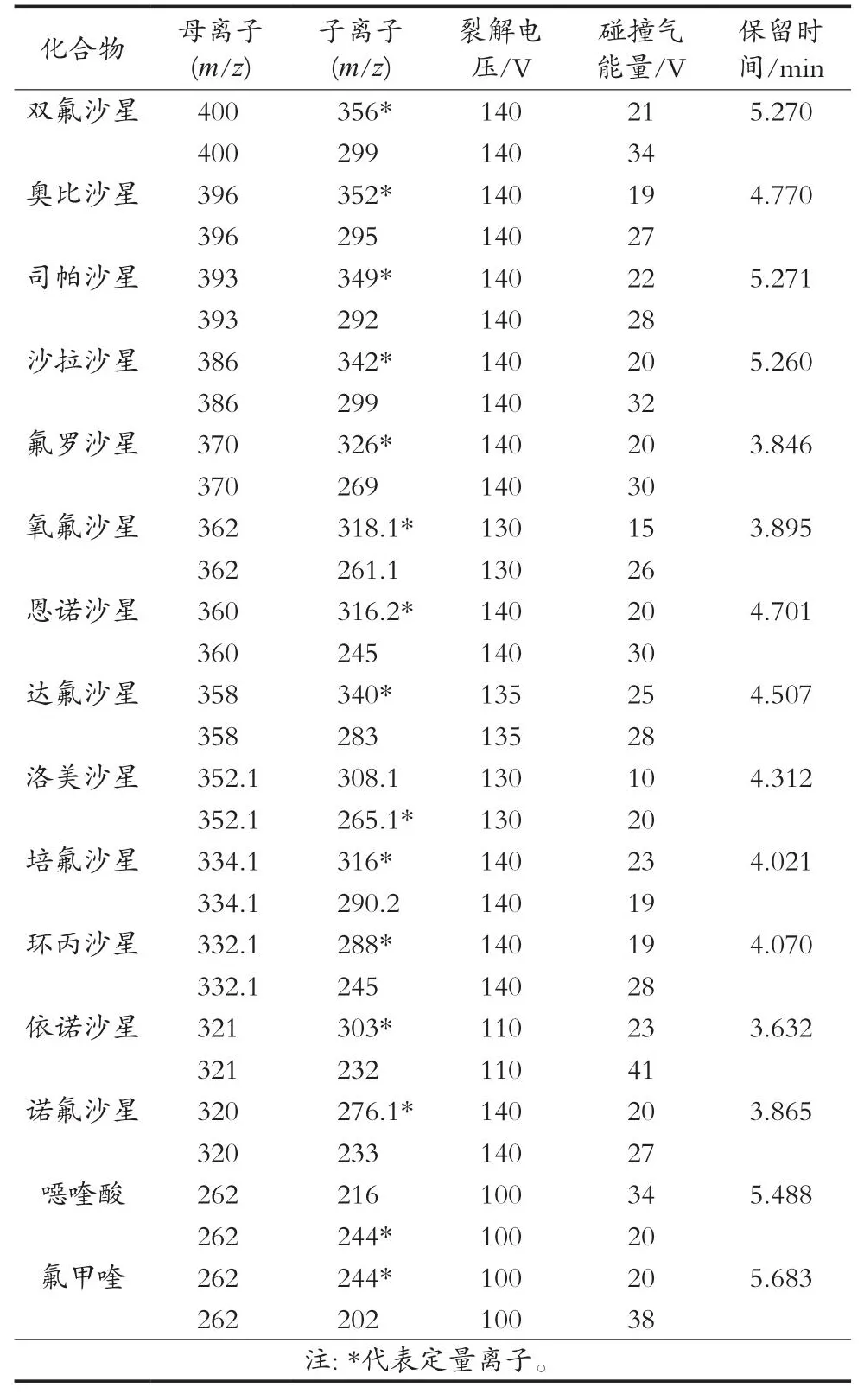
表2 15种喹诺酮类药物的质谱参数
1.3.5 数据处理
采用Microsoft Office Excel 2007软件进行数据处理与分析。
2 结果与分析
2.1 提取溶剂的选择
文献报道的前处理方法中,抗生素选用较多的提取溶剂有甲醇、乙腈、酸化乙腈和EDTA-Mcllvaine缓冲溶液等。与甲醇相比,乙腈具有较低的基质干扰效应,易于沉淀蛋白,更容易通过盐析从水相中分离出来,对于喹诺酮类药物而言,酸性提取剂可以提高目标物的离子化效率,促进[M+H]+峰的形成,提高质谱响应并改善峰形,回收率也会有所提升[19]。所以试验考察乙腈、1%甲酸乙腈、1%乙酸乙腈、EDTAMcllvaine缓冲溶液4种试剂作为提取溶剂进行前处理提取。经前处理试验验证,EDTA-Mcllvaine缓冲溶液提取出的溶液混沌度高,经高速冷冻离心后样品基质与提取液仍不能进行有效分离,可见EDTA-Mcllvaine缓冲溶液对豆芽中的脂肪蛋白质等杂质的去除效果较差,在后续检测过程中可能会损坏色谱柱,污染检测器,故排除此提取溶剂。其他3种提取溶剂经仪器测定,以化合物对应峰面积为指标,考察提取结果,结果如图1所示。结果显示,1%甲酸乙腈对豆芽中的15种喹诺酮类药物的提取效果较优,故选定1%甲酸乙腈溶液作为提取溶剂。
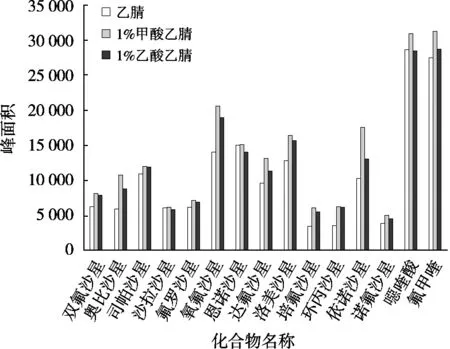
图1 不同提取试剂对豆芽中15种喹诺酮类药物的提取结果对比
2.2 净化条件的优化
N-丙基乙二胺(primary secondary amine sorbent,PSA)可去除样品基质中的极性干扰物质;C18作为一种反向硅胶键合吸附剂,可较好地吸附脂肪,除去样品中脂类杂质;无水硫酸镁(MgSO4)可快速吸附样本中多余的水分,降低目标物在水相中的溶解[19],故试验考察PSA、C18、无水硫酸镁3种净化材料对喹诺酮类药物回收率的影响,样品在使用相同提取试剂以及相同加标量10 μg/kg条件下分别考察净化材料单独使用与组合使用对待测物回收率的影响,效果对比如图2所示。结果表明100 mg MgSO4+100 mg C18对目标化合物的净化效果最好,所以选择100 mg MgSO4+100 mg C18作为净化剂。
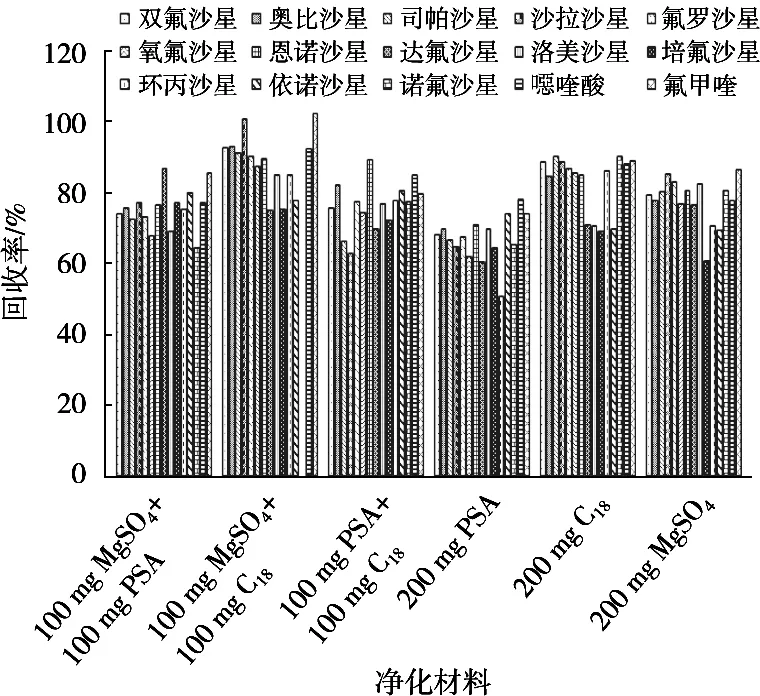
图2 不同净化条件下的净化效果比较
2.3 质谱条件的优化
由于喹诺酮类化合物的分子结构中含有羰基结构,在质谱ESI源的正离子模式下易于形成[M+H]+的准分子离子,正离子模式下的响应值远高于负离子模式[24]。所以试验采用ESI+模式对15种目标化合物进行质谱全扫描分析,得到相应的母离子后,通过测试不同的Fragmentor电压值下母离子的响应强度选出最佳电压值,而后进行子离子扫描,选出2个响应值最高的特征离子作为定量离子和定性离子。在MRM模式下优化碰撞能量(collision energy,CE),确定每种化合物的最佳质谱条件,15种喹诺酮类药物质谱参数优化结果见表2,标准物质提取的离子色谱图见图3。
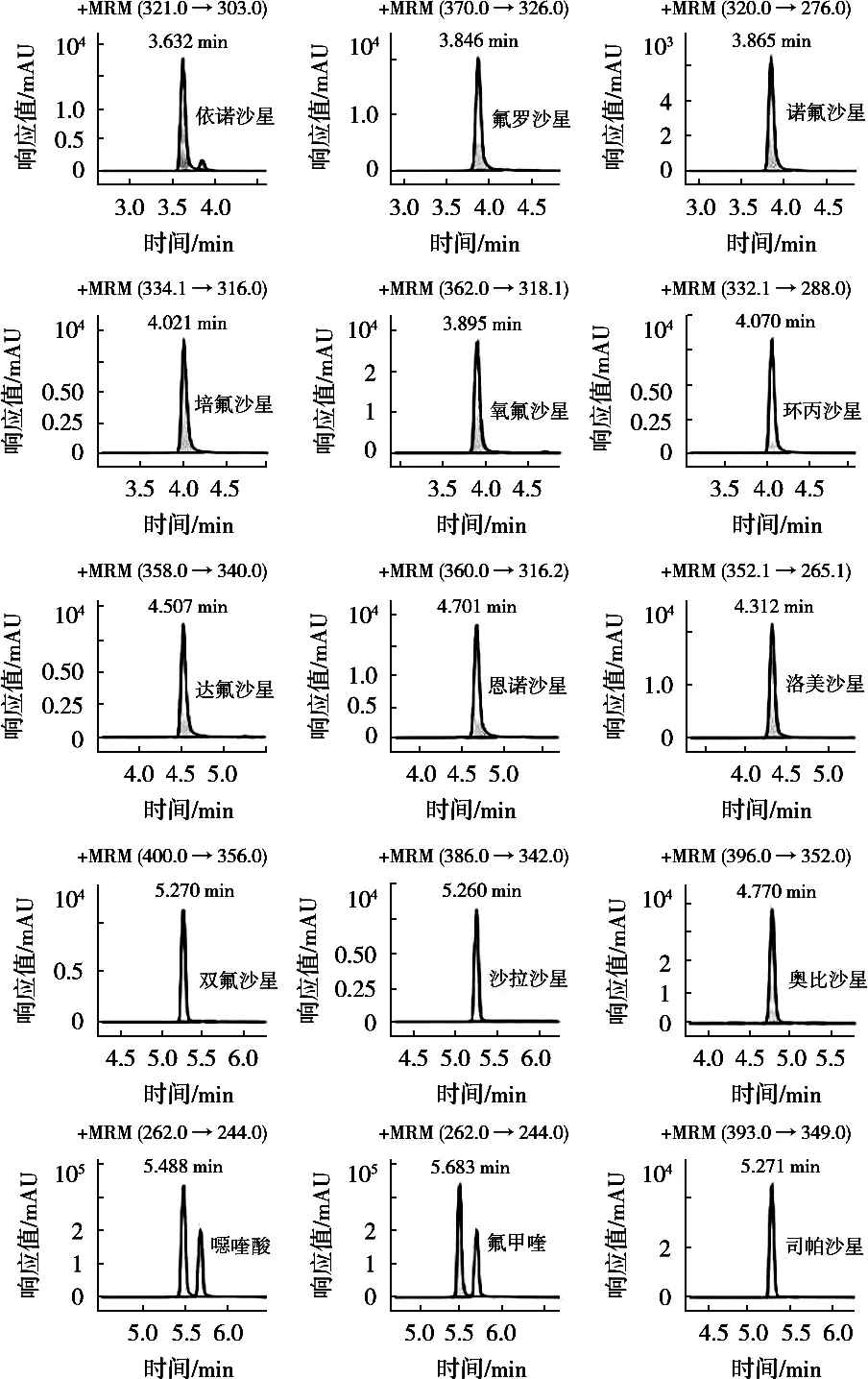
图3 15种喹诺酮类药物的离子色谱图
2.4 线性关系及定量限
将空白样品按上述前处理方法制得空白基质溶液,用空白基质溶液将混合标准溶液稀释成1,2,5,10,20和50 ng/mL的系列溶液。以目标化合物定量离子的峰面积为纵坐标,质量浓度为横坐标得到线性回归方程。15种喹诺酮类化合物在豆芽基质中的线性相关系数均大于0.997,表明在1~50 ng/mL范围内各化合物均呈良好的线性关系。通过豆芽的阴性样品加标测定,15种喹诺酮类药物在3 μg/kg的添加水平下经过前处理所得试液的信噪比(rSN)均大于10,表明该方法15种喹诺酮类化合物的定量限均可达3 μg/kg。线性方程、相关系数及定量限见表3。
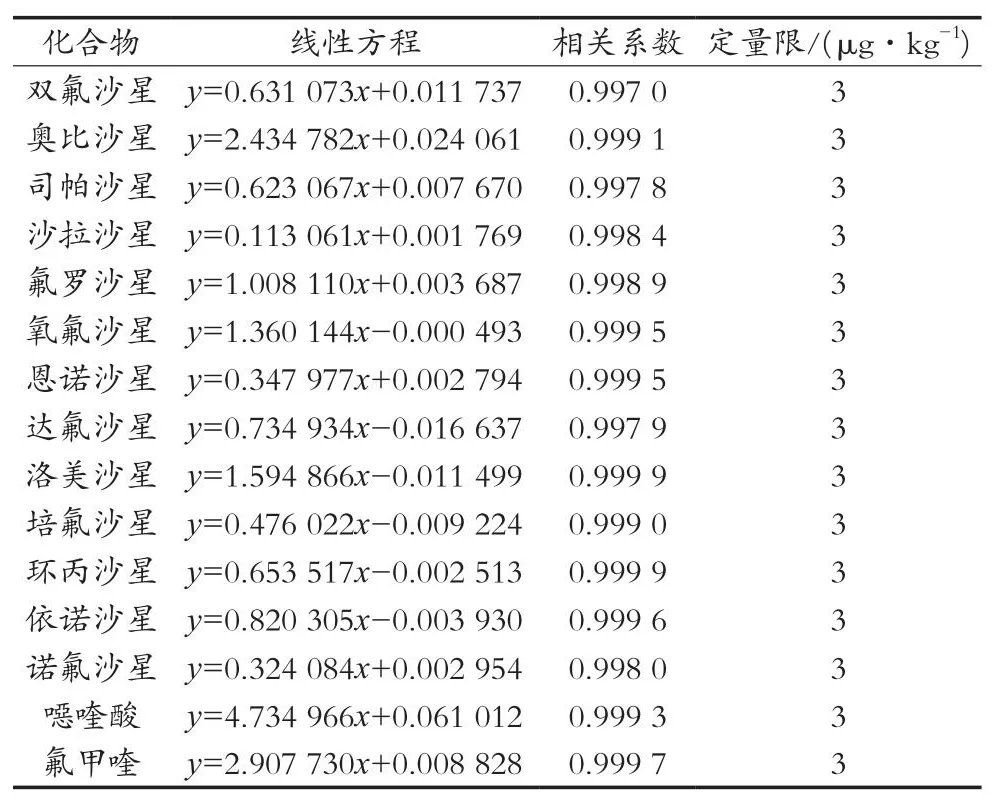
表3 豆芽中15种喹诺酮类药物的线性关系及定量限
2.5 方法回收率和精密度
分别制备相当于含15种喹诺酮类药物10,20和80 μg/kg的低、中、高3个浓度水平豆芽样品,每个水平分别做6份平行试验,计算回收率和精密度。15种喹诺酮类药物在豆芽中不同浓度的回收率及精密度见表4。结果显示,15种喹诺酮在10 μg/kg的添加水平下,回收率为75.1%~102.3%,相对标准偏差(SRSD)为2.4%~9.3%(n=6),在20 μg/kg的添加水平下,回收率为77.2%~97.4%,SRSD为1.3%~9.0%(n=6),在80 μg/kg的添加水平下,回收率为74.3%~96.6%,SRSD为2.2%~8.6%(n=6)。在不同的添加水平下,样品基质中的重现性与平行性均较好,可满足多种样品基质大批量检测的需求。表明该方法准确性、精密度和重复性良好。
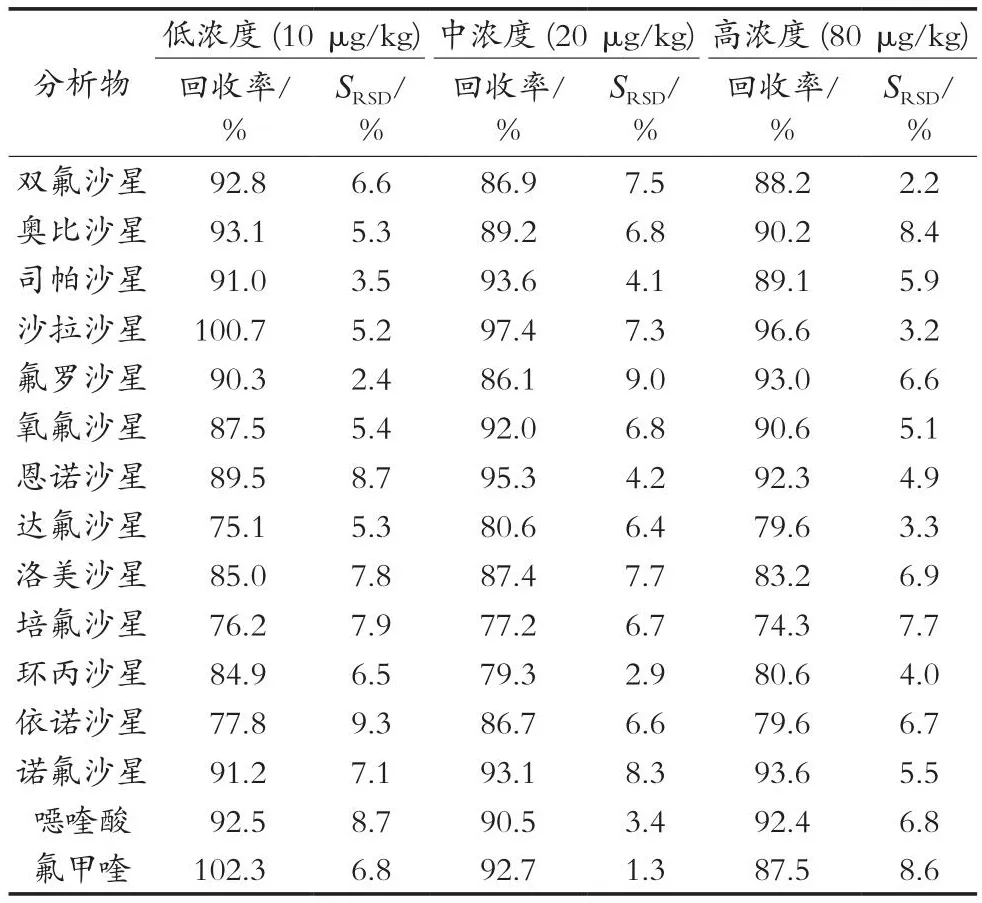
表4 豆芽中15种喹诺酮类药物的回收率及精密度(n=6)
2.6 实际样品检测
从周边不同市场随机购买28批豆芽进行检测,共有8个批次检出环丙沙星,含量介于20.9~685 μg/kg,检出率为28.6%。整个试验过程操作快速便捷,检验效率高,表明该方法适合用于大批量豆芽样品的检测。
3 结论
试验改进豆芽中15种喹诺酮类化合物测定的高效液相色谱串联质谱方法,从经济成本上考虑,QuEChERS前处理方法相较传统的HLB柱固相萃取柱净化法,节约了试验成本。从效率上考虑,QuEChERS前处理操作更加简单快速、净化效果良好、试验结果准确可靠,能一次性测定豆芽中15种喹诺酮类化合物,满足监管需要,可为豆芽中喹诺酮药物残留的风险监测提供技术支持。

