水热法制备高比表面积花球状二硫化钼的条件探索
任改梅,蔡文昊,涂川俊,刘艳丽
(湖南大学 材料科学与工程学院,湖南 长沙 410082)
具有3d 价电子层结构的过渡金属元素所构成的硫化物具有特殊的结构和物理化学性能[1-4].二硫化钼(MoS2)是一种具有金属光泽的黑色固体粉末,具有较高的催化活性和良好的稳定性,在催化剂应用方面具有很大的前景[5-7].为了采用简单、绿色、经济的合成方法制备优良催化性能的MoS2,科学工作者们对于MoS2的制备和改性做了许多深入研究[8-10].与普通MoS2相比,纳米MoS2具有高不饱和性和催化活性边缘结构,性能更加优越,主要表现在比表面积大、反应活性高、催化性能提升、吸附能力增强等优点[11-13].水热法在多种制备方法中,具有反应条件温和、操作简单、产物形貌可控及纯度较高等优点[14-16].因此,本文采用水热法,选择三氧化钼(MoO3)作为反应的钼源,硫氰化钾(KSCN)作为反应的硫源和还原剂,通过改变反应温度、体系的pH,添加表面活性剂十六烷基三甲基溴化铵(CTAB)以及使反应物中硫源大比例过量等,探索不同反应条件下,产物微观结构和形貌的变化,并对其反应机理进行探讨,研究产物微观结构与反应条件之间的联系.
1 实验部分
1.1 MoS2的制备
1)分别称取0.432 g MoO3和0.873 g KSCN 溶于80 mL的去离子水中,使得反应物中钼、硫摩尔比为1∶3,在磁力搅拌下逐滴加入1.0 mol/L稀盐酸,调节pH 分别为0.6、1.0、2.0,将所制得的溶液转移至100 mL 聚四氟乙烯内衬的反应釜中进行反应,反应温度设定为240 ℃,反应时间为24 h.反应完成后,反应釜随炉冷却至室温.将沉淀用KOH 稀溶液洗涤,再用去离子水和无水乙醇充分洗涤,离心,于60 ℃下干燥24 h.
2)改变反应温度,分别设定为180 ℃、210 ℃,调节反应体系pH值为0.6,其余过程同1).
3)称取0.02 g表面活性剂CTAB溶于40 mL去离子水中,超声至完全溶解,重复上述MoO3和KSCN 的配制过程,将所得混合溶液逐滴加入CTAB 溶液中,调节反应体系pH值为0.6,其余过程同1).
4)改变反应物中钼、硫摩尔比分别为1∶5、1∶10、1∶15,使反应物中硫源过量进行反应,其余过程同1).
1.2 样品表征
本实验采用Rigaku D/Max-2400 型转靶全自动X 射线粉末衍射仪,用Cu-Kα 线(λ=1.541 78×10-7mm)作为发射光源,加速电压为40 kV,电流为100 mA,步长为0.004°,扫描速度为8°/min,扫描角度为5°~80°.扫描电镜照片(FESEM)和能谱数据(EDS)来自型号为Hitachi S-4800 和JSM 6700F 冷场发射扫描电子显微镜,工作电压分别为10 kV和15 kV.紫外/可见漫反射(UV-Vis-DRS)吸收光谱来自装有小积分球的固相紫外/可见/近红外吸收光谱仪(Hitachi Model U-4100,日本日立公司),扫描范围为240~2 600 nm,测试均采用吸收模式,检测系统为积分球,狭缝设为4 nm.
2 结果与讨论
2.1 反应体系不同pH值对所得产物的影响
图1为水热反应温度为240 ℃,反应时间为24 h,反应物中钼、硫摩尔比为1∶3,不加任何表面活性剂,调节体系不同pH 值所制备产物的XRD 图谱,与标准图谱(JPCDS No.37-1492)比对发现,所有衍射峰(002)、(100)、(103)、(110)均属于六方晶系MoS2,图1 中并未发现其他杂质峰,说明在该条件下的水热反应可成功制备纯相的MoS2.当pH=0.6 和pH=1.0时,所得产物衍射峰高且尖锐,表明所得MoS2的结晶度较好,制备的粉末样品多为花瓣状.而当pH=2.0时,所得产物多为棒片状结构,且颗粒之间发生粘连,甚至形成了絮状,未形成层状堆垛;其XRD 图谱表现出明显的宽化以及弥散的背景,(002)衍射峰向低角度发生明显偏移,我们推测可能是因为MoS2层状结构发生弯曲导致晶格产生膨胀的结果.
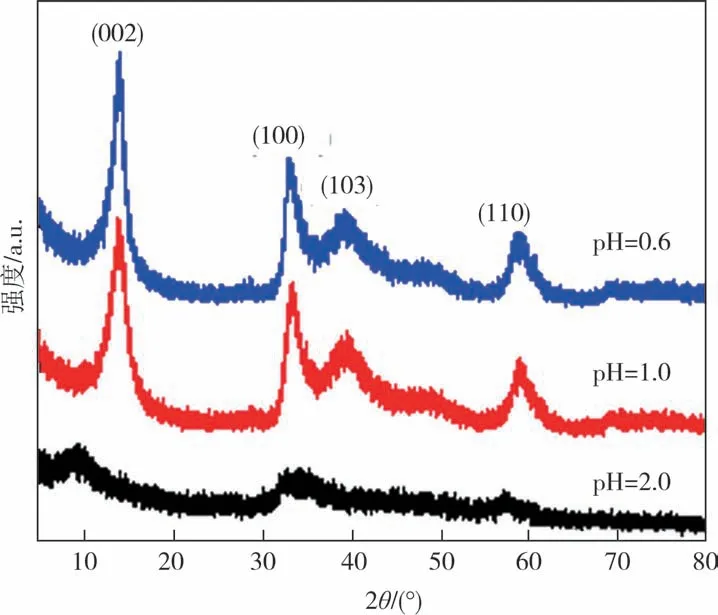
图1 不同pH值所得MoS2的XRD图谱Fig.1 XRD patterns of the samples obtained MoS2at different pH
图2 为反应体系在不同pH 值下所得MoS2的SEM 照片.由图2(a)可知,当反应体系pH=2.0 时,所得MoS2主要呈棒片状,直径为300 nm~1 μm,长度达到几个微米,且一些棒片的交界出现模糊,甚至形成絮状团簇.图2(b)为图2(a)的局部放大图,从图2(b)中可以很清晰地看出棒状MoS2的表面并不光滑,呈现出花纹状结构,花纹分布较为均匀,且无明显的选择性生长.由图2(c)可知,当反应体系的pH值降至1.0 时,所得产物已经没有明显的棒片结构,取而代之的是近似球形的絮状团簇,且该絮状团簇分散性较差,表面比棒片结构显得更为粗糙.经过进一步放大,如图2(d)所示,可以看到该絮状团簇表面由一些薄片组成.当反应体系的pH值降至0.6时,由图2(e)可知,所得产物出现了明显的球花状结构,球花的直径大约为400 nm,大小较为均一,球花的分散性也比上述絮状团簇好,该球花的放大图如图2(f)所示,从图2(f)可以看出球花的表面由许多花瓣状的薄片构成,薄片之间界限分明.
为进一步探索反应体系pH 值的变化对所得产物MoS2形貌改变的机理,观察了原料MoO3的微观结构,如图3 所示.从图3(a)中可以看出,原料MoO3为棒片状结构,直径在300 nm~1 μm;由图3(b)可知,原料MoO3的表面十分光滑,无任何花纹结构,因而可以推测,在反应过程中,随着pH值的降低,MoO3在反应体系中的溶解速度逐渐增大.当pH为2.0时,由于溶解的MoO3较少,而在棒片状MoO3周围的钼离子浓度较大,所以MoS2就以MoO3为形核基底和生长模板,从表层向内部生长.当pH 值继续降低时,MoO3溶解速度加快,扩散出的钼离子与溶液中的硫离子能够更充分地进行反应,因而得到的MoS2不再以棒片状MoO3为模板成核及生长,同时又为了降低其表面能,所以形成由层片状MoS2组成的球花状结构.

图3 原料MoO3的SEM照片Fig.3 SEM images of raw material MoO3
在水热反应过程中,KSCN 在不同的酸性条件下受到高温高压的作用,将MoO3还原生成MoS2,在MoS2晶核生长的过程中,在酸性条件的作用下,H+积聚在MoS2纳米结构表面及边缘中,由于H+电荷屏蔽效应的影响,边缘与表面、表面与表面之间发生大量的结合,阻止晶核进一步长大,从而只能自组装形成花球状的MoS2[17].
2.2 反应体系不同反应温度对产物的影响
图4 为反应温度为180 ℃,反应原料中Mo 和S的摩尔比为1∶3,反应体系pH 值为0.6 时,不加任何表面活性剂,水热反应24 h 所得产物的XRD 图谱.通过与标准图谱比对,发现其主要衍射峰(020)、(110)、(040)、(021)、(060)与斜方晶系的三氧化钼标准图谱相符合(JPCDS Card No.35-0609),其他衍射峰(100)、(200)、(300)则与JPCDS 标准卡片No.21-0569 六方晶系三氧化钼的标准图谱吻合,说明在该反应温度下并没有MoS2产物生成,得到的产物为分属两个不同晶系的三氧化钼.
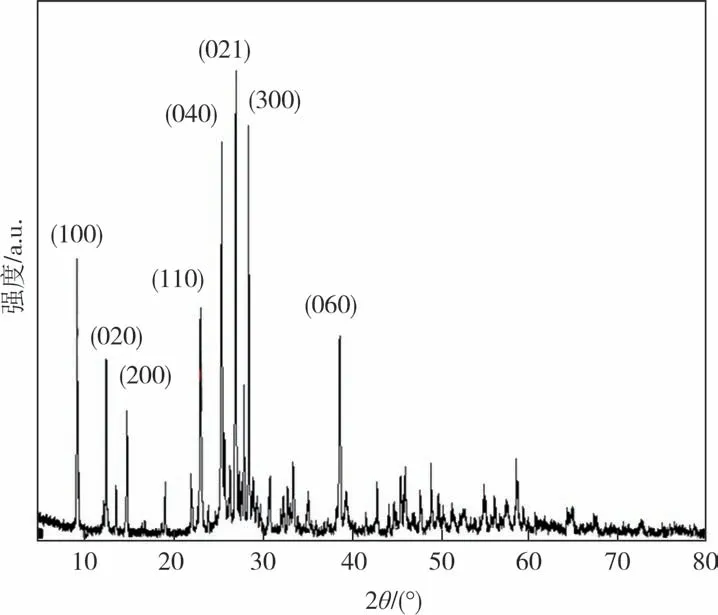
图4 180 ℃反应温度下所得产物的XRD图谱Fig.4 XRD pattern of the sample obtained at the reaction temperature 180 ℃
图5 为其他反应条件不变,而反应温度分别为210 ℃和240 ℃所得产物的XRD 图谱.通过与标准图谱比对,发现当反应温度为240 ℃时,所得产物所有衍射峰(002)、(100)、(103)、(110)均属于六方晶系MoS2(JPCDS Card No.37-1492),图中并未发现其他杂质峰,说明通过该条件下的水热反应可制得纯相的MoS2.而当反应温度为210 ℃时,所得产物的特征峰与反应温度为240 ℃时基本吻合,说明该温度下也得到了属于六方晶系的MoS2.但是反应温度为210 ℃所得产物的XRD 特征峰明显宽化,并且位于(103)位置的特征峰很不明显,说明该反应温度下得到的MoS2晶体颗粒较小,且合成的MoS2处于层状结构与花球状结构相结合的状态.
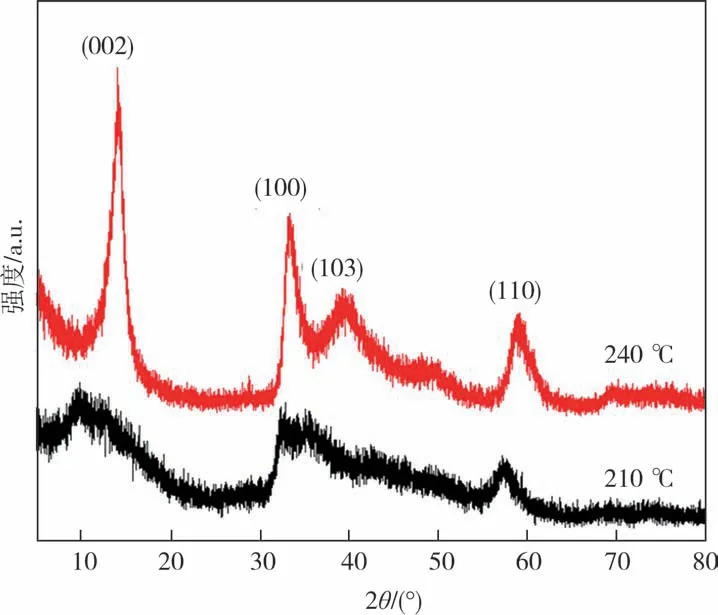
图5 不同反应温度下所得产物的XRD图谱Fig.5 XRD patterns of the samples obtained at different reaction temperature
图6 为不同反应温度下制得的MoS2的SEM 照片.由图6(a)和图6(b)可以看出,当反应温度为180 ℃时,所得产物具有棒片状结构,表面光滑,与原料MoO3相似(图3),且XRD 图谱表明产物以原料MoO3(图4)为主,图6(a)和图6(b)中显示MoO3比原料的破碎程度更高(图3),应该是溶液配制过程中的超声振荡导致.在实验过程中,当反应温度为180 ℃时,反应完全后,所得沉淀呈浅蓝色[图7(a)],并且经过洗涤过后蓝色褪去.当反应温度分别为210 ℃和240 ℃时,沉淀呈黑色[图7(b)和图7(c)],Mo6+水溶液为无色,而Mo5+水溶液呈蓝色,因而可以推测,该浅蓝色沉淀应该是由于Mo5+的存在所导致的.所以,在180 ℃的反应温度下,该反应体系无法得到MoS2,甚至反应物MoO3也只是少量溶解,且溶解的部分没有参与反应生成MoS2,而是被还原成Mo5+.另外,当反应温度为210 ℃时,由产物的SEM 照片[图6(c)和图6(d)]可以看出,所得产物开始形成类球状团簇,直径在400 nm 左右,而且团簇体表面呈现较浅的不规则片状花纹.随着反应温度的进一步升高,在240 ℃下所得产物则显示出了明显的球花状结构[图6(e)和图6(f)],球花的直径大约为400 nm,大小较为均一,球花的表面由许多花瓣状的薄片构成,薄片之间界限分明.因此,240 ℃是在该反应体系下制得球花状MoS2的最佳温度.

图6 不同反应温度下制得的MoS2的SEM照片Fig.6 SEM images of MoS2obtained at different reaction temperature

图7 不同反应温度下的产物照片Fig.7 Images of the samples obtained at different reaction temperature
在水热反应过程中,KSCN 受到高温高压的作用,将MoO3还原生成MoS2,由于温度的不同,所得到的产物的颗粒大小,团聚情况也有所差异,随着温度的升高,MoS2纳米结构表面及边缘的能量势垒高度降低,阻止了晶核长大,为降低表面能,从而只能自组装形成花球状的MoS2.
2.3 表面活性剂对所得产物的影响
图8 为未经煅烧所得产物的XRD 图谱.其具体条件是反应温度为240 ℃,n(Mo)∶n(S)=1∶3,pH=0.6,水热反应24 h,加入表面活性剂CTAB 与否所得产物的XRD 图谱.由图8 可以看出,当反应体系中加了CTAB 以后,所得产物在2θ=14°附近有较为明显的衍射峰,对应于MoS2的(002)晶面,说明制备的样品在c轴有较好的堆垛;在2θ=35°附近只有宽化的包,而在其他位置则只有弥散的背景,说明所得MoS2粒径较小,虽然形成了花状结构,但由于表面存在粘连,分布不均匀,衍射峰发生了偏移.体系中没有加入表面活性剂时,如前所述,为纯相的六方晶系MoS2,对应的PDF 卡片为JPCDS 标准卡片No.37-1492.
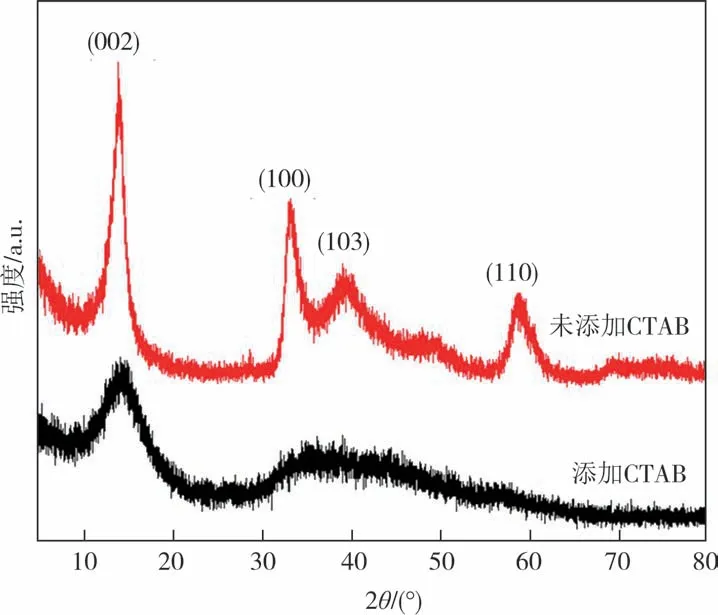
图8 未经煅烧所得产物的XRD图谱Fig.8 XRD patterns of the samples obtained without calcination
图9 为添加CTAB 时不同pH 值所得产物的SEM照片.其具体条件是反应温度为240 ℃,n(Mo)∶n(S)=1∶3,水热反应24 h.从图9 可以看出,当反应体系中加入表面活性剂以后,所得的MoS2表现出更为规整的球形,尺寸分布更加均匀,球的表面同样存在花瓣状的薄片结构,而且随着pH 的降低,花球直径减小.当pH=1.0 时,花球直径大约为800 nm[图9(a)和图9(b)];当pH=0.6 时,花球直径为200~300 nm[图9(c)和图9(d)].究其原因,可能是由于产物MoS2颗粒表面带负电,而阳离子型的表面活性剂CTAB具有带正电的基团,由于静电作用,反应过程中CTAB 会吸附在MoS2颗粒表面,由于CTAB 的“空间位阻”效应避免颗粒团聚,从而使所得的MoS2球更为规整.

图9 添加CTAB时不同pH值所得产物的SEM照片Fig.9 SEM images of the samples obtained with CTAB at different pH
2.4 不同反应物配比(硫源大比例过量)对产物的影响
图10 为反应物中不同钼、硫摩尔比反应所得产物的SEM 照片,从图10 中可以看出,随着反应物中KSCN 用量的增加,即反应物中钼、硫摩尔比的减小,所得球状产物的直径越来越小,当n(Mo)∶n(S)=1∶3时,产物的直径约为500 nm[图10(a)和图10(b)];当n(Mo)∶n(S)=1∶15 时,产物的直径降低到约为300 nm[图10(g)和图10(h)],并且产物表面片层结构的间距逐渐增大.我们推测产生这些变化的主要原因是:一方面,随着反应物KSCN的增加,在酸性体系下产生的H2S 的量也越来越多,从而使产物MoS2的成核数目增加,晶粒在生长过程中来不及进一步长大;另一方面,在反应釜密闭的环境中,H2S气体的量增多,导致反应体系的压强越来越大,在高压下,MoS2片层间吸附的物质增多,这些物质可能形成阻隔层,使得MoS2层间堆积的阻力增大,从而使片层结构的间距增大.

图10 反应物中不同钼、硫摩尔比反应所得产物的SEM照片Fig.10 SEM images of the products obtained by reacting with different molar ratios of molybdenum and sulfur in the reactants
3 结论
本文采用水热法,选择MoO3作为反应的钼源,KSCN 作为反应的硫源和还原剂,通过改变反应温度、体系的pH 值、添加表面活性剂(CTAB)以及使硫源大比例过量的方法,探索不同反应条件对产物微观结构和形貌的影响,并对其反应机理进行研究.主要结论如下:
1)随着反应体系pH 值的降低,所得产物结晶度增高,并且微观形貌从棒片状到絮状团簇,再向球花状转变.在反应温度为240 ℃,n(Mo)∶n(S)=1∶3,不添加表面活性剂,体系pH=0.6,所得产物为大小均一,直径大约为400 nm 的球花,并且球花的表面由许多花瓣状的薄片构成.
2)在本文的反应体系中,当反应温度为180 ℃时,无法得到MoS2,而随着反应温度的升高,所得产物结晶度变好,产物表面片状花纹加深,且更倾向于向球花的微观形貌转变.实验结果初步确定240 ℃为该体系下反应得到MoS2的最佳温度.
3)在反应温度为240 ℃,n(Mo)∶n(S)=1∶3,加入表面活性剂CTAB 以后,所得MoS2表现为更加规整的球形,尺寸分布也更加均匀,球的表面有花瓣状的薄片结构,而且随着反应体系pH 值的降低,所得MoS2球直径减小,pH=1.0 时大约为800 nm,而pH=0.6时,直径只有200~300 nm.
4)随着反应物中KSCN 的增加,反应物中钼、硫摩尔比减小,所得球状产物的直径尺寸越来越小.当n(Mo)∶n(S)=1∶3 时,产物的直径约为500 nm,当n(Mo)∶n(S)=1∶15 时,产物的直径降低到约为300 nm,并且产物表面片层结构的间距逐渐增大.
5)成功合成了花球状的MoS2,其球花表面由许多花瓣状薄片组成,且颗粒均匀,纯度较高,有望在固体润滑剂及光催化领域得到应用.

