高龄孕妇早发型重度子痫前期不良结局列线图模型的构建及验证
于 璐, 徐晓英
(南通大学附属海安医院 妇产科, 江苏 海安, 226600)
子痫前期(PE)和子痫是妊娠期高血压(PIH)的严重疾病类型,是导致围产期孕妇和新生儿死亡的重要原因之一,也是不良妊娠结局的重要危险因素[1]。相较于晚发型PE,早发型PE的发病孕周小于34周,对孕妇和胎儿的影响持续时间更长,导致的不良结局风险更大[2]。孕妇不良结局主要包括中枢神经系统疾病、心肺功能障碍、胎盘早剥、大出血、子宫切除以及溶血肝功能异常血小板减少综合征(HELLP)和死亡等,胎儿不良结局主要包括新生儿呼吸窘迫综合征、早产、宫内死亡等[3]。高龄被认为是PIH和PE的重要危险因素,年龄每增加1岁, PE的不良结局风险升高0.5倍[4]。既往预测PE不良结局的量化模型为UKAH U V等[5]建立的full PIERS模型,由于地区和种族的差异,该模型在中国推广受限,而且该模型不涉及PE高龄孕妇。还有一些模型缺乏外部数据验证,涵盖部分复杂性、难以获得的指标[6], 在临床实践中操作难度较大,不利于早期风险筛查。因此,本研究调查中国区域性高龄孕妇伴早发型重度PE(SPE)短期院内不良结局的发生率和危险因素,并构建定量列线图预测模型以指导临床实践。
1 资料与方法
1.1 一般资料
将2016年1月—2020年1月南通大学附属海安医院妇产科确诊的早发型SPE高龄孕妇316例作为训练集,根据院内结局不同将其分为不良组52例和良好组264例。另选择2020年2月—2022年5月90例早发型SPE高龄孕妇为验证集,其中16例出现不良结局。训练集年龄36~46岁,平均(40.2±4.8)岁; 孕周26~33周,平均(30.4±3.2)周; 不良结局发生率为16.5%(52/316); 验证集年龄35~47岁,平均(40.6±5.3)岁; 孕周27~32周,平均(30.5±3.3)周; 不良结局发生率为17.8%(16/90)。训练集与验证集年龄、孕周和不良结局发生率比较,差异无统计学意义(P>0.05), 具有可比性。纳入标准: ① 患者年龄≥35岁,正常妊娠,单活胎; ② 符合《妊娠期高血压疾病诊治指南(2020)》[7]早发型SPE的诊断标准,孕周<34周者; ③ 临床资料完整者。排除标准: ① 确诊为子痫,且为复发性PE者; ② 妊娠前诊断为原发性心、肺、肝、肾功能障碍,凝血功能异常,自身免疫性疾病者; ③重症感染,既往有脑卒中史、恶性肿瘤、严重精神性疾病者。
1.2 方法
对训练集不良组与良好组患者的临床资料和血液生化指标进行单因素分析,采用套索算法(LASSO)和多因素Logistic回归分析筛选最优预测因素,R软件建立列线图,采用受试者工作特征(ROC)曲线计算模型在训练集与验证集内预测不良结局的曲线下面积(AUC)。参照既往文献报道统计与不良结局有关的临床资料,包括年龄、孕周、产史、既往史(高血压、PIH、PE或子痫)、临床症状(头痛或头晕、恶心或呕吐、下肢水肿、视力模糊、胸痛或呼吸困难)、体质量指数、收缩压、舒张压和蛋白尿。血液生化指标主要包括白细胞计数、血红蛋白、血小板计数、D-二聚体、凝血酶原时间(PT)和PT活动度(PTA)、纤维蛋白原、活化部分凝血酶原时间(APTT)、白蛋白、丙氨酸转氨酶(ALT)、尿酸、总胆固醇、低密度脂蛋白、乳酸脱氢酶(LDH)、尿素氮(BUN)和肌酐,采用腹部超声检测胎儿双顶径、头围、羊水指数、胎儿心率、胎儿脐动脉收缩期最大血流速度与舒张期末期血流速度的比值(S/D)和阻力指数(RI)。
1.3 观察指标
本研究结局包括孕妇和胎儿不良结局,其中孕妇不良结局主要包括中枢神经系统疾病(子痫、脑血管意外、视网膜脱离、意识障碍等)、心肺功能障碍(心力衰竭、肺水肿、呼吸困难等)、胎盘早剥、大出血、弥散性血管内凝血、子宫切除以及HELLP和死亡等; 胎儿不良结局主要包括新生儿呼吸窘迫综合征、早产、宫内死亡等。
1.4 统计学方法
采用SPSS 20.0统计学软件统计数据,符合正态分布的计量资料以均数±标准差表示,组间比较采用t检验,计数资料以[n(%)]表示,比较采用χ2检验; 采用LASSO筛选非共线性指标,以10倍交叉验证法确定参数λ; 采用多因素Logistic回归分析确定最优预测因素,并采用逐步后退法进行分析; R软件建立列线图模型, bootstrap重复取样1 000次进行验证。采用ROC曲线计算AUC, Hosmer-Lemeshow 检验计算拟合优度,校正曲线计算一致性; 以双侧检验P<0.05为差异有统计学意义。
2 结 果
2.1 良好组和不良组临床资料和血液生化指标的单因素分析
不良组症状数量、收缩压、PT、ALT、尿酸、LDH、BUN和肌酐、脐动脉S/D和RI高于或长于良好组,而血小板计数、PTA和白蛋白低于良好组,差异有统计学意义(P<0.05)。见表1。

表1 良好组和不良组临床资料和血液生化指标的单因素比较
2.2 不良结局的LASSO分析
LASSO分析共筛选出6个非共线性指标,即症状数量、BUN、PT、LDH、血小板计数和白蛋白,见图1
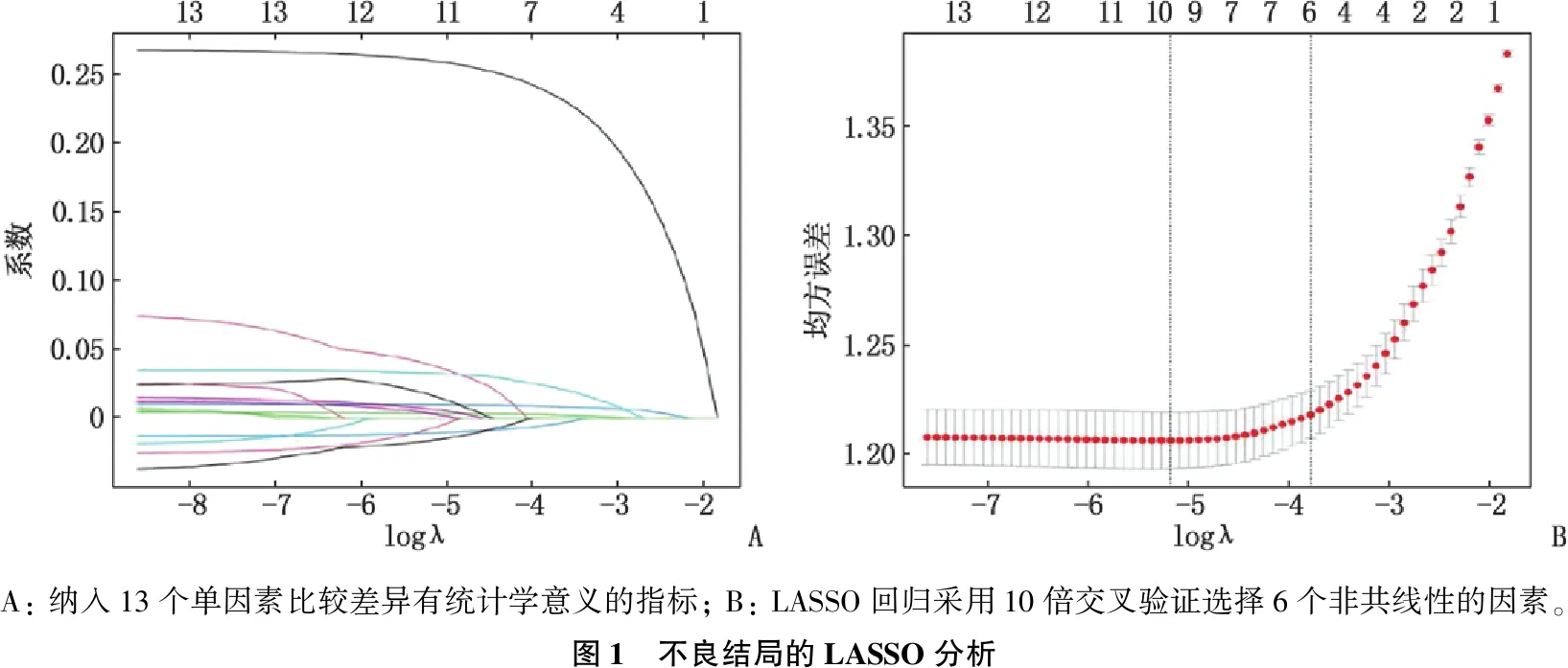
A: 纳入13个单因素比较差异有统计学意义的指标; B: LASSO回归采用10倍交叉验证选择6个非共线性的因素。图1 不良结局的LASSO分析
2.3 不良结局的Logistic回归分析
根据症状数量、BUN、PT、LDH、血小板计数和白蛋白的中位值转换为二分类变量,即症状数量为0个=0, ≥1个=1; BUN<5 mmol/L=0, ≥5 mmol/L=1; PT<10 s=0, ≥10 s=1; LDH<250 U/L=0, ≥250 U/L=1; 血小板计数≥100×109/L=0, <100×109/L=1; 白蛋白≥30 g/L=0, <30 g/L=1。多因素Logistic回归分析显示,症状数量≥1个、BUN≥5 mmol/L、PT≥10 s、LDH≥250 U/L、血小板计数<100×109/L和白蛋白<30 g/L是不良结局的独立预测因子(P<0.05), 见表2。
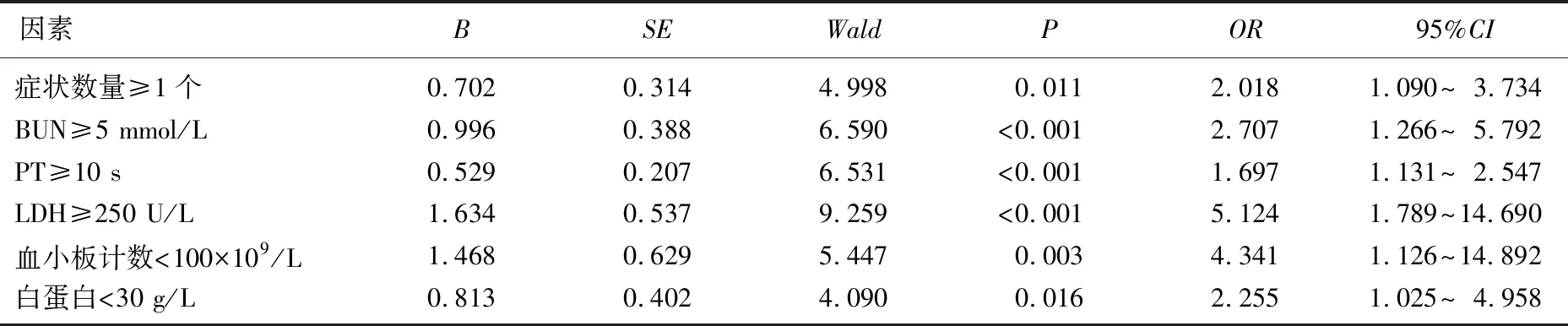
表2 不良结局的Logistic回归分析
2.4 不良结局的列线图模型
R软件根据Logistic回归筛选的主要预测因子对应权重建立列线图模型,总分240分,见图2。例如, 1例早发型SPE高龄孕妇入院表现为头晕、头痛,对应分值为18分; BUN为5.5 mmol/L, 对应分值为27分; PT为11 s, 对应分值为18分; LDH为260 U/L, 对应分值为26分; 血小板计数为185×109/L, 对应分值为15分; 白蛋白为40 g/L, 对应分值为27分。各项相加得到总分为131分,对应风险为0.78, 即不良结局的发生率相对较高。
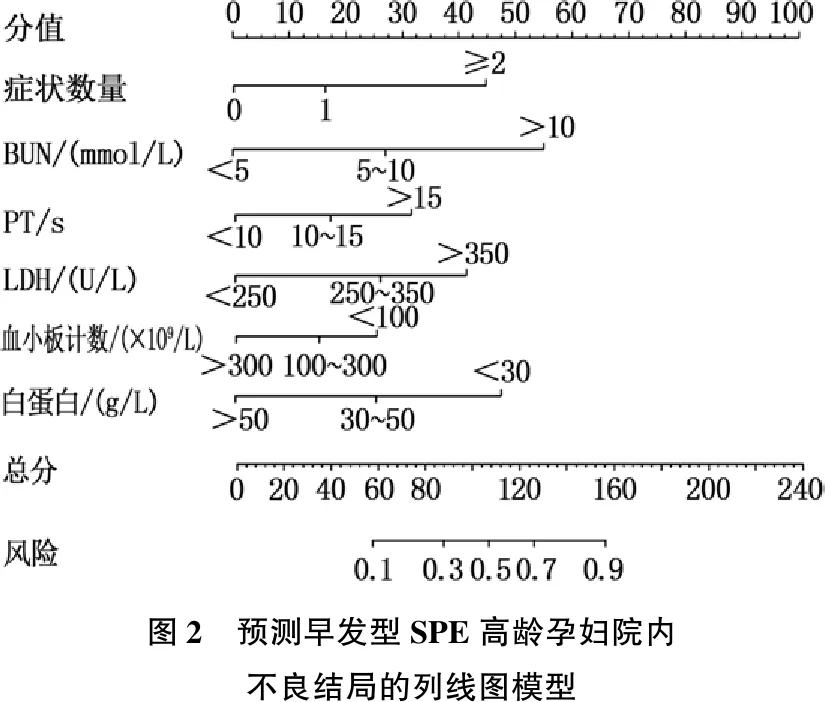
图2 预测早发型SPE高龄孕妇院内不良结局的列线图模型
2.5 列线图模型的ROC曲线分析
对训练集进行内部验证,列线图预测不良结局的AUC为0.895(95%CI: 0.822~0.943,P<0.001)。Hosmer-Lemeshow 检验显示其拟合优度良好(χ2=12.325,P=0.548)。对验证集进行外部验证,列线图预测不良结局的AUC为0.846(95%CI: 0.789~0.901,P<0.001), Hosmer-Lemeshow 检验显示其拟合优度良好(χ2=9.627,P=0.324), 见图3。
2.6 列线图的校正曲线
训练集与验证集的校正曲线显示,列线图模型预测不良结局的概率与实际发生率有较好的一致性。见图4。
3 讨 论
中国PE的总体发病率为2%~7%, 高龄孕妇伴早发型SPE的病情复杂且严重,显著增高了不良妊娠结局的风险[8]。目前临床无高效的预防策略,早期识别不良结局的高危患者是改善预后的重要途径。本研究显示,早发型SPE高龄孕妇短期院内不良结局的发生率为16.5%~17.8%。训练集与验证集患者的年龄、孕周和不良结局发生率具有可比性,体现了样本的随机性。进一步发现,不良组症状数量、平均收缩压、PT、ALT、尿酸、LDH、BUN和肌酐、脐动脉S/D和RI高于或长于良好组,而血小板计数、PTA和白蛋白低于良好组。入院患者与PIH和PE相关的临床症状越明显,数量越多,提示病情越严重。收缩压高于175 mmHg往往预示会出现高风险的并发症,如子痫、脑出血、胎儿死亡等[9]。PT延长和血小板计数下降提示出血风险增大。妊娠期高凝状态是PE的重要病理机制,易形成血栓,导致胎盘灌注不足和胎盘功能下降,进而导致胎儿生长受限和胎盘早剥[10-11]。PE患者血管内皮细胞损伤、血小板黏附和聚集导致血管内皮细胞缺血和缺氧加重血小板破坏,导致血小板减少。血清ALT、尿酸、BUN和肌酐升高提示肝、肾功能损伤。PE患者全身小动脉收缩导致胎儿缺血、缺氧,子宫和胎盘分离产生大量乳酸,酸性物质的排出能够抑制肾排泄尿酸,增高血清尿酸水平[12]。PE患者全身小动脉痉挛性收缩导致各种器官和组织缺血和缺氧,其中对肝脏和肾脏的损害最明显,肾功能的变化比肝功能的变化更早、更显著[13-14]。PE患者肾小动脉的广泛痉挛和收缩导致肾小球肿胀,肾血流量和肾小球滤过率降低,阻碍血液中尿酸、BUN和肌酐的清除和排泄,导致血清水平显著升高[15]。随着PE进展,血管壁张力、血管内皮细胞损伤和通透性增加,大量蛋白质和液体泄漏到组织空间,血浆蛋白质水平降低,血液黏度增加,血氧供应失衡,体内LDH水平升高[16-17]。因此, PE的发病是多系统、多途径共同作用的结果。
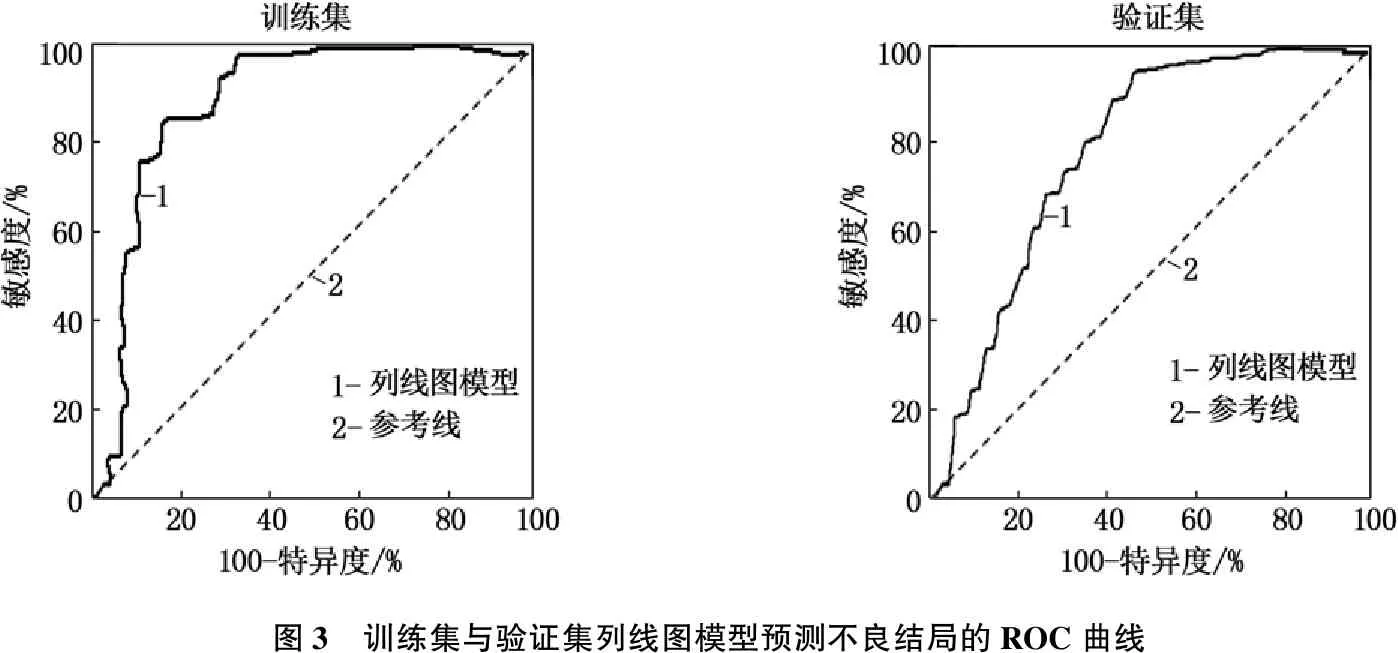
图3 训练集与验证集列线图模型预测不良结局的ROC曲线
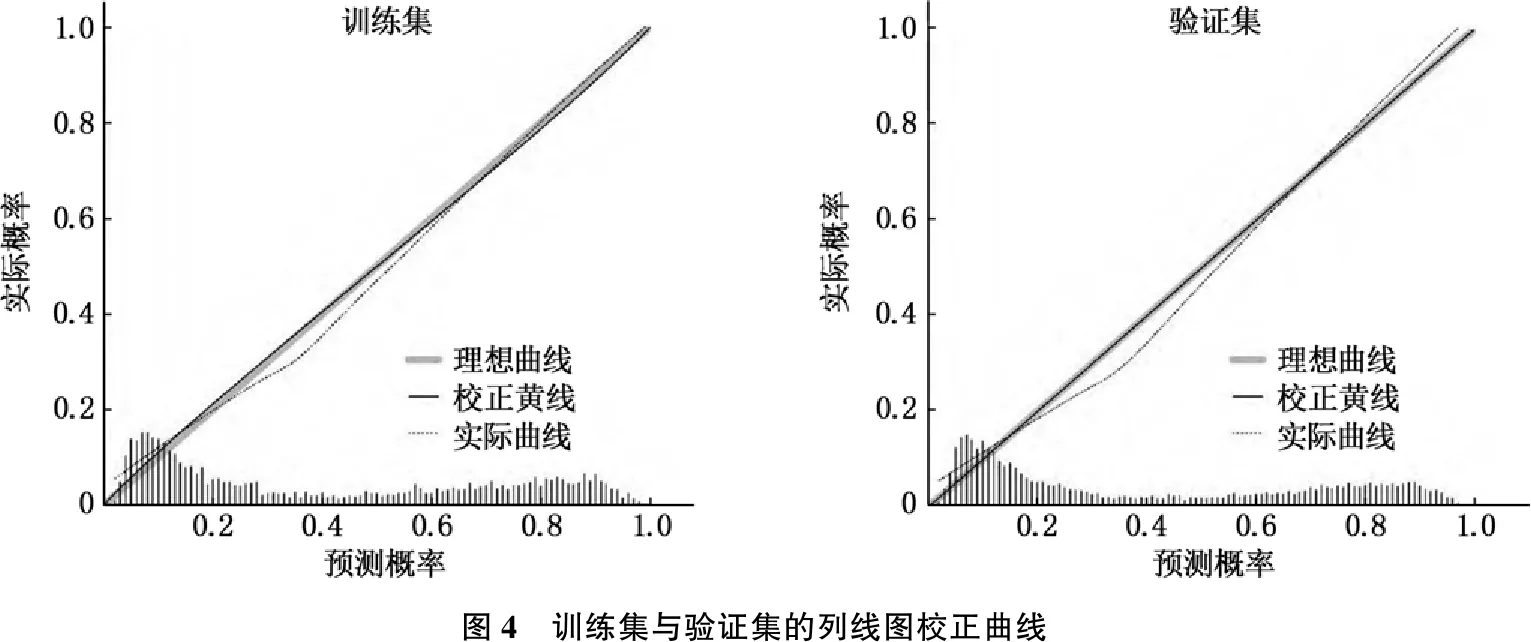
图4 训练集与验证集的列线图校正曲线
本研究通过LASSO分析筛选出6个非共线性指标,多因素Logistic回归分析显示,症状数量≥1个、BUN≥5 mmol/L、PT≥10 s、LDH≥250 U/L、血小板计数<100×109/L和白蛋白<30 g/L是不良结局的独立预测因子(P<0.05)。开发一款可视化强、操作简便、涵盖指标在临床中易于获得的列线图模型推广价值高。既往开发的预测模型,如full PIERS模型不涉及PE高龄孕妇,还有一些模型未能区别PE亚型,诊断特异性不高; 部分模型缺乏外部数据验证,涵盖部分复杂性、难以获得的指标,在临床实践中操作难度较大,不利于早期风险筛查。本研究开发的列线图经内部和外部验证,诊断性能均较好(AUC大、拟合优度和一致性好)。临床医生可以根据该模型并结合患者病情的变化快速评估疾病风险,以改进治疗计划,减少不良结局; 根据模型中每个因素的得分判断治疗重点,为每个患者制订恰当的个性化治疗方案,从而减少疾病危害,确保母婴健康[18-19]。本研究有一定局限性: 所有数据来自同一个研究中心,可能存在样本选择偏倚,下一步应通过多中心前瞻性队列研究的方法提供更强的循证医学证据; 临床实践中需要深入挖掘可能还存在其他未知的,且与PE尤其是高龄孕妇不良结局密切相关的因素。
综上所述,本研究开发的列线图模型可视化强、操作简便,可用于指导临床早期识别早发型SPE高龄孕妇的院内不良结局,有较好的预测效能,对中国区域性早发型SPE高龄孕妇的临床预后有重要应用价值。

